品川長夫・長谷川正光
NTT西日本東海病院外科平田公一・古畑智久・水口 徹
札幌医科大学医学部外科学第一講座長内宏之
札幌外科記念病院外科柳内良之
医療法人禎心会新札幌恵愛会病院外科秦 史壯
札幌道都病院外科佐々木一晃・染谷哲史・原田敬介・
大野敬祐
小樽掖済会病院外科時田捷司・中村誠志
登別厚生年金病院外科渋谷 均
市立室蘭総合病院外科長谷川 格・木村雅美・大島秀紀・前田豪樹
北海道済生会小樽病院外科向谷充宏・鬼原 史
北海道社会事業協会函館病院外科渡部公祥
市立赤平総合病院外科星川 剛・木村 仁
滝川市立病院外科牛島康栄・柳 在勲
独立行政法人国立病院機構 埼玉病院外科相川直樹・安倍晋也
慶應義塾大学医学部救急医学由良二郎
松波総合病院消化器センター竹山廣光・若杉健弘
名古屋市立大学大学院消化器外科学谷口正哲
大隈病院外科水野 勇・福井拓治
名古屋市立緑市民病院外科真下啓二
愛知県厚生連尾西病院外科石川 周
刈谷豊田総合病院高浜分院外科外科感染症分離菌とその薬剤感受性
— 2008
年度分離菌を中心に
—
(2010 年 1 月 27 日受付) 1982年7月から外科感染症分離菌に関する多施設共同研究を行ってきたが,ここでは 2008年度(2008年4月⬃2009年3月)の成績を中心にまとめた。1年間で調査対象と なった症例は215例であり,このうちの173例 (80.5%) から694株の細菌と18株の真菌 が分離された。一次感染症から357株,術後感染症から337株の細菌が分離された。一 次感染症では,嫌気性グラム陰性菌の分離頻度が高く,次いで好気性グラム陰性菌であ り,術後感染症では,好気性グラム陽性菌の分離頻度が高く,次いで嫌気性グラム陰性 菌であった。好気性グラム陽性菌については,一次感染症においてEnterococcus faecalis, Enterococcus faeciumやEnterococcus aviumなどのEnterococcus spp.の分離頻度が最も高 く,次いでStreptococcus anginosusなどのStreptococcus spp.,Staphylococcus aureusなど
水野 章
JA三重厚生連いなべ総合病院外科毛利紀章・角田直樹
知多厚生病院外科久保正二・李 栄柱
大阪市立大学大学院肝胆膵外科学・消化器外科学大村 泰
市立藤井寺市民病院外科小林康人・辻 毅
和歌山ろうさい病院外科山上裕機・川井 学
和歌山県立医科大学第二外科竹末芳生
兵庫医科大学感染制御学田中紀章
岡山大学大学院医歯薬学総合研究科 消化器・腫瘍外科学木村秀幸
岡山済生会病院外科岩垣博巳
独立行政法人 国立病院機構 福山医療センター外科末田泰二郎・檜山英三・村上義昭・
大毛宏喜・上村健一郎
広島大学大学院医歯薬学総合研究科 病態制御医科学講座外科学津村裕昭
広島市立舟入病院外科横山 隆
広島市医師会運営安芸市民病院竹内仁司・田中屋宏爾
独立行政法人国立病院機構 岩国医療センター外科安波洋一・笠 晋一朗
福岡大学医学部第一外科I.
対象と方法
1982年7月に開始した外科感染症分離菌感受性 調査研究会は,現時点で,消化器外科を中心とす る32施設の共同研究会となっている。 対象は消化器外科領域の感染症患者あるいは感 染を合併した入院患者である。一次感染症は,穿 孔性腹膜炎,急性胆嚢炎,急性胆管炎,肝膿瘍 などの腹腔内感染症である。術後感染症は,腹腔 内膿瘍や創感染などの消化器系手術後の術野感染 であり,術後の呼吸器系感染症,尿路感染症,血 管内留置カテーテル感染症あるいは敗血症などの 術野外感染症は含めなかった。同一患者からの分 離菌は初回のもののみを取り上げ,重複を避け, また,消化管と持続的に交通している腸瘻などを 伴う腹腔内感染は対象外とした。 病巣からの検体をケンキポーター®(クリニカ ルサプライ)に採取し,2002年3月までは東京総 合臨床検査センターへ,その後は山田エビデンス リサーチへ送付し,原因菌を分離・同定した。 山田エビデンスリサーチでの原因菌の分離・同 定の概要は以下の如くである。検査材料は,①グ ラム染色,②直接分離培養,③増菌培養を施行し た。染色結果から選択培地の追加が必要であれば 追加した。好気培養は,馬血液寒天培地とBTB 寒天培地を用いて,37°C培養で毎日1回,3日間 観察,嫌気培養はブルセラHK寒天培地,BBE寒 天培地,PEAブルセラHK寒天培地,PVブルセ ラHK寒天培地を用い,嫌気ジャーでアネロパッ ク®(三菱ガス化学)を使用して37°Cで3⬃7日 間観察,検出菌があればその都度純培養し,各菌 種の特徴的な性状を重点に従来法および同定キッ トを併用し同定した。増菌培養は増菌培地にのみ 菌が検出された時や,グラム染色結果と直接分離 培養結果で不一致があるときに分離して確認及び 追加をした。 薬剤感受性については,日本化学療法学会標準 法であるMIC2000システムを用いた微量液体希 釈法により測定した。感受性測定薬剤としては, Oxacillin (MPIPC), Ampicillin (ABPC), Tazobactam/Piperacillin (TAZ/PIPC), Cefazolin (CEZ),Cefotiam (CTM),Cefmetazole (CMZ), のStaphylococcus spp.であった。術後感染症からは,Enterococcus spp.の分離頻度が最も 高く,次いでStaphylococcus spp.であった。好気性グラム陰性菌では,一次感染症から Escherichia coliの分離頻度が最も高く,次いでKlebsiella pneumoniae,Pseudomonas aeruginosaなどであり,術後感染症からはP. aeruginosa,E. coli,Enterobacter cloacae, K. pneumoniaeの分離頻度が高かった。嫌気性グラム陽性菌では,一次感染症から Eg-gerthella lenta,Parvimonas micra,Streptococcus constellatus,Gemella morbillorum,術 後感染症からはE. lenta,P. micraの分離頻度が高かった。嫌気性グラム陰性菌では,一 次感染症からは,Bacteroides fragilisの分離頻度が最も高く,次いでBacteroides thetaio-taomicron,Bacteroides ovatus,Bilophila wadsworthiaであり,術後感染症からはB. frag-ilisの分離頻度が最も高く,次いでB. thetaiotaomicron,B. wadsworthia,B. ovatusであっ た。バンコマイシン耐性のメチシリン耐性黄色ブドウ球菌(MRSA) やEnterococcus spp. および多剤耐性緑膿菌は認められなかった。1982年7月から全国的に外科感染症における分離菌とその薬剤感受性の調査1⬃31)を 行ってきたが,今回は,2008年度(2008年4月⬃2009年3月)における分離菌の動向と その薬剤感受性成績を中心に検討した。
Flomoxef (FMOX),Cefmenoxime (CMX), Lata-moxef (LMOX),Ceftazidime (CAZ),Cefpirome (CPR),Cefepime (CFPM),Cefozopran (CZOP), Sulbactam/Cefoperazone (SBT/CPZ),Cefsulodin (CFS),Aztreonam (AZT),Carumonam (CRMN), Imipenem (IPM),Meropenem (MEPM), Gentam-icin (GM),Amikacin (AMK),Arbekacin (ABK), Isepamicin (ISP), Clindamycin (CLDM), Minocycline (MINO), Ciprofloxacin (CPFX), Levofloxacin (LVFX), Linezolid (LZD), Van-comycin (VCM), Teicoplanin (TEIC), Fosfo-mycin (FOM) を用いた。
II.
成績
1)細菌検出状況 2008年度の調査対象として検体が採取された症 例は215例であった。このうち173例 (80.5%) か ら694株の細菌と18株の真菌が分離されたが,残 る42例からは細菌あるいは真菌のいずれも分離 されなかった。 過去27年間の年度別検体数と総分離細菌株数 の推移をFig. 1に示した。本年度の総分離菌株数 は過去最高であった。 平均検体数は27年間で 195.5検体,最近の5年間では236.8検体であっ た。総分離細菌株数は,1990年代半ばから増加 し,更に最近の数年間では著増している。平均分 離細菌総株数は27年間で361.2株,最近の5年間 では567.8株であり,検体あたりの分離菌数の増 加がみられた。 感染症別の細菌分離例数をTable 1に示した。 一次感染症全体では,109例のうち75例 (68.8%) から細菌が分離された。内訳として,肝・胆道感 染症では35例中21例 (60.0%),腹膜炎では61例 中42例(68.9%) から細菌が分離された。術後感 染症全体では,106例中98例(92.5%) から細菌が 分離された。症例数が最も多い創感染では,66例 中63例(95.5%) から細菌が分離された。一次感 染症より術後感染症において細菌の陽性率が高 かった。 Fig. 1. 検体数と総検出細菌株数の推移分離菌が検出された材料としては,膿汁が99 検体 (57.2%) と最も多く,次いで腹水38検体 (22.0%),胆汁17検体(9.8%) の順であった (Fig. 2)。 全173検体から真菌を除き694株の細菌が分離 され,1検体平均で4.0株が分離された。173検体 中 の21.4%は 単 独 菌 分 離 ,16.8%は2菌 種 , 16.2%は3菌種,9.2%は4菌種,7.5%は5菌種, 28.9%は6菌種以上が分離された。検体別では, 腹 膜 炎 か ら の も の で 複 数 菌 分 離 が 最 も 多 く , 51.4%は5菌種以上の複数菌分離であった。一方, 肝・胆道感染からのものでは,複数菌分離は少な く,43.5%は単独菌分離であった(Fig. 3)。 Table 1. 感染症別例数 Fig. 2. 臨床検体の種類別頻度
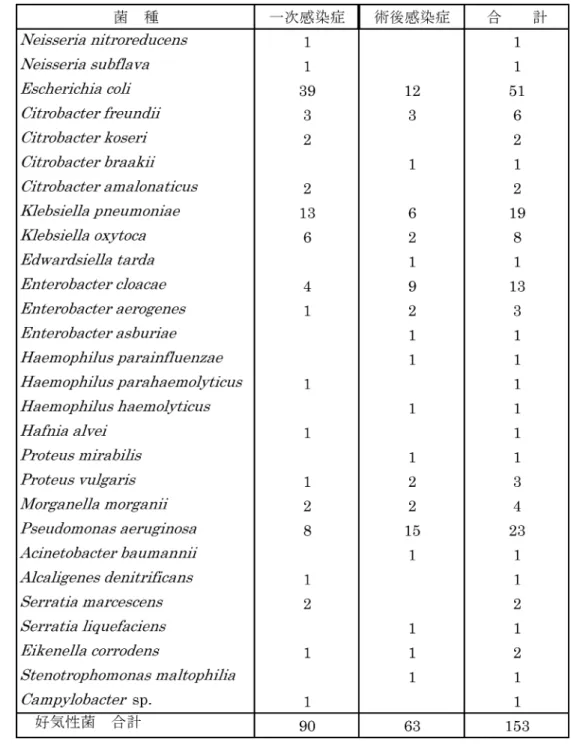
2)2008年度の分離菌 全分離菌の内訳をTable 2に示した。一次感染 症から357株,術後感染症から337株の細菌が分 離されているが,一次感染症では嫌気性グラム陰 性菌の分離頻度が最も高く,次いで好気性グラム 陰性菌であり,術後感染症では好気性グラム陽性 菌の分離頻度が高く,次いで嫌気性グラム陰性菌 であった。 真菌は,一次感染症から9株(Candida albicans
5株,Candida glabrata 2株,Candida kefyrと Zy-gosaccharomyces fermentatiの各1株),術後感染 症からも9株(C. albicans 8株とC. glabrata 1株) が分離された。 好気性グラム陽性菌については,一次感染症と 術後感染症をあわせ32菌種(属)の182株が分 離された。一次感染症からは,25菌種(属)の 64株,術後感染症からは,20菌種(属)の118 株であった(Table 3)。菌種別の頻度は,一次感染 Fig. 3. 検体毎の分離菌株数 Table 2. 外科感染症分離菌の内訳
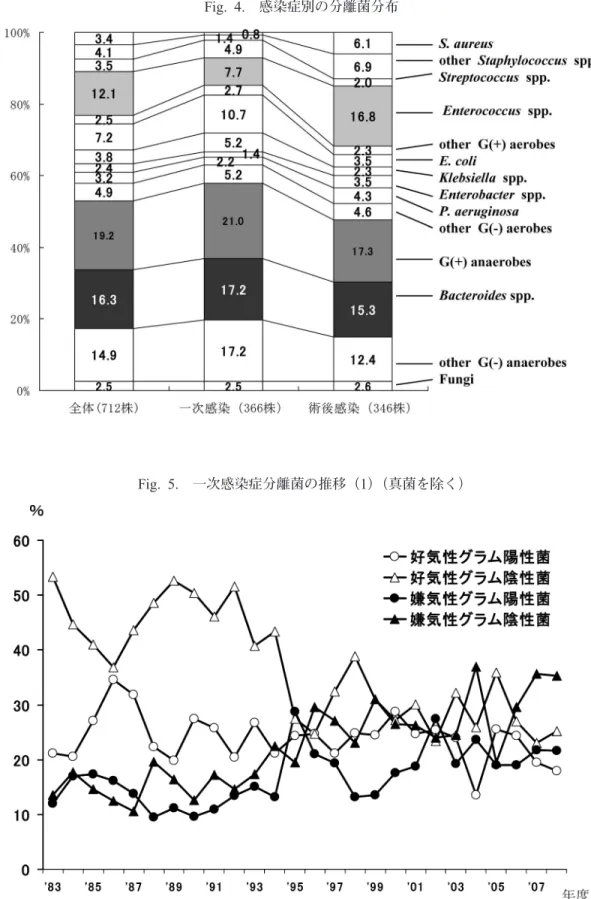
症でEnterococcus faecalisの分離頻度が最も高く, 次 い で Streptococcus anginosus,Enterococcus faecium, Enterococcus avium, Staphylococcus aureusであり,術後感染症からは,E. faecalisの 分離頻度が最も高く,次いでS. aureus, Staphylo-coccus epidermidis,E. faecium,E. aviumであっ た。属別では,一次感染症でEnterococcus spp.の 分離頻度が高く,次いでStreptococcus spp.であっ た。一方,術後感染症では,Enterococcus spp.の 分離頻度が高く,次いでStaphylococcus spp.で あった。 嫌気性グラム陽性菌については,一次感染症と 術後感染症をあわせ33菌種(属)の137株が分 離された。一次感染症からは,25菌種(属)の 77株,術後感染症からは,24菌種(属)の60株 で あ っ た (Table 4)。 一 次 感 染 症 か ら は , Eg-gerthella lentaの 分 離 頻 度 が 最 も 高 く , 次 い で Parvimonas micra, Streptococcus constellatus, Gemella morbillorumであり,術後感染症からは E. lentaの分離頻度が最も高く,次いでP. micra, Finegoldia magnaであった。 好気性グラム陰性菌については,一次感染症と 術後感染症をあわせ28菌種(属)の153株が分 離された。一次感染症からは,19菌種(属)の 90株,術後感染症からは,19菌種の63株であっ た(Table 5)。一次感染症からは,Escherichia coli の分離頻度が最も高く,次いで,Klebsiella pneu-moniae, Pseudomonas aeruginosa, Klebsiella oxytocaであった。一方,術後感染症からは,P. aeruginosaの分離頻度が最も高く, 次いでE. coli, Enterobacter cloacae, K. pneumoniaeで あった。 嫌気性グラム陰性菌については,一次感染症と 術後感染症をあわせ29菌種(属)の222株が分 離された。一次感染症からは,28菌種(属)の 126株,術後感染症からは,22菌種(属)の96 株であった (Table 6)。一次感染症からは, Bac-teroides fragilisの分離頻度が最も高く,次いで Bacteroides thetaiotaomicron,Bacteroides ovatus, Bilophila wadsworthiaであった。術後感染症から は,B. fragilisの分離頻度が最も高く,次いでB. thetaiotaomicron,B. wadsworthia,B. ovatusで あった。 全体として感染症別の分離菌分布をみると,一 次感染症分離菌は術後感染症分離菌と比較し,グ ラム陽性嫌気性菌,Bacteroides spp.およびその他 のグラム陰性嫌気性菌,E. coliなどの分離頻度が 高かった。一方,術後感染症分離菌は,一次感染 症分離菌と比較してEnterococcus spp.や Staphylo-coccus spp.の分離頻度が高く,さらに,P. aerugi-nosaなどの好気性グラム陰性桿菌の分離頻度が高 くなっていた(Fig. 4)。 3)分離菌の年次的変遷 一次感染症分離菌を好気性と嫌気性およびグラ ム陽性と陰性にわけて年次的推移 (Fig. 5) をみる と,1990年代後半からは嫌気性菌と好気性菌と の差が縮小し,嫌気・好気性菌共にややグラム陰 性菌の割合が高い状況が続いている。2007年度 は嫌気性グラム陰性菌の割合が最も高くなってお り,僅かの差で好気性グラム陽性菌の割合が最低 となったが,2008年度にはこの差がやや拡大し た。この推移を検体数あたりの菌種別頻度をみる と,腸内細菌叢として優位なE. coliの分離頻度の 高さはゆるぎなく,2007年度と2008年度にはさ らに高率となっている。B. fragilisは2番目の分離 頻度となっている(Fig. 6)。 同様に術後感染症分離菌の推移 (Fig. 7) をみる と,1990年代後半から好気性グラム陽性菌の分 離頻度が高いが,嫌気性菌では,1990年代から グラム陽性菌,陰性菌ともに増加傾向を示してき た。2006年度以降は,嫌気性グラム陰性菌の分 離頻度が好気性グラム陰性菌より高くなっている。 検体数あたりの菌種別分離頻度をみると,1993年
Fig. 4. 感染症別の分離菌分布
Fig. 6. 一次感染症分離菌の推移(2)(検体数あたり,真菌を除く)
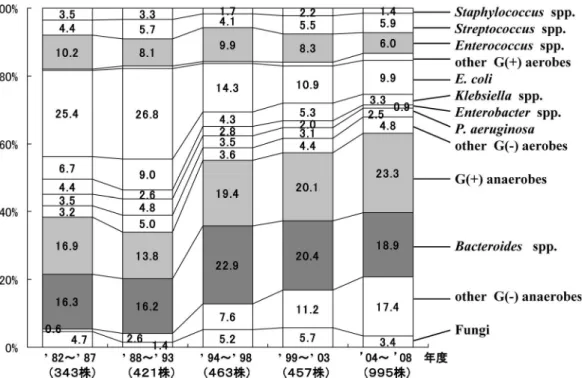
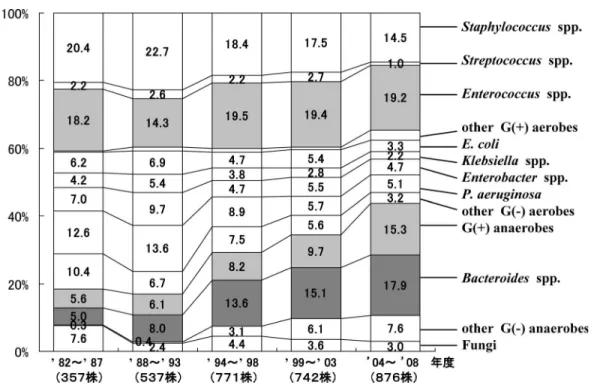
以 降 はE. faecalisの 分 離 頻 度 が ,1999年 度 と 2006年度を除き最も高い。S. aureusは,1992年 度以降はほぼ20%台の分離頻度であるが,1999 年度の分離頻度が最も高く,2005年度も高い。P. aeruginosaは1990年代の前半までは20⬃30%台 という高い分離頻度であったが,1998年度から は,2001年度を除き10%台の分離頻度と低下し ている。E. coliについては,ほぼ10%台の分離頻 度となっている(Fig. 8)。 MRSAの分離頻度については,1991年度と 1998年度にピークがあった。2005年度と2006年 度に再び高い分離頻度となったが,2007年度と 2008年度は低下している。S. aureus中に占める MRSAの比率は,2007年度までの3年間は低下し てきたが,2008年度は再び増加し,ほぼ80%と なった(Fig. 9)。 4)感染症別の分離菌の変遷 (1)腹膜炎分離菌 続発性腹膜炎分離菌は, 最近の5年間では, Bacteroides spp. (18.9%) を中心とする嫌気性グラ ム陰性菌の頻度が最も高く,次いで嫌気性グラム 陽性菌 (23.3%) の頻度が高い。次いで,E. coli (9.9%),Enterococcus spp. (6.0%),Streptococcus spp. (5.9%) などとなっている。以前ではE. coliの 分離頻度が高かったが,その後はグラム陽性,陰 性ともに嫌気性菌の分離頻度が高くなっており, 1990年後半からは嫌気性菌がほぼ半数以上を占 めている(Fig. 10)。 一方,術後腹膜炎では,最近の5年間で, En-terococcus spp. (18.5%) の分離頻度が最も高く, 次いでBacteroides spp. (15.0%),嫌気性グラム陽 性 菌 (12.7%), そ の 他 の 嫌 気 性 グ ラ ム 陰 性 菌 (12.0%),Staphylococcus spp. (10.1%) などとなっ ている。また1999年度以降Staphylococcus spp.の Fig. 8. 術後感染症分離菌の推移(2)(検体数あたり,真菌を除く)
Fig. 9. MRSA分離頻度の推移
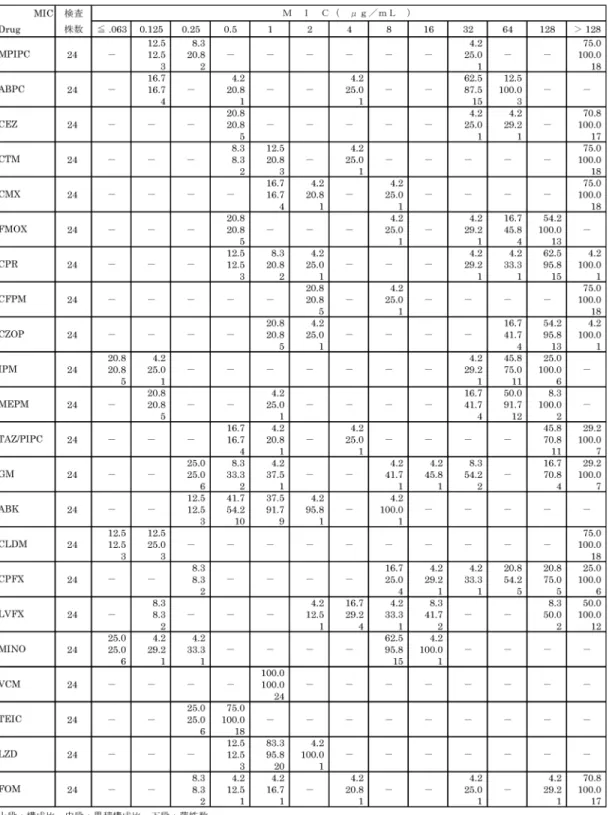
分離頻度がやや高くなってきている(Fig. 11)。 (2)肝・胆道感染症分離菌 胆嚢炎,胆管炎などの肝・胆道感染症分離菌に ついては,1990年代の中頃まではE. coliや Kleb-siella spp.などの分離頻度が高かったが,1994年 以降はEnterococcus spp.の頻度が高くなってきて いる。その反面,E. coliとKlebsiella spp.などの 好気性グラム陰性桿菌の分離頻度が低下傾向を示 してきたが,最近の5年間ではKlebsiella spp.の分 離頻度が再度高くなってきている。嫌気性菌の分 離頻度は低いが,近年やや増加傾向にある (Fig. 12)。 術後の肝・胆道感染症では,1994年度以降, 相変わらずEnterococcus spp.の分離頻度が高い。 最 近 の5年 間 で は ,Enterobacter spp. (16.1%), Klebsiella spp. (9.7%),P. aeruginosa (9.7%),E. coli (9.7%) などの好気性グラム陰性桿菌の分離頻 度が高くなってきた。逆に嫌気性菌の分離頻度は 低い(Fig. 13)。 (3)創感染分離菌 創感染からの分離菌は,最近の5年間をみると, Bacteroides spp.を中心とする嫌気性菌の分離頻度 が40.8%と高くなってきている。Enterococcus spp.の分離頻度に変化はないが,Staphylococcus spp.やE. coli,Klebsiella spp.などの好気性グラム 陰性菌の分離頻度の低下が顕著である(Fig. 14)。 5)分離菌の薬剤感受性 各種分離菌の薬剤感受性をTable 7⬃44に示し た。なお,少数株とMIC測定不能株は除いた。 (1)Staphylococcus spp.
S. aureus 24株についてのMPIPCのMICは,5 株は0.25mg/mL以下であり,残る19株 (79.2%)
Fig. 12. 一次性肝・胆道感染の分離菌の推移
は32mg/mL以上であった。ABPCについては,5 株はMICが0.5mg/mL以下であったが,1株は4 mg/mLであり,残る18株は32mg/mL以上であっ た。 総ての株はVCM,TEICおよびLZDには MIC 2mg/mL以下であった。また,ABKでは,1 株 がMIC 8mg/mLで あ っ た が , 残 り はMIC 2 mg/mL以 下 で あ っ た 。GMで は9株 が MIC 1 mg/mL以 下 で あ り , そ の 他 の 株 は 総 てMIC 8 mg/mL以上であった。CLDMには,6株がMIC 0.125mg/mL以下であり,残る18株はMIC 128 mg/mL以上の耐性株であった(Table 7)。
S. epidermidis 22株についてのMPIPCのMIC は,それぞれ1株がMIC 0.125mg/mLと1mg/mL であったが,残る20株は全株4mg/mL以上であっ た。MINOが最も優れた抗菌力を示し,全株MIC が0.25mg/mL以下であった。次いでMIC90でみる とLZD,ABK,VCM,TEIC,LVFX,CZOP, CTMの順に優れていた。一方,CLDMはMICが
0.125mg/mL以下の14株と128mg/mL以上の8株 と明確に抗菌力が分かれていた(Table 8)。
その他のStaphylococcus spp. 7株 (Staphylococ-cus capitisが3株 ,Staphylococcus capraeが2株 とStaphylococcus haemolyticusとStaphylococcus lugdunensisがそれぞれ1株)については,MIC90 でみるとMINOが最も優れ,次いでABK,TEIC, LZD,VCM,LVFXの抗菌力が優れていた(Table 9)。
(2)Streptococcus spp.
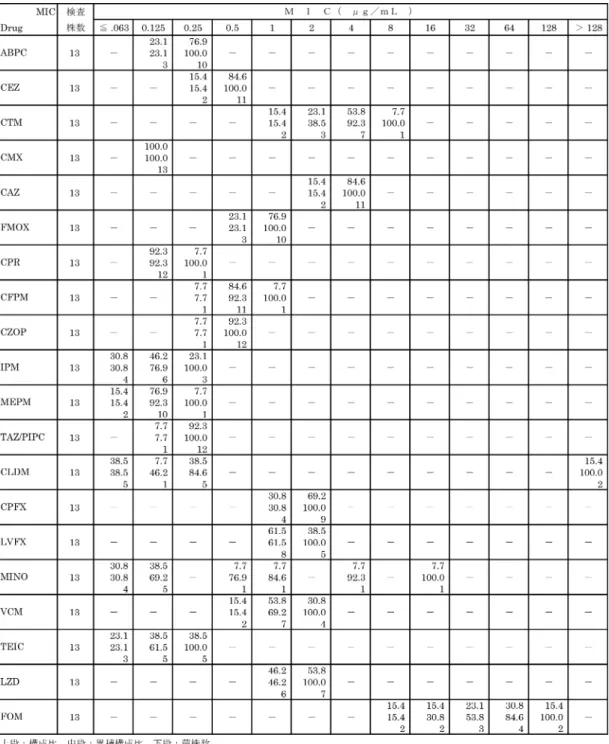
S. anginosusの13株については,CMXのMIC が最も優れ全株0.125mg/mL以下であり,次いで MEPM,IPM,CPR,TEIC,ABPC,TAZ/PIPC
でありMICは全株0.25m g/mL以下であった。
CLDMは2株がMIC 128mg/mL以上であったが,
残りは0.25mg/mL以下であった。FOMには耐性
株が多くみられた(Table 10)。
そ の 他 のStreptococcus spp.の12株 ( Strepto-coccus salivarius 3株 , Streptococcus oralisと Streptococcus mitisの2株,Streptococcus sanguis, Streptococcus parasanguinisとStreptococcus bovis のそれぞれ1株およびその他のStreptococcus spp. 2株)では,TEICの抗菌力が優れ,全株MICが 0.25m g/mL以下であり, 次いでCMX,CPR, IPM,MEPM,CFPM,CZOP,VCM,LZDが 優れていた(Table 11)。 (3)Enterococcus spp. E. faecalisの46株については,TEICの抗菌力 が最も優れており,全株MICは0.5mg/mL以下で あ っ た 。 次 い でABPC,LZD,VCM,IPM, TAZ/PIPCの抗菌力が優れていた(Table 12)。 E. faeciumの15株については,TEICの抗菌力 が最も優れており,全株MIC 0.5mg/mL以下,次 いでVCMは全株MIC 1mg/mL以下,LZDは全株 MIC 2mg/mL以下,MINOは全株MIC 8mg/mL 以下と優れた抗菌力を示した。しかし,その他の 薬剤では耐性株が多くみられた(Table 13)。 E. aviumの12株についても,TEICの抗菌力が 最も優れており,全株MIC 0.5mg/mL以下であ り,次いでVCM,LZD,CPFX,LVFX,MINO の抗菌力が優れていた(Table 14)。 その他のEnterococcus spp. 13株(Enterococcus pseudoaviumの3株 ,Enterococcus gallinarumと Enterococcus raffinosusの 各 2株 ,Enterococcus hiraeとEnterococcus mundtiiの各1株およびその 他のEnterococcus spp. 4株)については,TEIC, LZD,VCM,MINO,LVFX,CPFXの順に抗菌 力が優れていた(Table 15)。
(4)Corynebacterium spp.
Corynebacterium spp. 11株 (Corynebacterium striatum 5株 ,Corynebacterium minutissimumと Corynebacterium argentoratenseのそれぞれ1株お
よびその他のCorynebacterium spp. 4株)につい ては,LZDの抗菌力が最も優れ,次いでTEIC, VCM,MINOであった(Table 16)。
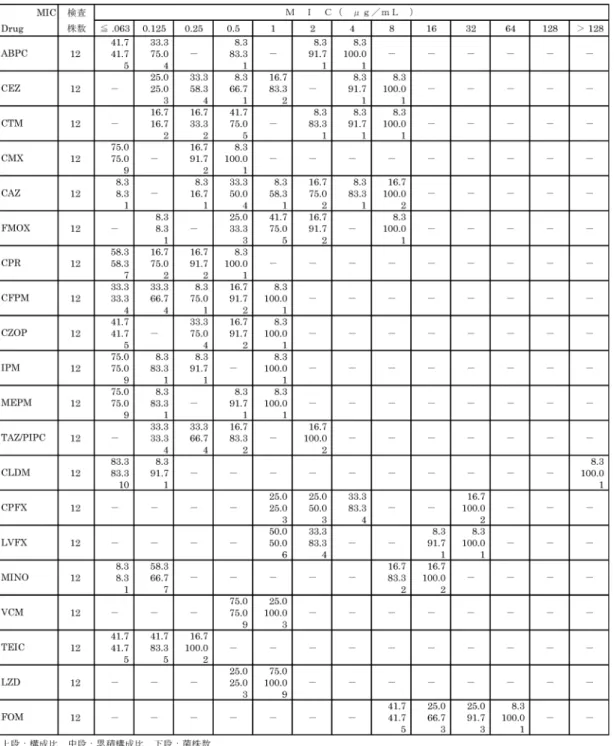
(5)Escherichia coli
E. coliの51株についてMIC90でみると,MEPM の抗菌力が最も優れ,次いでMIC90がいずれも 0 . 1 2 5m g/mLで あ るC F P M,C P R,C Z O P, CMX,FMOX,CRMNで あ り , 続 い て0.25 mg/mLであるIPM,AZT,LMOXなどであった。 一方,MICが128mg/mL 以上の株がABPCで12 株 ,C E Z,C T M,C M X,C P R,C Z O P, TAZ/PIPCが各2株あった。全体として第一世代 より第二世代,第二世代より第三世代セフェム薬 の抗菌力が優れる傾向であった(Table 17)。 (6)Klebsiella spp. K. pneumoniaeの19株については,第三,第四 世代セフェム薬,カルバペネム薬,ニューキノロ ン薬,モノバクタム薬とオキサセフェム薬の抗菌 力が優れていた。ABPCとFOMでは耐性株が多 くみられた(Table 18)。 K. oxytocaの8株については,K. pneumoniaeの 薬剤感受性に類似しているが,CEZ耐性株がみら れた(Table 19)。 (7)Enterobacter cloacae E. cloacaeの13株については,ペニシリン薬と 第一,第二世代セフェム薬,FOM,FMOXで耐 性株も多くみられた。MIC90でみると,MEPMが 0.125mg/mLと最も優れ,次いでCPFX,LVFX, GM,IPM,CFPM,AMK,MINO,CZOP, CPRの順で優れていた(Table 20)。
(8)Citrobacter spp.
Citrobacter spp. 11株(Citrobacter freundii 6株, Citrobacter koseriおよびCitrobacter amalonaticus
の各2株およびCitrobacter braakii 1株)について は,MEPMの抗菌力が最も優れ,次いでCFPM, CPR,CZOP,CRMN,CPFX,LMOXの抗菌力 が優れていた(Table 21)。 (9)Pseudomonas aeruginosa P. aeruginosaの23株 に つ い て , 最 も 小 さ い MIC90を示した薬剤はCPFX,CZOPとLVFXで あり,2mg/mLであった。次いでGMとCAZの4 mg/mLで あ っ た (Table 22)。IPMに MIC 16 mg/mL以上の株が5株(21.7%) あったが,いずれ もAMKおよびCPFXに感受性株であった。また CPFXにMIC 4mg/mL以 上 の 株 が1株 (4.3%) あったが,IPMおよびAMKに感受性株であった。 AMKにMIC 32mg/mL以上の株は認められず,3 薬剤ともに耐性の株(多剤耐性緑膿菌)は認めら れ な か っ た 。 セ フ ェ ム 系 薬 に 対 しMICが64 mg/mL以上の株はみられず,CZOPに対しては全 株MIC 4mg/mL以下と良好な感受性を示した。 (10)Streptococcus constellatus S. constellatusの12株については,IPMの抗菌 力が最も優れ,次いでCLDM,MEPM,TEIC, CMX,CPRの順であり,いずれの薬剤もMICは 0.25mg/mL以下であった(Table 23)。 (11)Gemella morbillorum G. morbillorumの10株 に つ い て は ,FOM, CAZ以外は良好な抗菌力を示した(Table 24)。 (12)Finegoldia magna F. magnaの7株については,TAZ/PIPCの抗菌 力 が 優 れ , 次 い で ,TEIC,MEPM,ABPC, FMOX,VCM,IPMの順であった(Table 25)。
(13)Parvimonas micra P. micraの18株については,CLDMに耐性株が みられたが,その他の薬剤は良好な抗菌力を示し た(Table 26)。 (14)Eggerthella lenta E. lentaの22株については,TEICの抗菌力が最 も優れ,全株MICが0.25mg/mL以下であった。 次いでLZD,MEPM,ABPC,VCM,IPMの順 に抗菌力が優れていた(Table 27)。
(15)Lactobacillus spp.
Lactobacillus spp.の 14株 (Lactobacillus aci-dophilus 5株 ,Lactobacillus casei 4株 , Lacto-bacillus gasseri 3株 お よ びLactobacillus fermen-tumとその他のLactobacillus sp. 各1株)について は,最も優れたMIC90を示したのはABPCであり, 全 株 がMIC 2mg/mL以 下 で あ っ た 。 次 い で , TAZ/PIPC,LZD,MINO,IPMの順に抗菌力が 優れていた(Table 28)。
(16)Bifidobacterium spp.
Bifidobacterium spp.の5株については,MINO, TEIC,ABPC,IPM,MEPM,LZD,VCMの順 に抗菌力が優れていた(Table 29)。
(17)Propionibacterium spp.
Propionibacterium spp.の8株 ( Propionibac-terium acnes 4株,Propionibacterium granulosum 2株,Propionibacterium thoeniiとその他の Propi-onibacterium sp.の各1株)については,IPMの抗 菌 力 が 最 も 優 れ , 次 い でA B P C,M I N O, TAZ/PIPC,MEPM,CMXなどであった (Table 30)。
(18)Clostridium spp.
Clostridium spp.の 19株 ( Clostridium clost-ridioforme 6株 ,Clostridium perfringens 3株 , Clostridium difficileとClostridium symbiosum各2
株,Clostridium bifermentansとClostridium para-putrificumの各1株及びその他のClostridium spp. の4株)については,TEIC,MEPM,LZDでは 総ての株はMIC 2mg/mL以下であり,VCMと FMOXでは4mg/mL以下であり,良好な抗菌力を 示した。ABPC,CTM,CFPM,CZOP,CLDM, LVFX,FOMではわずかながら高度耐性株がみら れた(Table 31)。 (19)Bacteroides spp. B. fragilis 37株 に つ い て MIC90で み る と , TAZ/PIPCが0.5m g/mLと最も優れ, 次いで1 mg/mLのIPM,2mg/mLのMEPM,4mg/mLの MINO,SBT/CPZなどであった(Table 32)。一方, CPR,CFPM,CZOPおよびCLDMに高度耐性株 が多数認められた。 B. thetaiotaomicron 27株についてMIC90でみる と,IPMが1mg/mLと最も優れ,次いで2mg/mL のMEPM,4mg/mLのMINO,8mg/mLのTAZ/ PIPC,SBT/CPZなどであった (Table 33)。一方, CPR,CFPM,CZOPおよびCLDMに高度耐性株 が多数認められた。
B. ovatus 19株 に つ い て MIC90で み る と , MEPMが1mg/mLと最も優れ,次いで2mg/mLの IPM,MINO,4mg/mLのTAZ/PIPC,8mg/mLの SBT/CPZなどであった(Table 34)。一方,CPR, CFPM,CZOPおよびCLDMに高度耐性株が多数 認められた。
Bacteroides uniformis 10株についてMIC90でみ ると,MEPMとIPMが0.5mg/mLと最も優れ,次 いで2mg/mLのMINOとTAZ/PIPC,8mg/mLの SBT/CPZなどであった(Table 35)。一方,CPR, CFPM,CZOPおよびCLDMには高度耐性株が認 められた。 上記のB. fragilis 37株,B. thetaiotaomicron 27 株 ,B. ovatus 19株 ,B. uniformis 10株 に 加 え Bacteroides vulgatus 8株,Bacteroides caccae 8株,
Bacteroides splanchnicus 1株およびその他の Bac-teroides spp. 6株の合計116株について,MIC90で みると,MEPMとIPMが1mg/mLと最も優れ, 次いで4mg/mLのMINO,8mg/mLのTAZ/PIPC とSBT/CPZな ど で あ っ た (Table 36)。 一 方 , CLDMでは,MIC50は1mg/mLと良好であった が ,44株 (37.9%) はMICが128mg/mL以 上 で あった。またCFPM,CZOP,CPRに高度耐性株 が多数認められた。 (20)Bilophila wadsworthia B. wadsworthiaの19株についてMIC90でみる と,MINOが2mg/mLと最も優れ,全株MICは2 mg/mL以下であった。次いでCPFX,LVFXの抗 菌力が優れていたが,中等度耐性株も多くみられ た。CLDMについては,MIC50は0.5mg/mLと優 れていたが,高度耐性株が2株認められた。ペニ シリン系薬,セフェム系薬,カルバペネム系薬に は高度耐性株が多く認められた(Table 37)。 (21)Veillonella spp. 嫌気性グラム陰性球菌であるVeillonella spp.の 8株については,TEIC,VCM,CAZなどを中心 にして全体的に耐性株が多くみられたが,CLDM では全株MICが0.25mg/mL以下であった (Table 38)。 (22)Fusobacterium spp. Fusobacterium nucleatum 12株 に つ い て は , TAZ/PIPC,MEPMの 抗 菌 力 が 優 れ , 次 い で MINO,CLDM,FMOX,IPMなどであった。 CLDMには高度耐性株が1株認められた (Table 39)。
そ の 他 のFusobacterium spp. 10株 ( Fusobac-terium varium 5株,Fusobacterium necrophorum 3 株,その他のFusobacterium spp. 2株)について は,MEPMの抗菌力が最も優れ,総ての株につい
てMICが0.5mg/mL以下であった。次いでMINO, CMX,FMOX,IPM,TAZ/PIPC の抗菌力が優れ ていた(Table 40)。
(23)Prevotella spp.
Prevotella intermedia 10株 に つ い て は , TAZ/PIPC,IPMの抗菌力が優れ,次いでMEPM, SBT/CPZ,LVFX,CPFX,MINOなどであった (Table 41)。
そ の 他 の Prevotella spp.の 17株 (Prevotella melaninogenica 5株 ,Prevotella oris 3株 , Pre-votella denticolaとPrevotella corporisの 各2株 , Prevotella buccae, Prevotella loescheiiと Pre-votella biviaの 各1株 お よ び そ の 他の Prevotella
spp. 2株)については,TAZ/PIPC,MEPMの抗 菌力が優れ,次いでIPM,SBT/CPZ,MINOの抗 菌力が優れていた(Table 42)。
(24)Porphyromonas spp.
Porphyromonas spp. 9株(Porphyromonas asac-charolytica 5株,Porphyromonas gingivalis 1株, Porphyromonas endodontalis 3株 ) に つ い て は , いずれの薬剤も良好な抗菌力を示した(Table 43)。
(25)Parabacteroides distasonis
P. distasonisの11株については,IPM,MEPM, MINOの抗菌力が優れていた。セフェム系薬には 耐性株が多く認められた(Table 44)。
III.
考察
近年,これまで記載のなかった菌種やphylotype が臨床検体からも分離されるとの報告32,33)が増加 している。さらに真正細菌 (Domain Bacteria) ば かりでなく,古細菌 (Domain Archaea)にも医学 的に重要な意味を持つ菌種の存在が明らかとなっ てきている。これまでも指摘してきたように,本 研究においても新しく記載されてきた細菌につい て,培養技術の向上により臨床材料からも分離・ 同定されるようになり,1検体あたりの分離細菌 株数の増加が認められてきた。とりわけここ数年 では著明な増加が認められているが,未知の腸内 細菌の存在からみれば,この傾向はさらに顕著に なると想像することは容易である。 一方,穿孔性腹膜炎の病態は,まさしく穿孔部 より漏れ出した腸内細菌による腹腔内の汚染34)で ある。未知の細菌も含めた細菌毒素ばかりでな く,未知の細菌の代謝産物などによる広範な汚染 である。腸内細菌は下部消化管で菌数が多く,下 部消化管穿孔などでは医学の発達した現在におい ても予後が極めて不良な疾患である。穿孔から手 術までの時間が経過した症例,高齢者,易感染性 要因を有する症例ではとりわけ予後不良35⬃38) で ある。新たな細菌ばかりでなく,未知の細菌も腹 膜炎の重篤化に関連していると想定され,腸内細 菌に対して,研究面でも治療面でも新たな考え方 で対応する必要があることを強調したい。 S. aureus中に占めるMRSAの割合は,ここ数 年では80%前後と高率で留まっている。しかし, VCMをはじめABK,TEICおよびLZDは,鋭い 抗菌力を維持しており,現在までに本研究におい て,これらに耐性の株はみられていない。またコ アグラーゼ陰性ブドウ球菌(CNS) についても,29 株中26株が,メチシリン耐性CNSであったが, これらに対してもVCM,ABK,TEIC,LZDは良 好な抗菌力を示していた。他の薬剤耐性ブドウ球 菌と区別し,注意を喚起させるための呼称として 「MRSA」が使用され,院内感染対策をはじめと して臨床面でも大きな効果があげられてきた。今 後,抗MRSA薬に耐性のMRSAも出現してくる と考えられるが,MRSAに対して有効なb-ラクタ ム薬が臨床使用可能となれば,またほとんどのブ ドウ球菌はペニシリンGに耐性であるような現状 を考えれば,「MRSA」と言うような薬剤耐性ブドウ球菌と区別するような呼び方は不必要となっ てくるであろう。 E. coliについては,1990年代の半ばでCEZに 100mg/mL以上のMICを示した株が10%ほどみ られ11,13⬃15),その後低下傾向となったが,2002 年度26) および2007年度31)に再びCEZ高度耐性 株が増加した。本年度はCEZに対するMICが128 mg/mL以上の株は2株のみであった。Extended
spectrum b-lactamases (ESBLs) 産生菌であるが, 近年増加傾向はなく,抗菌薬の適正使用が効を奏 していると考えられた。 本年度分離のP. aeruginosaについて,IPMに MIC 16mg/mL以上の株が5株(21.7%) あったが, いずれもAMKおよびCPFXに感受性株であった。 IPMへの耐性は,細菌の外膜蛋白であるD2ポー リンの減少など(もともとある遺伝子の変異によ る耐性で低度耐性となるが,高度耐性とはならな い)やプラスミド媒介性のメタロb-ラクタマーゼ の産生能力(高度耐性となる)の獲得である39)。 本年度分離のIPM耐性株はMICが16mg/mLある いは32mg/mLであり,低度耐性株である。すな わち本年度のIPM耐性株は全例が伝達性のプラス ミドにより支配されるものではなく,カルバペネ ム系薬使用によりもともとの遺伝子に変異が生じ た 耐 性 株 と 考 え ら れ た 。 ま たCPFXにMIC 4 mg/mL以上の株が1株 (4.3%) あったが,IPMお よびAMKに感受性株であった。CPFXなどのフ ルオロキノロン薬への耐性獲得には,この系統の 薬剤の標的分子であるDNAジャイレースやトポ イソメラーゼⅣという酵素の変異,および,薬剤 排出機構の機能亢進等が関与しており,染色体上 の遺伝子などの変異によるものである。一方, AMKなどのアミノ配糖体系薬への耐性は,リン 酸化酵素,アセチル化酵素,アデニル化酵素など によるアミノ配糖体の修飾不活化が関与している ものであり,主として伝達性のプラスミドにより 支配されている。このようなメタロb-ラクタマー ゼやアミノ配糖体修飾不活化酵素の産生を支配す る伝達性のプラスミドは,他の菌株や菌種に耐性 遺伝子が伝達,拡散するため,特段の警戒が必要 とされているものである。 本年度においてはAMKにMIC 32mg/mL以上 の耐性株は認められず,3薬剤ともに耐性の株で ある多剤耐性緑膿菌は認められなかった。このよ うな本年度の耐性菌の状況を臨床的に考えると, 伝達性プラスミドが院外から持ち込まれたとして も,院内においてその伝達性プラスミドの拡散な どが効果的な院内感染対策により防げていたと考 えられる。しかし,一方では,IPMを中心とする カルバペネム系薬の偏った使用により遺伝子の変 異が生じIPM低耐性菌株の増加がみられたと想定 される。とりわけCZOPをはじめとするセフェム 系薬に対する感受性が改善していることは,これ らの薬剤も含め抗緑膿菌薬の平均的な使用が必要 であることを物語っていると考えることができる。 嫌 気 性 菌 に つ い て は , 一 部 のLactobacillus spp.,Clostridium spp.およびBacteroides spp.の一 部とB. wadsworthiaは,カルバペネム系薬に耐性 を示す40,41)。また,E. lenta,B. fragilisを中心と
するBacteroides spp.,B. wadsworthia,C. gracilis およびPrevotella spp.などでは,臨床で使用頻度 の高いセフェム系薬に中等度から高度耐性株が多 い。これらはほとんどが好気性菌との混合感染と して認められるものであり,併用療法も考慮しな ければならない。起炎菌判明前に抗嫌気性菌薬と して併用すべき薬剤としてはMINOがあげられる が,多くの嫌気性菌が良好な感受性を示すものと 高度耐性のものの2群に分かれるCLDMについて は, 薬剤感受性を確認して使用する場合には MINOよりも有用であると考えられる。 本調査の全集積期間を通じてVCM耐性の腸球 菌やブドウ球菌などは認められていない。しかし, ESBLs産生E. coliやカルバペネム耐性P. aerugi-nosaが僅かながら認められ,さらにBacteroides
spp.,B. wadsworthiaやPrevotella spp.などのb‐ ラクタム薬耐性の嫌気性菌が認められているので, これらの動向には引き続き注意すべきである。 消化器外科を専門とする外科医においては,術 後の重症感染症にも遭遇することは多い。ここに は新たな細菌,未知の細菌も関与していることは 明白な事実であり,外科医であっても臨床的に腸 内微生物学に興味を持ち対応すべき時期であるこ とを強調したい。
文献
1) 由良二郎,品川長夫,石川 周,他:外科感 染症分離菌及び感受性調査(第1報)。Jpn. J. Antibiotics 39: 2557⬃2578, 1986 2) 由良二郎,品川長夫,石川 周,他:外科感 染症分離菌の様相と薬剤感受性の動向(第2 報)。Jpn. J. Antibiotics 41: 361⬃389, 1988 3) 品川長夫,由良二郎,石川 周,他:穿孔性 腹膜炎よりの分離菌とその薬剤感受性。日本 化学療法学会雑誌37: 731⬃743, 1989 4) 品川長夫,由良二郎,石川 周,他:外科感 染症分離菌とその薬剤感受性—特にメチシリ ン耐性黄色ブドウ球菌(MRSA) について—。 日本外科感染症研究2: 232⬃240, 1990 5) 品川長夫,由良二郎,石川 周,他:外科感 染症分離の嫌気性菌について。日本外科感染 症研究3: 103⬃108, 1991 6) 真下啓二,品川長夫,由良二郎,他:外科感 染症分離の緑膿菌とその薬剤感受性。日本外 科感染症研究4: 43⬃49, 1992 7) 真下啓二,品川長夫,由良二郎,他:術後感 染より分離したMRSAについて。日本外科感 染症研究5: 105⬃111, 1993 8) 品川長夫,由良二郎,石川 周,他:消化器 外科術後感染分離菌とその薬剤感受性の変 遷。Jpn. J. Antibiotics 47: 493⬃501, 1994 9) 品川長夫,水野 章,真下啓二,他:急性化 膿性腹膜炎よりの分離菌とその薬剤感受性に ついて。Jpn. J. Antibiotics 47: 1329⬃1343, 1994 10) 品川長夫,水野 章,真下啓二,他:外科感 染症分離の嫌気性菌について。日本嫌気性菌 感染症研究24: 40⬃45, 1995 11) 品川長夫,由良二郎,真辺忠夫,他:外科感 染症におけるEscherichia coliの分離頻度と 薬 剤 感 受 性 の 変 遷 。Jpn. J. Antibiotics 49: 456⬃464, 1996 12) 品川長夫,平田公一,傳野隆一,他:外科感 染症におけるPseudomonas aeruginosaの分 離頻度と薬剤感受性の変遷。Jpn. J. Antibi-otics 49: 544⬃554, 1996 13) 品川長夫,由良二郎,真辺忠夫,他:外科感 染症分離菌とその薬剤感受性—1994年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 49: 849⬃891, 1996 14) 品川長夫,小出 肇,平田公一,他:外科感 染症分離菌とその薬剤感受性—1995年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 50: 143⬃177, 1997 15) 真下啓二,品川長夫,平田公一,他:外科感 染症分離菌とその薬剤感受性—1996年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 52: 398⬃430, 1999 16) 品川長夫,真下啓二,山本俊信,他:外科感 染症分離のBacteroides fragilis groupとその 薬剤感受性。日本嫌気性菌感染症研究 28: 48⬃54, 1998 17) 品川長夫,真下啓二,山本俊信,他:外科感 染症分離の嫌気性菌とその薬剤感受性。日本 嫌気性菌感染症研究29: 104⬃111, 1999 18) 真下啓二,品川長夫,山本俊信,他:外科領 域感染症から分離された嫌気性菌の薬剤耐性 菌 の 動 向 。 日 本 嫌 気 性 菌 感 染 症 研 究3 0 : 36⬃43, 2000 19) 品川長夫,真下啓二,山本俊信,他:外科感 染症から分離された嫌気性菌の動向。日本嫌 気性菌感染症研究30: 141⬃147, 2000 20) 真下啓二,品川長夫,平田公一,他:外科感 染症分離菌とその薬剤感受性—1997年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 53: 533⬃565, 2000 21) 真下啓二,品川長夫,平田公一,他:外科感 染症分離菌とその薬剤感受性—1998年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 54: 497⬃531, 2001 22) 品川長夫,真下啓二,真辺忠夫,他:外科領 域感染症分離の嫌気性菌とその薬剤感受性。 日本嫌気性菌感染症研究32: 94⬃102, 200223) 真下啓二,品川長夫,平田公一,他:外科感 染症分離菌とその薬剤感受性—1999年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 55: 697⬃729, 2002 24) 品川長夫,平田公一,向谷充宏,他:外科感 染症分離菌とその薬剤感受性—2000年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 55: 730⬃763, 2002 25) 品川長夫,平田公一,桂巻 正,他:外科感 染症分離菌とその薬剤感受性—2001年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 56: 105⬃137, 2003 26) 品川長夫,平田公一,桂巻 正,他:外科感 染症分離菌とその薬剤感受性—2002年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 57: 33⬃69, 2004 27) 品川長夫,平田公一,桂巻 正,他:外科感 染症分離菌とその薬剤感受性—2003年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 58: 123⬃158, 2005 28) 品川長夫,平田公一,桂巻 正,他:外科感 染症分離菌とその薬剤感受性—2004年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 59: 72⬃116, 2006 29) 品川長夫,平田公一,桂巻 正,他:外科感 染症分離菌とその薬剤感受性—2005年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 60: 52⬃97, 2007 30) 品川長夫,平田公一,桂巻 正,他:外科感 染症分離菌とその薬剤感受性—2006年度分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 61: 122⬃171, 2008 31) 品川長夫,長谷川正光,平田公一,他:外科 感染症分離菌とその薬剤感受性—2007年度 分 離 菌 を 中 心 に—。Jpn. J. Antibiotics 62: 277⬃338, 2009
32) HEBB, J. K.; C. R. COHEN, S. G. ASTETE, et al.:
Detection of novel organisms associated with salpingitis, by use of 16S rDNA polymerase chain reaction. J. Infect. Dis. 190: 2109⬃ 2120, 2004
33) SIQUEIRA, J. F.; I. N. ROCAS, C. D. CUHA, et al.:
Novel bacterial phylotypes in endodontic in-fections. J. Dent. Res. 84: 565⬃569, 2005 34) 品川長夫,田中香お里,三鴨廣繁,他:穿孔 性腹膜炎からの分離菌とその薬剤感受性。 Jpn. J. Antibiotics 60: 206⬃220, 2007 35) 寺本健一,中村 豊,菱山豊平,他:大腸穿 孔症例の臨床的検討―術後死亡に関わる要因 に つ い て ― 。 日 本 臨 床 外 科 学 会 雑 誌6 2 : 1121⬃1128, 2001 36) 岩谷 昭,谷 達夫,飯合恒夫,他:大腸穿 孔症例の臨床的検討。日本外科感染症学会雑 誌3: 101⬃105, 2006 37) 斉藤人志,黒田雅利,松澤 研,他:大腸穿 孔に起因したSIRS症例に対するPMX-DHP の有用性と限界。日本外科感染症学会雑誌 3: 93⬃100, 2006 38) 加藤高明:消化器外科領域の周術期感染症。 日本臨床腸内微生物学会誌8: 26⬃30, 2006 39) 柴田尚宏,荒川宜親:MDRPの耐性機構。 臨床と微生物34: 83⬃86, 2007 40) 品川長夫,由良二郎,竹山廣光,他:外科感 染症分離のClostridium spp.とその薬剤感受 性。Jpn. J. Antibiotics 60: 171⬃180, 2007 41) 品川長夫,由良二郎,竹山廣光,他:外科感 染 症 分 離 のBilophila wadsworthia。Jpn. J. Antibiotics 59: 452⬃458, 2006