―技術報告―
イオントラップ型質量分析計を用いた 3カルボニルN(フルオロペンチル)
インドール骨格を有する危険ドラッグの位置異性体識別
春田祐輔
1,森田
敦
1,大槻光彦
1,中園陽子
2,
中山秀幸
2,八ヶ代一郎
2,内川貴志
1 1佐賀県警察本部刑事部科学捜査研究所 〒8408540 佐賀県佐賀市松原 1116 2佐賀県衛生薬業センター 〒8490925 佐賀県佐賀市八丁畷町 120Positional isomer diŠerentiation of designer drugs with 3carbonyl
N
‰uoropentylindole using ion trap mass spectrometry
Yusuke Haruta
1, Atsushi Morita
1, Mitsuhiko Ohtsuki
1, Yoko Nakazono
2,
Hideyuki Nakayama
2, Ichiro Yakashiro
2and Takashi Uchikawa
11
Forensic Science Laboratory, Saga Prefectural Police H.Q.
1
116, Matsubara, Saga 840
8540, Japan
2
Saga Prefectural Institute of Public Health and Pharmaceutical Research
120, Hatchonawate-machi, Saga 8400925, Japan
(Received 14 October 2016; accepted 16 December 2016
Published online 14 February 2017 in J
STAGE
DOI: 10.3408/jafst.724)
Several synthetic cannabinoids such as AM2201 contain the 3carbonylN
‰uoropentylindole structure. This structure has ‰uorine positional isomers on the
alkyl chain. In most cases, legal controls are placed only on the 5‰uoro analogue.
Thus, diŠerentiation of isomers is a signiˆcant issue in forensic science. In this
study, we developed a method for the diŠerentiation of positional isomers of
3car-bonylN‰uoropentylindole derivatives utilizing multiple-stage mass spectrometry
using an ion trap tandem mass spectrometer. In addition, the analogues whose
‰uo-rine atom was replaced with a chlo‰uo-rine atom or hydroxyl group were also examined.
With respect to each positional isomer of ‰uorine and chlorine, the ion at m/z
232 or m/z 248, obtained by MS
2analysis of [M+H]
+, were selected as the
precur-sor ions for MS
3analysis. The ion at m/z 232 and m/z 248 corresponded to the 3
carbonylN‰uoropentylindole and 3carbonylNchloropentylindole structures.
Furthermore, the ion at m/z 212, corresponding to the de-halogenated fragments of
the
3carbonylN‰uoropentylindole and
3carbonylNchloropentylindole-structures, was selected as the precursor ion for MS
4analysis. Consequently,
With respect to positional isomers with the hydroxyl group, however, the
frag-ment ion at m/z 212 was not observed from the MS
3analysis of m/z 230, which
cor-responds to the 3carbonylN‰uoropentylindole structure. Therefore,
diŠerentia-tion of each posidiŠerentia-tional isomer was not achieved by MS
nanalysis.
This method is useful for the diŠerentiation of positional isomers of 3carbonyl
N
‰uoropentylindole and 3carbonylNchloropentylindole derivatives.
Key words: 3carbonylN‰uoropentylindole, Positional isomer, Designer
drug, Ion trap mass spectrometer
緒
言
近年,様々な種類のデザイナードラッグの国内で の蔓延が社会問題となっており,これらの薬物が 「医薬品,医療機器等の品質,有効性及び安全性の 確保等に関する法律(旧薬事法)」や「麻薬及び向 精神薬取締法」において次々に規制されている13). このような薬物は,各種法律により規制される構造 が厳密に規定されているため,位置異性体のような 構造のわずかな違いにより規制する法律が異なるこ ともあれば,全く規制を受けないこともある.その ため違法薬物を分析する上で,異性体識別を行うこ とは法科学上大変重要である46). 一般に位置異性体を識別するためには,核磁気共 鳴分光法(NMR)や赤外分光分析(IR),ガスク ロマトグラフィー(GC)による保持時間の差違に より判断を行うなどの手法が考えられる.しかしな がら,NMR や IR を行うためには物質の単離・精 製が必要であり,微量分析も困難である.また IR や GC では各異性体の標準品を入手し分析する必要 があるが,そのすべてを入手することは大変困難で ある.質量分析を用いたデザイナードラッグの位置 異 性 体識 別に 関 する 研究 は いく つか 報 告が ある が410),シングルステージの質量分析計では,異性 体によっては質量スペクトルに差違が認められない か,あってもわずかであり4,5,7,8),GC による保持 時間情報と併せて判断することで識別を可能として いる.トリプル四重極型のタンデム質量分析計を用 いたものでは,MS2分析を行うことで位置異性体 識別の向上が認められていることから6,9,10),MS3 以上の多段分析が可能なイオントラップ型の質量分 析計を用いることでさらなる識別能力の向上が期待 されるが,そのような報告は見当たらない. 乱用されている薬物の中には[1(5Fluoropen-tyl) 1H indol 3 yl ] 1 naphthalenylmethanone (AM2201)のような 3カルボニルN(5フルオ ロペンチル)インドール骨格を持つ合成カンナビノ イド系薬物がみられる3,11,12).3カルボニルN(5 フルオロペンチル)インドール骨格にはペンチル基 上のフッ素の位置異性が存在するが,この位置異性 体の識別に関する報告は見当たらない.本研究で は,3カルボニルN(フルオロペンチル)インドー ル 骨 格 を 持 つ 麻 薬 で あ る AM 2201, [ 1 ( 5 Fluoropentyl ) 1H indol 3 yl ] ( 4 methyl 1
naphthalenyl) methanone (MAM2201), [1(5
Fluoropentyl)1Hindol3yl] (2,2,3,3
tetramethyl-cyclopropyl) methanone (XLR11)および 1(5
Fluoropentyl)1Hindole3carboxylic acid 8
quinolinyl ester (5FQUPIC)(Fig. 1ad)について,
多段階の MSn分析が可能なイオントラップ型質量 分析計を用い,3カルボニルN(フルオロペンチ ル)インドール骨格のペンチル基上のフッ素位置異 性体の識別について検討を行った.また,これらの 化合物以外に,3カルボニルN(フルオロペンチ ル)インドール骨格のフッ素原子が塩素原子に置換 した骨格を持つ[1(5Chloropentyl)1Hindol3
yl] (2,2,3,3tetramethylcyclopropyl) methanone
(UR144 5Cl analog)(Fig. 1e)や,水酸基に置換
した骨格を持つ[1(5Hydroxypentyl)1Hindol
3yl]1naphthalenylmethanone (JWH018 5OH
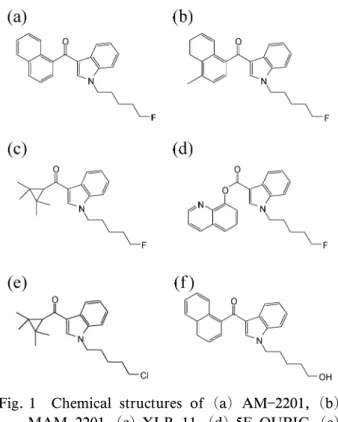
Fig. 1 Chemical structures of (a) AM2201, (b)
MAM2201, (c) XLR11, (d) 5FQUPIC, (e)
UR144 5Cl analog, (f) JWH018 5OH metabo-lite.
材料および方法
. 試薬
AM2201, MAM2201, XLR11, 5FQUPIC,
UR144 5Cl analog および JWH018 5OH
metabo-liteならびにこれらの化合物のペンチル基上のフッ 素,塩素または水酸基の 2~4 位の位置異性体の各 標準試薬はいずれも Cayman Chemical 社より購入 した.メタノールは和光純薬工業製の LC/MS グ レードのものを,1 mol/L 酢酸アンモニウム溶液は 和 光純 薬 工業 製 の HPLC グ レ ー ドの も のを 用 い た.各標準試薬はいずれもメタノール溶液とし,2 ppm に調製した. . 質量分析 装置は Thermo Fisher 製リニアイオントラップ型 LXQ 質量分析計を用いて,以下の測定条件で分析 を行った.イオン化法エレクトロスプレーイオン 化(ESI)ポジティブ,キャピラリー温度275°C, キャピラリー電圧29 V,ソース電圧5.0 kV,チ ューブレンズ電圧105 V,MSn分析の際の
Isola-tion width2, Normalized Collision Energy35, Wideband ActivationoŠ,試料導入液体クロマ トグラフ(島津製作所製 UFLC Prominence)を用 い,カラムは化学物質評価研究機構製 Lcolumn 2 ODS(内径1.5 mm×150 mm,粒子径 5 mm)を, 移動相は 5メタノール-10 mM 酢酸アンモニウ ム溶液と95メタノール-10 mM 酢酸アンモニウ ム溶液のリニアグラジエント,流速0.2 mL/min, 注入量 2 mL とした.なお,本研究では質量スペク トルのみを検討対象とし,ピークの保持時間は検討 の対象としなかった.
結果および考察
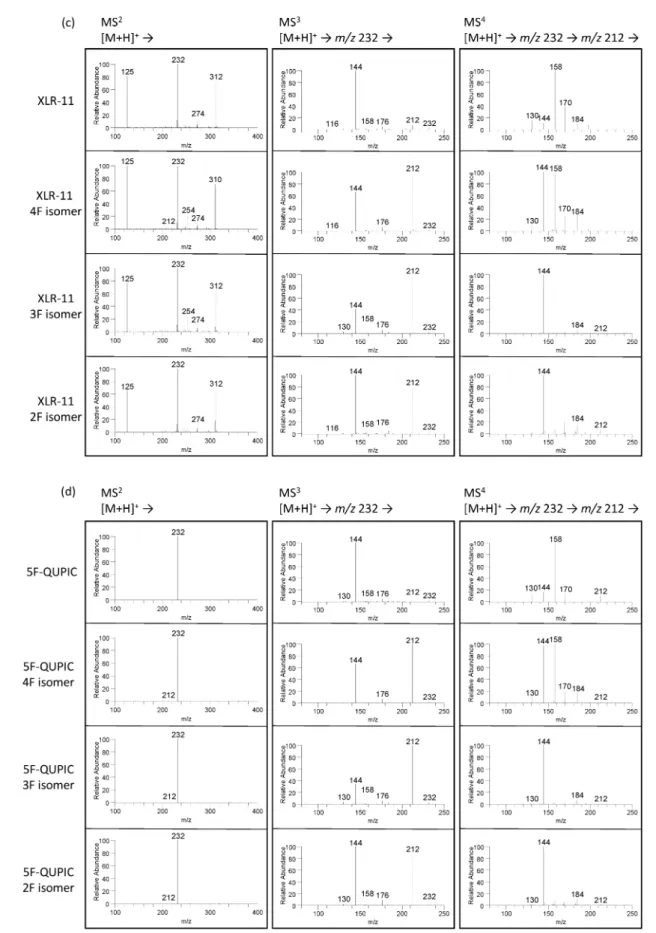
. フッ素異性体の位置異性識別AM2201, MAM2201, XLR11, 5FQUPICおよ
びこれらのフッ素位置異性体について,各化合物の プロ トン 付 加分 子 をプ リカ ー サー イオ ン とし た MS2分析を行ったところ,いずれの化合物からも 3 カルボニルN(フルオロペンチル)インドール骨 格に由来する m/z 232が共通して観察されたため, これをプリカーサーイオンとしてさらに MS3分析 を行った.その結果,ペンチル基の 5 位にフッ素が あ る AM 2201, MAM 2201, XLR 11 お よ び 5F QUPIC では強く観察されたフラグメントイオンは m/z 144のみであったが,他の異性体については m/z 144のほかに m/z 212が強く観察された.この とき 4 位または 3 位にフッ素がある場合,m/z 212, m/z 144の順に,2 位にフッ素が ある場合,m /z 144,m/z 212の順に強度が強く,異性体によってそ の比が異なっていることから,各位置異性体識別の 判断の一助となると考えられた.ここで観察された m/z 212は 3カルボニルN(フルオロペンチル) インドールから HF 分子が脱離したものと考えられ たため,さらにこれをターゲットとして MS4分析 を行ったところ,ペンチル基の 5 位にフッ素がある 場合には m/z 144以上に m/z 158が強く観察され, 4 位にフッ素がある場合にはm/z 144と m/z 158が 共に強く観察されたが,ペンチル基の 3 位または 2 位にフッ素がある場合では強く観察されたフラグメ ントイオンは m/z 144のみであった(Fig. 2).これ ら MS3および MS4分析の結果を合わせて判断する
Fig. 2 Product ion spectra of (a) AM2201, (b) MAM2201, (c) XLR11, (d) 5FQUPIC and their positional isomers obtained by the ion trap mass spectrometer.
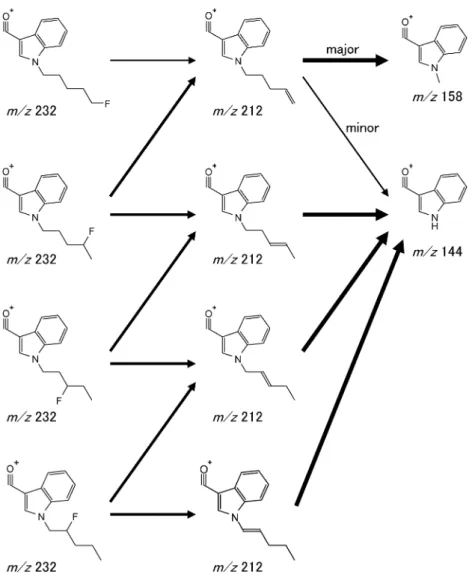
Fig. 3 Probable fragmentation pathway of 3carbonylN‰uoropentyl-indole type of synthetic cannabinoids. ことにより,各位置異性体の識別が可能と考えられ た.MS2分析の結果のみでは各位置異性体を識別 することは極めて困難であるが,イオントラップ型 質量分析計を用いた MS3分析さらには MS4分析を 行うことで,位置異性体識別能力の向上が可能とな った. なお,MS3分析における差異は,フッ素の結合 位置によって HF 分子の脱離の起こりやすさに違い があると考えられた.また MS3分析で HF 分子の 脱離により生じたペンテニル基は異性体間で二重結 合の位置が異なるが,MS4分析における差異は, この二重結合の位置の違いにより生じたと考えられ た.すなわち,HF 分子が 4ペンテニルの形に脱離 した場合に m/z 158のフラグメントが生成しやす く,それ以外の場合では m/z 144のフラグメントが 生成しやすいと考えられた(Fig. 3). 本分析手法は,いわゆるハーブといわれる危険ド ラッグのような夾雑が多い資料であっても,液体ク ロマトグラフ(LC)での分離に加え MSn分析時の 質量分離により異性体識別は可能であるが,同じ化 合物の位置異性体が混在している場合は MSn分析 時の質量分離が出来ないため,LC で十分な分離を 行うことで本手法の適用が可能と考えられる. また,本分析手法では,対象化合物のインドール 骨格のカルボニル基にどのような置換基が結合して いても,プロトン付加分子をプリカーサーイオンと した MS2分析により 3カルボニルN(フルオロペ ンチル)インドール骨格に由来するフラグメントイ
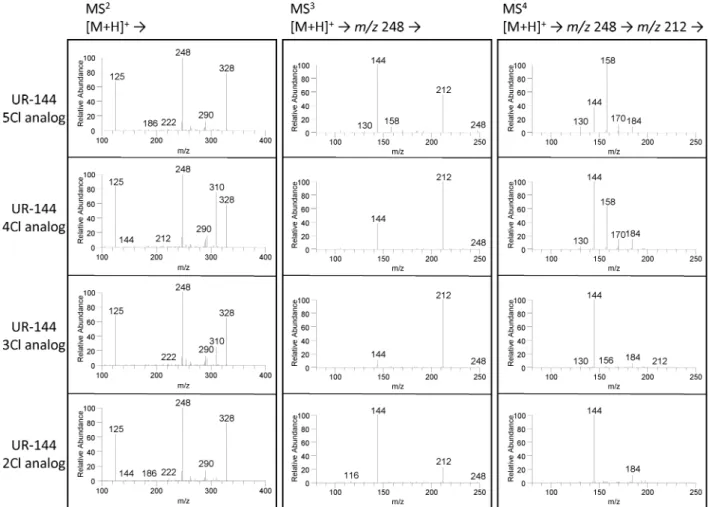
Fig. 4 Product ion spectra of UR144 5Cl analog and its positional isomers obtained by the ion trap mass spec-trometer. オンである m/z 232が確認されれば,これをターゲ ットとして MS3および MS4分析をすることによっ て,各種位置異性体を識別することが可能である. これにより,カルボニル基に結合した置換基を変化 させたような新規のデザイナードラッグであって も,そのフッ素位置異性体の各標準品の入手や分析 を必要とせずに,位置異性体を識別することが可能 となると考えられる. . 塩素異性体の位置異性識別 UR144 5Cl analog およびその塩素位置異性体に ついて,各化合物のプロトン付加分子をプリカー サーイオンとした MS2分析を行ったところ,いず れの化合物からも 3カルボニルN(クロロペンチ ル)インドール骨格に由来する m/z 248が観察され たため,これをプリカーサイオンとしてさらに MS3分析を行った.その結果,ペンチル基の 5 位 および 2 位に塩素がある場合は m/z 144, m/z 212の 順に強く観察され,4 位に塩素がある場合は m/z 212,m/z 144の順に強く観察された.また,3 位に 塩素がある場合は,m/z 212のみが強く観察され m/z 144はわずかに観察されるのみであった.ここ で観察された m/z 212は 3カルボニルN(クロロ ペンチル)インドールから HCl 分子が脱離したも のと考えられたため,さらにこれをターゲットとし て MS4分析を行ったところ,ペンチル基の 5 位ま たは 4 位に塩素がある場合には m/z 144の他に m/z 158が強く観察された.一方,ペンチル基の 3 位ま たは 2 位に塩素がある場合では m/z 144のみが強く 観察された(Fig. 4).これら MS3および MS4分析 の結果を合わせて判断することにより,各位置異性 体の識別が可能と考えられた. この結果を AM2201などのフッ素位置異性体と
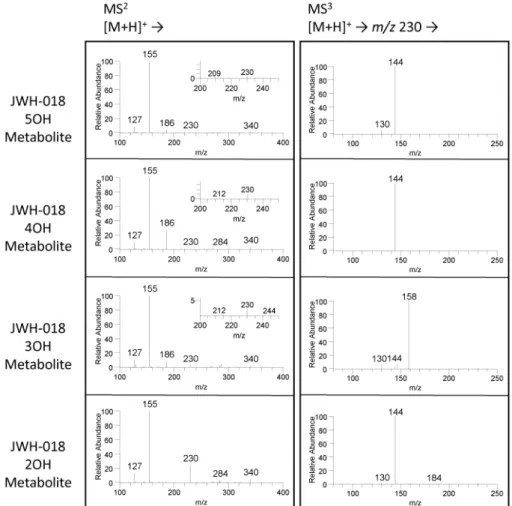
Fig. 5 Product ion spectra of JWH018 5OH metabolite and its positional isomers obtained by the ion trap mass spectrometer. 比較すると,HF 分子と HCl 分子の脱離のしやす さに多少の違いがあると考えられるが,MS3分析 では類似した傾向の質量スペクトルを,また MS4 分析では極めて類似した質量スペクトルを示した. . 水酸基異性体の位置異性識別 JWH018 5OH metabolite およびその水酸基位置 異性体について,各化合物のプロトン付加分子をプ リ カーサ ーイオ ンとし た MS2分析 を行っ たとこ ろ,3カルボニルN(ヒドロキシペンチル)イン ドール骨格に由来する m/z 230が強度は弱いながら も観察されたため,これをプリカーサイオンとし て MS3分析を行った.その結果,ペンチル基の 3 位に水酸基がある場合は m/z 158が,他の異性体で は m/z 144が強く観察されるのみであり,フッ素異 性体および塩素異性体で MS4分析のターゲットと した m/z 212は観察されなかったため,水酸基異性 体では MS4分析を行うことができなかった(Fig. 5).このとき,2 mL の注入量を10 mL まで増やして も 結 果 に 差 異 は 認 め ら れ な か っ た . MS2分 析 と MS3分析の結果を合わせて判断することにより各 位置異性体の識別は可能と考えられたが,対象骨格 に由来するフラグメントイオンをターゲットとした MS3および MS4分析による異性体識別は困難であ った.
結
語
3カルボニルNペンチルインドール骨格を有す る化合物において,ペンチル基の 2~5 位の水素の いずれか一つが,フッ素,塩素または水酸基に置換 した各種位置異性体をイオントラップ型質量分析計 で分析し,その識別の検討を行った.その結果,フ ッ素もしくは塩素の位置異性体については,プロトン付加分子に対する MS2分析により当該骨格に由 来するフラグメントイオン(フッ素異性体の場合 m/z 232,塩素異性体の場合 m/z 248)が確認され れば,これをターゲットとして MS3および MS4分 析をすることによって,各位置異性体を識別するこ とが可能であった.しかしながら,水酸基の位置異 性体については,当該骨格に由来するフラグメント イオン(m/z 230)をターゲットとしても MS3分析 までしか出来ず,その結果から異性体識別を行うこ とは困難であった. 本手法は,インドール骨格のカルボニル基に結合 する置換基にかかわらず,ペンチル基上のフッ素お よび塩素の位置異性を識別できることから,構造の 一部を変化させた新規のデザイナードラッグに対し ても,各異性体の標準品を用いることなく位置異性 体識別が可能と考えられ,3カルボニルNペンチ ルインドール骨格のペンチル基上のフッ素および塩 素の位置異性体の識別法として,大変有用であると 考えられる.
文
献
1) 厚生労働省医薬食品局監視指導・麻薬対策 課,薬物乱用の現状と対策.厚生労働省,東 京,2014. 2) 警察庁刑事局組織犯罪対策部薬物銃器対策 課,平成26年上半期の危険ドラッグに係る検挙 状況について(暫定値).警察庁,東京,2014. 3) 花尻(木倉)瑠理,内山奈穂子,河村麻衣子, 緒方潤,合田幸広,違法ドラッグを取り巻く国 内外における現状と規制について.Yakugaku Zasshi, 133, 3140, 2013. 4) 根岸祥子,中園裕紀子,神田康司,辻川健 治,桑山健次,金森達之,岩田祐子,宮元和 奈,糟谷史代,井上博之,GC/MS によるメチ ルアンフェタミン類の位置異性体識別.日本法 科学技術学会誌,19, 111119, 2014.5) Nakazono Y., Tsujikawa K., Kuwayama K.,
Kanamori T., Iwata Y., Miyamoto K., Kasuya F. and Inoue H., DiŠerentiation of regioisomeric ‰uoroamphetamine analogs by gas graphy-mass spectrometry and liquid
chromato-graphy-tandem mass spectrometry.Forensic Tox-icol., 31, 241250, 2013.
6) Kusano M., Yamanaka M., Zaitsu K.,
Nakayama H., Nakajima J., Moriyasu T., Tsuchihashi H. and Ishii A., Regioisomeric diŠerentiation of the alkyl-substituted synthetic
cannabinoids JWH122 and JWH210 by GC
EIMS/MS. Forensic Toxicol., 34, 304315,
2016.
7) Zaitsu K., Katagi M., Kamata H., Kamata T., Shima N. Miki A., Iwamura T. and Tsuchihashi H., Discrimination and identiˆcation of the six aromatic positional isomers of trimethoxyam-phetamine (TMA) by gas chromatography-mass spectrometry(GCMS). J. Mass Spectrom., 43, 528534, 2008.
8) Harris D.N., Hokanson S., Miller V. and
Jackson G.P., Fragmentation diŠerences in the EI spectra of three synthetic cannabinoid positional
isomers: JWH250, JWH302, and JWH201.
Int. J. Mass Spectrom., 368, 2329, 2014.
9) Zaitsu K., Miyagawa H., Sakamoto Y.,
Matsuta S., Tsuboi K., Nishioka H., Katagi M., Sato T., Tatsuno M., Tsuchihashi H., Suzuki K. and Ishii A., Mass spectrometric diŠerentiation of the isomers of mono-methoxyethylamphetamines
and mono-methoxydimethylamphetamines by
GCEIMSMS.Forensic Toxicol., 31, 292300, 2013.
10) Kusano M., Zaitsu K., Nakayama H.,
Nakajima J., Hisatsune K., Moriyasu T., Matsuta S., Katagi M., Tsuchihashi H. and Ishii A., Posi-tional isomer diŠerentiation of synthetic
cannabi-noid JWH081 by GCMS/MS. J. Mass
Spec-trom., 50, 586591, 2015.
11) Kikura-Hanajiri R., Uchiyama N., Kawamura
M. and Goda Y., Changes in the prevalence of new psychoactive substances before and after the introduction of the generic scheduling of synthetic cannabinoids in Japan.Drug Test. Anal., 6, 832 839, 2014.
12) Uchiyama N., Matsuda S., Kawamura M., Shimokawa Y., Kikura-Hanajiri R., Aritake K., Urade Y. and Goda Y., Characterization of four new designer drugs, 5chloroNNEI, NNEI
inda-zole analog,aPHPP andaPOP, with 11 newly distributed designer drugs in illegal products. Forensic Sci. Int., 243, 113, 2014.