はじめに 早期直腸癌に対して行われる治療法は,低侵襲 な内視鏡的切除や局所切除からリンパ節郭清を伴 う腸切除までさまざまである.経肛門的内視鏡下 マイクロサージェリー(Transanal endoscopic microsurgery:以下,TEM)はBuessら1)が提唱 して以来,現在までに全世界で用いられている経 肛門的局所切除術式である.しかし,TEMは高価 で複雑な専用器具や鉗子を用い,手技の複雑さの ため広く普及していないのが現状である2)3). 今回,われわれは,経肛門的低侵襲手術(Trans-anal Minimally Invasive Surgery:以下,TAMIS) を目的に開発されたGelPOINT® Path(Applied Medical社)を肛門管に装着し,下部直腸癌に対し て経肛門的低侵襲手術を行ったので報告する. 受付:2015年6月29日,採用:2015年7月27日 連絡先 能浦真吾 〒591-8025 大阪府堺市北区長曽根町1179-3 大阪労災病院外科 対象および手術手技 1 . 対象 腫瘍最大径3cm以下で腹膜反転部より肛門側に 存在し,内視鏡的治療が困難な症例とする.悪性 疾患の場合は,術前の画像診断で明らかなリンパ 節転移や遠隔転移を認めない症例とする. 大腸癌の場合は,深達度に応じて標準的な治療 法が大腸癌ガイドライン4)に記載されている.Tis, T1aは本術式の最も良い適応である.T1bは追加 切除を考慮する,T2ではリンパ節郭清を伴う腸切 除が標準とされている.T1b,T2が疑われる症例 では基本的には本術式の適応ではない.しかし, 全身状態不良例で標準手術は耐術不可能と判断さ れた症例あるいは標準手術を拒否された症例では 適応となる. 患者さんへのインフォームドコンセントに関し ては,十分な配慮が必要で,特に大腸癌の場合は, 全身状態を考慮して,大腸癌治療ガイドラインに 従った説明を心がければならない. 2 . 手術手技 術前の前処置は,通常の大腸手術と同様に経口 腸管洗浄剤による十分な機械的前処置を行う.ま 内容要旨 目的:GelPOINT® Path(Applied Medical社)を肛門管に装着し,下部直腸癌に対して経肛門的低 侵襲手術を2例経験した. 方法:全身麻酔下にGelPOINT® Pathを肛門管に装着し,LigaSureTM Vにて腫瘍を一括全層切除し, 十分に洗浄後に欠損部は開放創のままとした. 結果:手術時間は69分~110分,出血量は少量で,術後入院日数は7日であった.術後9~12カ月 経過しているが局所再発および遠隔転移は認めておらず,肛門機能に問題は認めていない. 結語:症例を集積し,長期のフォローアップが必要であるが,GelPOINT® Pathを用いた経肛門的 低侵襲手術は有用な手術手技である. 索引用語:直腸癌,経肛門的低侵襲手術,GelPOINT® Path
手技・機器の開発
GelPOINT® Pathを用いた経肛門的低侵襲手術の経験
大阪府立成人病センター消化器外科1),大阪労災病院外科2)能浦 真吾
1)2)大植 雅之
1)三吉 範克
1)Fig. 1 GelPOINT® Path. a-d : The GelPOINT® Path is inserted though the anus. Three accessory ports are at-tached to the GelPOINT® Path and the usual laparoscopic instruments are used. a b c d た,第2世代セフェム系抗生剤を術当日と翌日に 投与している. GelPOINT® Pathは3点から構成されている. GelSeal®キャップは柔軟な材質から出来ている (Fig. 1a ).付属のポートは5mmから10mmの器 具に対応可能である(Fig. 1b ).アクセスチャン ネルは4cmの径があり,優れた術野とアクセスが 可能である(Fig. 1c ).付属のポート3本をGelSeal® キャップに挿入し,GelSeal®キャップとアクセス チャンネルと合体させる(Fig. 1d ).全身麻酔下 に病変の位置に応じてJackknife positionもしくは 砕石位で体位を固定し,手術は術者とカメラ助手 の2名で行う.直腸鉤を用いて愛護的に肛門管を 拡張し,GelPOINT® Pathのアクセスチャンネル を肛門管に装着し絹糸にて固定する(Fig. 2a ). GelSeal®キャップの柔軟な支点により,容易なト ライアンギュレーションが可能である(Fig. 2b ). 炭酸ガスで送気を行い,送気圧は10mmHg,流 量は10L/minである.専用の器具は必要とせず, 通常の腹腔鏡下手術に使用しているフレキシブル スコープ,鉗子,超音波凝固切開装置などを用い て手術を施行する.生理食塩水で湿らせた手術用 ガーゼを直腸口側へ挿入し,口側腸管への炭酸ガ スの流入を抑える(Fig. 3a ).最初に,電気メス にて腫瘍から1cmのマージンを確保するため切離 予定線のマーキングを行う(Fig. 3b ).病変の深 達度に応じて剝離層を決定するが,悪性でcT1あ るいはT2と診断した場合は一括全層切除を基本と している.剝離は画面右側より開始し,腫瘍が露 出しないよう適切な層で行う(Fig. 3c ).当科で
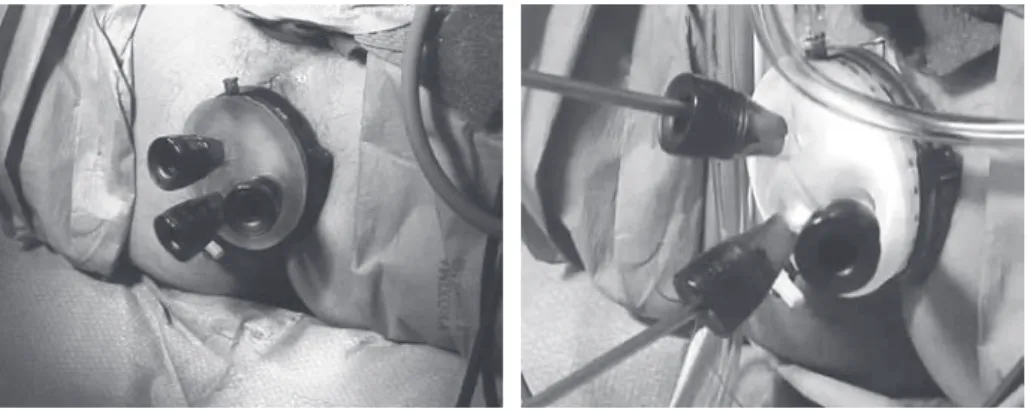
Fig. 2 Preparation of GelPOINT® Path. a-b : Operation is performed with the usual laparoscopic instruments. Fig. 3 TAMIS (Transanal minimally invasive surgery) procedure a : A wet gauze is inserted in the oral side of the tumor to prevent the spread of CO2 along the colon. b : The area to be excised was marked circumferentially with an electric cautery. c : An endoscopic grasper and vessel-sealing device are used to facilitate a full-thickness excision. d : The rectal wall defect is left open and not closed. a b c d a b は超音波凝固切開装置のキャビーテーションによ る周辺組織への損傷を避けるためVessel Sealing System(LigaSureTM Vディスポーザブルカッター 付ラパロ用ハンドピース,シャフト有効長 37cm, コヴィディエン社)を使用している.切除後は出 血のないことを確認し,腫瘍細胞の着床による局
所再発を防ぐため直腸内を1,000mlの生理食塩水で 十分に洗浄を行う.全層で切除した場合は,切除 病変に比べて欠損部は大きくなり縫合閉鎖が困難 なため開放創のままとしている(Fig. 3d ).術後 出血を予防するためヨードホルムガーゼ約30cmを 創部に充填し,術翌日に抜去している. 術翌日から飲水を開始し,血液検査所見,腹部 所見に異常がなければ,術後2日目より食事を開 始している. 3 . 結果 現在までに2例に本法を行った(Table 1, 2 ). 出血量は少量で,いずれも合併症なく順調に経過 し,術後7日間で退院した.術後の後治療に関し ては,いずれの症例も大腸癌治療ガイドライン4)に 従えば追加切除の適応もしくは考慮をする症例で はあるが,十分なインフォームドコンセントの上, 臨床試験「T1,T2下部直腸癌に対する補助療法併 用 縮 小 手 術 の 評 価 第 Ⅱ 相 臨 床 試 験 (UMIN000007184)」に登録し,追加切除はせず放 射線化学療法{放射線:1.8Gy/day×25日(5週), 総線量45Gy,化学療法:TS-1 80mg/m2,5日投 与2日休薬(5週)}を施行している.観察期間は 症例1は12カ月,症例2は9カ月と短いが,再発 兆候は認めず,肛門機能はいずれもWexner score は0点と良好である. 考 察 直腸癌に対する局所切除術は,経肛門,経括約 筋,経仙骨的切除に分類される5).経括約筋,経仙 骨的切除は後方アプローチで行われる術式であり, 経肛門的切除では切除困難な大きな腫瘍や高位の 腫瘍が適応となる6).経肛門的切除には,従来から 行われている開肛器などで肛門管を展開し直視下 に腫瘍を切除する術式のほかに,TEM,前田ら7) が報告したminimal invasive transanal surgery (MITAS)などがある.最近では,単孔式ポート などを肛門管に装着し,通常の腹腔鏡下手術に使 用する器具にて局所切除を施行するTAMISの報告 が散見される8)~12).TAMISに使用するポートは 様々な種類が報告されているが,筆者らの経験で はGelPOINT® Pathが鉗子の可動領域も広く操作 性は高いと思われる.TAMISはTEMと比べて, 高価な特殊器具は必要とせず,通常の腹腔鏡下手 術を経験している外科医であれば特殊なトレーニ ングを受けることなく可能な手技であるため,今 後は広く普及していくと考える.また,TAMISは TEMと同様に26,100点の診療報酬がついている (Table 3 ). 病変を切除した欠損部に関して縫合すべきかど うか問題が残るところであるが,閉鎖せずとも術 後の合併症,便失禁などの後遺症に関して差は認 められず13)14),約4カ月後の内視鏡検査にて欠損 部は84%の患者で完全に治癒すると報告されてい る(閉鎖症例では95%)13).したがって,当科では 閉鎖はせず開放創のままとしているが,特に問題 は認めていない. 下部直腸癌に対してリンパ節郭清を伴う腸切除 として腹会陰式直腸切断術が施行されれば,肛門 は切除され永久人工肛門となる.たとえ,低位前 方切除術や括約筋間直腸切除術が施行されたとし ても,頻回排便や便失禁などが起こり,術後1年 Table 1 Patient Characteristics
No. Age/Sex from anal verge Tumor location (cm)
Maximum Diameter
(cm)
Resection
margin Final pathology
1 62/F 4.0 2.7 Negative pT2, tub2, ly(-), v(+)
2 64/M 3.0 3.0 Negative pT1b (4,000 um), tub1, ly(-), v(+)
( ), depth of T1 invasion; ly, lymphatic invasion; v, venous invasion
Table 2 Operative and clinical results
No. Operative time (min) Blood loss (ml) Hospital stay (days) Morbidity and mortality Adjuvant therapy
1 69 5 7 None CRT
2 110 5 7 None CRT
後のWexner scoreは4.4~10.0点と不良である15)16). 本法の術後のWexner scoreは2例とも0点と非常 に良好である.TEMなどの経肛門的切除の大きな 利点として,従来の経腹的手術に比べ合併症や死 亡率は有意に低いことがあげられる17).しかし,出 血(1.7~2.7%)や骨盤内膿瘍(1~2.7%),死亡 率(0~2%)は低率ではあるが報告されてい る18).非常に稀ではあるが,TEM後に後腹膜気腫 などを認めることが報告されており注意が必要で ある19). 当科では現在までに41例の経肛門的局所切除を 経験している.欠損部を閉鎖した症例は20例,閉 鎖せず開放のままとした症例は21例であった. Clavien-Dindo分類のGrade Ⅲa以上の合併症は3 例で,出血が2例,広範な後腹膜気腫を発症し人 工肛門造設の緊急手術を要した症例が1例で,い ずれも閉鎖症例である.骨盤内膿瘍,死亡例は認 めていない(未発表データ). おわりに GelPOINT® Pathを用いた経肛門的低侵襲手術 を経験した.適応に関しては今後の症例集積とそ の長期成績を検討する必要がある.経肛門的内視 鏡手術は保険収載されており,さらに普及するも のと考える. 利益相反:なし 文 献 1) Buess G, Theiss R, Gunther M, et al : Transanal endoscopic microsurgery. Leber Magen Darm 15 : 271-279, 1985 2) Maslekar S, Pillinger SH, Sharma A, et al : Cost analysis of transanal endoscopic microsurgery for rectal tumours. Colorectal Dis 9 : 229-234, 2007 3) Koebrugge B, Bosscha K, Ernst MF : Transanal endoscopic microsurgery for local excision of rectal lesions : is there a learning curve? Dig Surg 26 : 372-377, 2009 4) 大腸癌研究会編:大腸癌治療ガイドライン 医師 用 2014年版.金原出版,東京,2014 5) 大腸癌研究会編:大腸癌取扱い規約 第8版.金 原出版,東京,2013 6) 武藤徹一郎,小西文雄,沢田俊夫,他:早期直腸 癌に対する局所切除術の適応と方法.消外 9: 187-197,1986 7) Maeda K, Hashimoto M, Nakajima K, et al : Trans-anal surgery with a new anal retractor and a stapler for tumours in the proximal rectum. Eur J Surg 163 : 219-221, 1997 8) Atallah S, Albert M, Larach S : Transanal mini-mally invasive surgery : a giant leap forward. Surg Endosc 24 : 2200-2205, 2010 9) Lim SB, Seo SI, Lee JL, et al : Feasibility of trans-anal minimally invasive surgery for mid-rectal lesions. Surg Endosc 26 : 3127-3132, 2012 10) Hayashi S, Takayama T, Yamagata M, et al : Single-incision laparoscopic surgery used to per- form transanal endoscopic microsurgery (SIL- STEM) for T1 rectal cancer under spinal anesthe-sia : report of a case. Surg Today 43 : 325-328, 2013 11) Albert MR, Atallah SB, deBeche-Adams TC, et al : Transanal minimally invasive surgery (TAMIS) Table 3 Therapy for early rectal cancer
Local resection Radical resection
TAE MITAS TEM TAMIS Lap - LAR Open - LAR
Anesthesia generalspinal/ spinal/general general spinal/ general general general
Aggression low low low low middle high
Instrument instrumentsusual motic instrumentsretractor anasto- instrumentsspecific laparoscopic instruments laparoscopic instruments instrumentsusual
Medical fee※ 4,010 16,700 26,100 26,100 83,930 66,300
Suture instruments ≤ 3 ≤ 3 no no ≤ 4 ≤ 4
Anastomotic instruments no no no no ≤ 1 ≤ 1
MITAS: minimally invasive transanal surgery, TEM: transanal endoscopic surgery, TAMIS: transanal minimally invasive surgery
Transanal Minimally Invasive Surgery (TAMIS)
with GelPOINT® Path for Lower Rectal Cancer
Shingo Noura1)2), Masayuki Ohue1) and Norikatsu Miyoshi1)
1)Department of Surgery, Osaka Medical Center for Cancer and Cardiovascular Diseases 2)Department of Surgery, Osaka Rosai Hospital Objective: We experienced two lower rectal cancer patients to perform transanal minimally invasive surgery (TAMIS) with GelPOINT® Path. Method: Under general anesthesia, complete full-thickness excision of the rectal lesion was performed using LigaSureTM V. We irrigated the defect to prevent local recurrence. But, we did not close the defect. Result: The operation time were 69 min and 110 min, blood loss was very little in each case. The pa- tients recovered uneventfully and were discharged 7 days after the operation. There was no anorec-tal dysfunction and no local and distant recurrence during the postoperative follow-up. Conclusion: Although we need to accumulate the cases and survey the long-term follow-up, TAMIS with GelPOINT® Path is a helpful operative procedure.
Key words: rectal cancer,transanal minimally invasive surgery (TAMIS),GelPOINT® Path