Kumamoto University Repository System
Title 種々の生体信号解析による睡眠呼吸障害の定量的評価法
Author(s) 大久, 典子
Citation
Issue date 2010-03-25
Type Thesis or Dissertation
URL http://hdl.handle.net/2298/17212
博士論文
種々の生体信号解析による睡眠呼吸障害の
定量的評価法
2010 年 3 月
熊本大学大学院自然科学研究科
大久典子
1-2. 論文の構成 ……4 第 2 章 睡眠と睡眠呼吸障害の評価 2-1. 睡眠と睡眠段階 ……5 2-2. 自律神経系 ……7 2 - 2 - 1 . 自 律 神 経 系 の 機 能 … … 7 2-2-2. 睡眠と自律神経 ……10 2-3. 睡眠障害 ……11 2 - 3 - 1 . 睡 眠 障 害 の 分 類 … … 1 1 2 - 3 - 2 . 閉 塞 型 睡 眠 時 無 呼 吸 低 呼 吸 症 候 群 … … 1 3 2 - 3 - 3 . 上 気 道 抵 抗 症 候 群 … … 1 6 2-4. 睡眠障害検査とその測定機器 ……17 2-4-1. 睡眠検査のタイプと睡眠障害に対するパラメータ ……17 2-4-2. 終夜睡眠ポリグラフ(Polysomnography, PSG) ……18 2 - 4 - 3 . 睡 眠 呼 吸 障 害 の 評 価 指 標 … … 2 0 2 - 4 - 4 . 簡 易 睡 眠 呼 吸 検 査 指 標 … … 2 1 2-5. 睡眠検査における生理学的データの解析方法 ……22 2-5-1. 時間領域解析法 ……22 2-5-2. 周波数領域解析法 ……23 2-5-2-1.高速フーリエ変換(FFT)法 ……23 2-5-2-2.自己回帰(AR)法 ……25 2-5-2-3. 最大エントロピー法(MEM)および MemCalc 法 ……25 第 3 章 睡眠検査指標と 自律神経活動評価指標との関連性 3-1. 閉塞型睡眠無呼吸低呼吸症候群における自律神経活動 ……28 3-1-1. はじめに ……28 3-1-2. 対象・方法 ……29 3-1-3. 結果 ……29 3-1-4. 考察 ……35
3-2-2. 対象・方法 ……37 3-2-3. 結果 ……38 3-2-4. 考察 ……46 第 4 章 各種生体信号解析による睡眠状態の評価 4-1. 脳波と下顎筋電図による睡眠段階判定の試み ……49 4-1-1. はじめに ……49 4-1-2. 対象・方法 ……50 4-1-3. 結果 ……50 4-1-4. 考察 ……54 4-2. 脳波エントロピー値による睡眠呼吸障害の評価 ……55 4-2-1. はじめに ……55 4-2-2. 対象・方法 ……55 4-2-3. 結果 ……56 4-2-4. 考察 ……63 4-3. 心電図エントロピー値による睡眠呼吸障害の評価 ……64 4-3-1. はじめに …… 6 4 4-3-2. 対象・方法 ……65 4-3-3. 結果 ……65 4-3-4. 考察 ……70 第 5 章 総括 5-1. 閉塞型睡眠時無呼吸低呼吸症候群(OSAHS)と自律神経活動 ……72 5-2. 携帯型生体信号計測装置(PBSM)を用いた MemCalc 法によるエントロピー値の解析 ……74 5-3. 今後の課題 ……78 参考文献 ……78 謝辞 ……88
第1章 序論
1-1. 研究の背景と目的
ヒトの一生の約1/3は睡眠時間である。睡眠がうまくとれないと、大脳の情 報処理能力に悪い影響が出る。睡眠不足のときに私たちが感じる不愉快な気分 や意欲のなさは、身体ではなくて大脳そのものの機能が低下していて、大脳が 休息を要求していることを意味している。この睡眠中の身体状況は、患者本人 のみならず家族にとっても、医療側にとってもブラックボックスである。睡眠 中における免疫系、内分泌系、血液凝固系、中枢神経系等のさまざまな因子の 応答の異常が、われわれの身体のホメオスタシスを破綻させる要因になってい る 1)。睡眠覚醒リズムに代表される意識活動は自律神経の支配を受けていて、 覚醒時には交感神経系が優位に働き副交感神経の活動が低下する。逆に、睡眠 時には副交感神経が亢進し交感神経の活動が低下する2-5)。ヒトの自律神経活動 は交感神経と副交感神経の拮抗支配をうけており、この両者の相対的な関係か ら自律神経活動を論じているにすぎない。最近、筋交感神経活動法と呼ばれる 方法が開発された。これは、タングステン微小電極を刺入して神経の活動電位 を直接記録すると、神経インパルスの群発が観測され、この群発の単位時間あ たりの頻度で交感神経の活動を直接評価できるものである。この方法により、 睡眠から急に覚醒する際に自律神経系の反応が必ず伴うことや、覚醒反応は致 死的な心室細動をもたらすこともあり、睡眠中の中途覚醒がかなり危険な現象 であることも解かってきた6-9)。 睡眠中に呼吸の異常を来す代表的な疾患として睡眠時無呼吸症候群(SleepApnea Syndrome, SAS)がある 10)。わが国における本症候群に関する研究は既
に 1970 年代後半より行われていたが、一般の臨床医に注目されるようになった のは、つい最近起こった山陽新幹線運転手の居眠り運転が SAS によるというこ
とが明らかとなり大きな社会問題になってからである11)。本疾患概念は、1976
年にスタンフォード大学の Guilleminault 教授により提唱された10)。10 秒以上
ム睡眠にわたって一晩に 30 回以上出現する症候群と定義されている。
無呼吸を来す原因で最も多いのは上気道の狭窄や閉塞により起こる閉塞型無 呼吸低呼吸症候群(Obstructive Sleep Apnea/Hypopnea Syndrome, OSAHS)であ
り、扁桃肥大や小顎12-14)、肥満15-16)などが原因で起こる場合が多く、脂肪が空 気の通り道を狭めてしまうことによる。この OSAHS では、“睡眠—上気道閉塞— 無呼吸—胸腔内圧低下、PaO2 低下、PaCO2 上昇—覚醒—上気道開放—睡眠”という エピソードを一夜に数百回程度繰り返す 17-19)。無呼吸発作時には化学受容体を 介して脳波上覚醒反応が生じることや化学受容体の感受性亢進などにより、交 感神経活動の亢進が起こるとされる20-21)。ノンレム睡眠(NREM)やレム睡眠(REM) による睡眠の周期には成長ホルモンや下垂体ホルモンのプロラクチンや腎臓ホ ルモンのレニンなども関与しており、免疫系や内分泌系、感覚神経系などとの 協調的調節による自律神経活動の破綻と OSAHS 発症との関連は興味深い22-23)。
また、最近では、心拍変動による VLF(very low frequency)指標が無呼吸の周期 を反映し、不整脈が原因となる死亡率との関連性が強く、生命予後の予測に特 に有用であるとの報告もある24-28)。OSAHS は、成人の約 2-7%にみられ、老人 では頻度が高くなるなど、けして稀なものではない 29-30)。肥満、高血圧、糖尿 病、高脂血症などいわゆる生活習慣関連疾患との合併例も多く、睡眠中の無呼 吸に伴う低酸素血症により、脳、心、肺、肝、腎臓など重要臓器に障害をもた らす。さらには、頻回なる断眠により日中過眠や活動度の低下などの精神身体 異常を来す。特に、SAS は高血圧の病因として独立した因子であり、二次性高血 圧の第一に選ばれている。これらのことから睡眠中における生体情報を知る事 は種々の疾患の診断、病態の解明に極めて重要である。 現在、睡眠中の中枢神経機能、呼吸機能及び循環機能をモニターする方法と して、脳波、筋電図、眼電図、呼吸運動、酸素飽和度および心電図等種々の測 定 方 法 を 駆 使 し て 睡 眠 中 の 生 体 信 号 を モ ニ タ ー す る 終 夜 睡 眠 ポ リ グ ラ フ (Polysomnography, PSG)がゴールドスタンダードである31-32)。 その実施にあたっては設備、人手、時間がかかるため SAS を疑われる全例に施 行することは困難である。また検査を実施できる医療機関にも限りがある。こ
れらの事はわが国にける SAS を中心とした睡眠医療の普及の制限因子ともなっ ている。従って、外来レベルで簡単に睡眠中の呼吸異常を検出できる簡易睡眠 モニター装置の開発が不可欠である。 わが国における OSAHS は肥満を伴わない重症例がいることが注目されており、 欧米とは異なった背景があると考えられる 33-36)。OSAHS の実態を明らかにする ためには、診断法、診断のための施設などの問題がある。OSAHS の診断のために は PSG が不可欠であり、専門の施設でないと診断がつかない。しかし、診断法 の煩雑性のため診断できる施設の普及が困難である。そこで、最近、幾つかの 簡易睡眠モニター装置が開発され、臨床の現場で使用されているパルスオキシ メータ、在宅睡眠時呼吸モニター装置は気流、酸素飽和度モニターによるもの である 37-41)。このような装置では無呼吸、低呼吸などの呼吸情報の評価は可能 であるが、睡眠時間、睡眠段階の評価および循環動態の評価は不可能である。 脳波を含めたモニターができないため、一部の睡眠呼吸障害を見逃す恐れがあ り、診断法として用いるには不適応との指摘もある。特に、上気道抵抗症候群 は OSAHS と同様に、日中の過眠といびきを訴えるにもかかわらず、胸腔内圧の 上昇に従って頻回の覚醒反応が見られるが、血中酸素飽和度の低下が無く、無 呼吸低呼吸指数も 5 以下であることから、病態的には OSAHS に分類されるが簡 易モニターでは見逃されることがある 37-41)。したがって簡易睡眠モニターにも 脳波や心電図の情報が加われば睡眠レベルの評価や睡眠中の循環動態の情報も 評価できるようになる。このことは、PSG から得られる情報水準までにはならな いものの、在宅での睡眠状態や循環動態の情報を呼吸情報とともに同時に得る ことができる携帯型の睡眠呼吸モニター機器の開発も可能となる。さらに、こ れに心電図の周波数解析を行うことができれば睡眠時の自律神経評価も可能な 睡眠検査システムの開発の可能性まで広がる。 したがって、本研究は、携帯型ホルター心電計および携帯型生体信号計測器 によって得られる生体信号に従来使用されていない新しい解析方法を行うこと で得られる結果と従来から使用されている PSG における生体信号の解析結果と を比較することで、睡眠呼吸障害の新しい定量的評価方法の検討を行った。
1-2. 論文の構成
本論文は以下の構成となっている。 第1章は序論であり、本論文の背景と目的、および論文の構成について述べ る。 第 2 章では、睡眠および睡眠障害の概要、およびこれらに密接に関連する自 律神経系のメカニズムについて現在までに解明されている生理学的知見につい て述べる。また、現在使用されている睡眠検査における種々の計測方法やこれ らの機器により計測された生体信号の解析方法について述べる。さらに日本国 内で使用されている携帯型生体信号計測機器の現状などについても言及する。 第 3 章では、ホルター心電図により閉塞型睡眠時無呼吸低呼吸症候群(OSAHS) 患者と健常者の心拍変動を24時間計測し、その心拍変動解析により OSAHS 患 者の睡眠病態について述べる。第 4 章は、PSG および携帯型生体信号計測器(Portable Bio-Signal Measurement Instrument, PBSM)から記録した生体信号の比較から、PBSM を使用した脳波およ び下顎筋電図による睡眠ステージの有効性を検討する。また、OSAHS の睡眠の質 的評価に関して、PBSM で記録した脳波および心電図の周波数解析により算出し たエントロピーの有効性について述べ、この方法による簡易型睡眠検査システ ムの可能性について言及する。 最後に第 5 章では本研究で得られた結果をまとめ、今後の課題および展望に ついて述べる。
第 2 章 睡眠と睡眠呼吸障害の評価
2-1. 睡眠と睡眠段階
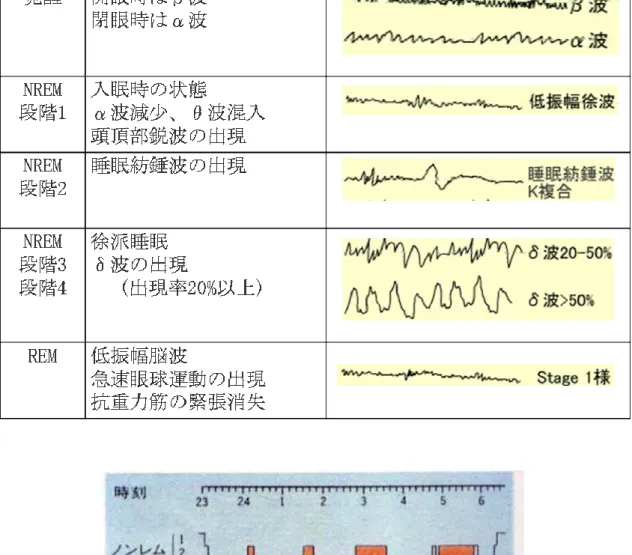
睡眠は単なる活動停止の時間ではなく、高度の生理機能に支えられた適応行 動であり、生体防御技術でもある。とりわけ、発達した大脳を持つ私たち人間 にとっては、睡眠の適否が質の高い生活を左右することになる。「よりよく生 きる」ことは、とりもなおさず、「よりよく眠る」ことなのである42)。 脳波が脳の意識水準とよく対応して変化し、特に睡眠中は著明な変化を示す ことから、脳波、眼球電図および下顎筋電図などを同時に記録し、総合的に睡 眠段階を判定する。睡眠段階は、覚醒期、ノンレム睡眠の段階 1、段階 2、段階 3、段階 4 およびレム睡眠に判別する。ノンレム睡眠段階 1〜4 は浅睡眠期(段 階 1 と段階 2)と深睡眠期(段階 3 と段階 4)とに大別される。 表 2-1 はこのような睡眠段階と脳波の大まかな特徴を示している。上段の覚 醒期には脳波の中でβ波やα波が出現する。ノンレム睡眠段階 1 では、α波に 代わって 4~7Hz のθ波が出現し、入眠期と呼ばれる状態である。脳波の変化に 加え、入眠期にはゆっくりとした眼球の振子運動(slow eye movement, SEM) がみられる。ノンレム睡眠段階 2 では、14Hz 前後の睡眠紡錘波(sleep spindle wave)が出現し始め、ゆっくりとした眼球運動は停止し、呼吸は規則正しい寝 息になる。深睡眠期では、眠りがさらに深くなり、脳波の周波数は 3Hz 以下に 下がり、振幅は 200~300μV くらいまで高くなる。この遅い波が大徐波あるい はδ波と呼ばれるものである。行動的にもっとも深い眠りである。眠りはじめ てからおよそ 1 時間半から 2 時間後に、突然、脳波パターンはノンレム睡眠段 階 1 へ移行する。しかし、入眠期と違ってゆっくりとした眼球運動はみられず、 逆に覚醒期のような急速眼球運動(rapid eye movement, REM)が起こる。さら にオトガイ筋など抗重力筋の緊張が著しく低下する。この睡眠をレム睡眠とい う。図 2-1 は、睡眠時における脳波と筋電図等の特徴に基づいて作成された睡眠 経過図(睡眠ダイヤグラム)を示す。睡眠ダイヤグラムとは、各睡眠段階の経
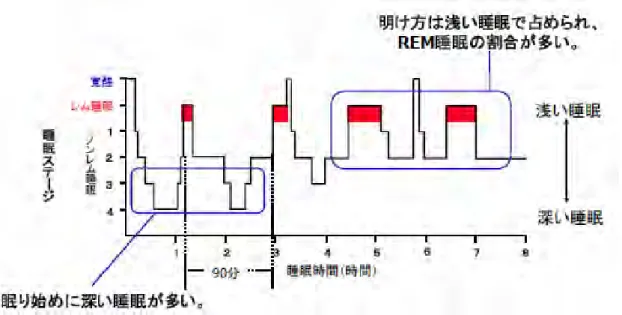
時的変化を図で表すことで、各睡眠段階の出現状況や睡眠の安定性など、睡眠 構築を視察的に把握することができ、睡眠中の様々な事象との時間的関連性を 知る上で有用である 43)。正常な成人の睡眠は、入眠とともに浅い眠りであるノ ンレム睡眠段階 1 からノンレム睡眠段階 2 へとすすみ、深睡眠期に入る。再び 眠りが浅くなり、レム睡眠がはじめて出現する。この間が、約 90 分で、この周 期を 4、5 回くりかえす(ウルトラディアンリズムとも言う)。図のように睡眠 の前半は深い眠りの成分が多く、睡眠の後半はレム睡眠の成分が多くなる。
表 2-1. 睡眠段階の脳波の特徴(Rechtscaffen&Kales;2006)
図 2-1. 成人の睡眠の時間経過図
2-2. 自律神経系
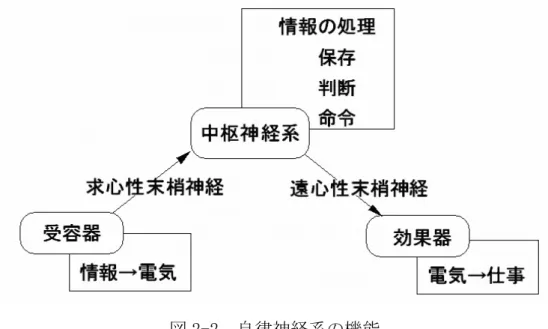
2-2-1. 自律神経系の機能 自律神経は、ヒトが意識をしないでも体内の臓器や器官を環境に合わせて生 理的恒常性を保つ役割を持っている。例えば、内臓感覚受容器(血管壁、胸腔・ 腹腔および骨盤腔の器官)で感受された内臓の状態を中枢神経の各部位にある 自律神経中枢に伝える求心性機序(内臓求心性神経系)と内臓諸臓器の機能を 調節する交感神経系、副交感神経系による遠心性機序(自律神経遠心路)によ り調節されるが、これらの情報処理は反射的に行われている(図 2-2)。 ひとつの臓器には交感神経と副交感神経の両系統の支配(二重支配)があり、 互に拮抗しながら相反する効果(拮抗支配、相反支配)を及ぼしている。たと えば心臓の活動(心拍数、心拍出量など)は交感神経により亢進し、副交感神 経により抑制される。一方、消化管、尿管、膀胱などの活動(収縮、蠕動、分 泌など)は副交感神経により亢進し、交感神経により低下する。一言で言えば、 交感神経は運動に必要な機能を亢進させる神経系であり、副交感神経は食後に 必要な機能を亢進させる神経系である(表 2-2)。 自律神経系は脊髄、脳幹、視床下部、大脳辺縁系などにある自律機能中枢や 脊髄にある高位中枢による中枢性調節、各種感覚入力による反射性調節を受け て、循環、呼吸、消化、発汗・体温、内分泌機能、生殖機能、および代謝のよ うな不随意な機能を制御する。その際、自律神経系ばかりでなく、1) 内分泌系、 2) 免疫系、3) 体性神経系も協調的に調節されて、生体のホメオスタシスが維 持される。図 2-2. 自律神経系の機能 http://physiol.umin.jp/nerv/intro/text/text.html より引用 表 2-2. 自律神経系と生体機能 生体機能 交感神経興奮 副交感神経興奮 心臓拍動 増加 減少 血圧 増加 低下 気管支 拡張 収縮 消化管運動 抑制 亢進 肝臓 グリコーゲン分解 グリコーゲン合成 瞳孔 散大 縮瞳
2-2-2. 睡眠と自律神経 睡眠中に分泌が増加するホルモンの中で、代表的なものとして成長ホルモン があげられるが、子供の骨や筋肉の発育には欠かせないものであるばかりでな く、大人にとっても新陳代謝に深く関係している。朝起きる頃になると、コル チゾール(副腎皮質ホルモン)の分泌のピークを迎え、このホルモンは身体を 目覚めさ、日中の活動を支え、やる気を起こさせる。一方、暗くなると脳の松 果体からメラトニンが分泌され、このホルモンには眠気を増進させる作用があ る。自律神経系は、昼間は体温が高く活動に適した状態では交感神経が優位に なり、心臓の拍動なども高まるが、睡眠中は心拍や呼吸などの自律神経系の機 能は副交感神経優位の方向へと変わる。通常、昼間は自律神経系の一つである 交感神経が優位になり、夜は副交感神経優位の方向へと変わることで、様々な ホルモンのバランスが整えられる(図 2-3)。 図 2-3. 睡眠と自律神経
2-3. 睡眠障害
2-3-1. 睡眠障害の分類 睡眠呼吸障害は単独疾患ではなく、上気道の易虚脱性や呼吸調節の異常によ り、睡眠中頻回に呼吸が停止する呼吸障害とそれによる睡眠障害を呈する症候 群である。その判断は、自覚症状の有無に関わらず、睡眠時に 10 秒以上(通常 20~50 秒)持続する呼吸停止または浅い呼吸(低呼吸)のエピソードが1時間 あたり 5 回以上反復し、呼吸障害に伴って覚醒反応が頻回に起こる状態を言う。 低呼吸とは 呼吸が止まらなくても、呼吸がしにくくなり、動脈血酸素飽和度の 低下状態のことを言う。アメリカ睡眠医学学会(AASM)の 1999 年の定義44)では、 低呼吸は呼吸の振幅の低下が 50%未満であっても、3%より大きい酸素飽和度の 低下または覚醒を伴う 10 秒以上の呼吸減弱としている。一方、睡眠時無呼吸低呼吸症候群(sleep apnea/hypopnea syndrome, SAHS) の定義は、睡眠呼吸障害があり、かつ日中傾眠または熟睡感の欠如や日中倦怠 感などの自覚症状を伴うものとされ、区別して扱うことが必要である。SAHS の 特徴を挙げると、夜間睡眠中に反復して呼吸停止あるいは呼吸低下の起るもの で、夜間睡眠が慢性的に妨げられるため、朝起床時に爽快感に乏しく、日中強 い眠気や全身倦怠感が毎日のように起こり、社会生活が妨げられる疾患である。 臨床的には高血圧症・虚血性心疾患・脳血管障害・不整脈などの原因の一部に なる。その主な要因としては繰り返す低酸素血症、頻回の睡眠中断による覚醒 反応、その結果としての持続的な交感神経系活動の亢進、インスリン抵抗性の 惹起が挙げられている。それらは、SAHS に合併することが多い肥満症・メタボ リック症候群と相まって、血管内皮細胞傷害・動脈硬化症を引き起こし、さら には臨床的な心血管系障害につながる。SAHS では中枢性にせよ閉塞性にせよ、 無呼吸に伴う動脈血酸素飽和度の低下が化学受容器を介して、また胸腔内圧の 変化が機械的受容器を介して交感神経系の亢進をもたらし、結果として夜間昇 圧が生じる。 SAHS を型で分類すると、肥満や扁桃腺肥大などによる上気道狭窄が原因で発 生し、胸郭の呼吸運動はあるものの鼻腔からの換気が停止し、覚醒反応により
苦悶性の激しいいびきを繰り返す閉塞型と、胸郭の呼吸運動が起らず呼吸停止 が反復する中枢型と、両者の混合した混合型が区別されているが、相互の移行 もある(図 2-4)。また完全な呼吸停止には至らないが、換気が低下するために 頻回の覚醒反応が起こる上気道抵抗症候群もあり、診断には食道内圧の測定が 有用である。 図 2-4. SAHS の各種病態(閉塞型・中枢型・混合型) 図に示す各種睡眠時無呼吸のそれぞれのチャンネルは、上より下へ、呼吸の気流、胸郭 の動き、腹壁の動き、いびき、体位、経皮的酸素飽和度を示す。閉塞型は上気道が閉塞し て気流が停止するもので、無呼吸中も胸部と腹部の呼吸運動が認められるが、その動きは 互いに逆になる奇異運動を示す。中枢型は呼吸中枢の機能異常により主としてレム睡眠期 に呼吸筋への刺激が消失して無呼吸となる。混合型は中枢型無呼吸で始まり、後半になっ て閉塞型無呼吸に移行する場合が多い。閉塞型無呼吸に分類されることが多い。
2-3-2. 閉塞型睡眠時無呼吸低呼吸症候群(OSAHS) OSAHS は SAHS の代表的病型であり、睡眠障害でもっとも頻度が高い。図 2-5 下段に OSAHS の睡眠ダイヤグラムを示す。OSAHS では上気道が虚脱しやすく、覚 醒中は上気道を開放する筋群の活動性が亢進しているとされているが、睡眠中 は筋活動が低下し、上気道は動的狭窄状態となる。気道が狭まっていると必要 な量の換気が行われず、血液中では酸素量が低下して二酸化炭素の量が増える という現象が起こる。そこで、血管壁にあるセンサーがこれを感知して延髄に ある呼吸中枢に働きかけ、この刺激で脳が一過性の覚醒現象を起こし、呼吸中 枢は呼吸筋に対して呼吸運動を活発にするよう指令を送る。呼吸筋はこれに促 されて呼吸運動を活発化し、空気を送る力を強めていく。この力が気道の狭く なっている部分の抵抗をはねのけたとき、気道が開放されて初めて大きな呼吸 をする。狭窄により生じる乱流が咽頭壁を激しく振動させるため、睡眠に伴っ て周囲にそれとわかる強い「いびき音」を伴うあえぎ様呼吸を繰り返す。気道 の状態は吸気初期には軽度の狭窄であっても吸気末期に向けて虚脱し、ついに は完全に閉塞する。したがって、閉塞部位は解剖学的に常時同一部位とは限ら ず、吸気努力によって生じる陰圧と気道開存性維持のための上気道筋の緊張度 との力学的バランス変化によって 1 回の呼吸サイクル中にも瞬時に移動する。 閉塞は筋緊張がもっとも失われるレム睡眠期に生じやすいが、他の睡眠相でも 観察されるのがこの病態における特徴である。このサイクルは、無呼吸が起こ る度に、脳が覚醒を繰り返していることであり、この脳の覚醒は意識に残るよ うなものではなく、大体は数秒間で再び眠りにつく程度のものである。しかし、 睡眠中に脳が覚醒するのは、眠りがその都度、分断され、ひと晩に 30 回以上、 重症の OSAHS では数 100 回にも及ぶ。眠りが分断されれば、それだけ睡眠も浅 くなり、習慣的にこれを繰り返していれば慢性的な睡眠不足に陥る。睡眠不足 が高じれば日中、突然に眠り込んだりすることもあり、実際、それが原因で起 こったさまざまな事故などが報告されている。
図 2-5. 睡眠ダイヤグラム 上段:健常人、下段:OSAHS
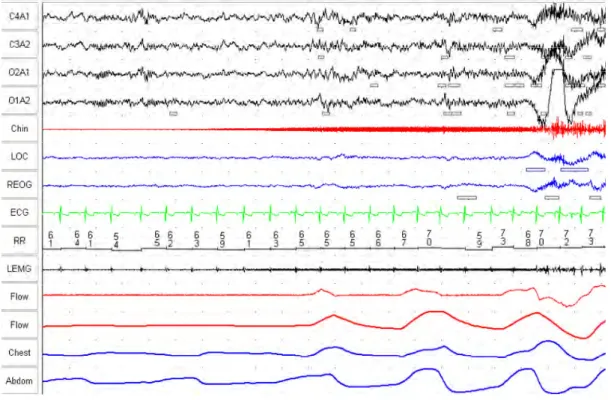
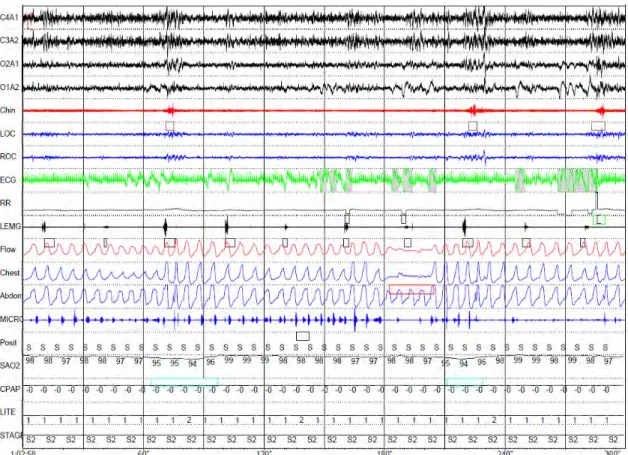
図 2-6 は、OSAHS 症例から得られた PSG の記録例である。呼吸に関する 4 個 の記録(上より 11 チャンネル(Flow)〜14 チャンネル(Abdom)は、記録開始時 より上下への変動が観察されず無呼吸状態である。その後、徐々に変動が始ま り呼吸が開始されている。上気道の閉塞によって呼吸が停止し、低酸素血症を 起こし、胸腔内圧の陰圧が増大し、覚醒反応が出現する。 図 2-6. OSAHS 症例 上気道の閉塞により呼吸が停止し、低酸素血症となり、覚醒反応が出現する。
2-3-3. 上気道抵抗症候群
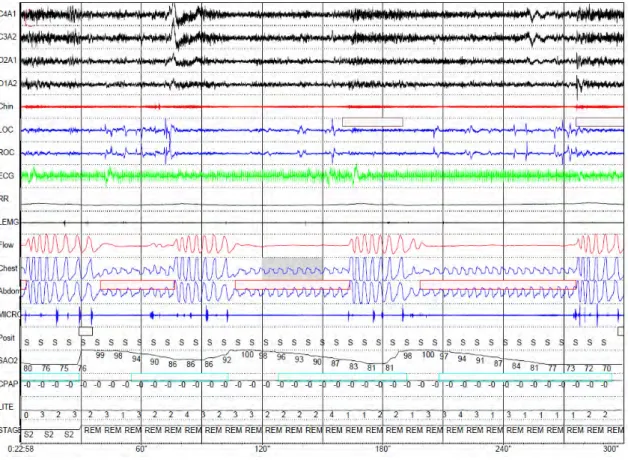
上気道抵抗症候群(upper airway resistance syndrome, UARS)は OSAHS の 亜型で、軽症の睡眠呼吸障害である。OSAHS では上気道の閉塞・狭窄により無呼 吸や低呼吸となり、覚醒反応が起こる(図 2-6)。一方、UARS は、明らかな無呼 吸や低酸素血症がみられないことが特徴(図 2-7)で、簡易診断装置では見過ごさ れる可能性が高い。正確な診断には鼻から食道にカテーテル(圧センサ)を挿 入し、食道内圧の測定が奨励されている。上気道の抵抗に対する覚醒、いわゆ る呼吸努力関連覚醒反応による睡眠の分断があるため、日中の過眠などがみら れる。実際の臨床の場では、自覚症状の評価、PSG 検査(特に呼吸波形)にて総 合的に判断する。UARS ではフローリミテーションが 5 回/時間以上ある。フロー リミテーションとは、気道が狭いために吸気量が制限され、ストローを通して 息を吸っているような状態であり、胸腔内圧が下がり、微小覚醒する。 図 2-7.上気道抵抗症候群(UARS)症例 明らかな無呼吸や低酸素血症がみられずに、覚醒反応が出現する。
2-4. 睡眠障害検査とその測定機器
2-4-1. 睡眠検査の型と睡眠障害に対する指標 睡眠検査の主目的は睡眠時無呼吸症の診断を確立するとともに、重症度の評 価、治療の選択、および治療効果の評価にある。 表 2-3 は睡眠検査のタイプと測定する指標を示している。日中の過眠症状を呈 する患者の鑑別診断のゴールドスタンダードは患者の観察と睡眠ステージの分 析、酸素飽和度、口・鼻気流の観察を含む PSG 検査である 43-47)。覚醒中の所見 は必ずしも睡眠中の病態を表現しないため、睡眠呼吸障害の診断は睡眠中の所 見に基づいて行われる必要がある。睡眠時無呼吸症と鑑別すべき疾患として、 単純イビキ症、睡眠障害、ナルコレプシー、不眠を伴ううつ病などがある。こ れらは治療の対象とならないものや、薬物療法が主体となる病態が含まれ、SAHS の治療方針とは大きく異なるため、より正確な鑑別が必要である。 しかし、PSG 検査は設備面(入院が必要である)や、熟練した検査技師による 装着、観察のもとに施行され、その解析にも熟練を要する。このため、多大な 労力とコストのかかる検査である。おのずと施行可能な検査数が限られ、スク リーニングには向かない。待機患者が増えていることなども問題となり、わが 国では様々に簡略された検査装置を用いることが可能になっている(表 2-3)。 表 2-3. 検査のタイプと測定する指標 検査のタイプ 測定する指標 Type1 標準的な検査室において検査技師の立ち 会いで実施する PSG 脳波、眼球電図、下肢筋電図、 下顎筋電図、心電図、酸素飽和度、 気流、換気運動 Type2 総合的なポータブル終夜睡眠ポリグラフ 脳波、眼球電図、下顎筋電図あるいは心 拍数、気流、呼吸努力、酸素飽和度を含 む最小 7 チャンネルのモニター Type3 睡眠時無呼吸に限定された簡易検査 換気量もしくは気流、心拍数あるいは心 電図、酸素飽和度を含む最小 4 チャンネ ルのモニター Type4 持続的に記録される 1 つあるいは 2 つの 生物学的指標 酸素飽和度あるいは気流を含む 1~2 チ ャンネルのモニター2-4-2. 終夜睡眠ポリグラフ(PSG) 一般に睡眠検査には PSG が使用され、SAHS の診断と治療方針の決定、治療効 果の確認などにおいて最も重要な測定方法である。脳波、眼球電図、下顎筋電 図、気流、動脈血酸素飽和度、換気努力、心電図などの記録により睡眠の状態、 呼吸の状態、イビキの状態、身体の酸素の状態、身体の向きなどを同時に解析 し、それぞれの関係を調べる。表 2-4 に各センサーと睡眠検査項目を示す。 表 2-4. 各種センサーと睡眠検査項目 脳波 眼球電図 下顎筋電図 口・鼻センサー 胸・腹センサー 心電図 酸素飽和度 下肢筋電図 体位 眠りの深さ、時間 眠りの深さ、時間 眠りの深さ、時間 無呼吸・低呼吸の有無、重症度 無呼吸・低呼吸の有無、重症度 不整脈、脈拍の変動 血液中の酸素濃度 夜間の下肢の動き どの向きで寝ているか 実際のセンサー装着は図 2-8A に示すように、脳波は耳朶を基準として頭皮上 左右の頭頂部、後頭部から導出した記録、眼球電図は鼻根を基準として左右の 眼瞼下から導出した記録、また筋電図は左右の下顎筋から導出した記録によっ て睡眠段階を判定する。呼吸のモニターとしては、鼻孔および口に装着して呼 吸に伴う気流の温度変化を検出するサーミスタ、鼻口カニューレからの気流を 圧力センサーにより電気信号へ変換する鼻腔圧センサー、胸郭及び腹壁の呼吸 運動に伴う電気抵抗の変化を検出するストレンゲージ、指先の酸素飽和度を検 出するパルスオキシメータ、頸部正中のいびきの振動を検出する振動センサー、 循環のモニターとしては心電図を記録している。図 2-8B は装着後の患者の例で ある。センサーが脱着しないようにセンサー装着後被験者は頭部からネットを
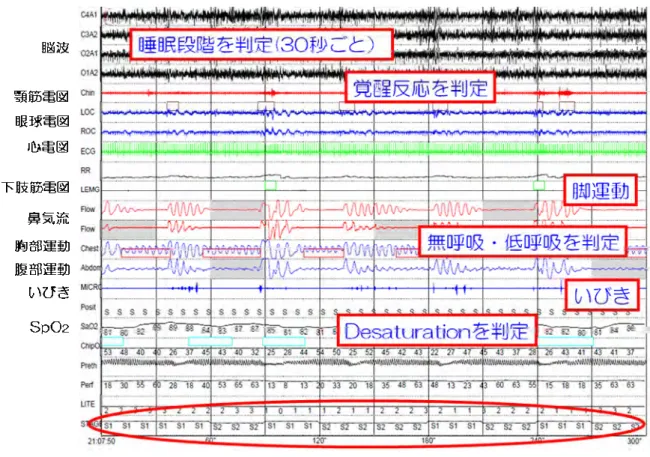
被ることになる。図 2-8C は実際の睡眠検査の風景である。図 2-8D はコンピュ ータに入力された PSG 記録を示している。 A B C D 図 2-8. PSG 検査風景 A: 検査項目と各種センサー、B:センサーを装着した患者(ネットをかぶり、センサー外れ を防止する)、C: 被験者の睡眠中の様子、D: コンピュータに入力された PSG 記録例
図 2-9.PSG 検査 30 秒間の記録例
2-4-3. 睡眠呼吸障害の評価指標
PSG は、睡眠状態を総合的に評価する検査であり、睡眠の深さ(睡眠段階)、 覚醒反応の有無、中途覚醒による睡眠の分断化、睡眠構築、睡眠効率などを呼 吸状態の詳細とあわせて、定量的に算出する。
1) 無呼吸低呼吸指数(Apnea/Hypopnea Index, AHI)
SAHS の重症度の指標であり、睡眠 1 時間あたりの無呼吸および低呼吸の回数 を示し、無呼吸と低呼吸の合計回数を全睡眠時間で割って算出する。無呼吸は 10 秒以上の換気停止であり、低呼吸は胸郭や腹壁の動きあるいは口鼻での気流 の低下が 30%以上で、10 秒以上続き、4%以上の動脈血酸素飽和度低下を伴うも のと定義される。
2) 酸素脱飽和度指数(Oxygen Desaturation Index, ODI) 睡眠 1 時間あたりに酸素飽和度が 3%以下に陥る回数と定義される。 3)覚醒反応(Arousal Index) 10 秒以上持続する睡眠中に突然、3 秒以上持続する周波数の変化(θ波、α 波、β波の出現)の 1 時間あたりの出現頻度と定義される。 4) 深睡眠比率 全睡眠時間の深睡眠時間の割合と定義される。 5) レム睡眠比率 全睡眠時間のレム睡眠時間の割合と定義される。 2-4-4.簡易睡眠呼吸検査指標 自宅で検査が可能となるように PSG の測定項目を省略したものであり、主と して、血液の酸素飽和度、鼻の気流、いびき音、胸郭の動き、心電図を測定す る(図 2-10)。脳波の情報がないため、睡眠呼吸障害の詳しい評価をすること ができないので、スクリーニング目的に使用される。検査の精度としては、PSG 検査の感度・特異度には及ばない。AHI はひと晩の無呼吸、低呼吸回数を総睡眠 時間で割ったものであるが、脳波の記録がない簡易モニターでは総睡眠時間が 得られないため、総記録時間で代用することが多い。これにより、睡眠呼吸障 害の程度を過小評価する可能性がある。また、簡易モニターを患者の自宅で用 いた場合には、一般的に擬陰性、擬陽性ともに増加し、現在得られるエビデン スのレベルも限られる。適切にデータを記録できない検査の失敗率は 3%から 18%とされている。OSAHS を精査する過程において PSG 検査を行う場合、通常、 事前に簡易検査による評価が必要となっている。
《Type 3》 《Type 4》 図 2-10. 簡易睡眠呼吸検査測定器 Type 3: 呼吸状態(無呼吸や低呼吸の回数、時間)および動脈血中の酸素飽和度と脈拍を 同時に測定する機器、Type 4: 動脈血中の酸素飽和度と脈拍を同時に測定する機器
2-5.睡眠検査における生理学的データの解析方法
睡眠検査から種々の生理学的データを測定する場合に、それらの信号に対す る解析方法は、臨床的に感度の良い指標を抽出するのに重要な役割を持ってい る 48-50)。臨床応用されているものとしては時間領域解析法と周波数領域解析法 による指標に大別される。 2-5-1. 時間領域解析法 時間領域解析法は数学的関数や物理的信号の時間についての解析法であり、 信号あるいは関数値が連続的な実数で表される連続時間と、ある間隔で値が示 される離散時間があり、信号が時間と共にどう変化するかを表すものである。 例えば心電図における RR 間隔を得るには、心電図波形を微分し、その微分値に トリガーをかけて R 波を検出する。そして、その間隔を算出する方法が一般的 であり、この場合は以下の様な指標が使用されている。 1)心拍変動係数(CVR-R) 心拍変動の度合い(心拍のバラツキ)を評価するもので、心電図 RR 間隔の標 準偏差を RR 間隔の平均値で除して 100 倍する式で求めることができ、心臓副交感神経系活動を表す指標とされる。 2-5-2. 周波数領域解析法 周波数解析は、信号の周波数分布(周波数スペクトル)をみることで、信号 の性質の把握、定量化を行うことができる。周波数領域解析法は関数や信号を 周波数に関して解析する方法であり、その信号にどれだけの周波数成分が含ま れているかを示す。各周波数成分の位相情報も含まれ、それによって各周波数 の正弦波を合成することで元の信号が得られる。 表 2-5.代表的な周波数領域解析方法 方法 仮定する モデル 周波数領域 の解析 PSD の判定 時間領域 の解析 短いデー タの解析 分解能 FFT なし 可 不可 不可 普通 普通 AR AR 可 不可 可 劣 普通 MEM なし 可 不可 不可 優 優
2-5-2-1. 高速フーリエ変換(Fast Fourier Transform, FFT)法
心電図 RR 間隔のゆらぎが周波数の異なった余弦関数の集まりと仮定してそれ らの関数の振幅を分離する方法である。任意の曲線を、様々な周期・大きさの 正弦波のグラフの和(AsinΘ+Bsin2Θ+Csin3Θ+…)と考えることで、曲線 を A、B、C、…という係数の集合として表現する方法である。時系列データの変 動を単振動の組み合わせとして表現する。ある時刻tの変動量D(t)は と表される。ここで、f(i)の周波数で振動する成分が強度 G(i)を持つとする。 実際の変動においては、n値(解析する周波数の数)は必ずしも有限ではない が、解析する際には、有限であるとする(解析による誤差発生要因の一つ)。 この変動を FFT 法で解析すれば、周波数 f(i)にピークを有し、強度が G(i)に依
存する分布を得る。この解析により、どの周波数成分が変動において主たる成 分であるかを解析する。不連続性を表現するためには、解析値(スペクトル分 布)は幅広い周波数成分を持つ必要がある。そこで、データ列の最初と最後で 連続的に0値になるような関数(窓関数;ハニング窓、ハミング窓と呼ばれる) をデータ列にかける。この窓関数により不連続性は無くなるが、データを歪め たことにより理想値と異なる。n 点の連続データをセグメントに分割し、それぞ れについて解析して得られた指標の経時変化を追うことで、時系列データの特 徴を捉えることができる。 図 2-11 では心電図の周波数分析について述べる。自律神経系によって制御さ れている心拍変動及び血圧変動には、ゆらぎの成分がみられる。心拍変動には 周波数帯域の異なる 2 つの変動成分がある。呼吸周波数と同じ周波数である高 周波(high frequency, HF, 0.15-0.45Hz)域における成分は、血圧では第 2 級 変動、心拍数では呼吸性洞性不整脈(respiratory sinus arrhythmia, RSA)と 呼ばれ、立位時低下することが知られている。RSA の発生には、主として脳幹に おける呼吸中枢から心臓血管中枢への干渉と、肺の伸展受容体からの心臓血管 中枢への入力が関与する。また、約 10 秒の周期をもつ成分である低周波(low frequency, LF, 0.04-0.15Hz)成分は、血圧の第 3 級変動、あるいは Mayer wave と呼ばれ、これが圧受容体反射を介して心拍に現われたと考えられるものを Mayer wave related sinus arrhythmia(MWSA)と呼ぶ。LF 成分は、HF 成分と は反対に、立位時に増加する傾向があることが知られている。血管運動性交感 神経活動による血管収縮反応は、交感神経の興奮から約 5 秒遅れて生ずること が報告されており、この遅れによって血圧調節系に振動が起こり、血圧に約 10 秒の周期のゆらぎを生ずることが理論的に明らかにされている。これらの成分 と自律神経系の活動との関わりについては、神経の切除手術や、薬品の投与な どの実験的な所見から解明されつつある。選択的に副交感神経系の活動性を遮 断する迷走神経切除術、あるいは atropine の投与によって LF 成分、HF 成分が 共にほぼ消失すること、交感神経系の活動性を遮断するβ受容体剤の投与によ り LF 成分が減弱することから、HF 成分はほぼ副交感神経系の活動性のみを反映
しているのに対し、LF 成分は交感神経系と副交感神経系の両方の活動性を反映 しているということが分かる。そこで、LF 成分と HF 成分の比である LH/HF 値が 交感神経系の活動性を示す指標として用いられている。LF 成分と HF 成分を媒介 する自律神経の差異は、交感神経と副交感神経による心拍調節の間の周波数特 性の差に起因する。副交感神経は 0Hz から 0.5Hz 付近までの心拍変動を伝達す るのに対し、交感神経は 0Hz から 0.15Hz までの心拍変動しか伝達できない。つ まり、副交感神経の変動は高い周波数まで心周期の変動に反映されるが、交感 神経活動の変動は、たとえそれが高い周波数の変動を含んでいても、0.15Hz 以 下のゆっくりした変動だけが心周期の変動として現れる(図 2-11)。 2-5-2-2. 自己回帰(Autoregressive, AR)法 ゆらぎが定常状態の自己回帰過程に従うと仮定して周波数を分離している。 AR モデルでは、現時点の値を過去の時点の値の線形結合で表現し、非線形部分 を “ゆらぎ”として、白色雑音と仮定している。しかし、実際、時系列の“ゆ らぎ”は、厳密には非線形効果を含み、非線形部分を白色雑音で補うことは、 時系列モデルとしては任意の時系列に成り立つような普遍的な条件ではなく、 AR 法を自己相似的な時系列に適用することはできない。AR 法では、選定される ラグ値が小さい値となってしまうために、スペクトル分解能は著しく低下し、 時系列の周期構造を決定できない。このために、自己相似的構造を本質とする 時系列の解析には限界がある。即ち、大きな時間スケ-ルの“基底変動”を取 り出すことが出来ないため、時系列の多重周期構造を解明できない。
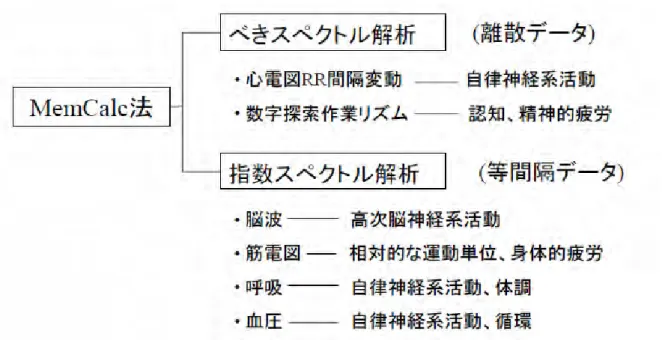
2-5-2-3. 最大エントロピー法(Maximum Entropy Method, MEM)および MemCalc 法
MEM はゆらぎが定常状態の自己回帰過程に従うと仮定して周波数を分離する 方法である。FFT 法よりも短いデータで解析が可能であり、窓関数などの処理が 不必要で、もとのデータをそのまま使えるのも利点である。スペクトルの分解 能も高く、定量性に優れているとされる。FFT 法と同様に、周波数が低くなるに
従いパワーが増大する成分(非調振動和成分)が認められ、DC 成分とも呼ばれ ている。この成分は周波数が 0 に近付くと急速にパワーが増加する。複数の周 波数により構成されている時系列データから重畳した複数の余弦関数を抽出し、 解析するのに有利である。欠点としては、データの測定間隔が不均等の時は適 用しにくいこと、パワー及び分散が推測できないことである。 次に、MEM の一種である MEM+非線形最小二乗あてはめ法(MemCalc 法51-54)、図 2-12)について述べる。この方法は、唯一、得られたスペクトルの妥当性を検 証することができる。時系列の“基底変動”を決定するために、周波数領域の 解析としての MEM と、時間領域の解析としての非線形最小二乗あてはめ法を用 いている。このとき MEM によって得られた周期構造を用いて、非線形最小二乗 法を線形化し、解の一義性を保証している。 時々刻々変動する“ゆらぎ”を明らかにするためには、大きな時間スケール にわたる小さな時間スケールでの解析(“瞬間スペクトル”を求めることを意 味する)が必要である。この方法では、時系列の変動を生み出すシステムの“瞬 間”の構造を問題にする立場から、時系列のセグメント解析を可能にした。 こ の方法では、大きな時間スケールで解析を行う場合、大きな時間スケールの変 動を“基底変動”とみなし、小さな時間スケールの変動をその“基底変動”に 対する“ゆらぎ”とみなして解析を進めることで、フラクタル構造をもつ時系 列の解析を可能にした。セグメント解析により、ある周波数帯におけるスペク トルの傾きとは、周波数の変化に伴ってその周波数近傍のパワーがどのように 変化するか、指定周波数帯全体にわたるその変化の傾向であるとすることがで きる。従ってこの方法を用いたシステムでは MEM スペクトルからある周波数の 近傍の(平均)パワーを計算し、これらの値(周波数、パワー)の系列について最 小二乗法により傾きを求めることになる。このシステムではスペクトルが鋭い ピークをもつ場合でもその面積が正確に計算されることから、より鋭いピーク の存在が算出するスペクトルの傾きに悪影響を及ぼすことはない。この方法の 特徴は、AR 法はラグ値が非常に小さな値になることでスペクトル分解能を著し く低下させていたが、MEM では可能な限りラグ値を大きくすることで従来の MEM
の限界を克服した。
図 2-11: 左図:安静時 9 分間の心拍変動、右図:心拍変動のスペクトル Mayer wave 成分と呼吸性変動成分は周期成分であるので、周波数解析により二峰性のピー クを持つ。
第3章 睡眠検査指標と自律神経活動評価指標との関連性
3-1. 閉塞型睡眠時無呼吸低呼吸症候群における自律神経活動
3-1-1. はじめに 睡眠は、内分泌系、免疫系、感覚系および自律神経系と密接な関連性を持っ ている。特に自律神経系と睡眠の間の関連性については多くの研究が行われて おり、自律神経系の交感神経と副交感神経とがうまくバランスを取ることによ って良質の睡眠が得られることが報告されている 55-56)。通常、睡眠時は副交感 神経が優位となり、血圧を下げ、脳への血流を減らして、眠くなる。しかし、 そのバランスが崩れると、交感神経が優位となり、血圧を上げ、脳への血流量 を増やし、同時に心拍数を上げて、眠気を覚ますことになる。このように自律 神経活動と循環器系は密接な関係にある。このため自律神経系の活動、すなわ ち、交感神経および副交感神経の活動状態を測定するために心電図 RR 間隔を測 定し、そのパワースペクトルなどの変化が調べられている24,57)。 近年、肥満や脂質代謝異常などのさまざまな生活習慣病において SAS の合併 が指摘されている。また、虚血性心疾患者では OSAHS を合併することがしばしば で、その予後は OSAHS の重症度に規定されることが報告されている58)。OSAHS の 重症度は、睡眠 1 時間あたりの AHI で評価され、AHI が 5 以上で睡眠時無呼吸・ 低呼吸と診断され、5~20 を軽症、20~30 を中等症、30 以上を重症と分類する 44)。OSAHS の症状は、上気道が閉塞しているために睡眠中のはげしいいびきを 伴う無呼吸や低換気と日中の過剰傾眠を特徴とする。OSAHS では自律神経のバラ ンスが崩れ、交感神経活動の亢進が睡眠時のみでなく、覚醒時にも認められる ことが報告されている 59-61)。この交感神経活動亢進の機序としては、無呼吸に 伴っておこる低酸素血症、高炭酸ガス血症、低心拍出状態、覚醒反応などが考 えられている 24,59-65)。また、OSAHS では無呼吸の出現と同期する心拍数の変動 も認められる。そして、この変動は心拍変動のスペクトル解析では低周波成分よ りもさらに低周波な成分(VLF,0.0033-0.04Hz)として捕らえられる可能性があることが報告されている24-28)。 そこで本研究では、まず OSAHS 患者の心電図 RR 間隔について 24 時間測定を 行い、得られたデータについて周波数解析を行い、この結果を健常者のそれと 比較することにより、OSAHS 患者の自律神経活動状態の特徴を明らかにする。次 に、無呼吸の出現と同期していると考えられている VLF が無呼吸の程度を表す AHI とどのような関係を持っているかを検討した。 3-1-2. 対象・方法 PSG 検査を施行して OSAHS と診断された症例 25 例、および肥満、高血圧、糖 尿病、高脂血症、喫煙習慣などの冠危険因子がなく、睡眠中の無呼吸症状のな い年齢、性を一致させた健常者 10 名を対照群とした。 事前に被験者全員に検査の趣旨を説明し同意を得た。また、行動記録表への記 入を依頼し、就寝および起床時間を確認した。検査実施時に身長、体重測定お よび既往歴をカルテまたは対象者から直接聴取し、血圧測定および血液の生化 学検査を実施した。 記録にはホルター心電図装置(FM-100、フクダ電子株、東京)を用い、24 時 間測定によって得られた洞調律の RR 間隔について周波数解析を実施した。得ら れたパワースペクトルから高周波成分として HF パワースペクトル値(HF パワー 値)、低周波成分として LF パワースペクトル値(LF パワー値)、および VLF パ ワースペクトル値(VLF パワー値)を測定した。自律神経の副交感神経活動指標 として HF パワー値を、交感神経活動指標として低周波数成分/高周波数成分の 比(LF/HF 値)を用いた。
統計学的検定には AVOVA 解析を用い、有意なものについては Mann Whitney ’s
test を行った。検定の有意は P <0.05 をもって有意と判定した。心拍変動と
AHI との相関係数の検定には回帰分析を用いた。
3-1-3. 結果
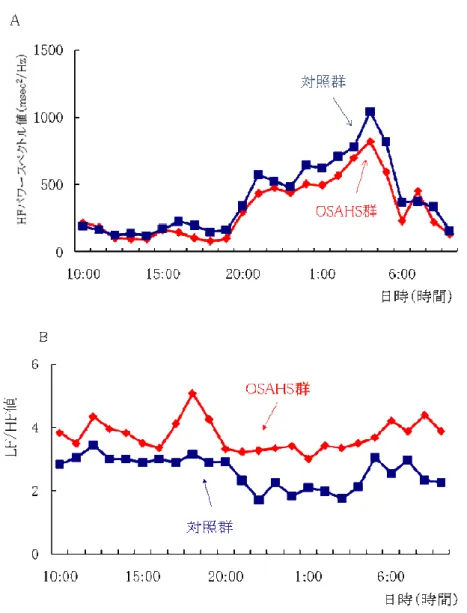
尿酸、中性脂肪および総コレステロールの数値をまとめたものである。OSAHS で は BMI が有意に高値を示し、また、血中の尿酸、中性脂肪、総コレステロール も有意に高かった。 表 3-1. 被験者の特徴 OSAHS群 対照群 (平均値±標準偏差) (平均値±標準偏差) 被検者数(男/女) 25(24/1) 10(10/0) 年齢 51±14 54±11 BMI (Kg/m2) 29.5±6.5 * 23.5±4.4 収縮期血圧 (mmHg) 139±17 128±14 拡張期血圧 (mmHg) 87±10 79±8 尿酸 (mg/dl) 7.21±1.4 * 5.3±0.9 中性脂肪 (mg/dl) 196±107 * 113±34 総コレステロール(mg/dl) 210±34 * 161±37 *P < 0.05 図 3-1A は、OSAHS 群および対照群における HF パワー値の日内変動を示して いる。各プロット点は1時間ごとのパワースペクトルの平均値である。HF パワ ー値は OSAHS 群および対照群ともに覚醒時と比較して睡眠時に増大傾向を示し、 その最高値はともに早朝 5 時であった。一方、図 3-1B は、LF/HF 値の日内変動 を示しており、各プロット点は1時間ごとの LF/HF 値の平均値である。LF/HF 値 は、両群ともに日内変動は小さかったが、OSAHS 群は対照群に比べ常に高めであ った。表 3-2 は、これらの結果を 24 時間、覚醒時(10:00am-6:00pm)および睡 眠時(0:00am-6:00am)の時間帯における各群の HF パワー値および LF/HF 値を まとめたものである。以上の結果より、OSAHS 群では、対照群に比べて睡眠時に HF パワー値が有意に低下し、逆に LF/HF 値は常に有意に高いことがわかった。
図 3-1.OSAHS 群と対照群の HF パワー値および LF/HF 値の 24 時間変動 表 3-2.OSAHS 群と対照群の各時間帯の HF パワー値と LF/HF 値 OSAHS群 対照群 (平均値±標準偏差) (平均値±標準偏差) 24時間 HF (msec2/Hz) 124±83 * 379±168 LF/HF 値 2.51±1.81 * 1.68±0.93 覚醒時 (10:00am-6:00pm) HF (msec2/Hz) 110±79 * 232±140 LF/HF 値 3.97±2.08 * 2.47±1.01 睡眠時 (0:00am-6:00am) HF(msec2/Hz) 478±426 560±560 LF/HF 値 3.06±2.10 * 1.85±1.34 *P < 0.05
次に、睡眠検査において OSAHS の重症度を表す AHI と自律神経活動を示す HF パワー値および LF/HF 値との関係を調べた。図 3-2 は、この結果を表している。 図 3-2A は AHI と HF パワー値との関係を示したものである。AHI の増加に伴い、 HF パワー値は大きく増加している。回帰分析を行った結果、指数関数曲線が最 もフィットしており、その式は y=47.27e0.032x となり、相関係数は 0.677 と有 意な相関を認めた。一方、AHI と LF/HF 値との関係は、回帰分析の結果、y= 1.421e0.016xとなり、その相関係数は 0.358 であった。このことから、AHI と自律 神経活動とは相関があることが示唆された。 図 3-2.PSG 検査による AHI と HF パワー値および LF/HF 値との関連 A: AHI と HF パワー値の関係、B: AHI と LF/HF 値の関係
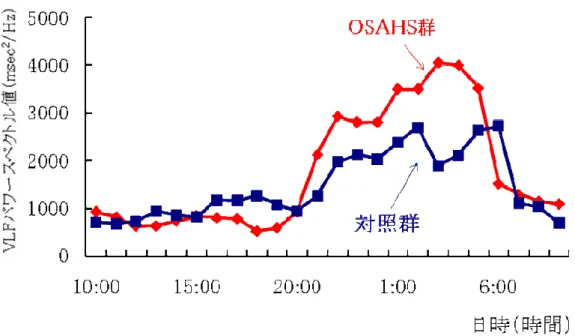
最近、0.0033-0.04 Hz という VLF が無呼吸の出現と同期しているのではない かとの報告がある24-28)。そこで、まず、OSAHS 群と対照群における VLF パワー 値の日内変動を調べた。図 3-3 はこれをまとめたものである。各プロット点は 1時間ごとの平均値を示している。この図より、睡眠時において OSAHS 群が対 照群に比べて VLF パワー値が増加していることがわかる。 表 3-3 は、24 時間、覚醒時(10:00am-6:00pm)および睡眠時(0:00am-6:00am) の時間帯における各群の VLF パワー値の平均値を示している。OSAHS 群、対照群 ともに覚醒時に比べて睡眠時では有意な増大を示していることがわかる。また、 24 時間を通して OSAHS 群では対照群に比べて常に有意に高かった。 そこで、PSG 検査で求めた AHI と VLF パワー値との関係を調べた。図 3-4 はそ の結果を示したものである。AHI の増加に伴い VLF パワー値は急激な増加を示し ており、回帰分析の結果、y=1045e0.024xで、R2=0.271(r=0.521)と有意な相関を 示した。
図 3-3. OSAHS 群と対照群における VLF パワー値の 24 時間変動 表 3-3. OSAHS 群と対照群の 24 時間、覚醒時、睡眠時における VLF パワー値 OSAHS群 対照群 VLF (msec2/Hz) (平均値±標準偏差) (平均値±標準偏差) 24時間 1739±787* 383±237 覚醒時 (10:00am-6:00pm) 1075±593* 718±604 睡眠時 (0:00am-6:00am) 3611±4246* 1842±1143 *P < 0.05 図 3-4. AHI と VLF パワー値との関連
3-1-4. 考察 OSAHS 患者はしばしば日中過度な眠気により交通事故や作業事故を起こすな ど重大な社会生活上の支障をきたすことがあり、日常生活面で QOL(quality of life) が低下している。OSAHS 発症のリスクファクターとしては、小顎症、扁桃肥 大などの局所の解剖学的異常33-36)、それに加えて、男性、加齢、肥満、家族性因子、 喫煙などがあげられる。また、OSAHS 患者は高血圧、虚血性心疾患、糖尿病なの 生活習慣病と密接に関連する疾患として位置付けられている 66-67)。しかし、最 近の多くの臨床成績は交感神経活動の抑制により心機能や予後が改善されるこ とを示しており8)、積極的な診断と治療が望まれる。 今回、OSAHS 群について、対照群との比較から検討を行った。その結果、OSAHS 群では BMI が有意に高値を示し、肥満がリスクファクターとなっていることが 確認された。また、OSAHS 群では血中の尿酸、中性脂肪、総コレステロールも有 意に高値を示した。さらに、虚血性心疾患を合併した症例は 25 例中 5 例(20%)、 高血圧を合併した症例は 25 例中 17 例(65.4%)と高率であった。 従って、本症 を早期に診断し、治療することは非常に重要である。 OSAHS 患者では対照群と比較し、HF パワー値は覚醒時には減少を示したこと から、覚醒時には副交感神経活動が抑制され、交感神経活動が優位であること が示唆された。また、OSAHS 群では対照群に比較して、LF/HF 値は終日、高値で あり、常に交感神経活動が優位に働いていることが示唆された。低酸素暴露下 では交感神経活動が有意に上昇し、交感神経活動上昇と肺動脈圧上昇が正相関 を示すとの報告がある24)。無呼吸を有する患者では覚醒時でも筋交感神経活動 や血漿ノルエピネフリン濃度が有意に高く、交感神経の亢進が睡眠時だけでな く覚醒時にも持ち越されると報告されている6-8)。本検討におい OSAHS 群では睡 眠時だけでなく覚醒時の LF/HF 値も有意に高値を示したことは覚醒時にも低酸 素状態にあることを示唆しているのかもしれない。低酸素性肺血管痙縮による 肺高血圧と交感神経作用とが相乗的に作用して、特に睡眠中に重篤な循環系の トラブルが起こりやすい状態となると考えられ、早期の治療が必要である。 今回、VLF パワー値は、両群でともに覚醒時に減少、睡眠時に増大していた。さ
らに OSAHS 群では対照群と比較して睡眠時の VLF パワー値が有意に高値を示し た。Akselrod ら 24)によれば、心拍数および酸素飽和度の変動を周波数解析する と、ともに無呼吸の周波数のところでコヒーレンスが高値を示し、VLF は無呼吸 の周期を反映すると報告している24-28)。また、塩見ら26)は、睡眠時無呼吸では 無呼吸中は徐脈を、無呼吸後の覚醒反応時には頻脈を生じると報告している。 その特徴的な不整脈は、25 秒から 120 秒の周期で繰り返す夜間睡眠中の呼吸変 動に一致した洞徐脈頻脈であるとしている。すなわち、レム睡眠時に生じる無 呼吸の短い周期が 25 秒、ノンレム睡眠時に生じる無呼吸の長い周期が 2 分であ ることから、周期は 0.008Hz から 0.04Hz で繰り返し表れ、VLF が睡眠時に増大 するとしている。J.Thomas ら25)は心筋梗塞慢性期の患者について心拍変動を心 不全の有無、左室駆出率の低下、ホルター心電図にみられる心室頻拍、加算平 均心電図にみられる心室遅延電位などの因子と比較した。その結果、心拍変動に よる VLF 指標は不整脈が原因となる死亡率との関連性が強く、生命予後の予測 に特に有用であると報告している24-28)。今回のわれわれの検討によると、OSAHS 群の心拍変動では、睡眠時の VLF パワー値が異常な増大を示し、塩見ら 26)の報 告を支持する結果を得た。 無呼吸や低換気の発生頻度を表す指標としては AHI が用いられている。AHI が 1 時間 5 回以上の場合、睡眠時無呼吸症候群と診断され、1 時間 40 回以上を重症 とする診断法が広く用いられている。本検討では、VLF パワー値と AHI の相関係 数が 0.521 と正の相関を示し、関連性が示唆されたことから、塩見ら26)の報告 のように VLF パワー値は OSAHS の重症度を反映する指標として有用である可能 性が考えられた。
3-2. 閉塞型睡眠時無呼吸低呼吸症候群における重症度と自律神経
活動
3-2-1. はじめに OSAHS は、睡眠時の上気道閉塞による呼吸障害により睡眠障害をきたす疾患で あり、呼吸障害に関連して脳波上覚醒反応や低酸素刺激による交感神経活動の 上昇が認められる 24,59-65)。われわれは、OSAHS 患者について、睡眠呼吸障害の 重症度の指標とされる AHI と心拍変動の周波数解析による自律神経活動につい て検討し、AHI が増加すると交感神経活動が亢進し、相対的に副交感神経活動が 低下するという関係を認め、睡眠呼吸障害の重症化に伴い交感神経活動が優位 になると考えられると報告した68)。また、前節で、AHI と無呼吸発生に関与して いると言われている VLF パワー値との間にも有意な相関が認められることを述 べた。しかしながら、OSAHS の重症度と自律神経活動と睡眠との関連性について 検討した報告は少ない。そこで、今回、私は、対象を AHI による重症度別に分 類し、重症度と自律神経活動との関係について検討した。 3-2-2. 対象・方法 OSAHS が疑われ、PSG 検査の目的で 2005 年 10 月から 2007 年 4 月の間に東北 大学病院感染症呼吸器内科に入院した 33 例、31~82 歳(56.2±14.7 歳、平均 ±標準偏差)を対象とし、PSG と携帯型生体信号計測器(PBSM、MemCalc-Makin2、 GMS 株、東京)による心電図測定を午後 8 時から翌朝 6 時まで施行した。睡眠段階の判定31-32)とともに、AHI、Arousal Index および ODI を算出した。AHI につ
いては、AHI 5 未満の健常群および 5 以上 15 未満の軽度障害群、15 以上 30 未 満の中等度障害群および 30 以上の重度障害群に分類した 44,69)。一方、Arousal Index については 30 未満と 30 以上の 2 群に分類した44,70)。 心臓の自律神経活動は、CM5 誘導(-電極:右胸骨上端、+電極:胸部 V5、 ボディアース:右側胸部)により心電図を導出し、交感神経活動の指標である LF/HF 値、及び副交感神経活動の指標である HF 成分のパワー値を求めた。
検討した測定値は平均値±標準偏差で表示し、統計学的検討は ANOVA 分散分析 を行い、有意なものについて Mann Whitney’s U test を実施した。また、危険 率5%以下を有意とした。さらに、相関については回帰分析を行い、その有意 性を検討した。 3-2-3. 結果 図 3-5、図 3-6、図 3-7 および図 3-8 は、それぞれ AHI で分類した 4 群、すな わち、健常範囲群(AHI5 未満)、軽度睡眠呼吸障害群(AHI5 以上 15 未満)、 中等度睡眠呼吸障害群(AHI15 以上 30 未満)および重度睡眠呼吸障害群(AHI30 以上)のそれぞれ1症例を示している。 図 3-5.AHI5 未満の生理的範囲内の症例の一例 無呼吸低呼吸の回数が生理的範囲内で、深睡眠(stage3、4)が存在する。
図 3-6.AHI が 5 以上 15 未満の軽度睡眠呼吸障害症例の一例 軽度の無呼吸低呼吸があり、それに伴い微小覚醒が存在する。
図 3-7.AHI が 15 以上 30 未満の中等度睡眠呼吸障害症例の一例 無呼吸低呼吸の回数が中程度で、それに伴い中途覚醒が出現している。
図 3-8.AHI が 30 以上の重度睡眠呼吸障害症例の一例 無呼吸低呼吸が頻繁に出現し、中途覚醒が多く、深睡眠は得られない。
これらの PSG 記録から AHI を求め、AHI により OSAHS 群 33 例を、5 未満の 6 例、5 以上 15 未満の 8 例、15 以上 30 未満の 6 例および 30 以上の 13 例の 4 群 に分類した。また、この AHI による分類に従い、PSG 記録から得られた深睡眠比 率およびレム睡眠比率を求めた。さらに、浅睡眠期(Stage 1+2)、深睡眠期(Stage 3+4)およびレム睡眠期(Stage REM)の時間を計算し、このステージ別における HF パワー値および LF/HF 値を求めた(表 3-4)。この表より、AHI30 以上の重度群 では AHI5 未満の健常範囲群に比較して深睡眠比率およびレム睡眠比率が有意に
減少していることがわかった。また、重度群においては、深睡眠期、浅睡眠期 およびレム睡眠期のいずれも HF パワー値が他の3群に比べて有意に減少してい ることがわかった。一方、LF/HF 値については、浅睡眠期に有意に増加していた。 これらのことは、OSAHS 群は睡眠時に交感神経が優位になっているというよりも、 むしろ副交感神経の活動状態が有意に低下しており、その結果、交感神経活動 が優位になっていることを示唆している。 表 3-4. AHI の数値により 4 群に分類した各群の特徴
AHI<5 5≦AHI<15 15≦AHI<30 30≦AHI
(平均値±標準偏差) (平均値±標準偏差) (平均値±標準偏差) (平均値±標準偏差) 6(5/1) 8(7/1) 6(5/1) 13(11/2) 53.1 ± 11.9 60.2 ± 10.6 57.2 ± 11.5 57.1 ± 15.2 16.0 ± 7.8 13.2 ± 6.3 13.2 ± 9.3 7.5 ± 4.7* 15.6 ± 6.4 12.7 ± 8.1 12.6 ± 8.4 10.2 ± 5.3* HF (msec2/Hz) 476.3 ± 585.1 469.4±630.4 421.2±375.4 212.8 ± 187.9* LF/HF値 2.54 ± 1.65 2.31±1.01 3.82 ± 2.54 4.02 ± 3.54* HF (msec2/Hz) 526.4 ± 647.5 443.9 ± 545.2 370.9 ±324.7 194.2 ± 136.5* LF/HF値 1.52 ± 0.61 1.30 ± 0.40 2.72 ± 3.38 1.97 ± 1.83 HF (msec2/Hz) 384.7 ± 306.0 475.1 ± 672.2 449.0 ±513.4 145.4 ± 97.2* LF/HF値 4.79 ± 3.10 3.75 ± 2.06 5.78 ± 5.06 6.26± 5.98 *P < 0.05 被験者数 (男/女) Stage REM 年齢 (歳) 深睡眠比率 (%) レム睡眠比率 (%) Stage 1+2 Stage 3+4 次に、AHI の睡眠呼吸障害重症度別に睡眠段階と自律神経活動を比較検討した。 図 3-9A は、AHI で分類した 4 群について、睡眠段階別に HF パワー値をプロット したものである。各群の睡眠段階別の変化を見ると、AHI が5未満の正常範囲群 の HF は、浅睡眠期および深睡眠期に比較してレム睡眠期に減少を示しているが 有意な減少としては認められなかった。他の3群についても同様であった。図 3-9B は、それぞれの睡眠段階で AHI による 4 群を比較したものである。これを 見ると、重度障害群は健常範囲群および軽度障害群に比較して浅睡眠時および 深睡眠時に HF パワー値が有意に低下していた。また、レム睡眠期には重度障害 群は健常範囲群とは有意差を示さなかったが、軽度障害群および中等度障害群 と比較して有意に減少を示した。このことは、睡眠呼吸障害の重症化に伴い副 交感神経活動状態が抑制されることを示唆している。
一方、図 3-10A は、AHI で分類した 4 群について、睡眠段階別に LF/HF 値を示 したものである。これを見ると、健常範囲群ではレム睡眠期の LF/HF 値は浅睡 眠期および深睡眠期のそれに比べて有意に増加していた。軽度障害群、中等度 障害群および重度障害群については、レム睡眠期の LF/HF 値は深睡眠期に対し てのみ有意に増加していた。図 3-10B は、それぞれの睡眠段階で AHI による重 症度別に 4 群の LF/HF 値を比較したものである。重度障害群の LF/HF 値は健常 範囲群および軽度障害群のそれに比べて有意に増加していた。このことは重度 障害群では浅睡眠期に交感神経活動が促進することを示している。 図 3-9. AHI で分類した 4 群それぞれの各睡眠段階間の HF パワー値 A:睡眠段階別の比較、B:AHI の重症度による比較
図 3-10.AHI で分類した 4 群それぞれの各睡眠段階間の LF/HF 値 A:睡眠段階別の比較、B: AHI の重症度による比較 次に、睡眠中の覚醒反応の割合を示す Arousal Index が 30 未満の群 13 例と 30 以上の群 20 例に分類し、同様に HF 成分のパワー値および LF/HF 値を両者間 で比較した。図 3-11A は睡眠段階別の各群の HF パワー値を示している。Arousal Index が 30 未満の群では、浅睡眠期の HF パワー値に比較して深睡眠期およびレ ム睡眠期のそれは減少を示したが有意差は認められなかった。Arousal Index が 30 以上の群でも有意な変動は認められなかった。図 3-11B は、それぞれの睡眠 段階に対して Arousal Index で分類した 2 群の HF パワー値の平均値を比較した ものである。全ての睡眠で Arousal Index が 30 以上の群は Arousal Index が 30 未満の群に比べて有意に低値であった。これは、Arousal Index が 30 以上では
副交感神経の活動状態が異常に低下していることを示している。
一方、図 3-12A は LF/HF 値の平均値についての結果である。Arousal Index が 30 以上の群では、深睡眠期のそれは浅睡眠期およびレム睡眠期のそれに比べて 有意に低下していた。また、睡眠段階の比較では、深睡眠期のみで、30 以上の 群で有意に低値であった(図 3-12B)。これらのことから、Arousal Index が 30 以上の群では深睡眠期に交感神経および副交感神経の両活動が低下しており、 自律神経機能の全体的な低下を示していることが示唆された。 図 3-11. Arousal Index の数値により 30 未満と 30 以上の 2 群に分類した各群 の HF パワー値 A:睡眠段階別の比較、B:Arousal Index の重症度による比較