改良 PCR 法を用いた健常成人の肺炎球菌保菌検出と莢膜型同定
1)椙山女学園大学看護学部,2)名古屋大学医学系研究科臨床感染統御学,3)愛知教育大学教育学部
石原 由華
1)2)岡本 陽
3)太田美智男
1)(平成 26 年 5 月 26 日受付)
(平成 26 年 11 月 10 日受理)
Key words : Streptococcus pneumoniae, PCR, capsule, serotype
要 旨
健常者の肺炎球菌保菌調査はこれまで咽頭培養によって行われてきた.しかし健常者に少数保菌されてい る肺炎球菌を, α 溶血を示す多数の常在口腔レンサ球菌の中から検出するのは容易ではなく,保菌頻度が低 く見積もられる恐れがある.近年 PCR による肺炎球菌検出法が報告されているので,我々は健常者咽頭ぬ ぐい液の混合増菌培養液から PCR によって肺炎球菌を検出し,さらに莢膜型を決定する改良法を検討した.
2011〜2013 年に名古屋市内の 40 歳以上の健常者 110 名から咽頭ぬぐい液を採取し,混合増菌培養液から DNA を抽出して PCR により肺炎球菌特異的遺伝子 lytA を検出した.さらに lytA 陽性混合培養液から PCR により,23 価ワクチンに含まれる莢膜型遺伝子を個別に検出した.その結果 110 名中 36 名(32.7%)が lytA 陽性で,肺炎球菌を咽頭に保菌していると考えられた.この結果は従来の培養法による健常者保菌報告と比 べて高かった.したがって PCR 検出法は健常者の肺炎球菌保菌をより高感度に検出すると思われる.さら に,36 名の lytA 陽性混合培養液から 28 名の 23 価莢膜型菌保有者を PCR で決定することができた.検出 された莢膜型の頻度は 14 型が最も多く,次いで 4,18C,6A ! B,の順だった.1,5,10A 型菌はそれぞれ 少数検出された.なお,lytA 陽性者 36 名の中で PPV23 を接種していたのは 5 名であり,そのうち 4 名が 保菌する菌が PPV23 に含まれていた.本研究により,PCR による莢膜型同定は,型血清による莢膜型決定 法が不可能な混合培養菌液でも可能であり,検出感度も良く,再現性に優れていることが明らかとなった.
〔感染症誌 89:375〜381,2015〕
序 文
肺炎球菌は成人の市中肺炎の主要原因菌であり,鼻 咽頭に定着して敗血症のような侵襲性肺炎球菌感染症
(invasive pneumococcal diseases,IPD)をしばしば 引き起こし致命的となる
1).肺炎球菌は病原因子とし て多糖体からなる莢膜をもち現在 93 の莢膜型に分類 されるが
2),特定の莢膜型菌が過去に流行する一方で
3), 国や地域で異なる様々な莢膜型の菌が分離されてい る
4).
23 価肺炎球菌ワクチン(PPV23)は 23 種類の莢膜 多糖体を含有する成分ワクチンであり,IPD の発症予 防のみならず高齢者肺炎に対する予防効果が報告され ている
5).そのため高齢者に対して本ワクチンの接種 が推奨されているが,接種率は 17.5% で依然他の先 進国に比べるとかなり低い
6).また PPV23 が普及した
欧米では PPV23 に含まれない莢膜型菌による IPD の 増加が報告されている
7).したがって一般市民の保菌 調査を定期的に行い,高頻度に保菌される莢膜型が PPV23 に含まれているのかどうかを常に監視する必 要がある.また老健施設などの入所者については,特 に施設内感染の防止のために肺炎球菌保菌とその莢膜 型の定期的な調査を行う必要がある.しかし健常者の 保菌する多種類の口腔レンサ球菌の多くは肺炎球菌と 同様に α 溶血を示し,その中から相対的に増殖が遅 い少数の肺炎球菌のコロニーを検出するのは容易では ないため
8),保菌の頻度について低く見積もられるな ど,培養分離法では信頼性のある結果を得ることが難 しい.Nagai らは肺炎球菌自己融解遺伝子 lytA を PCR で検出することによって特異的に肺炎球菌を同定でき ることを示し,他の論文でも確認された
9)10).さらに Pai らはマルチプレックス PCR によって莢膜多糖合 成遺伝子領域 cps 内の特異的配列を検出し,血清グ ループに型別できることを示した
11).また Carvalho
原 著別刷請求先:(〒464―8662)名古屋市千種区星が丘元町 17 番 地 3 号
椙山女学園大学看護学部 石原 由華
らは咽頭ぬぐい液の増菌培養液(混合培養液)を用い て PCR による lytA 遺伝子の検出とマルチプレックス PCR により莢膜型別が効率よくできることを示し た
12).そこで我々は中高年健常者の肺炎球菌保菌状況 を,咽頭ぬぐい液の混合増菌培養液から lytA 遺伝子 検出 PCR によって調べた.また lytA 陽性の混合増菌 培養液を用いて肺炎球菌の莢膜型同定を PCR によっ て行った.なお,予備実験で PCR の条件を検討し変 更した.また混合菌液では既報のマルチプレックス PCR 法による型別は必ずしも容易ではなく,単一の 莢膜型をそれぞれの条件の PCR で同定した.以上に より得られた中高年健常者の保菌状況を報告する.
方 法
1.対象者について
2011〜2013 年に人口 210 万人規模の市において市 内在住の本研究の趣旨の理解と同意を得られた 40〜
85 歳の健常者(本人が自覚する疾患を有さない者)110 名を対象とした.内訳は 40〜64 歳 38 名,65 歳以上 72 名であった.なお,本研究は椙山女学園大学看護学部 研究倫理審査委員会で承認された(承認番号:No.
108).
2.検体の培養ならびに DNA の抽出
Carvalho らの方法
12)をもとに,被験者の咽頭を滅 菌綿棒でぬぐい,全量 を 液 体 培 地(Mueller-Hinton Broth(日本 BD)5.0mL,rabbit serum(Life Technolo- gies)1mL,0.5% yeast extract(BD)100μL)に接 種した.37.0℃,CO
25% 下で 5 時間静置培養後,培 養混合菌液の 1.5mL を 20% グリセロール溶液とし て−80℃ で凍結保存し,残りの菌液を 70℃ で 30 分 間加熱後,4℃15,000rpm,1 分間遠心して,上清を捨 て沈殿を得た.100μL の lysis buffer(1% TritonX-100,
10mM Tris-HCl(pH 8.0),100mM NaCl,1mM EDTA
(pH 8.0))を加えて沈殿をピペッティングして懸濁し,
VORTEX で 10 秒撹拌した.懸 濁 液 を 100℃10 分 間 加 熱 後,4℃15,000rpm,1 分 間 遠 心 し,上 清 を PCR テンプレートとして−30℃ で保存した.
3.PCR 法による autolysin 遺伝子(lytA)検出
−30℃ 保存したテンプレート DNA を室温で解凍 後, lytA を PCR 法で検出した. lytA の検出プライマー は,Nagai ら
9)によって報告された配列(Table 1)を 用いた.増幅条件は 95.0℃5 分,94.0℃30 秒,54.0℃30 秒,72.0℃1 分とし,Thermal Cycler(Veriti Fast 100,
ABI)を用いて増幅反応を行った.Taq DNA polym- erase ならびに反応液は TaKaRa EX Taq(TaKaRa)
を用いた.反応後,定法にしたがって 1.2% アガロー スゲル電気泳動により増幅された DNA バンドを確認 し,lytA 陽性を肺炎球菌の保菌者とした.
4.莢膜型別について
lytA 陽性のテンプレート DNA に対して,肺炎球菌 の 93 種類の莢膜型の中で PPV23 に含まれる 23 莢膜 型について,PCR 法により莢膜型を決定した.既報 にしたがってマルチプレックス PCR による莢膜型別 を予備実験で行ったところ,混合培養菌液から抽出し たテンプレート DNA を用いた場合,単独培養菌液か ら得られたテンプレート DNA に比べて増幅されたバ ンドの判別が必ずしも容易ではなかった.したがって 莢膜型ごとに PCR を行い検出した.各莢膜型遺伝子 のプライマーは Pai ら
11)および Carvalho ら
12)によって 報告された配列を用いた(Table 1).なお既報に従っ て 6B の検出については 6A! B 検出プライマー,7F の検出については 7F! A 検出プライマー,9V の検出 には 9V ! A 検出プライマー,15B の検出には 15B ! C 検出プライマーをそれぞれ用いた.したがって 6A と 6B,7F と 7A,9V と 9A,15B と 15C の 莢 膜 型 に つ いてはそれぞれ区別できなかった.また 9N を検出す るプライマーは報告されていなかったので今回は検出 を行わなかった.PCR テンプレート DNA は lytA 検 出に用いた液を用いた.PCR の陽性対照菌株として Table 2にあげた菌株を用いた.上気道細菌叢研究会
(PRSP-BLNAR Research Group)株は明治製菓より 分与された臨床分離株である.ATCC 株は MicroBio- Logics より購入した.これらの陽性対照株は咽頭ぬ ぐい液を増菌した培地と同じ液体培地を用いて増菌 し,同様の手順でテンプレート DNA 液を得た.PCR の 反 応 条 件 は Nagai ら
9)な ら び に Pai ら
11)に 基 づ き 行ったが,アニーリング温度はそれぞれの莢膜型プラ イマーによって最適条件を再検討し Table 1に示した 値に設定後 PCR を行った.Taq DNA polymerase な らびに反応液,反応後の電気泳動は lytA 検出と同様 に行った.
結 果
1.lytA 陽性者の検出
混合増菌培養菌液を用いた PCR による lytA 遺伝子
の検出の条件をあらかじめ検討したところ,咽頭ぬぐ
い液の 5 時間培養で lytA の検出が可能であることが
わかった.したがって検体採取当日に培養を行い,直
ちにテンプレート DNA の抽出を行った.−30℃ に
分注保存したテンプレート DNA 液は少なくとも 1 カ
月間使用可能であった.被験者計 110 名中 PCR で検
出した lytA 陽性者は計 36 名であり,内 27 名が 65 歳
以上であった.lytA の陽性率は 2011 年秋の被験者で
は 36 名中 11 名(30.6%),2012 年秋の被験者では 39
名中 10 名(25.6%),2013 年秋の被験者では 35 名中
15 名(42.9%)であり,年度による違いがあるが健常
な中高齢市民の肺炎球菌保菌率は高い傾向を示した.
Table 1 Oligonucleotide PCR primers for the detection of lytA and serotyping. Primer pairPrimer sequence (5ʼ→3ʼ)Product size (bp)Annealing temperature (℃) lytA-fCAA CCG TAC AGA ATG AAG CGG30054 lytA-rTTA TTC GTG CAA TAC TCG TGC G 1-fCTC TAT AGA ATG GAG TAT ATA AAC TAT GGT TA28052 1-rCCA AAG AAA ATA CTA ACA TTA TCA CAA TAT TGG C 2-fTAT CCC AGT TCA ATA TTT CTC CAC TAC ACC29055 2-rACA CAA AAT ATA GGC AGA GAG AGA CTA CT 3-fATG GTG TGA TTT CTC CTA GAT TGG AAA GTA G37150 3-rCTT CTC CAA TTG CTT ACC AAG TGC AAT AAC G 4-fCTG TTA CTT GTT CTG GAC TCT CGA TAA TTG G43054 4-rGCC CAC TCC TGT TAA AAT CCT ACC CGC ATT G 5-fATA CCT ACA CAA CTT CTG ATT ATG CCT TTG TG36255 5-rGCT CGA TAA ACA TAA TCA ATA TTT GAA AAA GTA TG 6A/B-fAAT TTG TAT TTT ATT CAT GCC TAT ATC TGG25050 6A/B-rTTA GCG GAG ATA ATT TAA AAT GAT GAC TA 7F/7A-fTCC AAA CTA TTA CAG TGG GAA TTA CGG59954 7F/7A-rATA GGA ATT GAG ATT GCC AAA GCG AC 8-fCTA TAG ATA CTA GTA GAG CTG TTC TAG TCT20155 8-rCTA TAG ATA CTA GTA GAG CTG TTC TAG TCT 9V/9A-fGGG TTC AAA G TC AGA CAG TG A ATC TTA A81654 9V/9A-rCCA TGA ATG A AA TCA ACA TT G TCA GTA GC 10A-fGGT GTA GAT TTA CCA TTA GTG TCG GCA GAC62855 10A-rGAA TTT CTT CTT TAA GAT TCG GAT ATT TCT C 11A-fGGA CAT GTT CAG GTG ATT TCC CAA TAT AGT G46355 11A-rGAT TAT GAG TGT AAT TTA TTC CAA CTT CTC CC Primer pairPrimer sequence (5ʼ→3ʼ)Product size (bp)Annealing temperature (℃) 12F-fGCA ACA AAC GGC GTG AAA GTA GTT G37650 12F-rCAA GAT GAA TAT CAC TAC CAA TAA CAA AAC 14-fCTT GGC GCA GGT GTC AGA ATT CCC TCT AC20850 14-rGCC AAA ATA CTG ACA AAG CTA GAA TAT AGC C 15B/C-fTTG GAA TTT TTT AAT TAG TGG CTT ACC TA49652 15B/C-rCAT CCG CTT ATT AAT TGA AGT AAT CTG AAC C 17F-fTTC GTG ATG ATA ATT CCA ATG ATC AAA CAA GAG69355 17F-rGAT GTA ACA AAT TTG TAG CGA CTA AGG TCT GC 18-fCTT AAT AGC TCT CAT TAT TCT TTT TTT AAG CC57352 18-rTTA TCT GTA AAC CAT ATC AGC ATC TGA AAC 19A-fGTT AGT CCT GTT TTA GAT TTA TTT GGT GAT GT47850 19A-rGAG CAG TCA ATA AGA TGA GAC GAT AGT TAG 19F-fGTT AAG ATT GCT GAT CGA TTA ATT GAT ATC C30450 19F-rGTA ATA TGT CTT TAG GGC GTT TAT GGC GAT AG 20-fGAG CAA GAG TTT TTC ACC TGA CAG CGA GAA G51454 20-rCTA AAT TCC TGT AAT TTA GCT AAA ACT CTT ATC 22F-fGAG TAT AGC CAG ATT ATG GCA GTT TTA TTG TC64350 22F-rCTC CAG CAC TTG CGC TGG AAA CAA CAG ACA AC 23F-fGTA ACA GTT GCT GTA GAG GGA ATT GGC TTT TC38450 23F-rCAC AAC ACC TAA CAC ACG ATG GCT ATA TGA TTC 33F-fGAA GGC AAT CAA TGT GAT TGT GTC GCG33855 33F-rCTT CAA AAT GAA GAT TAT AGT ACC CTT CTA C
Table 2 Positive control strains for PCR-based serotyping.
Serotype S. pneumoniae strain Source
1 ATCC 6301 ATCC
2 ATCC 6302 ATCC
3 MSC-1267 Meiji Seika Pharma/PRSP-BLNAR Research Group 4 MSC-1110 Meiji Seika Pharma/PRSP-BLNAR Research Group
5 ATCC 6305 ATCC
6B MSC-1047 Meiji Seika Pharma/PRSP-BLNAR Research Group
7F ATCC10351 ATCC
8 ATCC 6308 ATCC
9A ATCC 8333 ATCC
10A ATCC 8334 ATCC
11A MSC-1271 Meiji Seika Pharma/PRSP-BLNAR Research Group
12F ATCC6312 ATCC
14 MSC-1245 Meiji Seika Pharma/PRSP-BLNAR Research Group
15B ATCC10354 ATCC
17F ATCC 6317 ATCC
18C ATCC10356 ATCC
19A MSC-1050 Meiji Seika Pharma/PRSP-BLNAR Research Group 19F MSC-1248 Meiji Seika Pharma/PRSP-BLNAR Research Group
20 ATCC 6320 ATCC
22F MSC-1710 Meiji Seika Pharma/PRSP-BLNAR Research Group 23F MSC-1249 Meiji Seika Pharma/PRSP-BLNAR Research Group
33F ATCC10370 ATCC
なお被験者に重複は無かった.
2.PCR によって決定した lytA 陽性者の莢膜型 PCR 法により,PPV23 に含まれるそれぞれの莢膜 型特異的 primer を用いて,lytA 陽性者 36 名に関し て 28 名の莢膜型を決定できた.ただし,lytA 陽性の 3 名について 6A と 6B は区別できなかった.したがっ て PPV23 に含まれる莢膜型菌の保菌率は 77.8%(あ るいは 69.4%)であった.lytA 陽性者 8 名の検体が PPV23 に 含 ま れ る 莢 膜 型 primer で は 増 幅 で き ず,
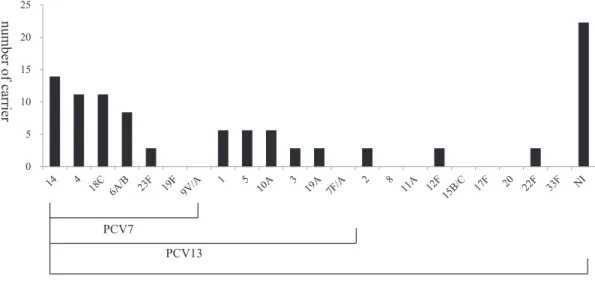
PPV23 以外の莢膜型菌を保菌していることが示唆さ れた.また,莢膜型を決定できた 28 名中 25 名(3 名 を 6B として)あるいは 22 名(3 名を 6A として)が 13 価小児肺炎球菌ワクチン(PCV13)に含まれる莢 膜型菌を保菌していることが示唆された.そのうち 7 価肺炎球菌ワクチン(PCV7)に含まれる莢膜型菌を 保菌していると思われたのは 17 名(あるいは 14 名)
であった(Fig. 1).
今回検出された莢膜型の中では 14 型が 5 名と最も 多く,次いで 4,18C,6A! B,1,5,10A 型の頻度順 にな っ て い た(Fig. 1).1,5,10A 型 は そ れ ぞ れ 2 検体と同数であった.PPV23 に含まれる莢膜型の中 で分離されなかったのは,19F,9V ! N,7F ! A,8,11A,
15B! C,17F,20,33F 型であった.
3.莢膜型と PPV23 接種の関連
2011〜2013 年の全被験者 110 名のうち過去 5 年以 内 に PPV23 を 接 種 し て い た の は 20 名 で 18.2% で あった.lytA 陽性者 36 名の中で PPV23 を接種して
いたのは 5 名であり,そのうち 4 名が保菌する肺炎球 菌の莢膜型が PPV23 に含まれている 4,10A,14 型 であった(Table 3).残りの 1 名は PPV23 に含まれ ない莢膜型菌を保有すると考えられた.
考 察
本研究では健常者の咽頭ぬぐい液から肺炎球菌を分 離培養せず,そのまま短時間混合増菌培養後,培養液 から直接肺炎球菌の検出を試みた.培養液から DNA を抽出してテンプレート DNA として用い,肺炎球菌 特異的遺伝子である lytA を PCR 法で検出し,lytA 陽 性を示す被験者を Nagai ら
9)や三鴨ら
10)の報告と同様 に肺炎球菌の保菌者とした.確認のためにそれらの陽 性反応を示した検体を血液寒天培地に塗抹培養したと ころ,一部の検体において,α 溶血を示したコロニー の中から肺炎球菌を疑わせるコロニーを分離すること ができ,肺炎球菌莢膜多糖抗原に対するラテックス凝 集反応キット(Slidex pneumo-Kit,シスメックス・
ビオメリュー社)を用いて肺炎球菌であることが確認
できた.しかし健常者の咽頭ぬぐい液の培養で出現す
る多数の α 溶血を示すコロニーの大部分は常在する
口腔レンサ球菌であり,肺炎球菌コロニーを見いだす
のは必ずしも容易ではなかった.また PCR で lytA 陽
性ではあるが肺炎球菌コロニーを見いだせない検体が
約 60% あった.したがって健常者に少数保菌されて
いる肺炎球菌を定法である血液寒天培地上で検出する
のは容易ではなく,検出の頻度は調査する個人の能力
と努力,熟練に依存すると思われた.
Fig. 1 Serotypes identified in the pharyngeal swab specimens from healthy adults.
Distribution of S. pneumoniae serotypes among PPV23 were identified for lytA-positive carriers with serotype-specific PCR.
PCV7, 7 valent pneumococcal vaccine for infants. PCV13, 13 valent vaccine modified for infants.
PPV23, 23 valent vaccine for elderly adults.
今回,混合増菌培養からの PCR 検出法による成人 健常者の肺炎球菌保菌率は 32.7% であり,従来の分 離培養法による本邦の保菌率の報告
13)より数倍高いこ とから,混合増菌培養からの PCR 検出法は分離培養 法に比べて検出感度が高いことが示唆された.また個 人の熟練に依存せず,検出に要する時間も分離培養法 に比べて短時間であった.今回の方法の普及により,
本邦における健常者の肺炎球菌保菌率は,より実情を 反映する値となることが期待される.
今回さらに我々は lytA 陽性咽頭ぬぐい液の混合増 菌培養液から抽出した DNA から,PCR による莢膜 型決定を試みた.
最も分離頻度が高かった莢膜型は 14 型で次いで 4,18C,6A! B などが多く検出された.Alanee らの 報告
14)では,10 カ国 21 施設から収集された,菌血症 を起こした成人患者 796 名(15 歳以上)から分離さ れた肺炎球菌株は 1 型が最も多く,次いで 14,4,3,
23F,6B 型の順になっており,14,4 型が多いのは我々 の結果と類似している.14,4 型菌は肺細胞に高い親 和性を有し肺炎の原因菌となりやすいこと
2)も関係し ているかもしれない.2006〜2007 年にかけて欧米,南 米,アジア,アフリカ地域から収集された 5 歳以下の 小児の IPD 感染症由来の 6 万株の解析報告
15)では,14 型が最も多く次いで 6B,1,23F,5 型の順になって いることから,地域,収集時期によって蔓延している 血清型が若干異なっていることが考えられる.また 3 型と 19F 型菌の感染は死亡率が特に高いとの報告
16)が
あるが,我々の結果では 3 型の検出頻度は低く,19F 型に関しては全く検出されなかった.この結果から,
常在型の肺炎球菌が侵襲性の感染症を必ずしも起こし ているわけではないことが推測された.なお,65 歳 以上の被験者由来肺炎球菌の血清型分布の傾向は全体 の集計結果と変わらなかった.
今回の解析では健常成人から検出された莢膜型の PPV23 のカバー率は最大 78.8% であり,千葉の報告 による IPD 症例分離株の 85% より低いが
2),一概に 比較することは難しいと思われる.今回用いた PCR 法によって,今後は対象・地域を広げて保菌されてい る莢膜型の傾向を調査する予定である.今回の調査で は PPV23 に含まれる莢膜型検出 primer を用いた.し かし約 20% の lytA 陽性者は PPV23 に含まれない莢 膜型菌を保菌していると思われる.今後,他の莢膜型 を検出する primer を用いて検出する範囲を広げ,そ れらの検体の解析を行う必要がある.また今回用いた primer では分別できない莢膜型の組み合わせについ ても,川口谷らの報告(第 87 回日本細菌学会総会抄 録 P1-050 p.143,2014)などを参考にして分別を試み る.
今回の被験者の中に,PPV23 を接種しているにも
かかわらず PPV23 に含まれている莢膜型を保有して
いるものが 4 名いた.したがって PPV23 による免疫
は,いわゆる粘膜免疫によって肺炎球菌の咽頭保菌を
減少させるというよりも,敗血症などの重症化を防ぐ
効果が期待されるワクチンと考えられる.あるいは,
Table 3 S. pneumoniae serotypes identified with PCR in the lytA-positive specimens.
Subject Serotype PPV23 vaccination*)
1 14 (−)
2 NI (−)
3 6A/B (−)
4 6A/B (−)
5 4 (−)
6 14 (−)
7 NI (−)
8 4 (−)
9 NI (−)
10 18C (−)
11 18C (−)
12 4 (+)
13 2 (−)
14 22F (−)
15 NI (−)
16 NI (−)
17 12F (−)
18 NI (−)
19 NI (+)
20 3 (−)
21 5 (−)
22 23F (−)
23 NI (−)
24 5 (−)
25 1 (−)
26 18C (−)
27 14 (−)
28 14 (−)
29 10A (+)
30 18C (−)
31 1 (−)
32 6A/B (−)
33 19A (−)
34 4 (−)
35 14 (+)
36 10A (+)
NI, not identified with the primers for PPV23 serotypes.
*), vaccinated during the past 5 years.
PPV23 の効果に個人差があり,感染防御に必要な十 分な抗体価を得られなかった可能性もある.
謝辞:本研究は文部科学省研究助成金「基盤研究 C,
24593541」ならびに椙山女学園大学研究助成金「平 成 25 年度学園研究 B」の助成によって行われた.
利益相反自己申告:申告すべきものなし
文 献1)Dockrell DH, Whyte MK, Mitchell TJ:Pneumo- coccal pneumonia:mechanisms of infection and resolution. Chest 2012;142:482―91.
2)千葉菜穂子:わが国における侵襲性肺炎球菌感
染症の実態とその予防としての肺炎球菌ワクチ ン.日化療会誌 2011;59:561―72.
3)Le Hello S, Watson M, Levy M, Marcon S, Brown M, Yvon JF,et al.:Invasive serotype 1 Streptococcus pneumoniaeoutbreaks in the South
Pacific from 2000 to 2007. J Clin Microbiol 2010;48:2968―71.
4)Hausdorff WP, Feikin DR, Kluqman KP:Epide- miological differences among pneumococcal se- rotypes. Lancet Infect Dis 2005;5:83―93.
5)Maruyama T, Taguchi O, Niederman MS, Morser J, Kobayashi H, DʼAlessandro-Gabazza C,et al.:Efficacy of 23-valent pneumococcal vaccine in preventing pneumonia and improv- ing survival in nursing home residents:double blind, randomized and placebo controlled trial.
BMJ 2010;340:1―7.
6)Fedson DS:Pneumococcal vaccination in the United States and 20 other developed countries, 1981―1996. Clin Infect Dis 1998;26:1117―23.
7)Elston JW, Santaniello-Newton A, Meigh JA, Harmer D, Allgar V, Allison T,et al.:Increas- ing incidence of invasive pneumococcal disease and pneumonia despite improved vaccination uptake:surveillance in Hull and East York- shire, UK, 2002―2009. Epidemiol Infect 2012;
140:1252―66.
8)Wemo AM, Murdoch DR:Laboratory diagnosis of invasive pneumococcal disease. Clin Infect Dis 2008;46:926―32.
9)Nagai K, Shibasaki Y, Hasegawa K, Davies TA, Jacobs MR, Ubukata K,et al.:Evaluation of PCR primers to screen forStreptococcus pneumo- niae isolates andβ-lactam resistance, and to de- tect common macrolide resistance determinants.
J Antimicrob Chemother 2001;48:915―8.
10)三鴨廣繁,末松寛之,田中香お里,渡邉邦友,松
原茂規,澤村治樹,他:岐阜県下における肺炎 球菌の疫学解析〜2002 年〜.The Japanese Jour- nal of Antibiotics 2004;57:172―85.
11)Pai R, Gertz RE, Beall B:Sequential multiplex PCR approach for determining capsular sero- types of Streptococcus pneumoniae isolate. J Clin Microbiol 2006;44:124―31.
12)Carvalho MG, Pimenta FC, Jackson D, Round- tree A, Ahmad Y, Millar EV,et al.:Revisiting pneumococcal carriage by use of broth enrich- ment and PCR techniques for enhanced detec- tion of carriage and serotype. J Clin Microbiol 2010;48:1611―8.
13)永田理希:健常児・成人の上咽頭由来肺炎球菌
の耐性化動向の傾向:感染症治療戦略を考慮し た上咽頭細菌の検討.金沢大学十全医学会雑誌 2006;115:75―85.
14)Alanee SR, McGee L, Jackson D, Chiou CC, Feldman C, Morris AJ,et al.:Association of se- rotypes ofStreptococcus pneumoniaewith disease severity and outcome in adults:an interna- tional study. Clin Infect Dis 2007;45:46―51.
15)Johnson HL, Deloria-Knoll M, Levine OS, Stoszek SK, Freimanis Hance L, Reithinger R,et al.:Systematic evaluation of serotypes causing
invasive pnemococcal disease among children under five:the pnemococcal global serotype project. PloS Med 2010;7:e1000348.
16)Weinberger DM, Harboe ZB, Sanders AME, Ndiritu M, Klugman KP, Rückinger S,et al.:
Risk of death from pneumococcal pneumonia is a stable serotype-associated property:a meta- analysis. Clin Infect Dis 2010;51:692―9.
Detection and Serotyping of Streptococcus pneumoniae Carried in Healthy Adults with a Modified PCR Method
Yuka ISHIHARA
1)2), Akira OKAMOTO
3)& Michio OHTA
1)1)Sugiyama Jogakuen University School of Nursing,
2)Department of Infectious Diseases, Nagoya University Graduate School of Medicine,
3)Faculty of Education, Aichi University of Education