2.6.2.2 効力を裏付ける試験 2.6.2.2.1 in vitro 試験 ソラフェニブは当初,生化学的検討により C-RAF 阻害物質の構造-活性相関を評価する過程で 発見された新規化合物である。ソラフェニブの活性について in vitro で行った試験の結果を,表 2.6.2-1 にまとめた。以下に,表に示した各試験の方法の概略について記載する。 キナーゼ阻害活性
RAF (C-RAF, B-RAF 及び V600E B-RAF*), MEK-1, ERK-1 に対する阻害活性は,γ-[33P] ATP を 用い,放射活性を測定することでリン酸化阻害活性を測定した。 受容体型チロシンキナーゼ(RTK)に対する阻害活性は,ユーロピウムで標識したリン酸化チ ロシン抗体を用いて,チロシンリン酸化阻害活性を検討した。 細胞を用いた系でのキナーゼ阻害活性 腫瘍細胞におけるMEK1/2,ERK1/2,及び PKB に対する阻害活性は,各細胞を種々の濃度のソ ラフェニブ存在下でインキュベートした後,細胞溶解液を調製し,MEK1/2,ERK1/2,及び PKB, 並びにそれぞれのリン酸化されたものに対する抗体を用いて検討した。 RTK の自己リン酸化に対する阻害活性は,各細胞を種々の濃度のソラフェニブ存在下でインキ ュベートした後,細胞溶解液を調製し,各RTK 及びそれぞれのチロシンリン酸化されたものに対 する抗体を用いて検討した。 細胞増殖阻害活性 腫瘍細胞は10% FCS 存在下で,血管平滑筋細胞は PDGF 存在下でそれぞれ培養し,種々の濃度 のソラフェニブを添加しインキュベートした後,前者は細胞内ATP 量を,後者は BrdU 取り込み 量を計測することで生存細胞数を評価した。
ソラフェニブは,低濃度で野生型C-RAF,B-RAF 及び変異型 V600E B-RAF*を強力に阻害した。 また,本薬は,腫瘍進行との関連が知られる RTK(FLT-3,c-KIT,VEGFR-2,VEGFR-3,PDGFR-βなど)についても同様に強力に阻害した(表2.6.2-1)。一方,MEK-1,ERK-1,EGFR,HER2/NEU, c-MET,PKA,PKB,IGFR-1,Cdk-1/サイクリン B,PIM-1,PKC-α及び PKC-γに対しては,10 µM の高濃度でも阻害作用を示さなかった(4.2.1.1.9,MRC-01264 [21])。 細胞を用いた系においても,ソラフェニブは,RAF/MEK/ERK シグナル伝達系において RAF の 下流に位置するMEK 及び ERK のリン酸化,並びに RTK の自己リン酸化を阻害した(表 2.6.2-1)。 また,腫瘍細胞あるいは血管平滑筋細胞の増殖に対しても,阻害活性を示した(表2.6.2-1)。 *:かつて V599E B-RAF として発見されたもの[22]
表 2.6.2-1 ソラフェニブの in vitro 薬理活性 Biochemical Assay a
(各キナーゼに対する阻害活性) IC50 (nM)
C-RAF b 6
B-RAF wild-type 22
B-RAF V600E mutant 38
VEGFR-2 90 VEGFR-2 (mouse) 6 VEGFR-3 (mouse) 12 PDGFR-β (mouse) 57 FLT-3 58 c-KIT 68 FGFR-1 580 Cellular Mechanism c (細胞を用いた系での各キナーゼに対するリン酸化阻害活性) IC50 (nM)
MDA MB 231 MEK phosphorylation (Breast) 40 MDA MB 231 ERK phosphorylation (Breast) 90 BxPC-3 ERK phosphorylation (Pancreatic) 1200 LOX ERK phosphorylation (Melanoma) 880 VEGFR-2 receptor phosphorylation (3T3 cells)d 30 VEGF-stimulated ERK phosphorylation (HUVECs)e
60 bFGF-stimulated ERK phosphorylation (HUVECs) 620 VEGFR-3 (mouse) receptor phosphorylation (293 cells) 100 PDGFR-β phosphorylation (HAoSMC)f 80
FLT-3 receptor phosphorylation (ITDi, 293 cells) 20 Cellular Proliferation
(細胞増殖阻害活性) IC50 (nM)
MDA MB 231 (10% FCS) g 2600
PDGFR-β-stimulated HAoSMC f (0.1% BSA) h 220 a Recombinant enzyme assay
b Raf kinase activated with Lck (full length CRAF) c Mechanistic cellular assays all performed in 0.1% BSA d Western blot assay format with Phospho-VEGFR-2 antibody e Human umbilical vein endothelial cells
f Human aortic smooth muscle cells g Fetal calf serum
h Bovine serum albumin i internal tandem duplication
2.6.2.2.2 In vivo 抗腫瘍活性
ソラフェニブの抗腫瘍効果について,in vivo で様々なヒト腫瘍細胞株を用いた異種移植マウス (担癌)モデルを用いて検討した。結腸癌細胞株であるHCT-116(4.2.1.1.1,MRC-01019),DLD-1 (4.2.1.1.9,MRC-01264),Colo-205 及び HT-29 [21](4.2.1.1.9,MRC-01264),非小細胞肺癌細
胞株である NCI-H460(4.2.1.1.1,MRC-01019),NCI-H23(4.2.1.1.8,RMI-00091)及び A549 (4.2.1.4.3,MRC-01195),乳癌細胞株である MDA-MB-231(4.2.1.4.3,MRC-01195)及び MX-1 (4.2.1.4.6,RMI-00085),膵癌細胞株である MiaPaCa-2(4.2.1.1.1,MRC-01019),AML 細胞株 であるMV4;11(4.2.1.1.10,MRC-01276),黒色腫細胞株である LOX IMVI(4.2.1.1.6,RMI-00120 及び 4.2.1.1.7,RMI-00121),卵巣癌細胞株である SK-OV-3(4.2.1.1.1,MRC-01019)などを用 いた担癌モデルに対し,皮下移植した腫瘍の生着が確認された時点から9 日間(DLD-1, Colo-205, HT-29, NCI-H23, LOX IMVI 及び MV4;11),10 日間(A549 及び MDA-MB-231)又は 14 日間(HCT-116, NCI-H460,MX-1,Mia-PaCa-2 及び SK-OV-3),本薬を 1 日 1 回経口投与した。ソラフェニブは遊 離型あるいはトシル酸塩の形で投与されたが,用量は全て遊離塩基当量として表示した。被験物 質の有効性は腫瘍増殖抑制率(TGI)で表示しており,(1-T/C)×100 [ただし T と C は,各試験 におけるソラフェニブ最終投与翌日の投与群(T)と対照群(C)の腫瘍の平均重量]で算出した。 各種ヒト腫瘍由来細胞株の異種移植モデルに対するソラフェニブの腫瘍増殖抑制効果を表 2.6.2-2 及び図 2.6.2-2 に示す。この表には,2 回の試験の平均値を示した。
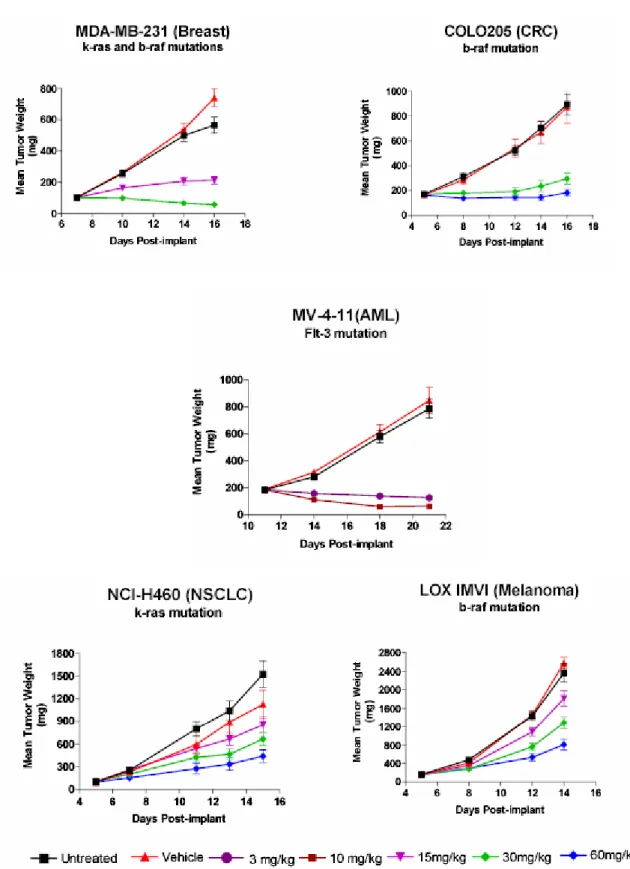
ソラフェニブは,変異型k-ras(DLD-1,Mia-PaCa-2)又は変異型 b-raf (Colo-205,HT-29)を 発現している腫瘍細胞株を用いた担癌モデルに対して腫瘍増殖抑制効果を示した。また,これら 両方の遺伝子が突然変異により活性化しているヒト乳癌細胞株 MDA-MB-231 担癌モデルにおい ても有効であった。さらに,ras と b-raf は野生型であるが増殖因子受容体である EGFR,Her2 を 過剰発現しているヒト卵巣癌細胞株 SK-OV-3 担癌モデルにおいても効果を示した。EGFR,Her2 からのシグナルもRAS/RAF/MEK/ERK 経路で伝達されるので,このモデルにおいてソラフェニブ が有効であることは,RAF 阻害薬が ras や b-raf の変異を持つヒト腫瘍に有効であるだけでなく, そのシグナル伝達経路の上流に位置する増殖因子受容体を過剰発現している腫瘍にも有効である ことを示唆している。また本薬は,活性型 FLT-3 変異を発現している AML 細胞株 MV4;11 担癌 モデルにおいても高い有効性を示した(4.2.1.1.10,MRC-01276)。
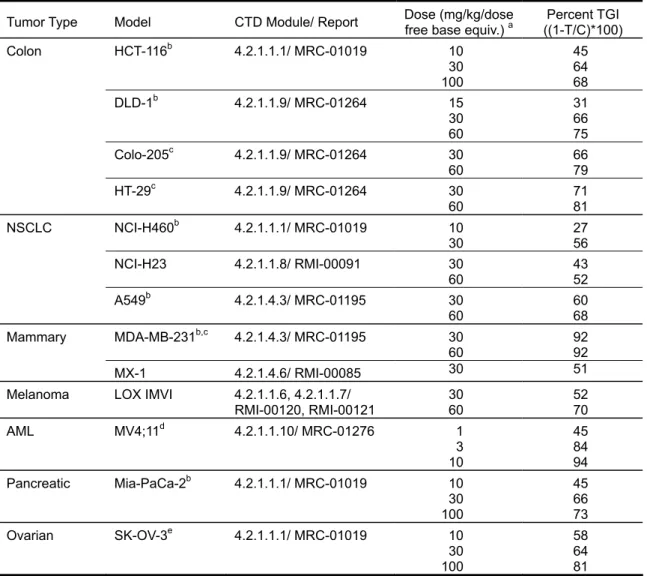
表 2.6.2-2 ヒト腫瘍細胞株を用いた異種移植マウスモデルにおけるソラフェニブの腫瘍増殖 抑制効果
Tumor Type Model CTD Module/ Report Dose (mg/kg/dose free base equiv.) a ((1-T/C)*100) Percent TGI
Colon HCT-116b 4.2.1.1.1/ MRC-01019 10 30 100 45 64 68 DLD-1b 4.2.1.1.9/ MRC-01264 15 30 60 31 66 75 Colo-205c 4.2.1.1.9/ MRC-01264 30 60 66 79 HT-29c 4.2.1.1.9/ MRC-01264 30 60 71 81 NSCLC NCI-H460b 4.2.1.1.1/ MRC-01019 10 30 27 56 NCI-H23 4.2.1.1.8/ RMI-00091 30 60 43 52 A549b 4.2.1.4.3/ MRC-01195 30 60 60 68 Mammary MDA-MB-231b,c 4.2.1.4.3/ MRC-01195 30 60 92 92 MX-1 4.2.1.4.6/ RMI-00085 30 51 Melanoma LOX IMVI 4.2.1.1.6, 4.2.1.1.7/
RMI-00120, RMI-00121 30 60 52 70 AML MV4;11d 4.2.1.1.10/ MRC-01276 1 3 10 45 84 94 Pancreatic Mia-PaCa-2b 4.2.1.1.1/ MRC-01019 10 30 100 45 66 73 Ovarian SK-OV-3e 4.2.1.1.1/ MRC-01019 10 30 100 58 64 81 a Compound dosed as BAY 43-9006 or equivalent dose levels of the tosylate salt, BAY 54-9085 b Contains an activating k-ras mutation
c Contains an activating b-raf mutation d Contains an activating Flt3 mutation e Contains both wild-type k-ras and b-raf
図 2.6.2-2 ヒト腫瘍細胞株を用いた異種移植マウスモデルに対するソラフェニブの腫瘍増殖 抑制効果
ヒト腎細胞癌細胞株 786-O をヌードマウスに皮下移植したモデルに対し,本薬 15~90 mg/kg/ 日を21 日間経口投与して腫瘍増殖に対する抑制効果を検討した。TGI は投与最終日の腫瘍体積よ り算出した。結果を図2.6.2-3 に示す。TGI は,28~74%であり,30 mg/kg/day 以上でほぼ完全に 増殖を抑制した(4.2.1.1.16, MRC-01328)。 図2.6.2-3 ヒト腎細胞癌細胞株 786-O 移植マウスモデルにおけるソラフェニブの腫瘍増殖抑制 効果 マウス腎細胞癌細胞株 RENCA をヌードマウスに皮下移植したモデルに対し,本薬 7.5~90 mg/kg/日を 8-9 日間経口投与して腫瘍増殖に対する抑制効果を検討した。TGI は投与最終日の腫瘍 体積より算出した。結果を図2.6.2-4 に示す。TGI は 30~84 %であった。(4.2.1.1.3,MRC-01271)。
0 200 400 600 800 1000 2 4 6 8 10 12 14
Days Post-Implant
Mean
T
umor W
eight
(mg)
Untreated Vehicle sorafenib (7.5mg/kg)
sorafenib (15mg/kg) sorafenib (30mg/kg) sorafenib (60mg/kg) sorafenib (90mg/kg) 図 2.6.2-4 マウス腎細胞癌細胞株 RENCA 移植マウスモデルにおけるソラフェニブの腫瘍増殖 抑制効果 DLD-1 結腸癌マウスモデルにおいて,様々な反復投与サイクルでソラフェニブ 60mg/kg/日を投 与した際の有効性を検討した。 すなわち,「標準1 サイクル群」(青線)では,試験6 日目に腫瘍が平均 100 mg となった後,10 日間の投与(1 回)を行った。「2 サイクル群」(緑線)には,10 日間の投与を 2 回施行した。2 回 目の投与サイクルは,平均腫瘍重量が約350~400 mg となった時点で開始した。「遅延1 サイクル 群」(赤線)は,2 サイクル群の 2 回目の投与サイクルで大きな腫瘍に対して投与した時のソラフ ェニブの有効性を評価するための対照とし,約350~400 mg の腫瘍に対して 1 サイクル投与した。 また,「連続投与群」(茶線)では,他の群の初回投与時から最終投与時まで,ソラフェニブを連 続投与した。 ソラフェニブは,「標準1 サイクル群」でも「遅延 1 サイクル群」でも腫瘍増殖を抑制し,TGD (腫瘍増殖遅延:TGD=T-C。ただし,T 又は C はそれぞれ投与群又は対照群の腫瘍が,規定の重 量に達するまでの日数の中央値)は投与期間に比例した。10 日間のサイクルを 2 回施行した場合 には10 日間 1 サイクルの約 2 倍の TGD が得られ,30 日間の連続投与では 10 日間 1 サイクル投
与時の約3 倍の TGD が得られた。初回投与サイクルで増殖が抑制され投与中止後再増殖した腫瘍 は,2 回目の投与サイクルにおいても反応した(4.2.1.1.2,MRC-01203)(図 2.6.2-5)。 0 200 400 600 800 1000 1200 1400 1600 0 5 10 15 20 25 30 35 40 45 50 Days Post-implant M ea n Tum or W ei g h t ( m g ) CONTROL QD x 10 (6, 26) QD x 10 (6) QD x 10 (13) QD x 29 (6) Vehicle QD x 18 (6) QD x 29 (start day 6) QD x 10 (start day 13) QD x 10 (start day 6)
QD x 10 (start day 6 and day 26)
QD:1日1回投与 図 2.6.2-5 DLD-1 ヒト結腸癌マウスモデルにおけるソラフェニブ反復投与サイクルの腫瘍増殖 抑制効果 2.6.2.2.3 作用機序 ソラフェニブの作用機序を,HT-29 及び Colo-205 結腸癌細胞株,並びに MDA-MB-231 乳癌細胞 株を皮下移植したマウスモデルを用いてex vivo で検討した[21](4.2.1.1.9,MRC-01264)。それ ぞれの試験で,腫瘍重量約100~250 mg の担癌マウスにソラフェニブ(1 日 1 回 30 又は 60 mg/kg) を5 日間経口投与した。最終投与から 3 時間後に腫瘍を摘出し,ERK リン酸化の変化をウエスタ ンブロット解析及び免疫組織化学染色(IHC)により評価し,ソラフェニブが RAF/MEK/ERK 経 路に及ぼす影響について検討した。一部のモデルの腫瘍検体については,血管新生阻害作用を評 価するため,CD31 に対するヤギポリクローナル抗体で染色し,微小血管面積及び微小血管密度を 画像分析により評価した。 HT-29 及び MDA-MB-231 細胞株を用いた担癌マウスより得た腫瘍組織では,ERK リン酸化と新 生血管の減少が認められたが,Colo-205 モデルより得た標本においては,新生血管の減少のみが 観察された。
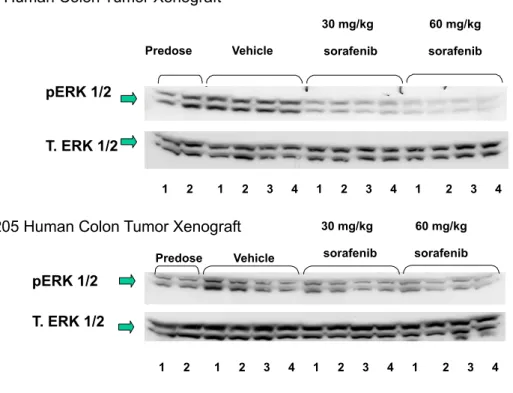
を用いた ERK リン酸化に対するソラフェニブの作用を検討したウエスタンブロット分析の結果 を図2.6.2-6 に示す。
pERK 1/2: リン酸化 ERK-1 及びリン酸化 ERK-2
T.ERK 1/2: リン酸化状態に関わらない ERK-1 及び ERK-2
図 2.6.2-6 ヒト腫瘍細胞株を用いた異種移植モデルにおける腫瘍組織中の ERK リン酸化 に対するソラフェニブ5 日間投与の効果 抗pERK 抗体と抗 ERK 抗体を用いたウエスタンブロット分析で,HT-29 ヒト結腸癌組織片では RAF/MEK/ERK 経路の活性化が阻害されたのに対し,Colo-205 ヒト結腸癌組織片では阻害されな かった。 前述したように,ソラフェニブはHT-29 及び Colo-205 結腸癌モデルのいずれに対しても増殖抑 制作用を示したが,この結果から,Colo-205 結腸癌モデルではソラフェニブの腫瘍増殖抑制作用 はRAF/MEK/ERK 活性化阻害によるものではないと考えられた。Colo-205 細胞も HT-29 細胞も同 じV600E BRAF 変異を持ち,この変異がこれらの細胞の異常増殖をもたらしていると考えられて いる。Colo-205 腫瘍では,RAF/MEK/ERK カスケードとは異なる経路が ERK 1/2 を活性化してい る可能性が示唆された。
HT-29 モデルと Colo-205 結腸癌モデルの腫瘍血管新生に対するソラフェニブの効果を,図 2.6.2-7 に示す。ソラフェニブは,HT-29 腫瘍と Colo-205 腫瘍のいずれにおいても,溶媒投与群と 比較して微小血管面積(MVA)と微小血管密度(MVD)を 50~80 %低下させた。
HT-29 Human Colon Tumor Xenograft
1 2 1 2 3 4 1 2 3 4 1 2 3 4 Predose Vehicle 30 mg/kg sorafenib pERK 1/2 T. ERK 1/2 Predose Vehicle pERK 1/2 T. ERK 1/2
Colo 205 Human Colon Tumor Xenograft
1 2 1 2 3 4 1 2 3 4 1 2 3 4 60 mg/kg sorafenib 30 mg/kg sorafenib 60 mg/kg sorafenib
***: p<0.001 v.s. vehicle treated group, @: p<0.05 v.s. untreated group
Microvessel Area-MVA Microvessel Density-MVD
M icr ov e sse l CT (#/ m m 2 ) 0 75 150 225 300 375
***
***
@ untreated vehicle sorafenib, 30 mg/kg sorafenib, 60 mg/kg 0.0 0.2 0.4 0.6 0.8 1.0***
***
@ Mic rov esse l A re a ( % ) untreated vehicle sorafenib, 30 mg/kg sorafenib, 60 mg/kg*: p< 0.05, **: p< 0.01, ***: p<0.001 v.s. vehicle treated group
0.0 0.4 0.8 1.2 1.6 2.0 Mi cr o ve s s el A rea ( % )
*
**
untreatedvehicle sorafenib, 30 mg/kgsorafenib, 60 mg/kg untreatedvehicle sorafenib, 30 mg/kgsorafenib, 60 mg/kg
0 50 100 150 200 250
***
***
Mic rov ess el C T (#/ m m 2 )HT-29
HT-29
Colo
-205
Colo
-205
A.
B.
Untreated Vehicle Sorafenib Sorafenib
C. CD-31 30 mg/kg 60 mg/kg
Mice with 150-250 mg HT-29 or Colo-205 tumors were treated for 5 days with either vehicle or oral sorafenib at 30 or 60 mg/kg. Tumors were collected, sectioned, and stained with anti-CD31 antibodies. A-B: The number and area of microvessels, indicated by CD31-positive objects in either HT-29 or Colo-205 tumors, were quantified and percent area and density of microvessel were calculated in each group. Data are presented as mean ± SE (4 samples per group). C: Detection of CD31-positive objects in Colo-205 tumor tissue was apparent in tumors obtained from untreated and vehicle treated animals (left 2 pictures), but was substantially reduced in sorafenib treated tumors (right 2 pictures).
*: p<0.01, **: p<0.01, ***: p<0.001 vs vehicle treated group (One-way ANOVA followed by Fisher’s PLSD) 図 2.6.2-7 HT-29 及び Colo-205 結腸癌マウスモデルの腫瘍組織における血管新生に対する
ソラフェニブ(5 日間投与)の効果
腎細胞癌におけるソラフェニブの作用機序を検討するために,マウス由来腎細胞癌細胞株 RENCA 及びヒト由来腎細胞癌細胞株 786-O をヌードマウスの皮下あるいは腎被膜下に移植した モデルを用いて,血管新生,細胞の増殖及びpERK の局在について,ex vivo で検討した(4.2.1.1.16, MRC-01328)。
フェニブ15, 30, 60, 90 mg/kg/日を 3 日間経口投与し,最終投与後に腫瘍を取り出し,それぞれ抗 CD-31 抗体又は抗αSMA 抗体を用いて免疫組織化学染色し,血管面積を測定した。ソラフェニブ 投与群では,未処置群又は溶媒投与群に比較して,血管面積の減少が認められた(図 2.6.2-8)。 また,ヌードマウスの腎被膜下に,RENCA 組織片 1mm3を移植し,ソラフェニブ15, 30, 60, 90 mg/kg/日を 10 日間経口投与した後,腎臓を摘出し,同様に抗 CD-31 抗体又は抗αSMA 抗体を用 いて免疫組織化学染色し,血管面積を測定した場合も,ソラフェニブ投与群では,未処置群又は 溶媒投与群に比較して,血管面積の減少が認められた。