シタフロキサシン水和物
グレースビット
®
錠 50 mg、細粒 10%
2.7.3(5 群)呼吸器感染症
臨床的有効性の概要
目 次
2.7.3(5 群)呼吸器感染症 臨床的有効性の概要 ... 1 1.(5 群)背景および概観... 1 2.(5 群)個々の試験結果の要約... 3 3.(5 群)全試験を通しての結果の比較と解析... 7 3.1(5 群)試験対象集団... 7 3.2(5 群)全有効性試験の結果の比較検討... 12 3.3(5 群)部分集団における結果の比較... 20 4.(5 群)推奨用法・用量に関する臨床情報の解析... 24 5.(5 群)効果の持続、耐薬性... 25 6.(5 群)付録... 29図の目次
図 2.7.3.3.1(5 群)-1 各種ニューキノロン系抗菌薬の MIC 分布 <呼吸器感染症の原因菌>... 11 図 2.7.3.3.1(5 群)-2 治験実施時期別の MIC 分布<呼吸器感染症の主な原因菌> ... 12 図 2.7.3.3.2(5 群)-1 AUC0-24h/MIC と消失率の関係(試験全体・全菌種) ... 18 図 2.7.3.3.2(5 群)-2 Cmax/MIC と消失率の関係(試験全体・全菌種)... 18表の目次
表 2.7.3.1(5 群)-1 有効性評価の対象となる臨床試験の一覧... 1 表 2.7.3.2(5 群)-1 PK/PD パラメータと細菌学的効果(消失率)の関係 ... 6 表 2.7.3.3.1(5 群)-1 被験者の内訳 ... 7 表 2.7.3.3.1(5 群)-2 解析対象集団の内訳... 7 表 2.7.3.3.1(5 群)-3 PPS 不採用理由... 8 表 2.7.3.3.1(5 群)-4 被験者背景 ... 9 表 2.7.3.3.1(5 群)-5 原因菌の内訳 ... 10 表 2.7.3.3.2(5 群)-1 疾患別臨床効果 ... 13 表 2.7.3.3.2(5 群)-2 原因菌別臨床効果 ... 14 表 2.7.3.3.2(5 群)-3 疾患別陰性化率 ... 15 表 2.7.3.3.2(5 群)-4 原因菌別 MIC 別消失率(非定型病原体除く) ... 16 表 2.7.3.3.2(5 群)-5 非定型病原体の MIC 別消失率... 17 表 2.7.3.3.2(5 群)-6 AUC0-24h/MIC と菌の推移との関係 ... 19 表 2.7.3.3.2(5 群)-7 Cmax/MIC と菌の推移との関係... 20表 2.7.3.3.3(5 群)-1 被験者背景別の臨床効果... 21 表 2.7.3.3.3(5 群)-2 直前抗菌化学療法無効被験者での臨床効果... 22 表 2.7.3.3.3(5 群)-3 無効被験者の被験者背景... 23 表 2.7.3.3.3(5 群)-4 無効被験者の原因菌の消長... 23 表 2.7.3.4(5 群)-1 疾患群別 1 日投与量別臨床効果... 26 表 2.7.3.4(5 群)-2 原因菌別 1 日投与量別 MIC 別の消失率 ... 27
付表の目次
付表 2.7.3(5 群)-1 臨床的有効性および安全性試験の要約... 29 付表 2.7.3(5 群)-2 有効性試験の結果 ... 30略号一覧 略号 名称 AUC0-24h 投与後 24 時間までの血清中濃度-時間曲線下面積 Cmax 最高血清中濃度 CI 信頼区間 CLcr クレアチニンクリアランス COPD 慢性閉塞性肺疾患 最小発育阻止濃度 MIC MIC90:90%発育阻止濃度 PPS 治験実施計画書に適合した対象集団 SD 標準偏差 菌名の略号一覧 略号 名称
C. pneumoniae Chlamydia pneumoniae E. aerogenes Enterobacter aerogenes E. coli Escherichia coli
GNB Gram-negative bacteria H. influenzae Haemophilus influenzae
K. pneumoniae Klebsiella pneumoniae
M. (B.) catarrhalis Moraxella (Branhamella) catarrhalis M. pneumoniae Mycoplasma pneumoniae
P. aeruginosa Pseudomonas aeruginosa S. aureus Staphylococcus aureus S. maltophilia Stenotrophomonas maltophilia S. pneumoniae Streptococcus pneumoniae S. pyogenes Streptococcus pyogenes
ニューキノロン系抗菌薬一覧 一般名(略号) 化学名 構造式 シタフロキサシン (STFX) (-)-7-[(7S)-7-amino-5-azaspiro[2.4]heptan-5-yl]-8-chloro-6-fluoro-1-[(1R,2S)-2- fluoro-1-cyclopropyl]-1,4-dihydro-4-oxo- 3-quinolinecarboxylic acid N N Cl F O COOH F H N H2 H H レボフロキサシン (LVFX) (-)-(S)-9-fluoro-2,3-dihydro-3-methyl-10- (4-methyl-1-piperazinyl)-7-oxo-7H-pyrido [1,2,3-de][1,4]benzoxazine-6-carboxylic acid N O N O F N C H3 CH3 COOH シプロフロキサシン (CPFX) 1-cyclopropyl-6-fluoro-1,4-dihydro-4-oxo-7-(piperazin-1-yl)-3-quinolinecarboxylic acid N O N F N H COOH トスフロキサシン (TFLX) (±)-7-(3-amino-1-pyrrolidinyl)-6-fluoro-1-(2,4- difluorophenyl)-1,4-dihydro-4-oxo- 1,8-naphthyridine-3-carboxylic acid N N O N F N H2 COOH F F スパルフロキサシン (SPFX) 5-amino-1-cyclopropyl-7-(cis-3,5- dimethyl-1-piperazinyl)-6,8-difluoro-1,4- dihydro-4-oxoquinoline-3-carboxylic acid F N O NH2 N F N H C H3 CH3 COOH ガチフロキサシン (GFLX) (±)-1-cycloproyl-6-fluoro-1,4-dihydro-8- methoxy-7-(3-methyl-1-piperazinyl)-4- oxo-3-quinolinecarboxylic acid O N O N C H3 F N H C H3 COOH
2.7.3(5 群)呼吸器感染症 臨床的有効性の概要
1.(5 群)背景および概観 1.1(5 群)臨床試験の構成 有効性評価の対象となる臨床試験の一覧を表 2.7.3.1(5 群)-1 に示す。 表 2.7.3.1(5 群)-1 有効性評価の対象となる臨床試験の一覧 試験名 添付資料番号(試験計画番号) 試験課題名 第 III 相試験 <肺炎・慢性肺疾患感染性増悪 DBT> 5.3.5.1(5 群)-1(DU6859a-30) DU-6859a第 III 相臨床試験 肺炎・慢性肺疾患の感染性増悪(慢性気道感染症の感染性増悪,慢性 呼吸器疾患の二次感染)を対象とした二重盲検比較試験 第 III 相試験<市中肺炎 DBT> 5.3.5.1(5 群)-2(DU6859a-42) DU-6859a第 III 相臨床試験 -市中肺炎を対象とした二重盲検比較検証試験- 第 III 相試験<呼吸器感染症オープン> 5.3.5.2(5 群)-1(DU6859a-44) DU-6859a第 III 相臨床試験 -呼吸器感染症を対象とした一般臨床試験- 第 III 相試験<市販 NQ 無効肺炎オープン> 5.3.5.2(5 群)-2(DU6859a-33) DU-6859a第 III 相臨床試験 (市販ニューキノロン剤無効の肺炎例を対象とした一般臨床試験) 第 III 相試験 <耳鼻咽喉科領域感染症オープン>a) 5.3.5.2(15 群)-1(DU6859a-45) DU-6859a第 III 相臨床試験 -耳鼻咽喉科領域感染症を対象とした一般臨床試験- a:咽喉頭炎、扁桃炎の成績を本項で記載し、中耳炎、副鼻腔炎の成績を 2.7.3(15 群)で記載する 1.2(5 群)対象被験者の選定 「抗菌薬臨床評価のガイドライン」1)に規定された 5 群の疾患のうち、咽喉頭炎 (咽頭炎のみも含む)、扁桃炎(扁桃周囲炎および扁桃周囲膿瘍を含む)、急性気管 支炎、肺炎および慢性呼吸器病変の二次感染患者を対象とした。感染症重症度は、 「呼吸器感染症における新規抗微生物薬の臨床評価法(案)」2)に規定された軽症お よび中等症を対象とした。ただし、咽喉頭炎および扁桃炎の感染症重症度は「第 3 回耳鼻咽喉科サーベイランス計画書」の基準を参考とし、中等症および重症の患者 を対象とした。 1.3(5 群)試験デザイン 比較試験は、市販されているニューキノロン系抗菌薬に対するシタフロキサシン 1 回 50 mg 1 日 2 回 7 日間投与時の臨床効果の非劣性を検証するために多施設共同 無作為化二重盲検比較試験とした。 第 III 相試験<肺炎・慢性肺疾患感染性増悪 DBT>(添付資料番号 5.3.5.1(5 群) -1 参照)では、肺炎・慢性肺疾患の感染性増悪の治療薬として汎用され、有効性お よび安全性の評価が確立したレボフロキサシンを対照薬とした。レボフロキサシン の用法・用量は、1 回 100 mg 1 日 3 回 7 日間とした。 第 III 相試験<市中肺炎 DBT>(添付資料番号 5.3.5.1(5 群)-2 参照)では、シタフロキサシンが肺炎球菌に対して強い抗菌力を有することを臨床的に検証するた め、肺炎球菌が主要原因菌となる市中肺炎を対象に、日本呼吸器学会が肺炎球菌性 肺炎の治療に推奨しているトスフロキサシンを対照薬とした。トスフロキサシンの 用法・用量は、1 回 150 mg 1 日 3 回 7 日間とした。 上記 2 試験に加え、呼吸器感染症に対する有効性および安全性の追加情報を得る ため、比較試験の対象となっていない疾患(咽喉頭炎、扁桃炎、急性気管支炎)に 対する有効性の検討および PK/PD の検討を行った。 第 III 相試験<呼吸器感染症オープン>および第 III 相試験<耳鼻咽喉科領域感染 症オープン>(添付資料番号 5.3.5.2(5 群)-1、5.3.5.2(15 群)-1 参照)では、シ タフロキサシン 1 回 50 mg 1 日 2 回または 1 回 100 mg 1 日 2 回を 7 日間投与した際 の有効性および安全性を検討するため、中央登録方式による多施設共同オープン試 験とした。第 III 相試験<呼吸器感染症オープン>では、母集団薬物動態パラメータ を用いてベイズ推定により各被験者の薬物動態パラメータを算出し、PK/PD パラメ ータと有効性との相関を検討することにより、臨床推奨用量の妥当性を検討した。 第 III 相試験<市販 NQ 無効肺炎オープン>(添付資料番号 5.3.5.2(5 群)-2 参照) では、市販ニューキノロン系抗菌薬が無効であった肺炎患者に対するシタフロキサ シンの効果を検討するため、シタフロキサシン 1 回 100 mg 1 日 1 回または 1 回 100 mg 1 日 2 回 3~7 日間の用法・用量で、多施設共同オープン試験を実施した。 1.4(5 群)評価方法 急性気管支炎、肺炎および慢性呼吸器病変の二次感染は、日本化学療法学会「呼 吸器感染症における新規抗微生物薬の臨床評価法(案)」2)を参考に、また咽喉頭炎 および扁桃炎は、「臨床薬物治療学大系 4 臨床薬効評価 耳鼻咽喉科疾患」3)の判定 基準を参考に臨床効果を評価した。なお、咽喉頭炎(咽頭炎のみも含む)、扁桃炎(扁 桃周囲炎および扁桃周囲膿瘍を含む)および急性気管支炎は、急性上気道感染症群 として評価した。 臨床効果は、急性気管支炎、肺炎および慢性呼吸器病変の二次感染では「有効」・ 「無効」・「判定不能」のいずれかで判定し、「有効」と判定された被験者の割合を有 効率とした。咽喉頭炎および扁桃炎では「著効」・「有効」・「やや有効」・「無効」・「判 定不能」のいずれかで判定し、「著効」および「有効」と判定された被験者の割合を 有効率とした。主要評価項目はいずれも投与終了・中止時の有効率とした。 細菌学的効果は陰性化率および消失率で評価した。陰性化率は、被験者ごとの細 菌学的効果を示すものであり、すべての原因菌が消失または原因菌分離材料が採取 できなくなった被験者の割合とした。消失率は、菌株ごとの細菌学的効果を示すも のであり、原因菌と判定された菌株のうち消失した菌株の割合とした。陰性化率お よび消失率は副次評価項目とした。 直前抗菌化学療法が無効であった被験者での評価にあたっては、治験薬投与開始
前 7 日以内に抗菌化学療法が 3 日間以上行われ、その効果が認められなかった被験 者を「直前抗菌化学療法無効被験者」とした。ただし、マクロライド系抗菌薬の少 量長期投与は「直前抗菌化学療法」として取り扱わなかった。 なお、すべての試験で主たる有効性の解析対象集団は治験実施計画書に適合した 対象集団(PPS)とした。また、比較試験での非劣性マージンは−10%と設定した。 2.(5 群)個々の試験結果の要約 個々の試験結果の要約を付表 2.7.3(5 群)-1 および付表 2.7.3(5 群)-2 に示す。 2.1(5 群)第 III 相試験<肺炎・慢性肺疾患感染性増悪 DBT>(DU6859a-30) ...添付資料番号 5.3.5.1(5 群)-1 2.1.1(5 群)臨床効果 有効率は、STFX 群で 92.5%(99/107、95%CI = 85.8%, 96.7%)、LVFX 群で 92.1% (93/101、95%CI = 85.0%, 96.5%)であった。有効率の差は 0.4%であり、その両側 90%CI の下限値は−5.6%、両群間の患者重篤度の不均衡を調整した後の下限値は −6.1%であった。いずれの下限値も−10%以上であることから、シタフロキサシン 50 mg × 2/日のレボフロキサシン 100 mg × 3/日に対する非劣性が検証された。 疾患別有効率は、肺炎では STFX 群が 96.4%(53/55、95%CI = 87.5%, 99.6%)、LVFX 群が 94.0%(47/50、95%CI = 83.5%, 98.7%)、慢性肺疾患の感染性増悪では STFX 群 が 88.5%(46/52、95%CI = 79.8%, 97.1%)、LVFX 群が 90.2%(46/51、95%CI = 82.0%, 98.4%)であった。 2.1.2(5 群)細菌学的効果 陰性化率は、STFX 群で 78.4%(40/51、95%CI = 64.7%, 88.7%)、LVFX 群で 80.4% (37/46、95%CI = 66.1%, 90.6%)であった。 消失率は、STFX 群で 85.2%(46/54、95%CI = 72.9%, 93.4%)、LVFX 群で 84.3% (43/51、95%CI = 71.4%, 93.0%)であった。 グラム陽性菌の消失率は STFX 群で 95.0%(19/20)、LVFX 群で 87.5%(21/24)、 グラム陰性菌では STFX 群で 79.4%(27/34)、LVFX 群で 81.5%(22/27)であった。 主な原因菌の消失率は、Streptococcus pneumoniae が STFX 群で 100%(16/16)、LVFX 群で 85.7%(18/21)、Haemophilus influenzae が STFX 群で 100%(17/17)、LVFX 群 で 100%(14/14)、Pseudomonas aeruginosa が STFX 群で 14.3%(1/7)、LVFX 群で 42.9% (3/7)であった。
2.2(5 群)第 III 相試験<市中肺炎 DBT>(DU6859a-42) ...添付資料番号 5.3.5.1(5 群)-2 2.2.1(5 群)臨床効果 有効率は、STFX 群で 93.3%(111/119、95%CI = 88.8%, 97.8%)、TFLX 群で 89.6% (95/106、95%CI = 83.8%, 95.4%)であり、群間差は 3.7%(95%CI = −3.7%, 11.0%) であった。群間差の 95%CI の下限値は−10%を上回り、シタフロキサシン 50 mg × 2 /日のトスフロキサシン 150 mg × 3/日に対する非劣性が検証された。 2.2.2(5 群)細菌学的効果 陰性化率は、STFX 群で 100%(42/42)、TFLX 群で 88.2%(45/51、95%CI = 79.4%, 97.1%)であった。 消失率は、STFX群で100%(48/48)、TFLX群で91.1%(51/56、95%CI = 83.6%, 98.5%) であった。 グラム陽性菌の消失率は、STFX 群で 100%(18/18)、TFLX 群で 88.0%(22/25)、 グラム陰性菌では STFX 群で 100%(23/23)、TFLX 群で 96.2%(25/26)、非定型病 原体では STFX 群で 100%(7/7)、TFLX 群で 80.0%(4/5)であった。 主な原因菌の消失率は、S. pneumoniae が STFX 群で 100%(14/14)、TFLX 群で 87.0% (20/23)、H. influenzae が STFX 群で 100%(17/17)、TFLX 群で 100%(18/18)であ った。Mycoplasma pneumoniae の消失率は、STFX 群で 100%(6/6)、TFLX 群で 80.0% (4/5)であった。 2.3(5 群)第 III 相試験<呼吸器感染症オープン>(DU6859a-44) ...添付資料番号 5.3.5.2(5 群)-1 2.3.1(5 群)臨床効果 有効率は全体で 92.5%(123/133、95%CI = 88.0%, 97.0%)であり、50 mg × 2/日 では 92.3%(96/104、95%CI = 87.2%, 97.4%)、100 mg × 2/日では 93.1%(27/29、95%CI = 83.9%, 100%)であった。 疾患別有効率は市中肺炎が 90.5%(57/63、95%CI = 83.2%, 97.7%)、慢性呼吸器病 変の二次感染が 92.9%(52/56、95%CI = 86.1%, 99.6%)、急性気管支炎が 100%(14/14) であった。 投与量別有効率は 50 mg × 2/日で市中肺炎が 89.6%(43/48、95%CI = 80.9%, 98.2%)、慢性呼吸器病変の二次感染が 93.2%(41/44、95%CI = 85.7%, 100%)、急性 気管支炎が 100%(12/12)であった。100 mg × 2/日では市中肺炎が 93.3%(14/15、 95%CI = 80.7%, 100%)、慢性呼吸器病変の二次感染が 91.7%(11/12、95%CI = 76.0%, 100%)であり、急性気管支炎患者 2 名はいずれも「有効」と判定された。
2.3.2(5 群)細菌学的効果 陰性化率は全体で 87.7%(71/81、95%CI = 80.5%, 94.8%)であった。50 mg × 2/ 日では 89.1%(57/64、95%CI = 81.4%, 96.7%)、100 mg × 2/日では 82.4%(14/17、 95%CI = 64.2%, 100%)であった。 消失率は全体で 91.7%(88/96、95%CI = 86.1%, 97.2%)であった。50 mg × 2/日 では 93.5%(72/77、95%CI = 88.0%, 99.0%)、100 mg × 2/日では 84.2%(16/19、95%CI = 67.8%, 100%)であった。 グラム陽性菌全体の消失率は 94.3%(33/35)で、50 mg × 2/日では 96.2%(25/26)、 100 mg × 2/日では 88.9%(8/9)であった。グラム陰性菌全体の消失率は 88.9% (48/54)で、50 mg × 2/日では 91.5%(43/47)、100 mg × 2/日では 71.4%(5/7) であった。
主な原因菌の消失率は、Staphylococcus aureus が 100%(11/11)で、S. pneumoniae が 91.7%(22/24)であった。Moraxella (Branhamella) catarrhalis 12 株および H. influenzae 24株はすべて消失した。
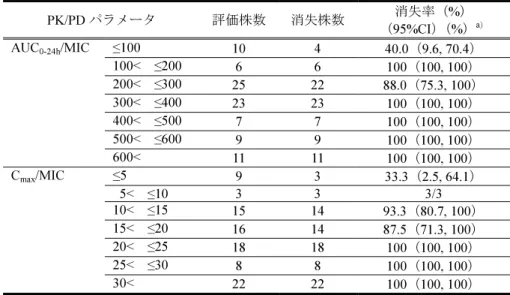
2.3.3(5 群)PK/PD パラメータと細菌学的効果(消失率)の相関性検討
PK/PD パラメータ(AUC0-24h/MIC または Cmax/MIC)と消失率の関係を表 2.7.3.2
(5 群)-1 に示す。
AUC0-24h/MIC が 100 以下の場合の消失率は 40.0%(4/10)、Cmax/MIC が 5 以下の場
合の消失率は 33.3%(3/9)と低かった。一方、AUC0-24h/MIC が 100 を超えた場合の 全体の消失率は 96.3%(78/81)であり、AUC0-24h/MIC が 200 を超えて 300 以下の場 合で 3 株が消失しなかった以外は、すべての菌株が消失した。また、Cmax/MIC が 5 を超えた場合の全体の消失率は 96.3%(79/82)であり、Cmax/MIC が 10 を超えて 15 以下の場合での 1 株、および 15 を超えて 20 以下の場合での 2 株が消失しなかった 以外は、すべての菌株が消失した。
S. pneumoniaeでは AUC0-24h/MIC が 100 以下の場合には 4 株中 2 株、Cmax/MIC が 5 以下の場合には 3 株中 1 株が消失したのみであったが、AUC0-24h/MIC が 100 を超え
表 2.7.3.2(5 群)-1 PK/PD パラメータと細菌学的効果(消失率)の関係 PK/PDパラメータ 評価株数 消失株数 消失率(%) (95%CI)(%)a) ≤100 10 4 40.0(9.6, 70.4) 100< ≤200 6 6 100(100, 100) 200< ≤300 25 22 88.0(75.3, 100) 300< ≤400 23 23 100(100, 100) 400< ≤500 7 7 100(100, 100) 500< ≤600 9 9 100(100, 100) AUC0-24h/MIC 600< 11 11 100(100, 100) ≤5 9 3 33.3(2.5, 64.1) 5< ≤10 3 3 3/3 10< ≤15 15 14 93.3(80.7, 100) 15< ≤20 16 14 87.5(71.3, 100) 20< ≤25 18 18 100(100, 100) 25< ≤30 8 8 100(100, 100) Cmax/MIC 30< 22 22 100(100, 100) a:正規近似による CI 2.4(5 群)第 III 相試験<市販 NQ 無効肺炎オープン>(DU6859a-33) ...添付資料番号 5.3.5.2(5 群)-2 2.4.1(5 群)臨床効果 市販ニューキノロン系抗菌薬が無効であった肺炎患者での有効率は 90.0%(9/10) であった。 2.4.2(5 群)細菌学的効果 原因菌として Klebsiella pneumoniae が 1 株分離されたが、消失しなかった。 2.5(5 群)第 III 相試験<耳鼻咽喉科領域感染症オープン>(DU6859a-45) ...添付資料番号 5.3.5.2(15 群)-1 2.5.1(5 群)臨床効果 咽喉頭炎・扁桃炎患者での有効率は 95.0%(19/20、95%CI = 85.4%, 100%)であっ た。 疾患別有効率は咽喉頭炎で 100%(7/7)、扁桃炎で 90.0%(9/10、95%CI = 71.4%, 100%)であった。その他、咽頭炎、扁桃周囲炎および扁桃周囲膿瘍はそれぞれ 1 名 で、いずれも「著効」であった。 2.5.2(5 群)細菌学的効果 陰性化率および消失率は、ともに 100%(12/12 および 13/13)であった。原因菌 は、S. aureus(3 株)、S. pneumoniae(1 株)、Streptococcus pyogenes(3 株)、H. influenzae (5 株)、Peptostreptococcus micros(1 株)であった。
3.(5 群)全試験を通しての結果の比較と解析 3.1(5 群)試験対象集団 3.1.1(5 群)試験対象集団の内訳 被験者の内訳を表 2.7.3.3.1(5 群)-1 に示す。 登録被験者 438 名中 392 名が完了し、46 名が未完了であった。未完了理由は、「被 験者の申し出」が 10 名、「効果不十分」が 11 名、「有害事象発現」が 14 名、「基準 に抵触」が 13 名、「来院せず」が 1 名であった。 表 2.7.3.3.1(5 群)-1 被験者の内訳 登録被験者数 438 完了被験者数 392(89.5) 未完了被験者数 46(10.5) 被験者の申し出 10 効果不十分 11 有害事象発現 14 基準に抵触 13 未完了理由a) 来院せず 1 括弧内の数値は% a:重複集計あり 解析対象集団の内訳を表 2.7.3.3.1(5 群)-2 に示す。 登録被験者 438 名中 49 名を除いた 389 名を PPS とし、細菌学的効果解析対象集 団は PPS から 202 名を除いた 187 名とした。なお、細菌学的効果解析対象集団は、 原因菌が分離された被験者 190 名(分離株数 219 株)から、投与終了・中止時の菌 検査が未実施であった被験者 5 名(分離株数 7 株)を除き、さらに原因菌は不明で あったが投与後出現菌が分離され、菌交代と判定された2名を加えた187名である。 表 2.7.3.3.1(5 群)-2 解析対象集団の内訳 登録被験者数 438 PPS 389 細菌学的効果解析対象集団 187 PPS 不採用理由を表 2.7.3.3.1(5 群)-3 に示す。 主な PPS 不採用理由は、「併用薬違反」が 17 名、「服薬違反」が 11 名、「対象外 疾患」が 9 名、「除外基準違反」が 6 名であった。
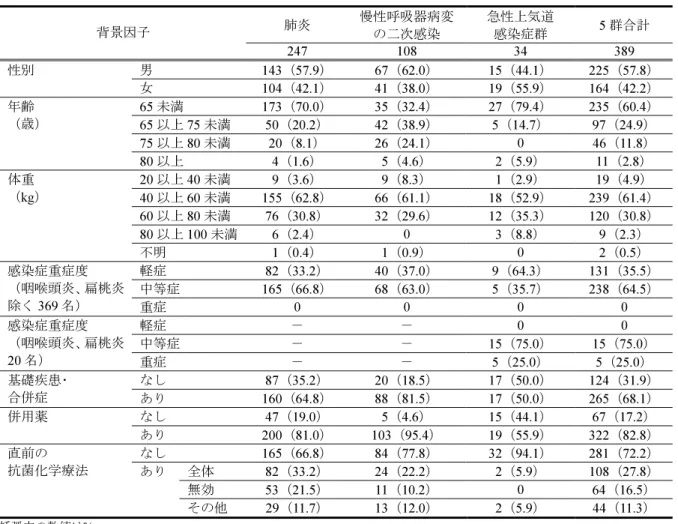
表 2.7.3.3.1(5 群)-3 PPS 不採用理由 PPS不採用被験者数 49(11.2) 未投与 2 対象外疾患 9 除外基準違反 6 服薬違反 11 併用薬違反 17 検査未実施等 3 不採用理由 来院せず 1 括弧内の数値は% 3.1.2(5 群)被験者背景 被験者背景を表 2.7.3.3.1(5 群)-4 に示す。 PPS 389 名のうち、肺炎患者が 63.5%(247/389)、慢性呼吸器病変の二次感染患者 が 27.8%(108/389)、急性上気道感染症群患者が 8.7%(34/389)であった。 年齢構成は、65 歳以上の被験者は肺炎患者が 30.0%(74/247)、慢性呼吸器病変の 二次感染患者が 67.6%(73/108)、急性上気道感染症群患者が 20.6%(7/34)であり、 慢性呼吸器病変の二次感染患者で高齢者の割合が高かった。 感染症重症度(咽喉頭炎、扁桃炎を除く)は、「中等症」は肺炎患者が 66.8%(165/247)、 慢性呼吸器病変の二次感染患者が 63.0%(68/108)、急性気管支炎患者が 35.7%(5/14) であり、急性気管支炎患者で「中等症」の割合が低かった。 基礎疾患・合併症が「あり」の被験者は、肺炎患者が 64.8%(160/247)、慢性呼 吸器病変の二次感染患者が 81.5%(88/108)、急性上気道感染症群患者が 50.0%(17/34) であり、急性上気道感染症群患者で基礎疾患・合併症が「あり」の割合が低かった。 併用薬が「あり」の被験者は、肺炎患者が 81.0%(200/247)、慢性呼吸器病変の 二次感染患者が 95.4%(103/108)、急性上気道感染症群患者が 55.9%(19/34)であ り、急性上気道感染症群患者で併用薬が「あり」の割合が低かった。 疾患別でのその他の背景因子の分布に違いは認められなかった。
表 2.7.3.3.1(5 群)-4 被験者背景 肺炎 慢性呼吸器病変の二次感染 急性上気道 感染症群 5群合計 背景因子 247 108 34 389 男 143(57.9) 67(62.0) 15(44.1) 225(57.8) 性別 女 104(42.1) 41(38.0) 19(55.9) 164(42.2) 65未満 173(70.0) 35(32.4) 27(79.4) 235(60.4) 65以上 75 未満 50(20.2) 42(38.9) 5(14.7) 97(24.9) 75以上 80 未満 20(8.1) 26(24.1) 0 46(11.8) 年齢 (歳) 80以上 4(1.6) 5(4.6) 2(5.9) 11(2.8) 20以上 40 未満 9(3.6) 9(8.3) 1(2.9) 19(4.9) 40以上 60 未満 155(62.8) 66(61.1) 18(52.9) 239(61.4) 60以上 80 未満 76(30.8) 32(29.6) 12(35.3) 120(30.8) 80以上 100 未満 6(2.4) 0 3(8.8) 9(2.3) 体重 (kg) 不明 1(0.4) 1(0.9) 0 2(0.5) 軽症 82(33.2) 40(37.0) 9(64.3) 131(35.5) 中等症 165(66.8) 68(63.0) 5(35.7) 238(64.5) 感染症重症度 (咽喉頭炎、扁桃炎 除く 369 名) 重症 0 0 0 0 軽症 - - 0 0 中等症 - - 15(75.0) 15(75.0) 感染症重症度 (咽喉頭炎、扁桃炎 20名) 重症 - - 5(25.0) 5(25.0) なし 87(35.2) 20(18.5) 17(50.0) 124(31.9) 基礎疾患・ 合併症 あり 160(64.8) 88(81.5) 17(50.0) 265(68.1) なし 47(19.0) 5(4.6) 15(44.1) 67(17.2) 併用薬 あり 200(81.0) 103(95.4) 19(55.9) 322(82.8) なし 165(66.8) 84(77.8) 32(94.1) 281(72.2) 全体 82(33.2) 24(22.2) 2(5.9) 108(27.8) 無効 53(21.5) 11(10.2) 0 64(16.5) 直前の 抗菌化学療法 あり その他 29(11.7) 13(12.0) 2(5.9) 44(11.3) 括弧内の数値は%
3.1.3(5 群)原因菌の内訳
原因菌の内訳を表 2.7.3.3.1(5 群)-5 に示す。
5 群全体で 219 株の原因菌が分離され、主な原因菌は S. aureus が 11.0%(24/219)、 S. pneumoniaeが 25.6%(56/219)、M. (B.) catarrhalis が 8.2%(18/219)、H. influenzae が 28.8%(63/219)であった。これらの原因菌のほか、肺炎では M. pneumoniae が 11.7%(13/219)、慢性呼吸器病変の二次感染では P. aeruginosa が 12.6%(11/87)と 多く認められた。 表 2.7.3.3.1(5 群)-5 原因菌の内訳 肺炎 慢性呼吸器病変の二次感染 急性上気道 感染症群 5群合計 原因菌 111 87 21 219 全体 46(41.4) 29(33.3) 8(38.1) 83(37.9) S. aureus 9(8.1) 12(13.8) 3(14.3) 24(11.0) S. pneumoniae 37(33.3) 17(19.5) 2(9.5) 56(25.6) グラム陽性菌 S. pyogenes 0 0 3(14.3) 3(1.4) 全体 51(45.9) 58(66.7) 12(57.1) 121(55.3) M. (B.) catarrhalis 5(4.5) 10(11.5) 3(14.3) 18(8.2) E. coli 0 1(1.1) 0 1(0.5) Citrobacter spp. 0 1(1.1) 0 1(0.5) K. pneumoniae 5(4.5) 7(8.0) 0 12(5.5) Klebsiella spp. 0 1(1.1) 0 1(0.5) E. aerogenes 1(0.9) 1(1.1) 0 2(0.9) H. influenzae 35(31.5) 21(24.1) 7(33.3) 63(28.8) Haemophilus spp. 3(2.7) 3(3.4) 1(4.8) 7(3.2) P. aeruginosa 2(1.8) 11(12.6) 1(4.8) 14(6.4) S. maltophilia 0 1(1.1) 0 1(0.5) グラム陰性菌 other GNB 0 1(1.1) 0 1(0.5) 全体 0 0 1(4.8) 1(0.5) 嫌気性菌 Peptostreptococcus spp. 0 0 1(4.8) 1(0.5) 全体 14(12.6) 0 0 14(6.4) C.pneumoniae 1(0.9) 0 0 1(0.5) その他 M. pneumoniae 13(11.7) 0 0 13(5.9) 括弧内の数値は% 分離された 219 株のうち、MIC が測定された菌株に対する各種ニューキノロン系 抗菌薬の MIC 分布を図 2.7.3.3.1(5 群)-1 に示す。 シタフロキサシンの MIC は≤0.025~3.13 µg/mL に分布し、MIC90は 0.1 µg/mL であ り、他のニューキノロン系抗菌薬と比較し、最も抗菌力が強かった。
また、主な原因菌である S. aureus、S. pneumoniae、M. (B.) catarrhalis、H. influenzae の合計 138 株を分離時期により前期と後期に分け、ニューキノロン系抗菌薬に対する MIC 分布を図 2.7.3.3.1(5 群)-2 に示す。前期は 1998~2001 年に実施した 2 試験(添 付資料番号 5.3.5.1(5 群)-1、5.3.5.2(5 群)-2)、後期は 2005~2006 年に実施した 3 試験(添付資料番号 5.3.5.1(5 群)-2、5.3.5.2(5 群)-1、5.3.5.2(15 群)-1)とした。
主な原因菌に対するシタフロキサシンの MIC90は前期が 0.1 µg/mL、後期が 0.05 µg/mL とほぼ同様の抗菌力を示し、感受性の低下は認められなかった。レボフロキサ シン、トスフロキサシンでも同様に感受性の低下は認められなかった。 0 10 20 30 40 50 60 70 80 90 100 累 積 百 分 率( %) STFX LVFX TFLX CPFX SPFX GFLX MIC a) (µg/mL) 0.025 ≦ 0.05 0.1 0.2 0.39 0.78 1.56 3.13 6.25 12.5 25 50 100 100 < 合計 STFX (64.5)111 (89.5)43 (93.0)6 (96.5)6 (98.8)4 (99.4)1 (100)1 172 LVFX 56 (32.6) 28 (48.8) 5 (51.7) 16 (61.0) 13 (68.6) 36 (89.5) 13 (97.1) 3 (98.8) 2 (100) 172 TFLX 95 (55.2) 12 (62.2) 23 (75.6) 29 (92.4) 3 (94.2) 4 (96.5) 2 (97.7) 1 (98.3) 2 (99.4) 1 (100) 172 CPFX 74 (43.0) 13 (50.6) 1 (51.2) 5 (54.1) 24 (68.0) 33 (87.2) 16 (96.5) 2 (97.7) 2 (98.8) 2 (100) 172 SPFX (46.6)62 (57.1)14 (63.2)8 (76.7)18 (93.2)22 (96.2)4 (97.0)1 (97.7)1 (100)3 133 GFLX 51 (38.6) 16 (50.8) 16 (62.9) 19 (77.3) 24 (95.5) 2 (97.0) 3 (99.2) 1 (100) 132 0 10 20 30 40 50 60 70 80 90 100 累 積 百 分 率( %) STFX LVFX TFLX CPFX SPFX GFLX MIC a) (µg/mL) 0.025 ≦ 0.05 0.1 0.2 0.39 0.78 1.56 3.13 6.25 12.5 25 50 100 100 < 合計 STFX (64.5)111 (89.5)43 (93.0)6 (96.5)6 (98.8)4 (99.4)1 (100)1 172 LVFX 56 (32.6) 28 (48.8) 5 (51.7) 16 (61.0) 13 (68.6) 36 (89.5) 13 (97.1) 3 (98.8) 2 (100) 172 TFLX 95 (55.2) 12 (62.2) 23 (75.6) 29 (92.4) 3 (94.2) 4 (96.5) 2 (97.7) 1 (98.3) 2 (99.4) 1 (100) 172 CPFX 74 (43.0) 13 (50.6) 1 (51.2) 5 (54.1) 24 (68.0) 33 (87.2) 16 (96.5) 2 (97.7) 2 (98.8) 2 (100) 172 SPFX (46.6)62 (57.1)14 (63.2)8 (76.7)18 (93.2)22 (96.2)4 (97.0)1 (97.7)1 (100)3 133 GFLX 51 (38.6) 16 (50.8) 16 (62.9) 19 (77.3) 24 (95.5) 2 (97.0) 3 (99.2) 1 (100) 132 括弧内の数値は累積百分率 □:MIC90 TFLX の MIC については、「12.5<」を「25」に表示 a:日本化学療法学会標準法 図 2.7.3.3.1(5 群)-1 各種ニューキノロン系抗菌薬の MIC 分布<呼吸器感染症の原因菌>
0 10 20 30 40 50 60 70 80 90 100 累 積 百 分 率( %) ST FX(1998~2001年) LVFX(1998~2001年) TFLX(1998~2001年) ST FX(2005~2006年) LVFX(2005~2006年) TFLX(2005~2006年) 時期 (µg/mL) MIC a) 0.025 ≦ 0.05 0.1 0.2 0.39 0.78 1.56 3.13 6.25 12.5 25 50 100 100< 合計 STFX 17 (58.6)(89.7)9 (96.6)2 (100) 1 29 LVFX 11 (37.9)(48.3)3 (55.2)2 (62.1)2 (75.9)4 (96.6) 6 (100) 1 29 1998~ 2001 年 b) TFLX 16 (55.2)(62.1)2 (72.4)3 (96.6) 7 (100) 1 29 STFX 76 (69.7)(97.2)30 (99.1)2 (100) 1 109 LVFX 42 (38.5)(50.5)13 (51.4)1 (64.2)14 (66.1)2 (90.8)27 (99.1) 9 (100) 1 109 2005~ 2006年 c) TFLX 66 (60.6)(65.1)5 (81.7)18 (99.1) 19 (100) 1 109 0 10 20 30 40 50 60 70 80 90 100 累 積 百 分 率( %) ST FX(1998~2001年) LVFX(1998~2001年) TFLX(1998~2001年) ST FX(2005~2006年) LVFX(2005~2006年) TFLX(2005~2006年) 時期 (µg/mL) MIC a) 0.025 ≦ 0.05 0.1 0.2 0.39 0.78 1.56 3.13 6.25 12.5 25 50 100 100< 合計 STFX 17 (58.6)(89.7)9 (96.6)2 (100) 1 29 LVFX 11 (37.9)(48.3)3 (55.2)2 (62.1)2 (75.9)4 (96.6) 6 (100) 1 29 1998~ 2001 年 b) TFLX 16 (55.2)(62.1)2 (72.4)3 (96.6) 7 (100) 1 29 STFX 76 (69.7)(97.2)30 (99.1)2 (100) 1 109 LVFX 42 (38.5)(50.5)13 (51.4)1 (64.2)14 (66.1)2 (90.8)27 (99.1) 9 (100) 1 109 2005~ 2006年 c) TFLX 66 (60.6)(65.1)5 (81.7)18 (99.1) 19 (100) 1 109 括弧内の数字は累積百分率 □:MIC90 a:日本化学療法学会標準法 b:添付資料番号 5.3.5.1(5 群)-1、5.3.5.2(5 群)-2 c:添付資料番号 5.3.5.1(5 群)-2、5.3.5.2(5 群)-1、5.3.5.2(15 群)-1 図 2.7.3.3.1(5 群)-2 治験実施時期別の MIC 分布<呼吸器感染症の主な原因菌> 3.2(5 群)全有効性試験の結果の比較検討 3.2.1(5 群)臨床効果 疾患別の臨床効果を表 2.7.3.3.2(5 群)-1 に示す。 有効率は全体で 92.8%(361/389、95%CI = 90.2%, 95.4%)であった。 疾患別有効率は、肺炎が 93.1%(230/247、95%CI = 90.0%, 96.3%)、慢性呼吸器病 変の二次感染が 90.7%(98/108、95%CI = 85.3%, 96.2%)、急性上気道感染症群が 97.1% (33/34、95%CI = 91.4%, 100%)であり、いずれの疾患においても 90%以上の有効 率であった。 肺炎での有効率は、細菌性肺炎が 93.1%(203/218)、マイコプラズマ肺炎が 89.5% (17/19)であり、クラミジア肺炎の 4 名、レジオネラ肺炎の 1 名および細菌性肺炎 と非定型肺炎を合併した患者の 5 名はいずれも「有効」と判定された。
慢性呼吸器病変の二次感染のうち主な疾患の有効率は、肺気腫の二次感染が 88.9%(24/27)、気管支拡張症の二次感染が 84.0%(21/25)、慢性気管支炎の二次感 染が 90.5%(19/21)、陳旧性肺結核の二次感染が 100%(14/14)、気管支喘息の二次 感染が 100%(11/11)であった。 表 2.7.3.3.2(5 群)-1 疾患別臨床効果 疾患名 有効被験者数/ 評価被験者数 (95%CI)有効率(%) (%)a) 全体 230/247 93.1(90.0, 96.3) 細菌性肺炎 203/218 93.1(89.8, 96.5) 全体 27/29 93.1(83.9, 100) マイコプラズマ肺炎 17/19 89.5(75.7, 100) クラミジア肺炎 4/4 − レジオネラ肺炎 1/1 − 細菌 + マイコプラズマ肺炎 3/3 − 肺炎 非定型肺炎 細菌 + クラミジア肺炎 2/2 − 全体 98/108 90.7(85.3, 96.2) 慢性気管支炎 19/21 90.5(77.9, 100) 気管支拡張症 21/25 84.0(69.6, 98.4) 気管支喘息 11/11 100(100, 100) 肺気腫 24/27 88.9(77.0, 100) 陳旧性肺結核 14/14 100(100, 100) 肺線維症 3/4 − 塵肺 2/2 − COPD 2/2 − 気管支拡張症 + 陳旧性肺結核 1/1 − 慢性呼吸器病変の 二次感染 気管支喘息 + 陳旧性肺結核 1/1 − 全体 33/34 97.1(91.4, 100) 扁桃炎 11/12 91.7(76.0, 100) 咽喉頭炎 8/8 100(100, 100) 急性上気道感染症群 急性気管支炎 14/14 100(100, 100) 5 群 全体 361/389 92.8(90.2, 95.4) a:正規近似による CI PPS 389 名のうち、原因菌が分離された 190 名の原因菌別臨床効果を表 2.7.3.3.2 (5 群)-2 に示す。 単独菌感染での有効率は 95.7%(157/164)、2 種の原因菌による複数菌感染では 100%(23/23)であり、3 種以上の原因菌による複数菌感染被験者 3 名のうち 2 名が 「有効」であった。複数菌感染においても単独菌感染とほぼ同じ有効率を示した。