健康・栄養食品研究 Vol. 17 No. 1 2020 doi: 10.20618/jhnfa.17.1_1
原著報文
Misatol GLのラットを用いた単回経口投与毒性試験及び
90日間経口投与毒性試験
河原 遼*
, †,山岡 一平**,平石 勝也***,金田 信也*
(受付日:2019年4月1日 受理日:2020年1月7日 オンライン発行日:2020年1月17日) Misatol GLをSD系ラット雌雄に単回及び90日間反復経口投与し,安全性について評価した.単回経口投与において, Misatol GL原液を5, 10及び15 mL/kgの用量で単回経口投与した結果,5 mL/kgでは異常は認められず,10及び15 mL/kgで 一過性の水様性下痢が認められた.90日間の反復経口投与において,Misatol GLを1.25, 2.5及び5 mL/kg/dayの用量で投与 した結果,雄のMisatol GL 1.25 mL/kg/day投与群及び5 mL/kg/day投与群及び雌のMisatol GL 2.5 mL/kg/day投与群及び 5 mL/kg/day投与群において,軽微な摂餌量の低下が,雄のMisatol GL 1.25 mL/kg/day投与群及び5 mL/kg/day投与群におい て,軽微な前胃の空胞化が認められたが,いずれも毒性学的な意義は低いと考えられた.一般状態,体重,尿検査,眼科学的 検査,血液検査,剖検及び器官重量において,Misatol GLに起因する変化は認められなかった.したがって,Misatol GLの 安全性は高いと考えられた.キーワード: Misatol GL,梅エキス,ラット,単回経口投与,90日間反復経口投与
Single dose and 90-day repeated dose oral toxicity studies of
a processed ume extract food Misatol in rats
Ryo Kawahara*
, †, Ippei Yamaoka**, Katsuya Hiraishi***, Shinya Kaneda*
Misatol GL is a neutralized processed food of ume extract which is a heated-concentrate of squeezed juice from green (immature) ume. Various biological effects of ume extract were reported, but its safety has not been evaluated. Hence, we evaluated safety of Misatol GL in SD rats by single dose and 90-day repeated oral administration. As a result of single oral dose, transient watery diarrhea was observed in Misatol GL 10 and 15 mL/kg groups, and this change was not observed in Misatol GL 5 mL/kg group. In 90-day repeated oral administration, a slight decrease in food consumption were observed in male Misatol GL 1.25 and 5 mL/kg/day groups and female Misatol GL 2.5 and 5 mL/kg/day groups. A slight vacuolation of forestomach were observed in male Misatol GL 1.25 and 5 mL/kg/day groups. These changes were considered to low toxico-logical significance. In addition, no changes caused by Misatol GL were observed in clinical signs, body weight, urinalysis, ophthalmology, blood test, necropsy and organ weight.
Key words: Misatol GL, ume extract, rat, single dose, 90-day repeated oral administration
Journal of Nutritional Food, 17(1), 1–17, 2019
† Corresponding author (E-mail: [email protected])
* Naruto Research Institute, Otsuka Pharmaceutical Factory, Inc., 115 Kuguhara, Tateiwa, Muya-cho, Naruto Tokushima 772–8601
** Medical Foods Research Institute Otsuka Pharmaceutical Factory, Inc., 115 Kuguhara, Tateiwa, Muya-cho, Naruto Tokushima 772–8601
*** AdaBio Co., Ltd., 21–2 Kenzaki-machi, Takasaki, Gunma 370–0883
* 株式会社大塚製薬工場 鳴門研究所 〒772–8601 徳島県鳴門市撫養町立岩字芥原115
** 株式会社大塚製薬工場 メディカルフーズ研究所 〒772–8601 徳島県鳴門市撫養町立岩字芥原115 *** AdaBio株式会社 〒370–0883 群馬県高崎市剣崎町21番地2
I.
緒言
梅(学名Prunus mume Sieb. et Zucc)は,バラ
科のサクラ属に属する植物で,その果実である梅果
実は,食用または民間薬として古くから利用されて
きた.梅の未成熟果実(青梅)を燻製にして乾燥さ
せた烏梅(ウバイ)は生薬として使用され,口渇や
吐き気の鎮静,止瀉,駆虫,解熱などの作用が知
られている(日本薬局方外生薬規格に収載).また,
青梅搾汁を加熱濃縮した青梅搾汁加熱濃縮液(いわ
ゆる梅エキスまたは梅肉エキス)は,黒褐色の粘性
のあるペースト状の液体で,梅果汁に由来する有機
酸(クエン酸やリンゴ酸など)を多量に含み,日本
では主に下痢や腹痛などの民間薬として利用され
てきた.近年では,この梅エキスに特有の成分とし
て,加熱によって生成する5-ヒドロキシメチル2-フルフラールとクエン酸がエステル結合したムメフ
ラールが,血流改善成分として報告されている
1).
現代においても,これらの長年の食経験を背景に,
多くの梅エキスに関連する市販食品が販売されてい
る.
青梅搾汁加熱濃縮液の試験研究用の中和加工物
(MK615,香料や甘味料等の食品添加剤不含)を
使用した研究では,様々なヒトがん細胞株に対し
て増殖抑制作用や細胞死誘導作用が報告されてお
り
2–7),最近ではがん細胞内に活性酸素種を蓄積さ
せることによりがん細胞の細胞死を誘導する作用が
報告されている
8).また,マウスのB16メラノーマ
の肺転移モデルを用いた検討で腫瘍細胞のNFκB
の活性化やPD-L1の発現を減弱し,T細胞介在性
の抗腫瘍作用や延命効果を有することが示唆され
ている
9).抗腫瘍作用以外の研究では,MK615が
D-galactosamine誘発急性肝障害モデルラットにお
いてAST及びALTの上昇を軽減させ,肝障害を軽
減させること,さらにヒトにおいても青梅搾汁加熱
濃縮液の中和加工食品であるMisatol ME(青梅搾
汁加熱濃縮液の含量がGLの半量)がC型慢性肝炎
患者及び非アルコール性脂肪性肝疾患患者におい
て,AST及びALTを低下させることが報告されて
いる
10).
このように青梅搾汁加熱濃縮液を含む食品素材
は,様々な生物作用を有する可能性が報告されてい
るが,系統立った試験評価系によってその安全性を
評価した報告はない.そこで,青梅搾汁加熱濃縮液
の中和加工物を含むMisatol GLをSD系ラット雌
雄に単回及び90日間反復経口投与したときの影響
について評価した.
II. 単回経口投与毒性試験
1. 被験物質及び投与液の調製法
Misatol GL(AdaBio株式会社)は,賞味期限内
(製造から2年以内)のものを使用した.投与液の
調製は行わず,原液をそのまま投与に用いた.今回
使用したMisatol GLは,製品形態として小袋(小
包)に分注されていて,1袋あたりに約6.5 g(規格
値で6.24 g以上)を含有し(容量で約5 mL),内容
物中に青梅搾汁加熱濃縮液に由来する沈殿物を含
む.本来,青梅搾汁加熱濃縮液は,含有するクエン
酸やリンゴ酸のために酸性を示すが,Misatol GL
では食品として中和加工されている.また,食品添
加物として香料,甘味料(スクラロース,
D-ソルビ
トール,環状オリゴ糖)等を含有し,粘性のある液
体である.エネルギー量は15kcal/6.5 gである.
2. 使用動物及び飼育条件
5週齢のCrl:CD(SD)系ラット雌雄各12匹を日
本チャールス・リバー株式会社より購入し,14日
間の馴化期間を設けた.飼料はCRF-1(オリエン
タル酵母工業株式会社)を給餌し,自由に摂取させ
た.投与日の2日前に一般状態の観察及び体重測定
を実施し,異常が認められなかったため,雌雄とも
全例(各12匹)を用いて体重層別無作為化抽出法
によって群分けを行った.1群の動物数は3匹(雌
雄各4群,合計24匹)とした.
動 物 の 飼 育 環 境 は, 温 度23±3°C, 湿 度55±
15%,換気回数9∼11回/時,人工照明1日12時
間(7:00∼19:00)に設定した施設で,1ケージに
つき1匹を収容して飼育した.飲料水は除菌濾過装
置を通した水道水を給水瓶にて自由摂取させた.
なお,本試験は,株式会社大塚製薬工場の動物実
験指針に従い,動物実験委員会の審査を受けて実施
した.
3. 投与方法及び投与量
Misatol GLの原液15 mL/kgを最高用量とし,以
下,10及び5 mL/kgの3群を設定した.
なお,ヒトの推奨摂取量は,1日3袋(約15 mL)
とした場合0.3 mL/kg(ヒト50 kg換算)となるた
め,投与量15, 10及び5 mL/kgは約50, 33及び16
倍となる.
投与は,経口ゾンデ及び注射筒を用いて単回経口
投与した.対照群には注射用水(容量:15 mL/kg)
を同様の方法で投与した.なお,投与前は16時間
以上絶食とした.
4. 観察,測定及び検査
1)一般状態
雌雄全例について,投与日は投与前及び投与後5
時間まで連続的に,投与翌日から観察期間終了日ま
では1日1回,死亡の確認を含めた一般状態の観察
を行った.
2)体重
雌雄全例について,投与日(投与前),投与2, 4,
6, 8, 10, 12及び14日後に電子天秤を用いて測定し
た.
3)摂餌量
雌雄全例について,投与日(投与前),投与2, 4,
6, 8, 10, 12及び14日後に電子天秤を用いて測定し,
2日間の総摂餌量から1日当たりの摂餌量を算出し
た.前値として,投与日の2日前から投与前日まで
の1日分も測定した.
4)病理学的検査
観察期間終了日に,生存例についてイソフルラン
麻酔下で放血安楽死させ,外表,内部器官及び組織
を肉眼的に観察した.
5. 統計学的処理
体重及び摂餌量について,各群の平均値と標準偏
差を求めたが,統計解析は実施しなかった.
6. 結果
観察期間を通じて死亡例はみられなかった.注
射用水投与群及びMisatol GL 5 mL/kg投与群では,
雌雄ともにすべての動物で異常は認められなかっ
た.雄のMisatol GL 10 mL/kg投与群の3例中1例
で,投与翌日及び投与2日後に水様性下痢が認めら
れた.雌のMisatol GL 10 mL/kg投与群では,すべ
ての動物で異常は認められなかった.Misatol GL
15 mL/kg投与群では,雌雄ともにすべての動物で,
投与翌日に水様性下痢が認められ投与2日後以降は
認められなかった.体重について,観察期間中のす
べての測定時において雌雄いずれの投与群において
も変動は認められなかった(Table 1).摂餌量につ
いて,雌雄ともに観察期間中のすべての測定時にお
いてほぼ同様に推移した(Table 2).また,剖検に
おいて,雌雄いずれの投与群においても肉眼的所見
Table 1 Body weight data (g) of rats orally administrated a single dose of Misatol GLSex (mL/kg)Dose Day
0 2 4 6 8 10 12 14 Male 0 238.1±19.4 279.0±28.6 292.2±30.2 307.0±33.7 320.2±37.0 335.8±40.2 345.2±47.0 358.1±49.1 5 246.8±13.1 285.4±16.9 305.6±20.1 318.7±22.1 336.1±25.4 358.0±30.0 364.9±33.0 385.3±37.9 10 240.2±5.2 278.0±4.9 293.1±5.1 305.6±4.5 318.3±9.4 335.0±11.3 342.3±12.5 357.6±13.1 15 238.4±7.6 275.2±10.9 291.0±16.1 304.6±22.9 317.2±27.9 332.3±28.2 341.8±29.8 353.8±31.7 Female 0 174.4±2.1 197.4±6.0 207.1±1.9 210.1±3.6 223.4±2.5 225.5±7.8 235.9±3.5 238.0±10.2 5 170.8±5.4 195.4±3.0 202.1±2.9 213.4±5.8 217.7±6.6 231.3±13.5 234.7±7.7 244.5±9.6 10 173.3±2.1 194.2±2.1 202.0±1.5 210.9±6.2 219.6±7.3 225.6±6.8 227.1±3.7 238.4±7.9 15 168.3±1.7 189.6±1.3 198.7±3.8 205.0±2.2 211.7±3.4 218.0±0.7 223.4±0.7 229.1±3.7 Means±SD
に異常は認められなかった.
III. 90日間反復経口投与毒性試験
1. 被験物質及び投与液の調製法
Misatol GL(AdaBio株式会社)は,賞味期限内
(製造から2年以内)のものを使用した.Misatol
GLの原液を注射用水(大塚蒸留水,株式会社大塚
製薬工場)で希釈し,Misatol GLの1/2, 1/4, 1/8希
釈液を調製した.今回使用したMisatol GLは,製
品形態として小袋(小包)に分注されていて,1袋
あたりに約6.5 g(規格値で6.24 g以上)を含有し
(容量で約5 mL),内容物中に青梅搾汁加熱濃縮液
に由来する沈殿物を含む.本来,青梅搾汁加熱濃縮
液は,含有するクエン酸やリンゴ酸のために酸性を
示すが,Misatol GLでは食品として中和加工され
ている.また,食品添加物として香料,甘味料(ス
クラロース,
D-ソルビトール,環状オリゴ糖)等を
含有し,粘性のある液体である.エネルギー量は
15kcal/6.5 gである.
2. 使用動物及び飼育条件
5週齢のCrl:CD(SD)系ラット雌雄各48匹を日
本チャールス・リバー株式会社より購入し,入荷
後,12日間の検疫を含む投与開始日までの馴化期
間を設けた.投与日の6日前に一般状態の観察及び
体重測定を実施し,異常が認められなかったため雌
雄とも全例(各45匹)を用いて体重層別無作為化
抽出法によって群分けを行った.1群の動物数は10
匹(雌雄各4群,合計80匹)とした.
動 物 の 飼 育 環 境 は, 温 度23±3°C, 湿 度55±
15%,換気回数13∼16回/時,人工照明1日12時
間(7:00∼19:00)に設定したSPF施設で,1ケー
ジにつき1匹を収容して飼育した.飲料水は除菌濾
過装置を通した水道水を自動給水ノズルから自由に
摂取させた.
なお,本試験は,株式会社大塚製薬工場の動物実
験指針に従い,動物実験委員会の審査を受けて実施
した.
3. 投与方法及び投与量
先に実施したMisatol GLのラットにおける4週
間反復経口投与毒性予備試験の結果から,Misatol
GLの5 mL/kg/day投与群で雌雄ともに摂餌量が,
雄で体重が注射用水投与群と比較して低値傾向で
あった.したがって,5 mL/kgを最高用量とし,以
下,2.5及び1.25 mL/kgの3群を設定した.なお,
ヒトの推奨摂取量は,1日3袋(約15 mL)として
0.3 mL/kg(ヒト50 kg換算)なので約16, 8, 4倍の
用量となる.
投与は経口ゾンデ及び注射筒を用いて1日1回90
日間反復経口投与した.対照群には注射用水を同様
の方法で投与した.投与容量はラットの経口投与に
おける推奨投与容量
11)である10 mL/kgとした.
Table 2 Food consumption data (g) of rats orally administrated a single dose of Misatol GL
Sex (mL/kg)Dose Day
0–2 2–4 4–6 6–8 8–10 10–12 12–14 Male 0 31.5±3.4 27.4±0.5 27.0±2.4 24.3±1.9 24.2±2.1 26.2±3.6 25.2±2.8 5 30.3±2.4 30.2±3.5 28.1±2.2 28.5±2.3 27.9±2.6 25.8±3.4 28.2±3.0 10 28.6±2.5 27.4±2.0 24.8±1.9 25.3±2.8 25.4±1.9 24.3±1.7 25.1±1.7 15 29.3±0.5 28.4±3.3 26.7±3.5 24.7±3.6 25.1±2.4 24.3±2.4 24.9±2.6 Female 0 22.2±0.5 19.5±1.8 17.8±0.8 20.3±1.2 16.4±1.0 19.6±0.8 17.7±1.0 5 21.2±1.9 19.7±3.4 19.2±1.1 18.3±1.1 18.4±2.1 18.5±0.5 19.0±1.3 10 19.5±1.7 19.2±0.8 18.9±2.1 19.1±0.8 17.6±1.7 18.2±1.0 18.6±2.0 15 18.8±0.2 19.1±1.2 17.2±1.5 17.7±0.9 16.5±0.9 18.1±1.3 16.9±0.9 Means±SD
4. 観察,測定及び検査
1)一般状態
雌雄全例について,投与期間中は毎日,投与前及
び投与後の1日2回観察した.
2)体重
雌雄全例について,週1回,投与前に測定した.
また,剖検日に器官比重量算出のための体重を測定
した.
3)摂餌量
雌雄全例について,投与期間中は週2回,午前
(投与期間中は投与前)に測定し,各期間の総摂餌
量から1日当たりの摂餌量を算出した.前値とし
て,投与開始日の前日から投与開始日までの1日分
も測定した.
4)尿検査
86日目の投与前に各群の動物番号の最初から実
施し,新鮮尿が採取できた最初の5例について実施
した.強制排尿により新鮮尿を採取した後,外観,
色調を観察し,定性検査としてマルティスティック
ス(シーメンスヘルスケア・ダイアグノスティクス
株式会社)を用いて,pH,蛋白質,ブドウ糖,ケ
トン体,ビリルビン,ウロビリノーゲン及び潜血に
ついて検査した.
5)眼科学的検査
各群の動物番号の最後から5例について,投与開
始5日前及び84日目の投与後に実施した.肉眼で,
外観及び光に対する瞳孔反射を観察後,散瞳剤によ
り散瞳させ,前眼部及び中間透光体を観察し,眼底
検査を実施した.
6)血液学的検査
各群の全例について,投与期間終了時の剖検に先
立ち,16時間以上絶食させた動物をイソフルラン
麻酔下で開腹し,後大静脈から採血を行った.採取
した血液の一部を抗凝固剤(EDTA-2K)入り採血
管に分注し,転倒混和した後,赤血球数(RBC),
血色素量(HGB),ヘマトクリット値(HCT),血
小板数(PLT),白血球数(WBC),平均赤血球容
積(MCV),平均赤血球色素量(MCH),平均赤血
球色素濃度(MCHC),網赤血球数(Ret.#),網赤
血球比率(Ret.%),好中球数比率(NEUT%),好
酸球数比率(EO%),好塩基球数比率(BASO%),
単 球 数 比 率(MONO%), リ ン パ 球 数 比 率
(LYMPH%)について測定した.血液凝固関連
の測定には,あらかじめ抗凝固剤を入れておいた
1 mL注射筒で採血し,遠心分離して得られた血漿
を使用し,プロトロンビン時間(PT),活性化部分
トロンボプラスチン時間(APTT)について測定し
た.
7)血液生化学的検査
血液生化学的検査には,採血後,30∼45分間室
温放置した後,遠心分離した血清を使用し,アスパ
ラギン酸アミノトランスフェラーゼ(AST),アラ
ニンアミノトランスフェラーゼ(ALT),アルカリ
フォスファターゼ(ALP),総蛋白(T-P),アルブ
ミン(ALB),A/G比(A/G),グルコース(GLU),
総 コ レ ス テ ロ ー ル(T-CHO), ト リ グ リ セ リ ド
(TG),総ビリルビン(T-BIL),リン脂質(PL),
尿素窒素(UN),クレアチニン(CRE),カルシ
ウム(Ca),無機リン(P)について,自動分析装置
7180(株式会社日立ハイテクノロジーズ)を用い
て測定し,ナトリウムイオン(Na),カリウムイオ
ン(K),塩素イオン(Cl)について,全自動電解質
分析装置EA07(株式会社エイアンドティー)を用
いて測定した.
8)剖検及び器官重量
血液を採取した後放血安楽死させ,外表,投与部
位,内部器官及び組織を肉眼的に観察し,脳(大
脳,小脳,延髄を含む),胸腺,脾臓,下顎腺,肝
臓,下垂体,甲状腺,副腎,心臓,腎臓,精巣,精
巣上体,前立腺,精嚢,卵巣,子宮については,器
官重量を測定し,剖検日の体重から器官重量体重比
(比重量)を算出した.
9)病理組織学的検査
重量を測定した器官に加えて,脊髄,坐骨神経,
下顎リンパ節,腸間膜リンパ節,大腿骨(骨,骨
髄),胸骨(骨,骨髄),舌,食道,胃(前胃,腺
胃),小腸(十二指腸,空腸,回腸),大腸(盲腸,
結腸,直腸),膵臓,上皮小体,気管,大動脈,膀
胱,膣,眼球,ハーダー腺,大腿筋,皮膚(乳腺)
について,10%中性緩衝ホルマリン液(眼球及び
ハーダー腺は1.5%グルタールアルデヒド・3%ホ
ルマリン液,精巣は12%ホルマリン・4%酢酸液)
で固定した.常法にしたがってパラフィン薄切標本
を作製後,ヘマトキシリン・エオジン(HE)染色
を施し,病理組織学的検査を実施した.病理組織
学的検査は,まず注射用水投与群及びMisatol GL
5 mL/kg投与群について実施した.被験物質の影響
として軽微な前胃の空胞化がMisatol GL 5 mL/kg/
day投与群の雄1例で認められたため,Misatol GL
2.5 mL/kg/day投与群及びMisatol GL 1.25 mL/kg/
day投与群の胃についても実施した.また,剖検に
おいて異常所見がみられたMisatol GL 1.25 mL/kg/
day投与群の雄1例の心臓,肺及び精嚢についても
実施した.
5. 統計学的手法
注射用水投与群を陰性対照として,体重,摂餌
量,血液検査及び器官重量について,Bartlettの方
法によって等分散性を検定した.その結果,等分
散のものについては一元配置分散分析によって解
析し,有意な群間差が認められた場合,Dunnettの
多重比較を行った.一方,不等分散を示したもの,
網赤血球比率及び白血球分類についてはKruskal–
Wallisの方法により解析し,有意な群間差が認め
られた場合,Steelの多重比較を行った.なお,有
意水準は5%とした.
6. 結果
1)切迫殺例
投与49日目の投与前に注射用水投与群の1例に
おいて,一般状態の悪化(重度の自発運動の低下,
鼻,耳,尾,四肢の蒼白,緩徐呼吸)が認められた
ため,試験継続は不可能と判断し,切迫殺を実施
した.血液学的検査において,RBC, HGB, HCT及
びPLTの低値,WBC, NEUT%の増加,血液生化
学的検査において,AST, ALT, UN, CRE, Kの異常
高値,P, T-BILの軽度高値,T-P, ALB軽度低下が
認められた.また,剖検において,腹腔内の血様腹
水,肝臓尾状葉の血腫様肥大,横隔膜及び胸壁の赤
色斑がみられ,病理組織学的検査において,肝臓の
重度のうっ血及び小葉中心性の肝細胞壊死,横隔膜
の出血がみられた.これらの変化は,注射用水投与
群での変化であることから,投与時の物理的な傷害
によるものであると判断した.
2)一般状態,体重,摂餌量
一般状態について,投与期間中,切迫殺例を除
き,雌雄いずれの投与群においても異常は認められ
なかった.
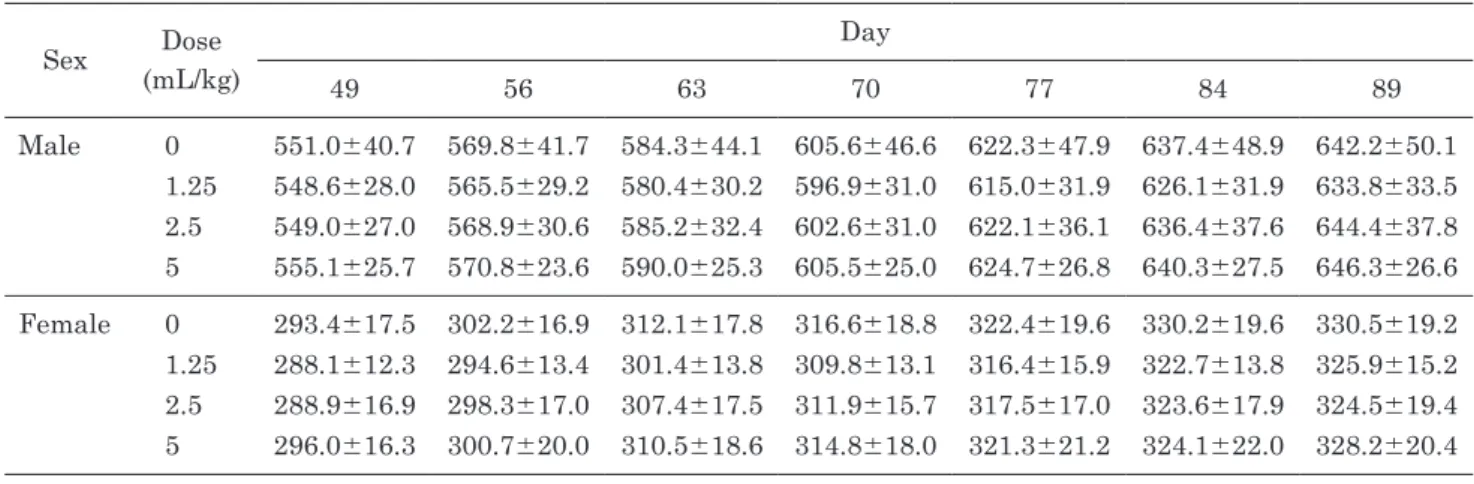
体重について,雌雄とも投与期間中のすべての測
定時において,群間差は認められなかった(Table
3-1∼3-2).
摂餌量について,雄のMisatol GL 1.25 mL/kg/
day投与群及び5 mL/kg/day投与群において,投
与9日後以降,注射用水投与群と比較して,摂餌
量が有意な低値を示す観察ポイントが散見された
Table 3-1 Body weight data (g) of rats orally administrated Misatol GL for 90 daysSex (mL/kg)Dose Day
0 7 14 21 28 35 42 Male 0 322.0±8.8 371.2±15.4 413.1±19.2 449.1±23.5 482.9±27.5 509.3±29.2 530.1±33.1 1.25 321.8±10.5 372.2±15.4 413.6±17.2 447.1±23.7 477.3±23.2 504.1±23.3 527.2±26.4 2.5 320.0±9.9 372.2±13.6 417.6±15.5 451.8±16.7 480.4±18.2 507.5±24.4 529.9±24.7 5 318.3±10.8 368.7±11.9 412.5±17.6 448.2±19.5 482.3±18.8 508.7±22.7 533.8±22.3 Female 0 210.7±9.2 227.8±10.9 244.6±14.6 258.9±16.3 271.0±14.8 280.2±14.5 288.0±16.6 1.25 203.0±9.3 219.7±9.2 236.6±12.5 252.2±12.1 260.5±14.1 272.0±11.2 281.7±9.5 2.5 207.6±9.8 227.7±13.4 242.7±13.2 252.4±16.9 266.8±16.1 276.8±15.3 284.3±15.4 5 207.1±11.8 226.8±10.2 242.2±9.6 254.9±10.4 267.8±13.8 280.6±13.3 288.8±13.9 Means±SD
(Table 4-1∼4-4).雌のMisatol GL 2.5 mL/kg/day
投与群及び5 mL/kg/day投与群において,投与30
日後以降,注射用水投与群と比較して,摂餌量が有
意な低値を示す観察ポイントが散見された(Table
4-1∼4-4).
Table 3-2 Body weight data (g) of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg) Day 49 56 63 70 77 84 89 Male 0 551.0±40.7 569.8±41.7 584.3±44.1 605.6±46.6 622.3±47.9 637.4±48.9 642.2±50.1 1.25 548.6±28.0 565.5±29.2 580.4±30.2 596.9±31.0 615.0±31.9 626.1±31.9 633.8±33.5 2.5 549.0±27.0 568.9±30.6 585.2±32.4 602.6±31.0 622.1±36.1 636.4±37.6 644.4±37.8 5 555.1±25.7 570.8±23.6 590.0±25.3 605.5±25.0 624.7±26.8 640.3±27.5 646.3±26.6 Female 0 293.4±17.5 302.2±16.9 312.1±17.8 316.6±18.8 322.4±19.6 330.2±19.6 330.5±19.2 1.25 288.1±12.3 294.6±13.4 301.4±13.8 309.8±13.1 316.4±15.9 322.7±13.8 325.9±15.2 2.5 288.9±16.9 298.3±17.0 307.4±17.5 311.9±15.7 317.5±17.0 323.6±17.9 324.5±19.4 5 296.0±16.3 300.7±20.0 310.5±18.6 314.8±18.0 321.3±21.2 324.1±22.0 328.2±20.4 Means±SD
Table 4-1 Food consumption data (g) of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg) Day −1 0–2 2–6 6–9 9–13 13–16 16–20 Male 0 25.5±1.4 25.9±2.0 26.7±1.8 26.1±1.9 26.3±1.7 26.1±1.9 26.4±2.0 1.25 24.6±1.7 25.6±1.7 25.7±1.5 25.6±1.5 25.6±1.2 25.6±1.6 25.8±1.7 2.5 25.0±1.7 25.0±1.5 25.5±1.2 25.5±1.1 26.3±1.2 25.8±1.2 26.0±1.1 5 25.0±2.4 24.3±2.3 24.6±1.7 24.1±2.1 24.3±1.6* 24.0±1.3* 24.3±1.1* Female 0 15.5±1.5 16.3±1.5 16.4±1.2 16.6±1.3 16.7±0.9 17.1±1.1 16.7±1.0 1.25 15.2±1.8 15.8±1.5 15.9±1.2 16.2±1.3 16.4±1.0 16.8±1.0 16.6±1.1 2.5 15.1±1.5 15.5±1.7 16.1±1.6 16.2±1.4 16.0±1.5 16.4±1.6 15.9±1.4 5 15.0±2.2 15.0±1.0 15.3±0.7 15.8±1.2 15.4±1.1 15.7±1.0 15.6±1.1 Means±SD
Significantly different from control group: *p<0.05
Table 4-2 Food consumption data (g) of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg) Day 20–23 23–27 27–30 30–34 34–37 37–41 41–44 Male 0 26.2±2.2 26.1±1.8 26.7±2.0 26.0±1.9 26.0±1.7 26.0±2.5 26.0±2.3 1.25 24.2±4.0 25.3±1.2 25.2±1.6 24.9±1.2 24.9±1.6 25.1±1.2 25.2±1.3 2.5 25.4±1.2 25.1±1.1 25.6±1.7 24.8±1.2 24.7±1.4 25.1±1.3 25.1±1.2 5 24.2±1.4 24.8±1.4 24.6±1.3* 24.6±1.5 24.1±1.5 24.4±1.8 24.0±1.6 Female 0 16.9±1.2 16.9±1.2 16.6±1.6 16.7±1.1 16.9±1.1 16.6±1.4 16.6±1.4 1.25 16.7±1.3 16.7±1.0 16.0±1.7 16.4±0.8 15.9±1.4 16.3±0.8 15.9±1.7 2.5 16.1±1.6 16.0±1.4 15.8±1.3 15.8±1.4 15.3±1.6* 15.7±1.4 15.9±1.5 5 16.0±1.0 15.7±1.4 15.2±1.6 15.2±1.2* 15.1±1.5* 14.8±1.2** 14.9±1.5 Means±SD
3)尿検査,眼科学的検査
雄 のMisatol GL 5 mL/kg/day投 与 群 の1例 に
おいて,尿の混濁(白濁)が認められた(Table
5-1).本変化は当該群の他の個体では認められな
かったことから偶発的変化であると考えられた.尿
の色調及びpHについては,雌雄いずれの投与群
においても異常は認められなかった(Table 5-1∼
5-2).雄のいずれの投与群においてもケトン体陽性
(±∼2+)となった(Table 5-5)が,注射用水投
与群においても認められたことから,Misatol GL
による影響ではないと考えられた.その他,Misa-tol GLの雌雄いずれの投与群においても蛋白質陽
性(±∼2+),潜血反応陽性(±∼1+, ±はいずれ
も溶血)となる個体が散見された(Table 5-3, 5-6)
が,注射用水投与群においても認められたことか
ら,Misatol GLによる影響ではないと考えられた.
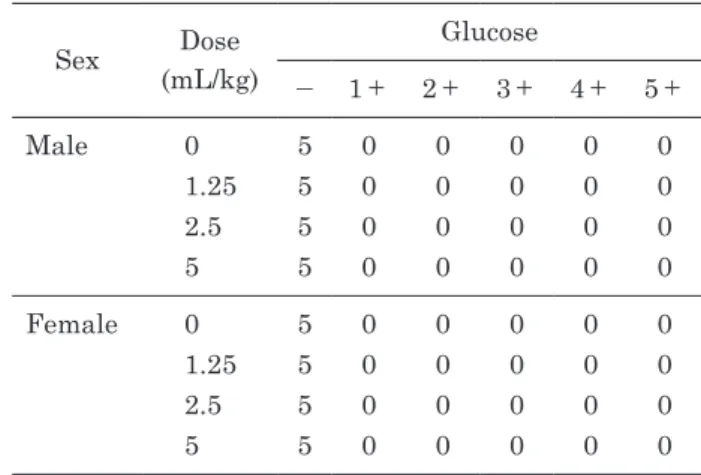
ブドウ糖,ビリルビン,ウロビリノーゲンについて
は,雌雄いずれの投与群においても陽性反応は認め
られなかった(Table 5-4, 5-5, 5-6).
Table 4-3 Food consumption data (g) of rats orally administrated Misatol GL for 90 days
Sex (mL/kg)Dose Day
44–48 48–51 51–55 55–58 58–62 62–65 65–69 Male 0 26.7±2.7 25.7±2.6 26.9±2.6 27.1±2.7 26.6±2.3 26.8±2.7 26.9±2.1 1.25 26.0±1.6 24.9±1.5 25.3±1.1 25.1±1.4 25.6±1.1 24.8±1.5 25.1±1.4* 2.5 25.3±1.5 24.9±1.3 25.2±1.7 25.2±1.3 25.1±1.5 25.8±1.4 25.7±1.0 5 24.3±1.6* 23.3±1.6* 23.9±1.7** 23.9±1.2* 24.0±1.5** 23.5±1.6** 24.4±1.4** Female 0 16.4±1.6 16.1±1.7 16.5±1.7 16.6±2.0 16.5±2.0 16.4±2.1 16.5±1.8 1.25 16.1±1.4 15.7±1.6 15.8±1.1 15.8±1.3 15.9±1.5 16.0±1.3 15.8±1.3 2.5 15.6±1.6 14.7±1.4 15.3±1.5 15.4±1.5 15.4±1.3 15.4±1.8 15.1±1.5 5 14.5±1.3* 14.7±1.3 14.4±1.4** 14.2±1.5** 14.6±1.6 14.3±1.7 14.1±1.6** Means±SD
Significantly different from control group: *p<0.05, **p<0.01
Table 4-4 Food consumption data (g) of rats orally administrated Misatol GL for 90 days
Sex (mL/kg)Dose Day
69–72 72–76 76–79 79–83 83–86 86–89 Male 0 27.1±2.5 27.4±2.8 27.6±2.9 27.0±2.4 27.7±3.9 25.5±2.5 1.25 26.0±1.4 25.9±1.3 25.9±1.4 25.3±1.6 25.1±1.6 24.2±1.8 2.5 25.6±1.1 25.9±1.4 26.2±1.8 25.8±1.5 25.0±1.2 23.8±1.4 5 24.6±1.3** 24.4±1.2* 25.2±1.9 24.6±1.5* 23.8±1.8* 22.8±1.2** Female 0 16.6±1.3 16.6±1.5 16.4±1.1 16.5±1.6 16.0±1.9 15.2±1.4 1.25 15.9±1.5 16.2±1.4 16.6±2.1 16.3±1.2 15.8±1.4 14.9±1.2 2.5 15.4±1.3 15.8±2.0 15.1±1.4 15.4±2.1 14.8±2.0 14.1±2.3 5 14.3±1.3** 14.1±1.6** 14.8±1.6 14.2±1.4** 13.8±2.1 13.1±2.2 Means±SD
Significantly different from control group: *p<0.05, **p<0.01
Table 5-1 Urinalysis data of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg) Appearance Color CL WT WFM CL LY Y B OTH Male 0 5 0 0 0 4 1 0 0 1.25 5 0 0 0 5 0 0 0 2.5 5 0 0 0 4 1 0 0 5 4 1 0 0 3 2 0 0 Female 0 5 0 0 0 3 2 0 0 1.25 5 0 0 0 2 3 0 0 2.5 5 0 0 0 3 2 0 0 5 5 0 0 0 3 2 0 0
眼科学的検査については,雌雄いずれの投与群に
おいても,Misatol GLに起因する変化は認められ
なかった.
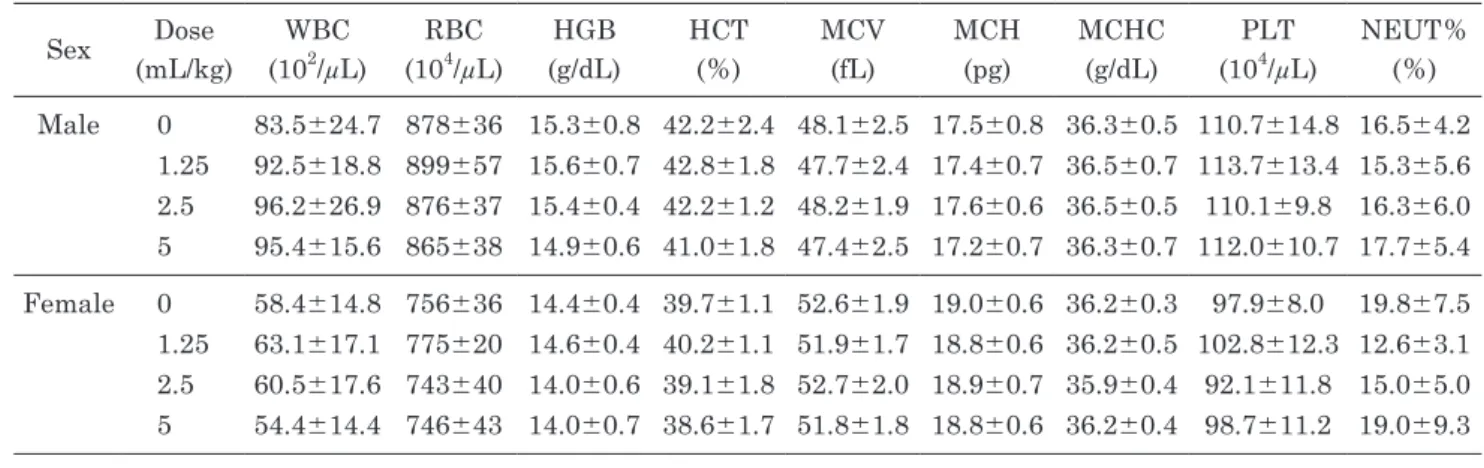
4)血液検査
血液学的検査の結果をTable 6-1∼6-2に示す.
雄のMisatol GL 1.25 mL/kg/day投与群において,
注射用水投与群と比較して,Ret.#の有意な上昇が
認められた.また,雌のMisatol GL 1.25 mL/kg/
day投与群において,注射用水投与群と比較して
LYMPH%の有意な上昇,2.5 mL/kg/day投与群に
おいて,注射用水投与群と比較してBASO%の有意
な低下が認められた.いずれの変化も軽微な変化
であること,用量依存性が認められないことから,
Misatol GLによる影響ではないと考えられた.そ
の他の測定項目については,雌雄いずれの投与群に
おいても群間差は認められなかった.
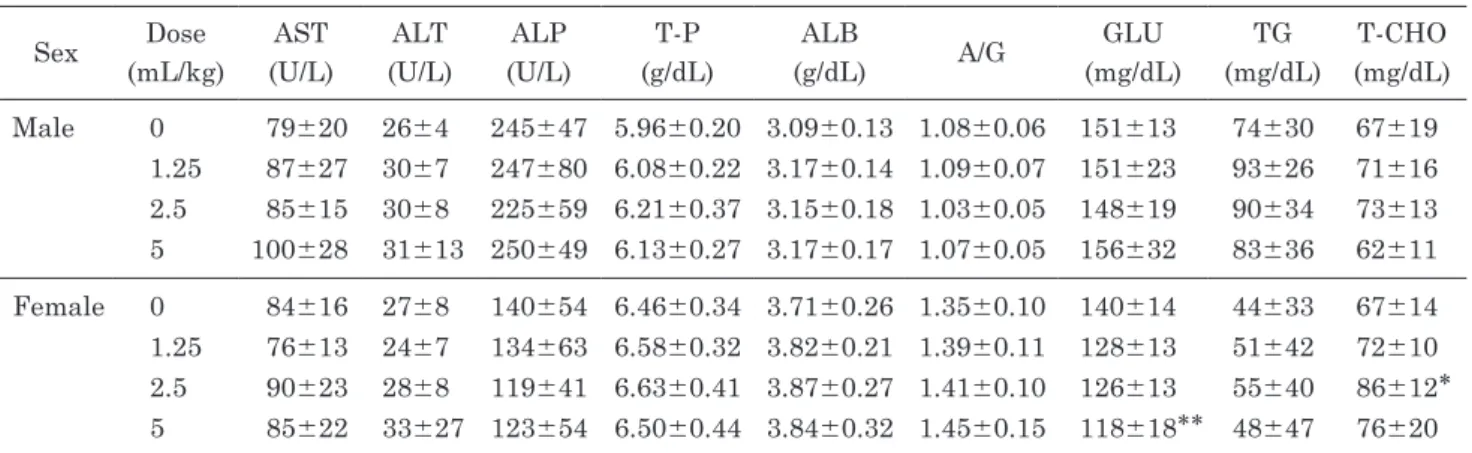
血液生化学的検査の結果をTable 7-1∼7-2に示
Table 5-2 Urinalysis data of rats orally administratedMisatol GL for 90 days
Sex Dose (mL/kg) pH 5 6 6.5 7 7.5 8 8.5 Male 0 0 0 0 0 2 1 2 1.25 0 0 1 0 0 2 2 2.5 0 0 0 0 0 1 4 5 0 0 2 0 1 2 0 Female 0 0 1 2 0 0 2 0 1.25 0 0 2 0 0 3 0 2.5 0 0 0 1 1 2 1 5 0 0 0 2 0 2 1
Table 5-3 Urinalysis data of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg) Protein − +/− 1+ 2+ 3+ 4+ Male 0 0 0 3 2 0 0 1.25 0 1 3 1 0 0 2.5 0 1 3 1 0 0 5 0 0 3 2 0 0 Female 0 2 2 1 0 0 0 1.25 0 3 2 0 0 0 2.5 0 1 4 0 0 0 5 0 1 4 0 0 0
Protein: −, Negative; +/−, Trace; 1+, 30; 2+, 100; 3+, 300; 4+, 1000 (mg/dL).
Table 5-4 Urinalysis data of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg) Glucose − 1+ 2+ 3+ 4+ 5+ Male 0 5 0 0 0 0 0 1.25 5 0 0 0 0 0 2.5 5 0 0 0 0 0 5 5 0 0 0 0 0 Female 0 5 0 0 0 0 0 1.25 5 0 0 0 0 0 2.5 5 0 0 0 0 0 5 5 0 0 0 0 0 Glucose: −, Negative; 1+, 100; 2+, 250; 3+, 500; 4+, 1000; 5+, 2000 (mg/dL).
Table 5-5 Urinalysis data of rats orally administrated Misatol GL for 90 days
Sex Dose
(mL/kg)
Ketone Body Bilirubin
− +/− 1+ 2+ 3+ 4+ − 1+ 2+ 3+ Male 0 0 0 2 3 0 0 5 0 0 0 1.25 0 1 1 3 0 0 5 0 0 0 2.5 0 1 1 3 0 0 5 0 0 0 5 0 0 3 2 0 0 5 0 0 0 Female 0 3 2 0 0 0 0 5 0 0 0 1.25 5 0 0 0 0 0 5 0 0 0 2.5 5 0 0 0 0 0 5 0 0 0 5 5 0 0 0 0 0 5 0 0 0
Ketone Body: −, Negative; +/−, 5; 1+, 15; 2+, 40; 3+, 80; 4+, 160 (mg/dL). Bilirubin: −, Negative; 1+, Slight; 2+, Moderate; 3+, Severe.
す.雄のMisatol GL 5 mL/kg/day投与群において,
注射用水投与群と比較して,T-BILの有意な上昇が
認められた.雌のMisatol GL 5 mL/kg/day投与群
において,注射用水投与群と比較して,GLUの有
意な低下,Misatol GL 2.5 mL/kg/day投与群におい
てT-CHOの有意な上昇が認められた.いずれの変
化も軽微で生理的変動内であるか,用量依存性のな
い変化であることから,Misatol GLによる影響で
Table 6-1 Hematology data of rats orally administrated Misatol GL for 90 daysSex (mL/kg)Dose (10WBC 2/µL) (10RBC 4/µL) (g/dL)HGB HCT (%) MCV (fL) MCH (pg) MCHC (g/dL) (10PLT 4/µL) NEUT% (%) Male 0 83.5±24.7 878±36 15.3±0.8 42.2±2.4 48.1±2.5 17.5±0.8 36.3±0.5 110.7±14.8 16.5±4.2 1.25 92.5±18.8 899±57 15.6±0.7 42.8±1.8 47.7±2.4 17.4±0.7 36.5±0.7 113.7±13.4 15.3±5.6 2.5 96.2±26.9 876±37 15.4±0.4 42.2±1.2 48.2±1.9 17.6±0.6 36.5±0.5 110.1±9.8 16.3±6.0 5 95.4±15.6 865±38 14.9±0.6 41.0±1.8 47.4±2.5 17.2±0.7 36.3±0.7 112.0±10.7 17.7±5.4 Female 0 58.4±14.8 756±36 14.4±0.4 39.7±1.1 52.6±1.9 19.0±0.6 36.2±0.3 97.9±8.0 19.8±7.5 1.25 63.1±17.1 775±20 14.6±0.4 40.2±1.1 51.9±1.7 18.8±0.6 36.2±0.5 102.8±12.3 12.6±3.1 2.5 60.5±17.6 743±40 14.0±0.6 39.1±1.8 52.7±2.0 18.9±0.7 35.9±0.4 92.1±11.8 15.0±5.0 5 54.4±14.4 746±43 14.0±0.7 38.6±1.7 51.8±1.8 18.8±0.6 36.2±0.4 98.7±11.2 19.0±9.3 Means±SD
Table 6-2 Hematology data of rats orally administrated Misatol GL for 90 days
Sex (mL/kg)Dose LYMPH% (%) MONO% (%) EO% (%) BASO% (%) (10Ret.# 4/µL) Ret.% (%) (sec)PT APTT (sec) Male 0 78.4±5.5 3.6±1.5 1.4±0.6 0.1±0.1 27.89±4.27 3.18±0.54 12.7±3.9 19.3±2.4 1.25 79.1±6.0 4.1±1.4 1.4±0.3 0.1±0.1 33.32±3.57** 3.71±0.36 11.9±1.7 19.0±1.3 2.5 77.9±6.8 3.9±1.4 1.8±0.7 0.1±0.1 28.39±4.17 3.25±0.52 11.3±0.6 18.8±0.8 5 76.9±5.9 3.6±0.7 1.8±0.6 0.1±0.0 30.16±3.00 3.49±0.39 11.2±0.8 18.4±0.9 Female 0 74.8±7.1 3.4±1.1 1.8±1.0 0.1±0.1 23.89±3.27 3.17±0.49 9.9±0.2 17.4±0.7 1.25 83.2±4.0* 2.7±0.8 1.5±0.6 0.1±0.1 24.36±4.23 3.14±0.54 10.0±0.2 17.3±0.4 2.5 80.2±5.6 3.2±0.6 1.6±0.6 0.0±0.0* 23.03±3.58 3.11±0.55 9.9±0.2 17.2±1.1 5 75.8±9.8 3.3±1.3 1.8±0.6 0.0±0.1 22.07±3.09 2.96±0.35 9.9±0.2 17.1±0.6 Means±SD
Significantly different from control group: *p<0.05, **p<0.01
Table 5-6 Urinalysis data of rats orally administrated Misatol GL for 90 days
Sex (mL/kg)Dose Occult Blood Urobilinogen
− +/− 1+ 2+ 3+ +/− 1+ 2+ 3+ Male 0 2 3 0 0 0 5 0 0 0 1.25 2 3 0 0 0 5 0 0 0 2.5 3 1 1 0 0 5 0 0 0 5 3 2 0 0 0 5 0 0 0 Female 0 5 0 0 0 0 5 0 0 0 1.25 4 0 1 0 0 5 0 0 0 2.5 5 0 0 0 0 5 0 0 0 5 4 1 0 0 0 5 0 0 0
Occult Blood:−, Negative; +/−, Trace; 1+, Slight; 2+, Moderate; 3+, Severe. Urobilinogen: +/−, 0.1-1; 1+, 2; 2+, 4; 3+, 8 (Ehrlich Unit/dL).
はないと考えられた.その他の測定項目について
は,雌雄いずれの投与群においても群間差は認めら
れなかった.
5)病理学的検査
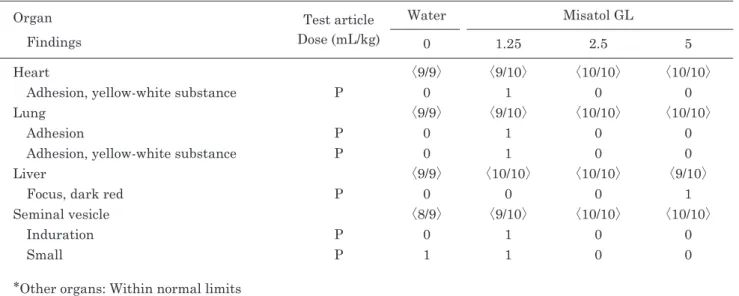
剖検結果をTable 8-1∼8-2に示す.注射用水投
与群の雄1例において,右側の精嚢及び凝固腺の小
型化がみられた.Misatol GL 1.25 mL/kg/day投与
群の雄1例において,心外膜及び肺門部への黄白色
物質の付着,胸壁と肺右後葉の癒着,左側の精嚢
及び凝固腺の小型化及び硬結がみられた.Misatol
GL 5 mL/kg/day投与群の雄1例において,肝臓尾
状葉の暗赤色巣がみられ,雌1例において,右側の
ハーダー腺の欠損がみられた.
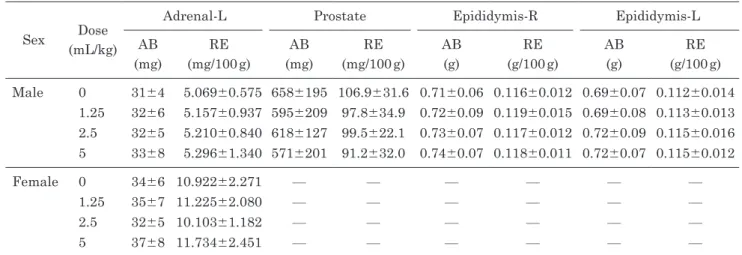
器官重量測定の結果をTable 9-1∼9-6に示す.
雌雄ともに,いずれの器官・組織においても,重量
及び比重量に群間差は認められなかった.
病理組織学的検査の結果をTable 10-1∼10-2に
示す.被験物質の影響として軽微な前胃の空胞化
がMisatol GL 5 mL/kg/day投 与 群 の 雄1例 及 び
1.25 mL/kg/day投与群の雄1例で認められた.
Misatol GL 5 mL/kg/day投与群について,雄1例
において剖検で認められた肝臓の暗赤色巣は病理組
織学的に肝臓の重度のうっ血であった.雌1例にお
いて剖検で認められたハーダー腺の欠損は病理組織
学的に無形成であった.これらの変化はそれぞれ注
射用水投与群(切迫殺例:手技による状態悪化のた
め)でも認められる変化及び発生異常に関連する変
化であり毒性学的意義のない変化と考えられた.雌
1例において肝臓で肝細胞の局所壊死が中等度にみ
られたが,本変化は実験動物の化学物質投与によ
る誘発例はまれであり,ラットにおいては若齢のも
のから自然発生がみられる
12)こと,単発性の変化
Table 7-1 Blood biochemistry data of rats orally administrated Misatol GL for 90 days Sex Dose (mL/kg) AST (U/L) ALT (U/L) ALP (U/L) T-P (g/dL) ALB (g/dL) A/G GLU (mg/dL) TG (mg/dL) T-CHO (mg/dL) Male 0 79±20 26±4 245±47 5.96±0.20 3.09±0.13 1.08±0.06 151±13 74±30 67±19 1.25 87±27 30±7 247±80 6.08±0.22 3.17±0.14 1.09±0.07 151±23 93±26 71±16 2.5 85±15 30±8 225±59 6.21±0.37 3.15±0.18 1.03±0.05 148±19 90±34 73±13 5 100±28 31±13 250±49 6.13±0.27 3.17±0.17 1.07±0.05 156±32 83±36 62±11 Female 0 84±16 27±8 140±54 6.46±0.34 3.71±0.26 1.35±0.10 140±14 44±33 67±14 1.25 76±13 24±7 134±63 6.58±0.32 3.82±0.21 1.39±0.11 128±13 51±42 72±10 2.5 90±23 28±8 119±41 6.63±0.41 3.87±0.27 1.41±0.10 126±13 55±40 86±12* 5 85±22 33±27 123±54 6.50±0.44 3.84±0.32 1.45±0.15 118±18** 48±47 76±20 Means±SD
Significantly different from control group: **p<0.01
Table 7-2 Blood biochemistry data of rats orally administrated Misatol GL for 90 days Sex Dose (mL/kg) PL (mg/dL) T-BIL (mg/dL) UN (mg/dL) CRE (mg/dL) Ca (mg/dL) P (mg/dL) Na (mEq/L) K (mEq/L) Cl (mEq/L) Male 0 106±21 0.07±0.01 18.3±3.8 0.33±0.05 10.0±0.3 6.4±0.3 144.7±0.9 4.69±0.37 104.4±1.1 1.25 115±15 0.07±0.01 19.0±2.3 0.33±0.03 10.0±0.3 6.4±0.7 144.1±1.1 4.69±0.19 104.5±1.3 2.5 114±17 0.06±0.01 20.7±2.9 0.34±0.05 10.1±0.3 6.3±0.6 144.2±0.8 4.74±0.19 104.3±1.0 5 104±16 0.08±0.01* 18.4±2.5 0.32±0.04 10.1±0.3 6.4±0.8 143.6±1.0 4.74±0.25 103.0±1.7 Female 0 133±26 0.09±0.02 19.5±3.3 0.33±0.05 9.9±0.3 5.5±1.2 143.4±0.8 4.01±0.17 104.5±1.3 1.25 146±18 0.11±0.03 18.5±1.9 0.31±0.03 9.9±0.2 5.3±0.9 142.9±0.9 4.13±0.17 104.0±0.7 2.5 159±21 0.11±0.02 22.3±3.4 0.33±0.03 9.9±0.3 5.4±1.1 143.3±0.8 3.93±0.22 104.2±1.2 5 150±33 0.12±0.04 18.8±4.3 0.31±0.07 9.9±0.4 5.4±1.0 142.3±1.2 3.88±0.30 102.6±1.9 Means±SD
であったことから,偶発的な変化と考えられた.ま
た,膵臓の限局性の萎縮が雄2例で認められたが,
本変化はラットで最も一般的に認められる自然発生
性の変性性変化である
13)ことから,自然発生性の
変化と考えられた.また,Misatol GL 5 mL/kg/day
投与群のみでみられた,肝臓の脂肪変性(雄1例),
腎臓の近位尿細管における硝子円柱(雄1例),肺
における限局性の炎症(雄1例),ハーダー腺の間
Table 9-1 Organ weight data of rats orally administrated Misatol GL for 90 daysSex (mL/kg)Dose Body weight (g)
Pituitary Thyroid Adrenal-R
AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) Male 0 618.6±48.3 13±2 2.044±0.371 34±8 5.481±1.234 29±6 4.613±0.785 1.25 610.8±34.0 13±3 2.176±0.415 30±4 4.865±0.761 32±5 5.247±0.780 2.5 623.0±39.5 15±2 2.387±0.242 28±5 4.507±0.646 29±4 4.577±0.500 5 626.8±25.0 15±2 2.362±0.309 33±5 5.195±0.885 32±7 5.073±1.242 Female 0 315.9±19.3 17±4 5.401±1.187 21±4 6.690±1.159 32±4 10.205±1.399 1.25 310.8±14.0 17±4 5.364±1.515 21±5 6.638±1.473 33±6 10.674±1.816 2.5 311.2±18.2 16±5 5.136±1.602 19±2 6.171±0.824 31±3 9.979±0.869 5 314.9±20.4 15±2 4.831±0.662 20±3 6.348±0.857 32±6 10.236±1.728 Means±SD, AB: Absolute weight, RE: Relative weight by body weight
Table 8-2 Summary of necropsy findings of female rats orally administrated Misatol GL for 90 days
Organ Test article
Dose (mL/kg)
Water Misatol GL
Findings 0 1.25 2.5 5
Harderian gland 〈10/10〉 〈10/10〉 〈10/10〉 〈9/10〉
Defect P 0 0 0 1
*Other organs: Within normal limits
〈 〉: Not remarkable/Number of animals examined P: Non-graded change
Table 8-1 Summary of necropsy findings of male rats orally administrated Misatol GL for 90 days
Organ Test article
Dose (mL/kg)
Water Misatol GL
Findings 0 1.25 2.5 5
Heart 〈9/9〉 〈9/10〉 〈10/10〉 〈10/10〉
Adhesion, yellow-white substance P 0 1 0 0
Lung 〈9/9〉 〈9/10〉 〈10/10〉 〈10/10〉
Adhesion P 0 1 0 0
Adhesion, yellow-white substance P 0 1 0 0
Liver 〈9/9〉 〈10/10〉 〈10/10〉 〈9/10〉
Focus, dark red P 0 0 0 1
Seminal vesicle 〈8/9〉 〈9/10〉 〈10/10〉 〈10/10〉
Induration P 0 1 0 0
Small P 1 1 0 0
*Other organs: Within normal limits
〈 〉: Not remarkable/Number of animals examined P: Non-graded change
質における単核細胞浸潤(雌1例)はいずれも単発
性であることから偶発的な変化と考えられた.その
他の変化は,注射用水投与群でも認められる変化及
びラットで一般的に認められる所見であり,偶発的
な変化と考えられた.
Misatol GL 1.25 mL/kg/day投与群の雄1例にお
Table 9-2 Organ weight data of rats orally administrated Misatol GL for 90 daysSex Dose (mL/kg)
Adrenal-L Prostate Epididymis-R Epididymis-L
AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) AB (g) RE (g/100 g) AB (g) RE (g/100 g) Male 0 31±4 5.069±0.575 658±195 106.9±31.6 0.71±0.06 0.116±0.012 0.69±0.07 0.112±0.014 1.25 32±6 5.157±0.937 595±209 97.8±34.9 0.72±0.09 0.119±0.015 0.69±0.08 0.113±0.013 2.5 32±5 5.210±0.840 618±127 99.5±22.1 0.73±0.07 0.117±0.012 0.72±0.09 0.115±0.016 5 33±8 5.296±1.340 571±201 91.2±32.0 0.74±0.07 0.118±0.011 0.72±0.07 0.115±0.012 Female 0 34±6 10.922±2.271 — — — — — — 1.25 35±7 11.225±2.080 — — — — — — 2.5 32±5 10.103±1.182 — — — — — — 5 37±8 11.734±2.451 — — — — — —
Means±SD, AB: Absolute weight, RE: Relative weight by body weight
Table 9-3 Organ weight data of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg)
Testis-R Testis-L Semi.Ves Ovary-R
AB (g) RE (g/100 g) AB (g) RE (g/100 g) AB (g) RE (mg/100 g) AB (mg) RE (mg/100 g) Male 0 1.76±0.20 0.286±0.042 1.76±0.17 0.286±0.038 2.03±0.39 332.1±72.1 — — 1.25 1.77±0.15 0.290±0.031 1.77±0.14 0.290±0.029 2.20±0.44 361.1±75.2 — — 2.5 1.78±0.14 0.285±0.022 1.76±0.15 0.284±0.029 2.16±0.17 347.4±32.6 — — 5 1.78±0.19 0.285±0.029 1.78±0.20 0.284±0.029 2.29±0.40 365.7±61.5 — — Female 0 — — — — — — 42±9 13.45±3.10 1.25 — — — — — — 43±8 13.62±2.13 2.5 — — — — — — 38±8 12.33±2.41 5 — — — — — — 41±9 12.89±2.70
Means±SD, AB: Absolute weight, RE: Relative weight by body weight
Table 9-4 Organ weight data of rats orally administrated Misatol GL for 90 days
Sex Dose (mL/kg)
Ovary-L Uterus Submaxillary G. Thymus
AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) Male 0 — — — — 847±125 136.8±16.4 355±142 57.1±20.5 1.25 — — — — 768±74 126.4±15.8 357±80 58.4±11.9 2.5 — — — — 770±85 124.1±15.2 343±100 55.4±16.9 5 — — — — 776±110 123.5±13.9 388±92 61.7±13.3 Female 0 43±6 13.59±1.65 595±229 188.8±71.7 443±39 140.2±10.8 250±65 78.9±20.0 1.25 42±8 13.32±2.17 697±330 224.8±108.2 462±45 148.6±11.1 288±70 92.4±20.9 2.5 41±8 13.23±2.00 622±152 200.7±51.9 434±43 139.9±15.1 250±56 80.4±16.6 5 39±8 12.24±2.31 651±283 206.1±86.8 421±44 134.2±16.9 238±55 75.6±16.5 Means±SD, AB: Absolute weight, RE: Relative weight by body weight
いて剖検で認められた心臓及び肺の黄白色物質は病
理組織学的に線維化がみられ,肺門部においては血
管新生や褐色色素の沈着もみられた.本変化は単発
性であり,偶発的な変化と考えられた.精嚢及び凝
固腺の小型化及び硬結は病理組織学的に低形成が認
められたが,注射用水投与群でも同様の所見が認め
られることから,自然発生性の変化と考えられた.
IV. 考察及び結論
青梅搾汁を加熱濃縮した梅エキスを含む加工食品
であるMisatol GLを雌雄ラットに単回及び90日間
反復経口投与し,その影響について検討した.
Misatol GL原 液 を5, 10及 び15 mL/kgの 用 量
で単回経口投与し,14日間観察した結果,雄の
10 mL/kg以 上 の 投 与 群 及 び 雌 のMisatol GLの
15 mL/kg投与群において,一過性の水様性下痢
が認められた.これは,希釈(通常,1回1袋を
50 mLの水で希釈し,これを1日に1∼3回,時間
を空けて飲用)して経口摂取するMisatol GL原液
を大量に経口投与したことによる刺激のための腸管
運動異常に起因する影響であると考えられた.体
重,摂餌量及び剖検については,影響は認められな
かった.したがって,Misatol GL原液をラットに
単回経口投与した結果,認められた影響は一過性の
水様性下痢のみであった.
Misatol GLを1.25, 2.5及 び5 mL/kg/day( 原 液
としての用量)となるように注射用水で希釈した
溶液を雌雄ラットに90日間反復経口投与した結果,
雌雄ともにMisatol GL投与群で,注射用水投与群
と比較して摂餌量の有意な低値を示す観察ポイント
が散見され,特に5 mL/kg/dayでは投与中期から後
期にかけて恒常的に観察された.本変化はいずれも
Table 9-5 Organ weight data of rats orally administrated Misatol GL for 90 daysSex Dose (mL/kg)
Lung Spleen Brain Heart
AB (mg) RE (mg/100 g) AB (mg) RE (mg/100 g) AB (g) RE (g/100 g) AB (g) RE (g/100 g) Male 0 1677±189 271.7±29.9 873±184 140.2±20.8 2.23±0.07 0.362±0.033 1.64±0.12 0.266±0.020 1.25 1712±115 279.2±8.7 898±186 146.9±29.6 2.21±0.11 0.364±0.030 1.68±0.11 0.276±0.020 2.5 1669±108 268.1±11.4 849±47 136.4±5.7 2.18±0.09 0.352±0.032 1.61±0.12 0.259±0.020 5 1689±103 269.7±15.6 914±153 145.6±22.4 2.21±0.10 0.352±0.013 1.68±0.15 0.268±0.020 Female 0 1193±69 378.6±28.5 465±67 147.5±20.4 1.99±0.12 0.632±0.068 0.94±0.07 0.299±0.024 1.25 1184±73 381.0±14.7 511±125 163.8±35.9 1.93±0.09 0.624±0.043 0.89±0.06 0.287±0.019 2.5 1173±90 377.0±18.4 510±72 163.6±19.9 1.94±0.07 0.625±0.031 0.90±0.07 0.289±0.019 5 1153±89 366.7±27.2 502±74 159.5±21.0 2.02±0.07 0.643±0.043 0.90±0.09 0.285±0.023 Means±SD, AB: Absolute weight, RE: Relative weight by body weight
Table 9-6 Organ weight data of rats orally administrated Misatol GL for 90 days Dose
(mL/kg)
Kidney-R Kidney-L Liver
AB (g) RE (g/100 g) AB (g) RE (g/100 g) AB (g) RE (g/100 g) Male 0 1.76±0.13 0.285±0.019 1.77±0.13 0.288±0.029 15.86±1.73 2.567±0.247 1.25 1.84±0.20 0.303±0.036 1.82±0.21 0.299±0.035 16.25±1.63 2.659±0.203 2.5 1.82±0.22 0.293±0.035 1.82±0.24 0.293±0.037 16.61±1.85 2.668±0.250 5 1.93±0.20 0.309±0.041 1.95±0.19 0.312±0.038 17.28±1.24 2.758±0.197 Female 0 0.96±0.06 0.305±0.024 0.93±0.07 0.296±0.025 7.61±0.54 2.411±0.131 1.25 0.94±0.08 0.301±0.023 0.92±0.07 0.295±0.020 7.41±0.73 2.380±0.154 2.5 0.98±0.12 0.315±0.029 0.96±0.10 0.309±0.025 7.66±0.98 2.459±0.255 5 1.01±0.12 0.323±0.039 0.99±0.11 0.315±0.037 7.65±0.80 2.428±0.185 Means±SD, AB: Absolute weight, RE: Relative weight by body weight
軽微な変化であり,体重に影響がなかったこと,剖
検及び病理組織学的検査において消化管に対応する
異常が認められなかったことから,毒性学的な意義
は低いと考えられた.また,病理組織学的検査に
おいて,軽微な前胃の空胞化がMisatol GL 5 mL/
kg/day投与群の雄1例及び1.25 mL/kg/day投与群
の雄1例で認められた.本変化は薬物の刺激あるい
は加齢性変化としてみられること
14)が知られてお
り,変化の程度は軽微であったこと,腺胃に変化が
みられなかったことから毒性学的な意義は低いと考
えられた.その他,一般状態,体重,尿検査,眼科
学的検査,血液検査,剖検及び器官重量において,
Misatol GLによる影響は認められなかった.
以上,Misatol GLを雌雄ラットに単回及び90日
間反復経口投与し,過剰摂取及び長期摂取の影響に
ついて検討した結果,過剰摂取による影響として,
Table 10-1 Summary of histopathological findings of male rats orally administrated Misatol GL for 90 daysOrgan Test article
Dose (mL/kg) Water Misatol GL Findings 0 1.25 2.5 5 Heart 〈4/9〉 〈0/1〉 〈0/0〉 〈5/10〉 Fibrosis, pericardium + 0 1 0 0 Hemorrhage, focal ± 1 0 0 0
Myocardial degeneration/necrosis, focal ± 4 0 0 3
Mononuclear cell infiltration, interstitium ± 4 0 0 4
Fibrosis, focal ± 1 0 0 0
Lung 〈9/9〉 〈0/1〉 〈0/0〉 〈9/10〉
Fibrosis, hilus, serosa + 0 1 0 0
Inflammation, focal ± 0 0 0 1
Kidney 〈8/9〉 〈0/0〉 〈0/0〉 〈9/10〉
Regeneration, tubule ± 1 0 0 0
Hyaline cast, proximal tubule ± 0 0 0 1
Forestomach 〈9/9〉 〈9/10〉 〈10/10〉 〈9/10〉
Vacuolation, limiting ridge ± 0 1 0 1
Jejunum 〈7/9〉 〈0/0〉 〈0/0〉 〈10/10〉
Mineralization, Peyer s patch ± 2 0 0 0
Liver 〈7/9〉 〈0/0〉 〈0/0〉 〈6/10〉
Congestion 3+ 0 0 0 1
Microgranuloma ± 2 0 0 4
Fatty change, periportal ± 0 0 0 1
Pancreas 〈8/9〉 〈0/0〉 〈0/0〉 〈8/10〉
Atrophy, focal ± 0 0 0 2
Pigment deposition, brown ± 1 0 0 0
Prostate 〈5/9〉 〈0/0〉 〈0/0〉 〈5/10〉
Mononuclear cell infiltration, interstitium ± 4 0 0 5
Seminal vesicle 〈8/9〉 〈0/1〉 〈0/0〉 〈10/10〉
Hypoplasia P 1 1 0 0
Spleen 〈2/9〉 〈0/0〉 〈0/0〉 〈2/10〉
Extramedullary hematopoiesis ± 1 0 0 3
Pigment deposition, brown ± 7 0 0 8
Harderian gland 〈4/9〉 〈0/0〉 〈0/0〉 〈2/10〉
Porphyrin deposition ± 5 0 0 8
*Other organs: Within normal limits
〈 〉: Not remarkable/Number of animals examined
一過性の水様性下痢が認められ,長期投与による影
響として,軽微な摂餌量の低下及び軽微な前胃の空
胞化が認められた.長期投与により認められた影響
については,いずれも毒性学的な意義は低いと考え
られた.したがって,Misatol GLの安全性は高い
と考えられた.
利益相反
著者らは株式会社大塚製薬工場とAdaBio株式会
社の社員である以外,開示するCOIはありません.
参考文献
1) 忠田吉弘,小野裕嗣,亀山眞由美,永田忠博,菊池佑 二:梅肉エキス中の血流改善成分,ヘモレオロジー研 究会誌,1, 65–68, 1998.2) Adachi M, Suzuki Y, Mizuta T, Suzuki K, Shiojima K, Araki Y, Masuda K, Uchiyama M, Oyamada T, Clerici M: The Prunus mume Sieb. et Zucc (Ume) is
a rich natural source of novel anti-cancer substance. Int. J. Food Prop., 10(2), 375–384, 2007.
3) Nakagawa A, Sawada T, Okada T, Ohsawa T, Adachi M, Kubota K: New antineoplastic agent, MK615, from UME (a Variety of) Japanese apricot inhibits growth of breast cancer cells in vitro. Breast J., 13(1), 44–49, 2007.
4) Okada T, Sawada T, Osawa T, Adachi M, Kubota K: A novel anti-cancer substance, MK615, from ume, a variety of Japanese apricot, inhibits growth of he-patocellular carcinoma cells by suppressing Aurora A kinase activity. Hepatogastroenterology, 54(78), 1770–1774, 2007.
5) Mori S, Sawada T, Okada T, Ohsawa T, Adachi M, Kubota K: New anti-proliferative agent, MK615, from Japanese apricot Prunus mume induces strik-ing autophagy in colon cancer cells in vitro. World J. Gastroenterol., 13(48), 6512–6517, 2007.
6) Yamai H, Sawada N, Yoshida T, Seike J, Takizawa H, Kenzaki K, Miyoshi T, Kondo K, Bando Y, Oh-nishi Y, Tangoku A: Triterpenes augment the inhibi-Table 10-2 Summary of histopathological findings of female rats orally administrated Misatol GL for 90 days
Organ Test article
Dose (mL/kg)
Water Misatol GL
Findings 0 1.25 2.5 5
Jejunum 〈9/10〉 〈0/0〉 〈0/0〉 〈8/10〉
Mineralization, Peyer s patch ± 1 0 0 2
Liver 〈5/10〉 〈0/0〉 〈0/0〉 〈3/10〉
Necrosis, hepatocyte, focal 2+ 0 0 0 1
Microgranuloma ± 5 0 0 6
Pancreas 〈8/10〉 〈0/0〉 〈0/0〉 〈10/10〉
Cell infiltration, mononuclear cell, interstitium
± 2 0 0 0
Thyroid 〈8/10〉 〈0/0〉 〈0/0〉 〈10/10〉
Ultimobranchial body P 1 0 0 0
Cell infiltration, mononuclear cell, interstitium
± 1 0 0 0
Spleen 〈0/10〉 〈0/0〉 〈0/0〉 〈0/10〉
Extramedullary hematopoiesis ± 1 0 0 1
Pigment deposition, brown + 10 0 0 10
Harderian gland 〈1/10〉 〈0/0〉 〈0/0〉 〈0/10〉
Aplasia P 0 0 0 1
Cell infiltration, mononuclear cell, interstitium
± 0 0 0 1
Porphyrin deposition ± 9 0 0 10
*Other organs: Within normal limits
〈 〉: Not remarkable/Number of animals examined
tory effects of anticancer drugs on growth of human esophageal carcinoma cells in vitro and suppress ex-perimental metastasis in vivo. Int. J. Cancer, 125(4), 952–960, 2009.
7) Sunaga N, Hiraishi K, Ishizuka T, Kaira K, Iwasaki Y, Jimma F, Adachi M, Mori M: MK615, A Com-pound Extract from the Japanese Apricot Prunus mume Inhibits In vitro Cell Growth and Interleu-kin-8 Expression in Non-small Cell Lung Cancer Cells. J. Cancer Sci. Ther., 01(S11), S11-S002, 2012. 8) Hattori M, Kawakami K, Akimoto M, Takenaga K,
Suzumiya J, Honma Y: Antitumor effect of Japanese apricot extract (MK615) on human cancer cells in vitro and in vivo through a reactive oxygen species-dependent mechanism. Tumori, 99(2), 239–248, 2013.
9) Yanaki M, Kobayashi M, Aruga A, Nomura M, Ozaki M: In Vivo Antitumor Effects of MK615 Led by PD-L1 Downregulation. Integr. Cancer Ther., 17(3), 646–653, 2018.
10) Hokari A, Ishikawa T, Tajiri H, Matsuda T, Ishii O, Matsumoto N, Okuse C, Takahashi H, Kurihara T, Kawahara K, Maruyama I, Zeniya M: Efficacy of
MK615 for the treatment of patients with liver dis-orders. World J. Gastroenterol., 18(31), 4118–4126, 2012.
11) Diehl KH, Hull R, Morton D, Pfister R, Rabemampia-nina Y, Smith D, Vidal JM, van de Vorstenbosch C; European Federation of Pharmaceutical Industries Association and European Centre for the Validation of Alternative Methods: A good practice guide to the administration of substances and removal of blood, including routes and volumes. J. Appl. Toxicol.,
21(1), 15–23, 2001.
12) 日本毒性病理学会:新毒性病理組織学 第1版,消化 器系7肝臓,216–254, 西村書店,2017.
13) Nolte T, Brander-Weber P, Dangler C, Deschl U, El-well MR, Greaves P, Hailey R, Leach MW, Pandiri AR, Rogers A, Shackelford CC, Spencer A, Tanaka T, Ward JM: Nonproliferative and Proliferative Lesions of the Gastrointestinal Tract, Pancreas and Salivary Glands of the Rat and Mouse. J. Toxicol. Pathol.,
29(1)(Suppl 1), 1S–125S, 2016.
14) 日本毒性病理学会:新毒性病理組織学 第1版,消化 器系5胃,168–187, 西村書店,2017.