環境負荷の低い有機酸溶液による
SUS304 鋼電解研磨面の不働態化処理
石見 清隆
a,*,井田 義明
b,津高 文幸
c,杉本 克久
d aマルイ鍍金工業㈱ 千葉・柏工場(〒 277︲0805 千葉県柏市大青田 692︲1) b マルイ鍍金工業㈱ 本社(〒 672︲8023 兵庫県姫路市白浜町甲 402) cマルイ鍍金工業㈱ 姫路工場(〒 672︲8022 兵庫県姫路市白浜町宇佐崎南 1︲29) d東北大学 名誉教授(〒 982︲0222 宮城県仙台市太白区人来田 2︲11︲18)Passivation Treatment of Electro-polished Type 304 Stainless Steel
in Environmentally Friendly Organic Acid Solutions
Kiyotaka ISHIMI
a,*, Yoshiaki IDA
b, Fumiyuki TSUTAKA
cand Katsuhisa SUGIMOTO
d a Chiba・Kashiwa Factory, Marui Galvanizing Co., Ltd.(692-1, Oaota, Kashiwa, Chiba 277-0805)b Head office, Marui Galvanizing Co., Ltd.(402, Ko, Sirahama, Himeji, Hyogo 672-8023)
c Himeji Factory, Marui Galvanizing Co., Ltd.(1-29, Usazaki-minami, Sirahama, Himeji, Hyogo 672-8022) d Professor Emeritus, Tohoku University(2-11-18, Hitokita, Taihaku-ku, Sendai, Miyagi 982-0222)
Anodic polarization curves of electro-polished Type 304 stainless steel were measured in organic acid solutions of eight types to develop a safe and environmentally friendly passivation treatment. The pitting potentials of the steel passivated in the solutions were examined in a deaerated 3.5%NaCl solution. Among the organic acid solutions, 8%DL-malic acid, 8%citric acid, 8%L-tartaric acid and 8%glucono-δ-lac-tone were found to be suitable as treatment solutions because of the low current densities(<0.02 A・m-2)of the passive state and high pitting
potentials(>700 mV vs. Ag/AgCl(sat. KCl))of the passive films. Passive films formed on Type 304 stainless steel by natural immersion into 8%DL-malic acid+0.98%H2O2, 8%citric acid+0.98%H2O2, 8%L-tartaric acid+0.98%H2O2 and 8%glucono-δ-lactone+0.98%H2O2 showed
high pitting potentials(>1000 mV)in NaCl solutions of 3.5% - saturation concentration. For solutions containing H2O2, the
pitting-potential-raising effects were greater on an electro-polished surface than on a buffer(#400)-polished surface.
Keywords : Passivation Treatment, Organic Acid Solution, Type 304 Stainless Steel, Electropolishing, Pitting Potential
1 .緒 言
医薬品工業,食品工業などでは,ステンレス鋼製の製造装 置が多く使われている。これらの製造装置の内面は,耐食性 向上と洗浄性向上の観点から電解研磨処理がなされることが 多い。しかしながら,このような処理をされた装置において も,製品の製造原料に塩分などが含まれているときには,使 用時間経過後装置内面に孔食が発生することがある。孔食部 から溶出した金属イオンは製造物を汚染するので,品質管理 上の問題を引き起こす。そのため,電解研磨面の耐孔食性を 一層向上させる方策が望まれている。 ステンレス鋼の耐孔食性を向上させるためには不働態皮膜 の耐食性を高めることが重要であり,このための処理として は硝酸(HNO3)処理がよく知られている1), 2)。HNO3処理によ れば高い耐孔食性が得られるので,既に工業的にも利用2)さ れている。しかし,HNO3は強酸性であるため取り扱い作業 の安全確保や使用済み廃液の中和操作などの環境保全対策が 必要である。HNO3以外の酸化剤としては,過酸化水素(H2O2) が検討されている3),4)。H 2O2は,オキシドールとして家庭で も使用されているように,低濃度であれば安全な薬品である が,ステンレス鋼の表面状態によっては処理による耐孔食性 向上効果が十分でないことから4),工業的に一般的に用いら れるには至っていない。 本研究では,上述のような HNO3の欠点を避けかつ HNO3 不働態皮膜に匹敵する耐孔食性を有する不働態皮膜を電解研 磨面に形成しうる化学的不働態化処理液を開発することを目 的とする。そのため,取り扱い作業上の安全性が高くかつ環 境負荷が低い電解液として,以下の範疇のものを対象とした。 (1)毒物及び劇物取締法5)で毒物,劇物に扱われない濃度範 囲の無機酸化剤溶液 (2)食品衛生法6)に酸味料として規定されている有機酸溶液 (1),(2)とも低濃度であれば人体にとって安全であり,不 働態化処理後装置内に残留しても人体や環境に有害な影響を 及ぼす恐れが少ないと考えられる。 ステンレス鋼を化学的に不働態化させるためには,一般に, 不働態化処理液中に酸化剤を添加する必要がある。ここでは, 技 術 論 文 * E-mail : [email protected]Vol. 67, №3, 2016 SUS304 鋼電解研磨面の不働態化処理 151 酸化剤として(1)に該当する H2O2を取り上げ,これを不働態 化処理液に添加することを検討する。H2O2は単独でも不働態 化効果を示すが,低濃度ではその効果は十分ではないので4), 他の不働態化処理液と組み合わせて有効に使用することを考 える。次に,ベースとなる不働態化処理液としては,(2)に 該当する有機酸溶液を検討する。有機酸の内キレート形成能 のあるものは,不働態皮膜中の Fe と反応するとキレートと して Fe を除去し,皮膜の Cr 濃度を高める。その様な有機酸 でステンレス鋼表面を酸洗すると金属イオン溶出量の少ない 表面が得られるので,食品工業ではクエン酸がステンレス鋼 容器の洗浄液7)として,あるいは不働態化処理液2)として, 用いられている。有機酸の酸化力は弱いので有効な不働態化 処理液として用いられるケースは少ないが,適当な酸化剤と 組み合わせれば効果の高い処理液になる可能性がある。 以上のような理由から,本研究では,種々の濃度の H2O2 を添加した各種の有機酸中での電解研磨 SUS304 ステンレス 鋼の不働態化処理を行い,処理後 NaCl 溶液中で孔食電位を 測定し,高い耐孔食性が得られる H2O2と有機酸の組み合わ せを探索した。
2 .実験方法
2.1 試 料 試料には電極部(20l× 5w× 0.3(mm))に柄部(180t l× 3w × 0.3(mm))が付いた形状の SUS304 鋼薄板試験片(組成t Cr:18.08,Ni:8.02,C:0.05,Si:0.06,Mn:0.99,P:0.03, S:0.005 mass%(以降 mass% は単に % と表示する))を用いた。 最終表面状態はバフ# 400 研磨仕上げおよびバフ# 400 研磨 後電解研磨仕上げ(以降これを電解研磨と言う)の 2 種類とし た。電解研磨は,45 ℃の硫酸-リン酸電解液(98%H2SO4: 85%H3PO4= 3:1(容量比))中で 8 V,360 s 間行った。電解 研磨後,純水洗浄,純水超音波洗浄,窒素ガス乾燥を順次実 施した。バフ# 400 研磨についても同様の後処理をした。 2.2 電解液 有機酸としては,食品衛生法に規定されている有機酸であ る 8%L- アスコルビン酸(C6H8O6),8% クエン酸(C6H8O7), 8%L- 酒 石 酸(C4H6O6),8%DL- リ ン ゴ 酸(C4H6O5),8% グ ル コ ノ デ ル タ ラ ク ト ン(C6H10O6),8 vol% 乳 酸(C3H6O3), 8 vol% 酢酸(C2H4O2),8 vol% グルコン酸(C5H12O7)を用いた。 (注:溶液の場合の %(質量 %)は溶液 100g 中に含まれる溶 質の g 数,vol%(容量 %)は溶液 10−4 m3(100 cc)中の溶質の 10−6 m3数(cc 数)。) 上記の各有機酸に H2O2を x%(x = 0.98 ~ 3.5)添加した溶 液,すなわち 8% クエン酸+ x%H2O2溶液,8%DL- リンゴ酸 + x%H2O2溶液,8 vol% グルコン酸+ x%H2O2溶液,8% グ ル コ ノ デ ル タ ラ ク ト ン + x%H2O2溶 液,8%L- 酒 石 酸 + x%H2O2溶液,を不働態化処理液として用いた(これらの溶 液を H2O2添加有機酸溶液と総称する)。また,比較のために, 無機不働態化処理液として 1 kmol・m−3 Na 2SO4+ x%H2O2溶 液も使用した。(注:kmol・m−3(モル濃度)は 10−3 m3(1l)の 溶液中に含まれる溶質のグラム分子数。) よく使用した 8%DL- リンゴ酸+ 0.98%H2O2溶液は pH1.9, 8% ク エ ン 酸 + 0.98%H2O2溶 液 は pH1.8,8%L- 酒 石 酸 + 0.98%H2O2溶液は pH 1.7,8% グルコノデルタラクトン+ 0.98%H2O2溶液は pH 2.2 であった。ベースの有機酸溶液の pH もこれらと同一であった。 2.3 アノード・カソード分極曲線の測定 有機酸溶液中において,電解研磨 SUS304 鋼の分極曲線を - 500 mV のカソード域から 2000 mV のアノード域まで動電 位法で測定した。分極曲線上で電流が 0 に収斂する電位が自 然電極電位であり,この電位よりも高い領域がアノード分極 曲線,低い領域がカソード分極曲線である。なお,アノード 分極曲線のみの測定においては,自然電極電位から酸素発生 電位までの分極挙動を測定した。測定にはポテンショスタッ トを用い,電位掃引速度は 0.333 mV・s−1,溶液は N 2ガス脱気, 温度は 25 ℃とした。照合電極には Ag/AgCl(飽和 KCl)電極 を使用した。本文の電位は全てこの電極基準で示す。なお測 定においては,試料の電極面 100 mm2(20l× 5w(mm))とな る部分以外を絶縁被覆(主成分:メチルエチルケトン)した。 2.4 定電位不働態化処理 有機酸溶液中で測定したアノード分極曲線を比較し,活性 態ピーク電流密度が小さく,不働態維持電流密度が小さく, そして過不働態溶解ピーク電流密度が小さい溶液を 6 種選ん だ。選んだ 6 種の溶液中において,不働態域の低い電位(自 然電極電位), 不働態域の中央付近の電位(500 mV),および 過不働態域の電位(1200 mV),の三つの電位で電解研磨 SUS304 鋼を不働態化処理した。ただし,自然電極電位での 処理は自然浸漬状態で,そして 500 mV と 1200 mV での処理 は定電位で,行った。処理時間は 2 h,温度は 25 ℃とした。 2.5 化学不働態化処理 x = 0.98 ~ 3.5 の 範 囲 の 8% ク エ ン 酸 + x%H2O2溶 液, 8%DL- リンゴ酸+ x%H2O2溶液,8vol% グルコン酸+ x%H2O2 溶液,8% グルコノデルタラクトン+ x%H2O2溶液,8%L- 酒 石酸+ x%H2O2溶液,および 1 kmol・m−3Na2SO4+ x%H2O2溶 液へ各種表面研磨をした SUS304 鋼を浸漬することによって化 学不働態化処理をした。処理時間は 2 h,温度は 25 ℃であった。 2.6 塩化物溶液中での孔食電位の測定 定電位的あるいは化学的に不働態化処理した試料について, 25 ℃,脱気 3.5%NaCl 溶液中でのアノード分極測定から孔食 電位を求め,不働態化処理の違いによる耐孔食性の違いを検 討した。また,NaCl 濃度による耐孔食性の変化を知るために, 濃度 3.5% ~飽和の脱気 NaCl 溶液中でのアノード分極測定 も行った。さらに,3.5%NaCl 溶液中の孔食電位の差異が小 さ く 耐 孔 食 性 の 優 劣 の 判 断 が 難 し い 場 合 に は, 脱 気 0.1 kmol・m−3 HCl 溶液中でのアノード分極測定も実施した。 分極曲線の測定方法と測定条件は,溶液の違いを除けば,2.3 で述べたところと同じである。分極曲線は同一条件で 5 本測 定した。分極曲線上の不働態維持電流域から孔食の成長に よって電流が 1 A・m−2以上まで急激に増加し始める電位を 孔食電位とした。なお,本文中で示す孔食電位の値は,測定 された 5 本の分極曲線の内偏差の少ない 3 本から求めた平均 値を指す。 2.7 表面仕上げの違いが耐孔食性に及ぼす影響 表面仕上げの違いが不働態化処理に及ぼす影響を知るため に,バフ# 400 研磨および電解研磨 SUS304 鋼について,各種の H2O2添加有機酸溶液中で不働態化処理し,その後脱気 3.5%NaCl 中でアノード分極曲線を測定した。得られた孔食 電位の高低から,表面仕上げと処理液の種類が耐孔食性向上 効果に及ぼす影響を評価した。 2.8 NaCl 溶液への長期間浸漬による耐食性の変化の測定 不働態化処理で形成した不働態皮膜がその後腐食環境に曝 された時,いつの時点で劣化するかを知る必要がある。その ために,H2O2添加有機酸溶液中で不働態化処理をした試料 を大気開放,25 ℃,3.5%NaCl 溶液中に 1 ~ 183 d 浸漬し, その後脱気 3.5%NaCl 溶液中で孔食電位を測定した。孔食電 位の浸漬日数による変化から,不働態化処理によって得られ た皮膜の Cl−イオンによる劣化過程を検討した。また,183 d 浸漬後の各試料表面を走査電子顕微鏡(SEM)で観察し,孔 食の発生の有無を調べた。 2.9 X 線光電子分光法による皮膜組成の分析 不働態化処理をした試験片表面を X 線光電子分光法 (XPS)で分析した。分析機器にはアルバック・ファイ株式会 社製 ESCA5600Ci を使用した。分析には MgKα線を用いた。 線源の出力は 400 W,電圧は 15 kV であった。XPS スペクト ル の 測 定 は C1s,O1s,Cr2p,Fe2p,Ni2p,Mo3d の各電子 について行った。測定した各スペクトルの結合エネルギーは, C1s ピークの結合エネルギーを 285.00 eV として補正した (1 eV = 1.60218 × 10−19 J)。スペクトルの測定は生成したま まの皮膜の表面およびこれに 6 s 間隔でアルゴンイオンス パッタリング(1 回当たり 6 s)を行った後の表面について 行った。アルゴンイオンの加速電圧は 4 kV であった。
3 .結果と考察
3.1 有機酸溶液中のアノード分極曲線 不働態化処理液として検討したアスコルビン酸,クエン酸, L- 酒石酸,DL- リンゴ酸 , グルコノデルタラクトン,乳酸, 酢酸,グルコン酸の各溶液中における機械研磨 SUS304 鋼の アノード分極曲線が,これらの溶液中での同鋼の腐食特性を 調べている研究の中で報告されている8)。それによると,こ れらの酸の 10% 溶液中では明瞭な活性態電流ピークがア ノード分極曲線上に自然電極電位より少しアノード分極した 所に認められる8)。このことは,10% 以上の濃度のこれらの 有機酸溶液中では SUS304 鋼の不働態化に必要な酸化剤の濃 度が大きくなること,またある濃度の酸化剤を添加して不働 態化させても酸化剤が消費されて濃度が下がると脱不働態化 が起こり,SUS304 鋼に腐食が起こる可能性があることなど から,10% 以上の溶液を不働態化処理液として用いるのは 好ましくないことを示している。そのため,本研究では活性 態電流ピークがほとんど出なくなる 10% 以下の濃度の溶液 について検討した。 8%L- ア ス コ ル ビ ン 酸,8% ク エ ン 酸,8%L- 酒 石 酸, 8%DL- リンゴ酸,8% グルコノデルタラクトン,8 vol% 乳酸, 8 vol% 酢酸,8 vol% グルコン酸の各有機酸溶液中における 電解研磨仕上げ SUS304 鋼のアノード・カソード分極曲線を 図 1 に示す(自然電極電位(- 400 mV 付近)の右側がアノー ド分極,左側がカソード分極)。いずれの溶液中のアノード 分極曲線も自然電極電位付近の- 430 ~- 300 mV にごく小 さい活性態電流ピークを示した後不働態域に入っている。活性 態電流ピークの大きさは,何れの溶液でも 0.03 ~ 0.09 A・m−2 であり不働態維持電流密度とほとんど同じ大きさであること から,何れの溶液中でも電解研磨 SUS304 鋼は自然浸漬する だけで自己不働態化するとみられる(したがって,活性態電 流ピークと呼んでいるが,正しくは皮膜の欠陥を通して流れ る酸化電流ピーク)。不働態域(- 300 ~ 800 mV)では,アス コルビン酸を除き , 各溶液の不働態維持電流密度(0.01 ~ 0.02 A・m−2の範囲)にはほとんど差が無く,不働態維持電流 密度が最も小さくなる 500 mV における電流密度はグルコノ デルタラクトン≧乳酸≒酢酸≒リンゴ酸≒クエン酸≒酒石酸 ≒グルコン酸である。アスコルビン酸のみが 200 mV 付近か ら溶解を起こし,500 mV では 0.4 A・m−2の溶解電流密度を 示す。過不働態域(800 ~ 1300 mV)では,1200 mV の所で比 較すると,溶解電流の大きさはアスコルビン酸>酒石酸>乳 酸>クエン酸≧リンゴ酸>グルコン酸>グルコノデルタラク トン>酢酸の順になっている。酸溶液の種類によって電位は 異なるが,約 1300 mV 以上は酸素ガス発生域である。活性 態域,不働態域および過不働態域の電流密度が共に低い酸溶 液が不働態化処理液として適していると考えると,不働態域 ではアスコルビン酸を除いたその他の酸の,また,過不働態 域ではアスコルビン酸と酒石酸を除いたその他の酸の,8% 溶液が有望である。 3.2 有機酸溶液中で定電位的に生成した皮膜の耐孔食性 各有機酸溶液中で自然電極電位(約- 380 mV),不働態域 の電位 500 mV,および過不働態域の電位 1200 mV において 皮膜を形成した試料の孔食電位を脱気 3.5%NaCl 溶液中で測 定した。その一例として,8%DL- リンゴ酸中で処理した試 料 の ア ノ ー ド 分 極 曲 線 を 図 2 に 示 す。 自 然 電 極 電 位, 500 mV および 1200 mV での処理に対して孔食電位はそれぞ れ 463 mV,1097 mV および 320 mV であることが分かる。 すなわち,不働態域の 500 mV での処理が最も高い孔食電位 を与えている。 同様の測定を不働態化処理に用いた他の 7 種類の有機酸に ついて行い,不働態化処理電位と 3.5%NaCl 中での孔食電位 の関係をまとめた結果を表 1 に示す。8%DL- リンゴ酸の場 0.0001 0.001 0.01 0.1 1 10 100 1000 10000 -500 0 500 1000 1500 2000 C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) 8% DL-malic acid 8% citric acid8vol% gluconic acid 8vol% lactic acid
8% L-ascorbic acid
8% glucono-δ-lactone 8% L-tartaric acid
8vol% acetic acid
Fig. 1 Anodic polarization curves of electro-polished Type 304 stainless
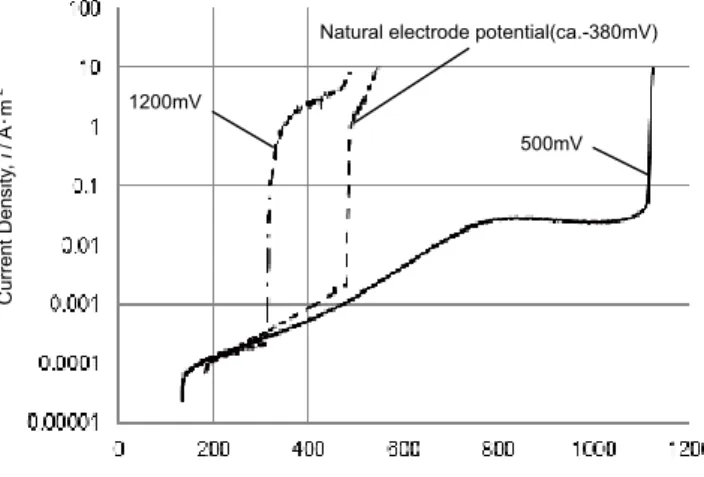
Vol. 67, №3, 2016 SUS304 鋼電解研磨面の不働態化処理 153 合と同じように,他の有機酸についても処理電位による孔食 電位の高低は,500 mV 処理>自然電極電位処理> 1200 mV 処理の順になっている。すなわち,不働態域のほぼ中央の電 位で形成した皮膜の耐孔食性が最も高い。それに対して,過 不働態電位で形成した皮膜は孔食抑制効果が低い。8 種類の 有 機 酸 の 中 で,8% ク エ ン 酸 お よ び 8%DL- リ ン ゴ 酸 の 500 mV 形成皮膜はそれぞれ 1117 mV および 1097 mV の極め て高い孔食電位を示す。これらの酸の自然電極電位形成皮膜 の孔食電位もそれぞれ 477 mV および 463 mV であり,自然 浸漬だけでも比較的耐孔食性の高い皮膜を形成することがで きる。8% グルコノデルタラクトンおよび 8%L- 酒石酸中で の 500 mV 形成皮膜の孔食電位はそれぞれ 700 mV および 860 mV であり,また,自然電極電位形成皮膜の孔食電位も それぞれ 447 mV および 457 mV と比較的高い。したがって, 8% クエン酸,8%DL- リンゴ酸,8% グルコノデルタラクト ンおよび 8%L- 酒石酸中(特に前二者中)において 500 mV で 処理すれば , 高い耐孔食性を持つ皮膜を形成することができ る。これらの酸中では,自然電極電位においても比較的高い 耐孔食性を持つ皮膜が得られる。H2O2単独溶液を用いて H2O2濃度と SUS304 鋼の自然電極電位の関係を測定した結 果によれば4),0.98%H 2O2のときの自然電極電位は 440 mV であった。したがって,極少量の H2O2をこれらの酸に添加 すれば , 処理に適した 500 mV 付近の電位を化学的に得られ るのではないかと推測できる。 3.3 H2O2添加有機酸溶液中におけるアノード・カソー ド分極曲線 有機酸溶液へ H2O2を添加した場合,H2O2がどのような作 用をするかを知るために,H2O2添加有機酸溶液中において アノード・カソード分極曲線を測定した。一例として,脱気 し た 8%DL- リ ン ゴ 酸 単 独 溶 液 お よ び 8%DL- リ ン ゴ 酸 + x%H2O2(x = 0.98 ~ 9.8)溶液中の電解研磨 SUS304 鋼のア ノード・カソード分極曲線を図 3 に示す(自然電極電位 (500mV 付近)よりも低電位側がカソード分極,高電位側が アノード分極)。8%DL- リンゴ酸+ x%H2O2溶液中の電解研 磨 SUS304 鋼の自然電極電位は,0.98%H2O2の 380 mV から 9.8%H2O2の 540 mV まで,H2O2濃度の増加につれて高くなっ ている。これらの電位はいずれも 8%DL- リンゴ酸単独溶液 中の電解研磨 SUS304 鋼の不働態域にある。8%DL- リンゴ酸 + x%H2O2溶液中のアノード・カソード分極曲線の電流密度 は,H2O2濃度の増加につれて共に大きくなっている。これ に対して,8%DL- リンゴ酸単独溶液中の 500 mV 付近のア ノード分極曲線は一定の微小な不働態維持電流を示すだけで ある。このことより,8%DL- リンゴ酸+ x%H2O2溶液中にお ける 500 mV 付近を中心にしたアノード・カソード分極曲線 のカソード部分は H2O2の還元挙動を,またアノード部分は H2O2と SUS304 鋼の酸化挙動の重畳を表していると解する ことができる。 H2O2-H2O 系電位 -pH 図における H2O2の酸化還元挙動は, Pourbaix と de Zoubov9)によって解説されている。それに基づ くと,500 mV 付近よりも低電位側のカソード分極域では, H2O2が H2O へ 還 元 さ れ(H2O2+ 2H++ 2e−→ 2H2O),H2O2 は酸化剤として作用する。一方,500 mV 付近よりも高電位 側のアノード分極域では,H2O2の O2への酸化(H2O2→ O2 + 2H++ 2e−)が行われる。800 mV 以上になると,SUS304 鋼の過不働態溶解電流が大きくなるので,アノード電流には 500mV C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) 1200mV
Natural electrode potential(ca.-380mV)
Fig. 2 Anodic polarization curves of electro-polished and then
passiv-ation-treated Type 304 stainless steels in deaerated 3.5%NaCl. Passivation treatment: Natural immersion or potentiostatic oxida-tion at 500 mV and 1200 mV in deaerated 8%DL-malic acid solu-tion for 2 h. 0.000001 0.00001 0.0001 0.001 0.01 0.1 1 10 100 1000 10000 -500 0 500 1000 1500 2000 C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) 8% DL-malic acid 8% DL-malic acid+0.98%H2O2 8% DL-malic acid+1.75%H2O2 8% DL-malic acid+3.5%H2O2 8% DL-malic acid+7.0%H2O2 8% DL-malic acid+9.8%H2O2
Fig. 3 Anodic and cathodic polarization curves of electro-polished Type
304 stainless steels in deaerated malic acid and 8%DL-malic acid + x%H2O(x = 0.98-9.8)solutions.2
Treatment condition Object of
measurement
Treatment solution
Passivation treatment potential, Epass
Natural electrode potential
500 mV 1200 mV
Pitting potential,Epit/mV
(vs.Ag/AgCl(sat.KCl))
8% DL-malic acid 463 1097 320
8% citric acid 477 1117 393
8% L-tartaric acid 457 860 270
8% glucono-δ-lacton 447 700 258
8vol% gluconic acid 427 667 257
8vol% lactic acid 427 380 303
8vol% acetic acid 400 390 383
8% L-ascorbic acid 353 416 153
Table 1 Relationship between passivation treatment potential in organic
acid solutions and pitting potential of electro-polished Type 304 stainless steel in deaerated 3.5%NaCl.
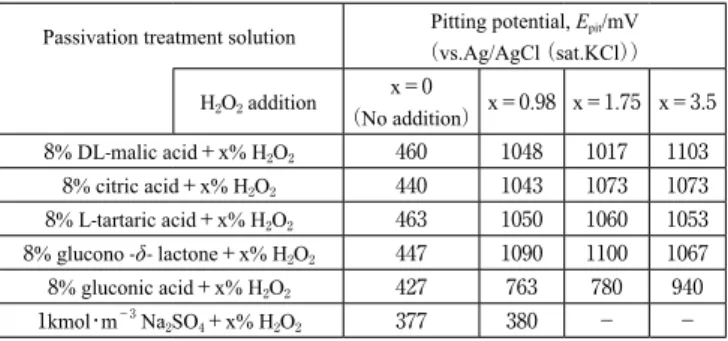
その影響が明瞭に顕われる。 以上のように,8%DL- リンゴ酸に添加された H2O2は酸化 剤として働き,0.98 ~ 9.8% の添加により電解研磨 SUS304 鋼の電位を不働態域の 500 mV 付近に化学的に保持すること ができる。 8% クエン酸+ x%H2O2溶液および 8%L- 酒石酸+ x%H2O2 溶液についてもアノード・カソード分極挙動は図 3 と同じで あり,H2O2の作用については 8%DL- リンゴ酸+ x%H2O2溶 液の場合と同様のことが言える。 3.4 H2O2添加有機酸溶液中で化学的に形成した皮膜の 耐孔食性 500 mV 形成皮膜の耐孔食性が高かった有機酸溶液に H2O2 を添加し,SUS304 鋼の自然電極電位が 500 mV 付近になる ようにすれば,その溶液中に SUS304 鋼を自然浸漬すること により耐孔食性の高い皮膜を化学的に形成できることが期待 される。 図 4 は,8%DL- リ ン ゴ 酸 + 0.98%H2O2,8% ク エ ン 酸 + 0.98%H2O2,8% グルコン酸+ 0.98%H2O2,8% グルコノデル タラクトン+ 0.98%H2O2および 8%L- 酒石酸+ 0.98%H2O2の 各溶液中に浸漬して不働態化処理した電解研磨 SUS304 鋼の 脱気 3.5%NaCl 溶液中におけるアノード分極曲線を示す。図 中には,1 kmol・m−3Na 2SO4+ 0.98%H2O2溶液中で処理した 場合の例も示した。リンゴ酸,クエン酸,グルコノデルタラ クトン,酒石酸をベースにした各溶液で処理した試料はいず れも過不働態域内の孔食電位を示し,高い耐孔食性改善効果 が得られることが分かる。グルコン酸ベースの溶液で処理し た試料は不働態域の高電位側で孔食を起こすが,やはり耐孔 食性改善効果は認められる。しかし,Na2SO4ベースの溶液 で処理した試料は不働態域内の低い電位で孔食を起こし,耐 孔食性改善効果は得られなかった。 つぎに,H2O2添加量の影響を知るために,x = 0 ~ 3.5% の範囲の各種有機酸+ x%H2O2溶液中で処理した電解研磨 SUS304 鋼についても図 4 と同様の測定を行った。得られた 孔食電位の値を表 2 にまとめて示す。x = 0.98 ~ 3.5% のリ ンゴ酸+ x%H2O2,クエン酸+ x%H2O2,酒石酸+ x%H2O2お よびグルコノデルタラクトン+ x%H2O2の各溶液で処理した 試料は,すべて 1000 mV を超す高い孔食電位を示す。それ ゆえ,これらの試料の表面皮膜の耐孔食性にはほとんど差が ないと考えられる。一方,同じ H2O2濃度範囲のグルコン酸 + x%H2O2溶液で処理した試料の孔食電位は 700 mV 台で, これらよりも少し低い。したがって , グルコン酸ベース溶液 による皮膜の耐孔食性は少し劣ると言える。 高い耐孔食性を得るのに必要な H2O2添加量については, 表 2 に見るように,リンゴ酸,クエン酸,酒石酸およびグル コノデルタラクトンベース溶液では,1000 mV 以上の高い孔 食電位が得られる H2O2添加量は 0.98 ~ 3.5% であり,この 濃度範囲では差がない。それゆえ,0.98%H2O2で十分と考え られる。 0.98%H2O2単独溶液で電解研磨 SUS304 鋼を処理したとき の孔食電位は 840 mV である(後の図 6 参照)。また,8%DL-リンゴ酸単独溶液で処理したときの孔食電位は 460 mV であ る(表 2 の x = 0 の欄参照)。これに対して,8%DL- リンゴ 酸+ 0.98% H2O2溶液で処理した試料の孔食電位は 1048 mV である(表 2)。すなわち,リンゴ酸溶液への H2O2添加によ り孔食電位が大幅に向上する。このようなことは,クエン酸, 酒石酸,グルコノデルタラクトンの各溶液についても同様に 認められる。 上述のように,0.98%H2O2を含む 8%DL- リンゴ酸,8% ク エン酸,8%L- 酒石酸および 8% グルコノデルタラクトンの 各 溶 液 で 処 理 し た 試 料 は, い ず れ も 3.5%NaCl 中 で は 1000 mV 以上の高い孔食電位を示し,耐孔食性の優劣が付け 難い。そこで,これらの試料については,腐食環境がもう少 し厳しい 0.1 kmol・m−3 HCl 溶液中で孔食電位を求めた。図 5 に脱気 0.1 kmol・m−3HCl 溶液中での各試料のアノード分極曲 線を示す。アノード分極曲線から得られる孔食電位の高低を ベース溶液で示すと,リンゴ酸≒酒石酸>グルコノデルタラ クトン>クエン酸の順となる。リンゴ酸処理と酒石酸処理は ほぼ同等の耐孔食性を与えると考えられる。しかし,酒石酸 処理皮膜は大気開放下 3.5%NaCl 浸漬では比較的早く劣化す ること(後の 3.7 参照)および酒石酸は価格が高いこと(リン ゴ酸の約 14 倍)などの難点があるので,工業的不働態化処理 としてはリンゴ酸処理の方が優位であると思われる。 0.00001 0.0001 0.001 0.01 0.1 1 10 100 0 200 400 600 800 1000 1200 C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) 8%DL-malic acid+0.98% H2O2 8%citric acid+0.98% H2O2 1kmol・m-3Na 2SO4+0.98% H2O2 8%gluconic acid+0.98% H2O2 8%L-tartaric acid+0.98% H2O2 8%glucono-δ-lacton+0.98% H2O2
Fig. 4 Anodic polarization curves of electro-polished and then
passiv-ation-treated Type 304 stainless steels in deaerated 3.5%NaCl. Passivation treatment: Natural immersion in organic acid or inor-ganic salt solutions containing 0.98%H2O2 for 2 h.
Passivation treatment solution Pitting potential, Epit/mV
(vs.Ag/AgCl (sat.KCl))
H2O2 addition (No addition)x=0 x=0.98 x=1.75 x=3.5
8% DL-malic acid+x% H2O2 460 1048 1017 1103 8% citric acid+x% H2O2 440 1043 1073 1073 8% L-tartaric acid+x% H2O2 463 1050 1060 1053 8% glucono -δ- lactone+x% H2O2 447 1090 1100 1067 8% gluconic acid+x% H2O2 427 763 780 940 1kmol・m-3 Na 2SO4+x% H2O2 377 380 - -
Table 2 Pitting potentials of electro-polished and then passivation-treated
Type 304 stainless steels in deaerated 3.5%NaCl. Passivation treatment: Natural immersion in organic acid or inorganic salt solutions containing x%H2O2 for 2 h.
Vol. 67, №3, 2016 SUS304 鋼電解研磨面の不働態化処理 155 3.5 表面仕上げの違いが耐孔食性に及ぼす影響 本研究では,試料の表面仕上げは電解研磨を標準にしてい る。電解研磨によれば , 試料表面から研磨傷などの機械的欠 陥や非金属介在物などの化学的欠陥を除去することができる。 したがって,H2O2添加有機酸溶液による SUS304 鋼の耐孔 食性改善効果も欠陥密度の小さい電解研磨面と欠陥密度の大 きい機械研磨面では異なるものと考えられる。 このことを確かめるために,バフ# 400 研磨および電解研 磨をした SUS304 鋼を 0.98%H2O2単独溶液,8%DL- リンゴ 酸+ 0.98%H2O2溶液および 8% クエン酸+ 0.98%H2O2溶液 のそれぞれの中で不働態化処理し,その後脱気 3.5%NaCl 中 でアノード分極曲線を測定した。得られたアノード分極曲線 を図 6 に示す。バフ# 400 研磨試料のアノード分極曲線は, いずれの溶液中で不働態化処理をしたものも 0 mV 付近から 立ち上がり,電位の上昇と共に電流密度が単調に増加する。 すなわち,H2O2添加有機酸溶液による耐食性改善効果はほ とんど認められない。これに対して電解研磨試料のアノード 分極曲線は,200 mV 付近からかなり高い電位まで不働態域 を示し,その後不働態化処理液の種類に応じた孔食電位を示 す。0.98%H2O2単独溶液で処理した電解研磨面の孔食電位は 840 mV であるが,8%DL- リンゴ酸+ 0.98%H2O2溶液および 8% クエン酸+ 0.98%H2O2溶液で処理した電解研磨面の孔食 電位は 1000 mV を超えている。 以上のことより,H2O2添加有機酸溶液による SUS304 鋼 の耐孔食性改善効果は,バフ# 400 研磨面では小さいが電解 研磨面では極めて大きいことが分かる。このように,耐孔食 性改善効果が試料の表面研磨状態に大きく依存する現象は, 30%HNO3処理10)および 3.5%H2O2処理4)についても認めら れている。 3.6 濃度の異なる NaCl 溶液中における耐孔食性 H2O2添 加 有 機 酸 溶 液 中 で 不 働 態 化 処 理 し た 電 解 研 磨 SUS304 鋼の耐孔食性が溶液の NaCl 濃度によってどのよう に変化するかを確かめた。電解研磨 SUS304 鋼を 8% DL- リ ンゴ酸+ 0.98%H2O2溶液中で不働態化処理した後,濃度 3.5% から飽和までの脱気 NaCl 溶液中でアノード分極曲線を測定 した結果を図 7 に示す。分極曲線の形状,不働態維持電流密 度および孔食電位の値は NaCl 濃度によってほとんど変化し ていない。孔食電位は 1053 mV(3.5%NaCl)から 1050 mV(sat. NaCl)の 範 囲 に あ る。 こ の よ う な 測 定 を 8% ク エ ン 酸 + 0.98%H2O2,8%L- 酒石酸+ 0.98%H2O2,8% グルコノデルタ ラクトン+ 0.98%H2O2の各溶液中で不働態化処理した電解 研磨 SUS304 鋼についても行った。いずれの溶液中で不働態 化処理した試料の分極曲線も,8% DL- リンゴ酸+ 0.98%H2O2 溶液中で処理した試料と同様,NaCl 濃度による変化はほと んどなく,高い孔食電位を示した。すなわち,3.5% NaCl ~ 飽和 NaCl の範囲で,8% クエン酸+ 0.98%H2O2溶液処理試 料は 1063 ~ 1043 mV,8%L- 酒石酸+ 0.98% H2O2溶液処理 試 料 は 1053 ~ 1033 mV,8% グ ル コ ノ デ ル タ ラ ク ト ン + 0.98%H2O2溶液処理試料は 1080 ~ 1020 mV,の孔食電位を 示した。それゆえ,0.98% H2O2を含む 8%DL- リンゴ酸,8% クエン酸,8%L- 酒石酸および 8% グルコノデルタラクトン 0.000001 0.00001 0.0001 0.001 0.01 0.1 1 10 100 0 200 400 600 800 1000 1200 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) C urren t D en si ty ,i / A ・m -2 8%DL-malic acid+0.98% H2O2 8%citric acid+0.98% H2O2 8%L-tartaric acid+0.98% H2O2 8%glucono- δ -lactone+0.98% H2O2
Fig. 5 Anodic polarization curves of electro-polished and then
passiv-ation-treated Type 304 stainless steels in deaerated 0.1 kmol・m−3
HCl. Passivation treatment: Natural immersion in organic acid solutions containing 0.98%H2O2 for 2 h.
0.00001 0.0001 0.001 0.01 0.1 1 10 100 -200 0 200 400 600 800 1000 1200 C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) Electropolishing/ 8%citric acid+0.98%H2O2 Buffer #400 polishing/ 0.98%H2O2 Buffer #400 polishing/ 8%DL-malic acid+0.98%H2O2 Buffer #400 polishing/ 8%citric acid+0.98%H2O2 Electropolishing/ 8%DL-malic acid+0.98%H2O2 Electropolishing/ 0.98%H2O2
Fig. 6 Anodic polarization curves of passivation-treated Type 304
stain-less steels with different surface finishing in deaerated 3.5%NaCl. Passivation treatment: Natural immersion in single 0.98%H2O2 or
organic acid solutions containing 0.98%H2O2 for 2 h.
C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) 3.5%NaCl : 10%NaCl : 20%NaCl : Saturated NaCl : 25%NaCl : Test solutions
Fig. 7 Anodic polarization curves of electro-polished and then
passiv-ation-treated Type 304 stainless steels in deaerated NaCl solutions with concentrations from 3.5% to saturation. Passivation treat-ment: Natural immersion in 8%DL-malic acid solution containing 0.98%H2O2 for 2 h.
の各溶液で処理した試料は,3.5% から飽和までの NaCl 溶液 中において十分高い耐孔食性を持っている。 3.7 NaCl 溶液中に長期間浸漬した後の耐孔食性 H2O2添加有機酸溶液で不働態化処理した電解研磨 SUS304 鋼を大気開放下の 3.5%NaCl 溶液に長期間浸漬した後脱気 3.5%NaCl 溶液中で孔食電位を測定した。測定結果の一例と して,8%DL- リンゴ酸+ 0.98%H2O2溶液で処理した電解研 磨 SUS304 鋼の NaCl 溶液浸漬日数に伴うアノード分極曲線 の変化を図 8 に示す。浸漬日数が経過しても分極曲線の形状, 不働態維持電流密度および孔食電位の値にほとんど変化は見 られない。すなわち,この処理溶液中で形成された皮膜は 183 d 経過後もほとんど損傷を受けていない。同様の測定を 他の溶液で不働態化処理した試料についても行い,浸漬日数 と孔食電位の関係を図 9 にまとめて示す。この図から以下の ことが分かる。 8%DL- リンゴ酸+ 0.98%H2O2溶液処理試料は,上述のよ うに,183d の間 1050 ~ 1110 mV の孔食電位を維持し,孔食 電位の低下は見られなかった。8% グルコノデルタラクトン + 0.98%H2O2溶液処理試料および 8% クエン酸+ 0.98%H2O2 溶液処理試料は,100 d までは孔食電位に変化はなかったが, 183d では孔食電位はそれぞれ 850 mV および 770 mV に低下 した。8%L- 酒石酸+ 0.98% H2O2溶液処理試料は,100d で 孔食電位が 660 mV に低下した。以上のような浸漬日数によ る孔食電位の変化から判断すると,不働態皮膜の塩化物によ る損傷に対する耐久性は,8%DL- リンゴ酸+ 0.98%H2O2溶 液処理皮膜が最も良く,次いで 8% グルコノデルタラクトン + 0.98%H2O2および 8% クエン酸+ 0.98%H2O2溶液処理皮 膜がほぼ同等でそれに続き,8%L- 酒石酸+ 0.98%H2O2溶液 処理皮膜はこれらよりも少し劣っている。 大気開放 3.5%NaCl 溶液中に 183d 浸漬後の 8%DL- リンゴ 酸+ 0.98%H2O2,8% グルコノデルタラクトン+ 0.98%H2O2, 8% クエン酸+ 0.98%H2O2の各溶液で処理した試料および 100d 浸漬後の 8%L- 酒石酸+ 0.98%H2O2溶液で処理した試 料の表面 SEM 写真(1000 倍)を図 10(a)~(d)にそれぞれ示す。 いずれの試料も平滑かつ均一な電解研磨面のままであり,孔 食による侵食は全く認められなかった。8%DL- リンゴ酸+ 0.98%H2O2溶液処理試料以外は,浸漬試験終了時点で孔食電 位は最初の値より低下しているが,この程度の低下では,孔 食の発生には至らないことが分かる。 3.8 X 線光電子分光法による皮膜組成の分析結果 0.98%H2O2溶 液 の み の 処 理 お よ び 8%DL- リ ン ゴ 酸 + 0.98%H2O2溶液処理について,処理後の電解研磨 SUS304 鋼 表面を XPS 測定した。これらのうち,8%DL- リンゴ酸+ 0.98%H2O2溶液処理した表面の XPS スペクトルのスパッタ リング回数による変化を図 11 に示す。スパッタリング回数 C urren t D en si ty ,i / A ・m -2 Potential , E / mV(vs.Ag/AgCl(sat.KCl)) 0d(before immersion) : 1d : 10d : 30d : 183d : 20d : 100d : 60d :
Immersion time in aerated 3.5%NaCl
Fig. 8 Change in anodic polarization curves of electro-polished and
then passivation-treated Type 304 stainless steel in deaer-ated 3.5%NaCl with immersion time in aerdeaer-ated 3.5%NaCl. The electro-polished steel was passivated in 8%DL-malic acid + 0.98%H2O2 solution for 2 h and then immersed in aerated
3.5%NaCl at 25 ℃ for 1-183d before the measurement of anodic polarization curves in deaerated 3.5%NaCl.
Immersion Time, t / d 8%glucono- δ -lacton + 0.98% H2O2 8%DL-malic acid + 0.98% H2O2 8%citric acid + 0.98% H2O2 8%L- tartaric acid + 0.98% H2O2 Pitting P otent ial , E pit / mV(vs.A g / A gCl(sa t.KCl))
Fig. 9 Pitting potential of electro-polished Type 304 stainless steel in
deaerated 3.5%NaCl as a function of immersion time in aerated 3.5% NaCl solution. The electro-polished steel was passivated in organic acid solutions containing 0.98%H2O2 for 2h and then
immersed in aerated 3.5%NaCl at 25 ℃ for 1-183d before the measurement of pitting potential in deaerated 3.5% NaCl.
(a) (b)
(d) (c)
Fig. 10 Scanning electron-micrographs of surfaces of electro-polished
and passivation-treated Type 304 stainless steels after immer-sion in aerated 3.5%NaCl at 25 ℃. Passivation treatment was performed in(a)8%DL-malic acid + 0.98%H2O2,(b)8%citric
acid+0.98%H2O2,(c)8%glucono-δ-lactone+0.98%H2O2, and
(d)8%L-tartaric acid + 0.98%H2O2. Immersion time in aerated
Vol. 67, №3, 2016 SUS304 鋼電解研磨面の不働態化処理 157 による変化の特徴は,次の通りである。 Cr2p3/2スペクトル(図 11(a)):スパッタリングしていない Cr2p3/2スペクトルは,577.0 eV にピークを示す。このピーク は,CrOOH の Cr2p3/2の結合エネルギー 577.0 ± 0.4eV11)と一 致している。それゆえ,皮膜中のクロムは CrOOH の形で存 在していることが分かる。スパッタリングを 7 回行なうと, スペクトルには CrOOH のピークに加えて 574.0 eV に別の ピークが現れる。このピークは金属 Cr0の Cr2p 3/2の結合エネ ルギー 574.4 ± 0.1 eV11)と一致している。スパッタリングに より皮膜が薄くなり,下地の影響が顕われ始めたことを示し ている。スパッタリング 9 回では,574.4 eV の金属 Cr0のピー クのみになる。 Fe2p3/2スペクトル(図 11(b)):スパッタリングしていない Fe2p3/2スペクトルは,711.0 eV と 706.8 eV のピークからなる。 711.0 eV の ピ ー ク は,Fe2O3の Fe2p3/2の 結 合 エ ネ ル ギ ー 710.9 ± 0.1 eV11)と一致しており,また 706.8 eV のピークは 金属 Fe0の Fe2p 3/2結合エネルギー 707.0 ± 0.3 eV11)と一致し ている。これから,皮膜中の鉄は Fe2O3の形で存在している ことおよび下地由来の金属 Fe0が検出されていることが分か る。5 回スパッタリングをすると Fe2O3ピークが小さくなり, Fe0ピークが大きくなる。7 回スパッタリングをすると下地 からの Fe0ピークのみとなる。 O1s スペクトル(図 11(c)):スパッタリングしていない O1s スペクトルは,531.0 eV にピークを示す。このピークは かなりブロード(幅広)なピークであり,通常 SUS304 鋼の不 働態皮膜の O1s ピークは水酸化物型結合の酸素によるピー クと酸化物型結合の酸素によるピークの二つから成ること12), および 2 回スパッタリングすると 530.3 eV に主ピークを, そして 532.0 eV にショルダー(肩)を示すピークになること から,530.3 eV ピークと 532.0 eV ピークから成っていると 考えられる。530.3 eV ピークは酸化物型結合の酸素(M-O 結 合,M:金属)の結合エネルギー 529.6 ± 1.5 eV11)と一致して いる。また,532.0 eV ピークは水酸化物型結合の酸素(M-OH 結合)の結合エネルギー 531.5 ± 0.6 eV11)と一致している。ス パッタリング 4 回のスペクトルではほとんど 530.3 eV の M-O 結合のピークのみとなる。 以上のことから,皮膜は CrOOH 型結合の Cr,Fe2O3型結 合の Fe および M-O 結合と M-OH 結合の O から成り,皮膜 上層部では M-OH 結合の割合が大きく,逆に皮膜下層部で は M-O 結合の割合が大きいと言える。 皮膜の深さ方向の組成変化を知るために,スパッタリング 時間に伴う XPS スペクトルの変化を測定した。各時間で測 定 さ れ た O1s,C1s,Cr2p,Fe2p,Ni2p,Mo3d 電子のピー ク強度比から皮膜構成元素の原子分率を半定量的に求めた。 図 12(a)および(b)に 0.98% H2O2溶液処理および 8%DL- リ ンゴ酸+ 0.98%H2O2溶液処理の場合の皮膜構成元素の原子 分率とスパッタリング時間の関係をそれぞれ示す。クロム分 率の曲線から皮膜中の Cr が最も濃縮した部分の平均クロム 分率を求めると,0.98%H2O2溶液処理皮膜では 33.3at% であ り,8%DL- リンゴ酸+ 0.98%H2O2溶液処理皮膜では 36.3at% であった。8%DL- リンゴ酸+ 0.98%H2O2溶液処理皮膜の方が, 平均クロム分率が僅かに高い。リンゴ酸はキレート剤であり, 特定の金属原子(イオン)に選択的に配位してキレート化合物 (錯体)を形成する作用がある。このような作用によって皮膜 中の Fe 原子(イオン)がキレート錯体として選択的に除去さ れた可能性もある。また,酸素分率の曲線上で酸素分率が半 分になる時間から膜厚を求めると,0.98%H2O2溶液処理皮膜 では 3.3nm,8%DL- リンゴ酸+ 0.98%H2O2溶液処理皮膜で Binding Energy , Eb / eV C ounting R at e , CR / c ounts / s 0 10000 20000 30000 40000 565 570 575 580 585 590 595 0 10000 20000 30000 40000 565 570 575 580 585 590 595 0 10000 20000 30000 40000 565 570 575 580 585 590 595 0 20000 40000 60000 80000 100000 700 705 710 715 720 725 730 0 20000 40000 60000 80000 100000 700 705 710 715 720 725 730 0 20000 40000 60000 80000 100000 700 705 710 715 720 725 730 0 10000 20000 30000 40000 50000 60000 525 527 529 531 533 535 537 0 10000 20000 30000 40000 50000 60000 525 527 529 531 533 535 537 0 10000 20000 30000 40000 50000 60000 525 527 529 531 533 535 537 (a)Cr2p Frequency of
sputtering:0 CrOOH577.0eV
(c)O1s Frequency of sputtering:0 (b)Fe2p Frequency of sputtering:0 Frequency of sputtering:7 times (42s) Frequency of sputtering:9 times (54s) CrOOH 576.8eV Cr0 574.0eV Cr0 574.4eV Frequency of sputtering:5 times (30s) Frequency of sputtering:7 times (42s) Frequency of sputtering:2 times (12s) Frequency of sputtering:4 times (24s) Fe2O3 711.0eV Fe0 706.8eV Fe2O3 710.8eV Fe0 706.9eV Fe0 707.0eV M-O 530.3eV M-OH 532.0eV M-O 530.3eV M-O 530.3eV M-OH 532.0eV
Fig. 11 Changes in XPS spectra of electro-polished Type 304 stainless steel passivated in 8%DL-malic acid + 0.98%H2O2 solution with frequency of
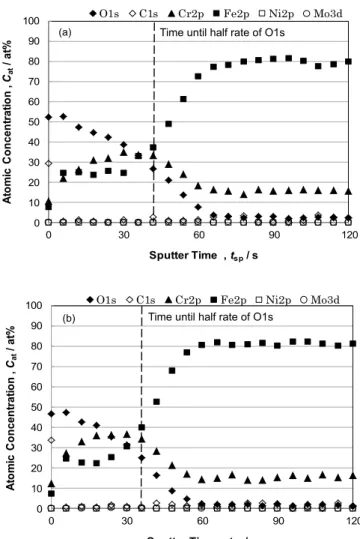
は 2.8 nm(それぞれ SiO2換算 7.83 × 10-2 nm/s として)となっ た。8%DL- リ ン ゴ 酸 + 0.98% H2O2溶 液 処 理 皮 膜 は 0.98% H2O2溶液処理皮膜よりも少し薄い。
4 .結 論
安全性が高くかつ環境負荷が低い不働態化処理液を開発す ることを目的として,8 種類の有機酸溶液およびこれに H2O2 を添加した溶液中での電解研磨 SUS304 鋼のアノード分極挙 動と不働態化処理後の耐孔食性について検討した。結果は以 下のようにまとめられる。 (1)8%DL- リンゴ酸,8% クエン酸,8%L- 酒石酸および 8% グルコノデルタラクトンの中でのアノード分極曲線の不 働態維持電流密度は小さく,不働態域の中央付近の電位 (500 mV)で形成した皮膜は高い孔食抑制効果を示す。 (2)8%DL- リンゴ酸+ 0.98%H2O2,8% クエン酸+ 0.98%H2O2, 8%L- 酒石酸+ 0.98%H2O2および 8% グルコノデルタラ クトン+ 0.98%H2O2の各溶液への浸漬処理により形成 0 10 20 30 40 50 60 70 80 90 100 0 30 60 90 120 At om ic C on ce nt ra tion , Cat / a t% Sputter Time , tsp/ sO1s C1s Cr2p Fe2p Ni2p Mo3d
0 10 20 30 40 50 60 70 80 90 100 0 30 60 90 120 At om ic C on ce nt ra tion , Cat / a t% Sputter Time , tsp/ s
O1s C1s Cr2p Fe2p Ni2p Mo3d
(a)
(b)
Time until half rate of O1s
Time until half rate of O1s
Fig. 12 Composition of passive films as a function of sputter time
obtained from counting rates of O1s, C1s, Cr2p, Fe2p, Ni2p and Mo3d electron peaks in XPS spectra.(Conversion rate: 7.83 × 10−2nm/s as SiO
2)
(a)0.98%H2O2 treatment,(b)8%DL-malic acid + 0.98%H2O2
treatment した不働態皮膜は,3.5% ~飽和 NaCl 溶液中で過不働態 域の電位に相当する高い孔食電位を示す。 (3)0.1 kmol・m−3HCl 中での孔食電位は,8%DL- リンゴ酸 + 0.98%H2O2および 8%L- 酒石酸+ 0.98%H2O2溶液処理 皮膜ではほぼ同程度で高いが,8% グルコノデルタラク トン+ 0.98%H2O2および 8% クエン酸+ 0.98%H2O2溶 液処理皮膜ではこれらよりも低くなる。 (4)H2O2添加有機酸溶液による不働態化処理の耐孔食性改 善効果は,バフ# 400 研磨面ではそれほど著しくないが, 電解研磨面では顕著である。 (5)8%DL- リンゴ酸+ 0.98%H2O2溶液処理試料は,3.5%NaCl へ 183d 浸漬しても孔食電位が低下しない。8% クエン 酸+ 0.98%H2O2および 8% グルコノデルタラクトン+ 0.98%H2O2溶液処理試料はこれよりも少し早く,そして 8%L- 酒石酸+ 0.98%H2O2溶液処理試料はさらに早く, 孔食電位が低下する。 (6)8%DL- リンゴ酸+ 0.98%H2O2溶液処理皮膜は CrOOH 型 結 合 の Cr,Fe2O3型 結 合 の Fe お よ び M-O 結 合 と M-OH 結合の O から成り,皮膜上層部では M-OH 結合 の割合が大きく,皮膜下層部では M-O 結合の割合が大 きい。膜厚は 2.8 nm であった。 (7)以上の結果を総合すると,8%DL- リンゴ酸+ 0.98%H2O2 溶液処理による皮膜は,NaCl 溶液中における孔食電位 が高いことおよび NaCl 溶液中に長期間浸漬しても孔食 電位が低下しないことから,検討した 8 種類の有機酸に よる処理皮膜の中で最も優れている。
(Received September 25, 2015 ; Accepted December 28, 2015)
文 献
₁ )金子 智 ; ステンレス鋼便覧 第3版, ステンレス協会編, p.417(日 刊工業新聞社, 1995).
₂ )ASTM A 967-05 Standard Specification for Chemical Passivation Treatments for Stainless Parts.
₃ )T. Shibata ; Zairyo-to-Kankyo, 59, 464(2010).
₄ )K. Ishimi, Y. Ida, F. Tsutaka, K. Sugimoto ; J. Surf. Finish. Soc. Jpn.,
65, 330(2014). ₅ )毒物及び劇物取締法(昭和25年12月28日法律第303号, 最終改正 平成13年6月29日). ₆ )食品衛生法(昭和22年12月24日法律第233号, 最終改正平成21年6 月5日法律第49号). ₇ ) 原 田 和 加 太, 足 立 俊 郎, 名 越 敏 郎 ; 特 開2000-345301(P2000-345301A)(2000).
₈ )K. Takizawa, Y. Nakayama, Y. Shimizu, I. Tamura ; Boshoku Gijutsu (presently Zairyo-to-Kankyo), 35, 551(1986).
₉ )M. Pourbaix, N. de Zoubov ; Atlas of Electrochemical Equilibria in Aqueous Solutions, M. Pourbaix, p. 106(National Association of Corrosion Engineers, 1974).
10)K. Ishimi, Y. Ida, F. Tsutaka, K. Sugimoto ; J. Surf. Finish. Soc. Jpn.,
66, 158(2015).
11)XPS(X線光電子分光)データベース http://techdb.podzone.net 12)K. Sugimoto, K. Kishi, S. Ikeda, Y. Sawada ; J. Jpn. Inst. Met., 38, 54