(株)島津テクノリサーチ
ペルフルオロオクタンスルホン酸
Perfluorooctanesulfonic acid (別名:PFOS)ペルフルオロオクタン酸
Perfluorooctanoic acid (別名:PFOA) 【対象物質及び構造式】Perfluorooctanesulfonic acid (PFOS) CAS 番号 1763-23-1
Perfluorooctanoic acid (PFOA) CAS 番号 335-67-1 【物理化学的性状】 分子量 沸点(℃) 蒸気圧 (mmHg) 水溶解度 log Pow PFOS (C8F17SO3K) 538.2 277~280 3.31*10-4 (20 ℃) 1 g /L - PFOS (C8F17SO3H) 500 149/15 mmHg - >10 wt% 4.9 *1 PFOA (C8F15CO2H) 414.1 37-50) 1333(25 ℃) 3400 mg/L 6.30 *2 *1 :NCBI PubChem 検索による
*2 :MEYLAN,WM & HOWARD,PH (1995)
C
C
C
C
C
C
C
C
F
F
F
F
F F
F
F
F F
F F
F
F
F
OH
O
C
C
C
C
C
C
C
C
S
O
O
OH
F
F
F
F
F F
F
F
F F
F F
F
F
F F
F
【毒性、用途等】 毒 性 情 報 : 反復投与毒性 : PFOS 経口投与(サル) NOAEL= 0.15 mg/kg・d (182 日間、K 塩) 経口投与(ラット) LOAEL = 2 mg/kg・d (K 塩、肝臓酵素増加、肝臓 空胞変性及び肝細胞肥大、 胃腸障害、血液異常、体重低下、発作、死亡 経口投与(ラット) NOAEL = 0.5ppm(オス)、2ppm(メス) (52 週間、K 塩、肝臓障害所見) LOAEL = 2ppm(オス)、5ppm(メス) (52 週間、K 塩、肝臓障害所見 反復投与毒性 :PFOA 経口投与(CD-1マウス) LOEL= 3ppm (2 週間、アンモニウム塩、 肝臓肥大) 経口投与(ニュージーランドシロウサギ) LOAEL=50 mg/kg ・ d (懐胎 6 ~ 18 日、アンモニウム塩、生殖毒性) 急性毒性等 :PFOA LD50(ラット、腹腔内) >189 mg/kg 用 途 : PFOS 消化剤、撥水剤、紙の表面処理剤 PFOA 樹脂改質剤、合成原料
§1 分 析 法
(1) 分析法の概要
全血および母乳 3 ml に 2 ng のサロゲート物質(13C4-PFOS、13C4-PFOA:50 ng/mL)、12 ml の 1%ギ酸溶液を加え、攪拌した後、超音波抽出を 5 分間行う。次 に固相カートリッジに通した後、ミリQ水 10 mL、40%メタノール/水 5 mL で洗浄 し、2%アンモニア水/メタノール 5 mL で溶出させる。抽出液を窒素気流下で約 2 mL に濃縮する。その検液を LC-MS/MS(ESI negative)にて測定する。 なお必要に応じて、0.2 µm のフィルターでろ過したものを分析試料とする。(2) 試薬・器具
【試薬】 ペルフルオロオクタンスルホン酸 (PFOS) ペルフルオロオクタン酸(PFOA) 13C 4-ペルフルオロオクタンスルホン酸 (PFOS) 13C 4-ペルフルオロオクタン酸(PFOA) 固相カートリッジ メタノール アセトニトリル ミリQ水(超純水) ぎ酸 アンモニア水 : : : : : : : : : :3M Co. (St. Paul, MN, USA)
又 は FLULKA 社 Heptadecafluorooctane
sulfonic acid Potassium salt
(lot + Filling No. 451564/1 33103304) 3M Co. (St. Paul, MN, USA)
又は FULKA 社 Pentadeca fluorooctane acid
Ammonium salt
(lot + Filling No. 444131/1 50705017) WELLINGTON LABORATORIES WELLINGTON LABORATORIES
Oasis HLB Plus Waters 社製(200 mg-6 mL)
残留農薬試験用(5000 倍濃縮) 残留農薬試験用(5000 倍濃縮) 超純水装置で精製した比抵抗16 MΩ・cm 以 上の水 (ミリQ 水) 和光純薬工業製 特級 (純度99%以上) 和光純薬工業製 特級 (25%以上) 【器具】 PP 製容器(ふた付) バイアル 0.2 µm フィルター 遠心分離器 : : : 50 mL 又は 15 mL (注 1) HPLC 用バイアル
(3) 分析法
【試料採取】 環境省「化学物質環境調査における試料採取にあたっての留意事項」に従う。 【試料溶液の調製】 全血または母乳3 mL に PFOS/PFOA 各 2 ng のサロゲート物質(13C4-PFOS、 13C 4-PFOA:50 ng/mL)、12 mL の 1%ギ酸水溶液を加えて攪拌した後、超音波抽出 を5 分間行う。次に予め、メタノール 10 mL、ミリQ水 10 mL でコンディショニ ングしたOasis HLB 固相カートリッジに通した後、ミリQ水 10 mL、次いで 40% メタノール/水 5 mL で洗浄する。その後、測定対象物質を 2%アンモニア水/メタ ノール5 mL で溶出させる。その抽出液を窒素気流下で約 2 mL に濃縮する。その 検液をLC-MS/MS(ESI negative)にて測定する。(注 2) 全血試料について、抗凝固剤が予め添加されていない場合、フィブリンや血餅 が発生するため、Oasis HLB 固相カートリッジに添加する前に取り除く操作が必要 である。また採血後すぐに測定できない場合、一旦凍結保存を行い、解凍後使用 する全血試料は、血球が溶血するために不要物が発生する可能性がある。この場 合も同様に不要物を除いた試料で Oasis HLB 固相カートリッジに添加する必要が ある。 なお必要に応じて、メタノール20 mL で予備洗浄した 0.2 µm のフィルター(注 3)でろ過したものを分析試料とする。 【標準原液及び検量線用標準液の調製】Heptadeca fluorooctanesulfonic acid potassium salt 及び Pentadeca fluorooctane acid Ammonium salt を正確にそれぞれ 10.8 mg 及び 10.4 mg 秤量し、メタノールを
用い正確に10 mL にして標準原液を作成する。PFOS 及び PFOA の標準原液として の濃度は、それぞれ1.0 ng/mL となる。この標準原液をメタノール:水(7:3)で 順次希釈し、検量線用標準液を作成する。検量線用標準液の各濃度は、0.1~5 ng/mL とする。またそれぞれの検量線用標準液は13C4-PFOS 及び13C4-PFOA が 50 ng/mL となるように調整する。 なお各試料にはサロゲート物質(13C4-PFOS、13C4-PFOA:50 ng/mL)を 40 µL 添 加する。
【測定】 <LCMS 測定条件> 〔LC 条件〕 機種 : SHIMADZU LC-20A システム カラム : Inertsil ODS-SP 2.1×150 mm(5 µm)GL サイエンス社製 移動相 A : 10 mM 酢酸アンモニウム 移動相 B : アセトニトリル グラジエント : (検討時) 0-2 min A:90% B:10% 2-12 min A:90→20% B:10→80% 12-17 min A:20% B:80% 17-25 min A:90% B:10% (ブランク低減を考慮した条件) 0-2 min A:65% B:35% 2-7 min A:65→20% B:35→80% 7-10 min A:20% B:80% 10-15 min A:65% B:35% 移動相流量 : 0.2 mL/min カラム温度 : 40 ℃ 試料注入量 : 10 µL 〔MS 条件〕
機種 : Applied Biosystems LC-MS/MS API 3200
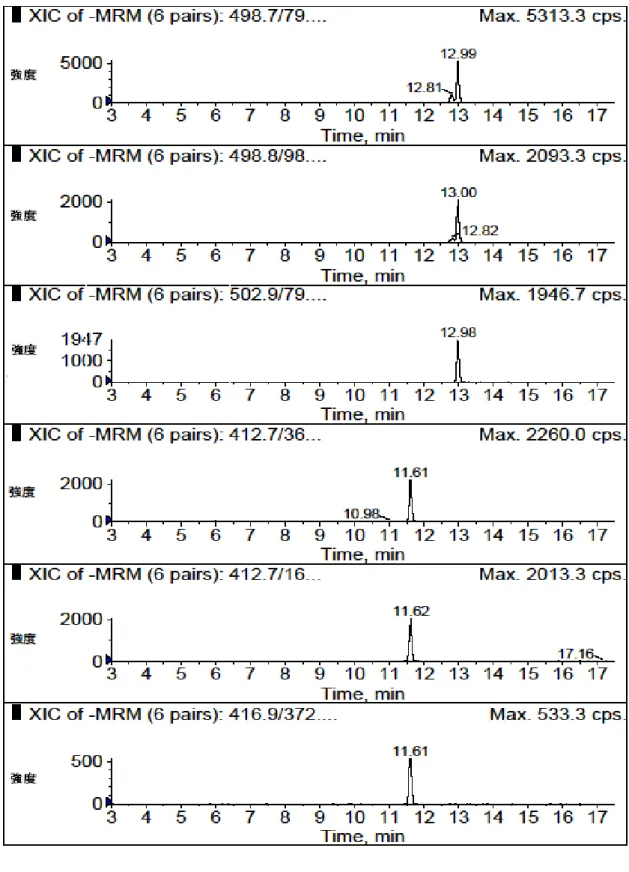
イオン化法 : ESI negative モニターイオン : PFOS 498.7E79.9(定量イオン) 498.7→98.9(確認イオン) PFOA 412.7E368.8 (定量イオン) 412.7E169.0 (確認イオン) 13C 4-PFOS 502.9E79.9 13C 4-PFOA 416.9E372.0
<検量線の濃度> 検量線は、0.1~5 ng/mL の濃度で調製する。 項目 検量線用標準液濃度 検量線濃度 PFOS (0.05)、0.1、0.2、0.5、1、5 ng/mL 検量線濃度 PFOA (0.05)、0.1、0.2、0.5、1、5 ng/mL [検量線] 検量線用標準液(0.1~5 ng/mL)10 µL を LC-MS/MS に導入し、対象物質のサロゲ ート物質に対する相対ピーク面積と濃度の比から検量線を作成する。 [定量] 試料溶液 10 µL を LC-MS/MS に導入し、対象物質のサロゲート物質に対する相 対ピーク面積を求め、検量線と比較して得られた濃度比から定量値を求める。 [濃度の算出] 試料の濃度C (ng /g)は、以下の式から算出する。 As - At C (ng /g) = v C : 測定物質の濃度(ng /g) As : 試料中の測定対象物質の重量(ng) At : 測定対象物質の操作ブランク値(ng) v : 試料採取量(g) [装置検出下限(IDL)] 本分析に用いたLC-MS/MS の IDL を下表に示す(注 4)。 物質 IDL (ng/mL) 試料量 (g) IDL 試料換算値 (ng/g) PFOS 0.0110 3 0.0073 PFOA 0.0229 3 0.0153 なお、母乳・臍帯血・血液の比重を1 として算出した。
本測定法における検出下限及び定量下限を以下に示す(注 5)。 物質 採取量 (mL) 検出下限値 MDL (pg/g) 定量下限値 MQL (pg/g) PFOS(母乳) 3 0.0087 0.0335 PFOA(母乳) 3 0.0137 0.0527 PFOS(全血) 3 0.0082 0.0317 PFOA(全血) 3 0.0101 0.0390 なお、母乳・臍帯血・血液の比重を1 として算出した。 全血においては、13C4安定同位体を用いて検討した結果である。
注
解
(注 1) ガラス器具や PP チューブ等は、使用前にメタノールで洗浄すること。 (注 2) LC-MS/MS 測定時は、ブランクとして大きなピークが検出される場合が あるため、HPLC 用メタノールやアセトニトリルを注入し、PFOS 及び PFOA の ピークが検出しなくなるまで溶離液を流し装置全体をクリーニングしてから測定 すること。 (注 3) 0.2 µm フィルターは、使用前にメタノール 20 mL で洗浄すること。 (注 4) IDL(装置検出下限値)は、「化学物質環境実態調査実施の手引き」(平成 17 年 3 月) に従って算出し、表1 に示した。(参考) 表1 装置検出下限(IDL)の算出 対象物質名 PFOS PFOA 試料量(g mL) 3 3 最終液量(mL) 2 2 注入濃度(ng/mL) 0.1 0.1 装置注入量(µL) 10 10 結果1 (ng/mL) 0.0995 0.0997 結果2 (ng/mL) 0.0958 0.102 結果3 (ng/mL) 0.0967 0.102 結果4 (ng/mL) 0.0982 0.0996 結果5 (ng/mL) 0.0950 0.116 結果6 (ng/mL) 0.0913 0.106 結果7 (ng/mL) 0.0991 0.100 平均値(ng/mL) 0.0965 0.1036 標準偏差 0.0028 0.0059 IDL(ng/mL) 0.0110 0.0229 IDL 試料換算値(ng/g) 0.0073 0.0153 S/N 15 7 CV(%) 2.9 5.7 ※IDL = t(n-1, 0.05)×In-1×2 なお、母乳・臍帯血・血液の比重を1 として算出した。(注 5) 測定方法の検出下限(MDL)及び定量下限(MQL)は、「化学物質環境実態調査実施 の手引き」(平成 17 年 3 月)に従って算出し、表 2、3 に示した。 表2 測定方法の検出下限(MDL)及び定量下限(MQL)の算出(母乳) [母乳] 対象物質名 PFOS PFOA 試料量(g) 3 3 標準品添加量 (ng) 0.1 0.1 試料換算濃度 (ng/g) 0.033 0.033 最終液量(mL) 2 2 注入濃度(ng/mL) 0.05 0.05 装置注入量(µL) 10 10 操作ブランク平均(ng/g) ① 0 0 無添加平均(ng/g) ② 0.0091 0.0310 結果1 (ng/g) 0.0339 0.0662 結果2 (ng/g) 0.0349 0.0540 結果3 (ng/g) 0.0410 0.0636 結果4 (ng/g) 0.0391 0.0614 結果5 (ng/g) 0.0382 0.0628 結果6 (ng/g) 0.0355 0.0707 結果7 (ng/g) 0.0429 0.0591 平均値 (ng/g) 0.0379 0.0625 標準偏差 0.0033 0.0053 MDL (ng/g) 0.0087 0.0137 MQL (ng/g) 0.0335 0.0527 S/N 10 7 CV(%) 8.8 8.4 ※MDL= t (n-1, 0.05)×σn-1×2 ※MQL=σn-1×10 ① 操作ブランク平均: 試料マトリックスがない状態で他は同様の操作を行い、測定した値の平均値 ② 添加平均: MDL 算出用試料に標準品を添加していない状態で含まれる濃度の平均値 ③ 試料調製は、30 mL 試料に標準品を 1 ng 添加した ④ なお、母乳・臍帯血・血液の比重を1 として算出した。
表3 測定方法の検出下限(MDL)及び定量下限(MQL)の算出(全血) [全血]13C4安定同位体を用いて検討 対象物質名 13C4-PFOS 13C4-PFOA 試料量(g) 3 3 標準品添加量 (ng) 0.1 0.1 試料換算濃度 (ng/g) 0.033 0.033 最終液量(mL) 2 2 注入濃度(ng/mL) 0.05 0.05 装置注入量(µL) 10 10 操作ブランク平均(ng/g)① 0 0 無添加平均(ng/g) ② 0 0 結果1 (ng/g) 0.0395 0.0315 結果2 (ng/g) 0.0383 0.0307 結果3 (ng/g) 0.0338 0.0339 結果4 (ng/g) 0.0331 0.0310 結果5 (ng/g) 0.0381 0.0417 結果6 (ng/g) 0.0405 0.0357 結果7 (ng/g) 0.0332 0.0360 平均値 (ng/g) 0.0366 0.0361 標準偏差 0.0032 0.0039 MDL (ng/g) 0.0082 0.0101 MQL (ng/g) 0.0317 0.0390 S/N 10 7 CV(%) 8.7 10.8 ※MDL= t (n-1, 0.05)×σn-1×2 ※MQL=σn-1×10 ① 操作ブランク平均: 試料マトリックスがない状態で他は同様の操作を行い、測定した値の平均値 ③ 添加平均: MDL 算出用試料に標準品を添加していない状態で含まれる濃度の平均値 ③ 試料調製は、30 mL 試料に13C4安定同位体標準品を1 ng 添加した ④ なお、母乳・臍帯血・血液の比重を1 として算出した。
§ 2 解 説
【分析法】 [フローチャート] 以下に分析フローを示す。 図1 分析フロー図 [検量線及びマススペクトル] 検量線及びマススペクトルを以下に示す。 図2 PFOS の検量線 (0.1~5 ng/mL) 母乳・全血 3g サロゲート:2ng 添加 1%-ギ酸 12mL 2%アンモニア/メタノール 5mL 振とう 超音波 Oasis HLB カートリッジ (メタノール 10 mL、超純水 10mL でコンディショニング) 洗浄 前捨て 1. ミリQ水 10mL 2. 40%メタノール/水 溶出 窒素パージ LC-MS/MS ESI(Negative)PFOS_A070301-m ilke.rdb (PFOS): "Linear" Regression ("1 / x" weighting): y = 0.783 x + 0.00692 (r = 0.9993)
0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6 1.8 2.0 2.2 2.4 2.6 Analyte Conc. / IS Conc.
0.0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 1.8 1.9 2.0 2.1 2.2 A n al yt e A re a / IS A re a
図3 PFOA の検量線 (0.1~5 ng/mL) PFOS_A070301-m ilke.rdb (PFOA): "Linear" Regression ("1 / x" weighting): y = 0.536 x + 0.00531 (r = 0.9990)
0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6 1.8 2.0 2.2 2.4 2.6 Analyte Conc. / IS Conc.
0.0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 1.1 1.2 1.3 1.4 1.5 A n a ly te A re a / IS A re a
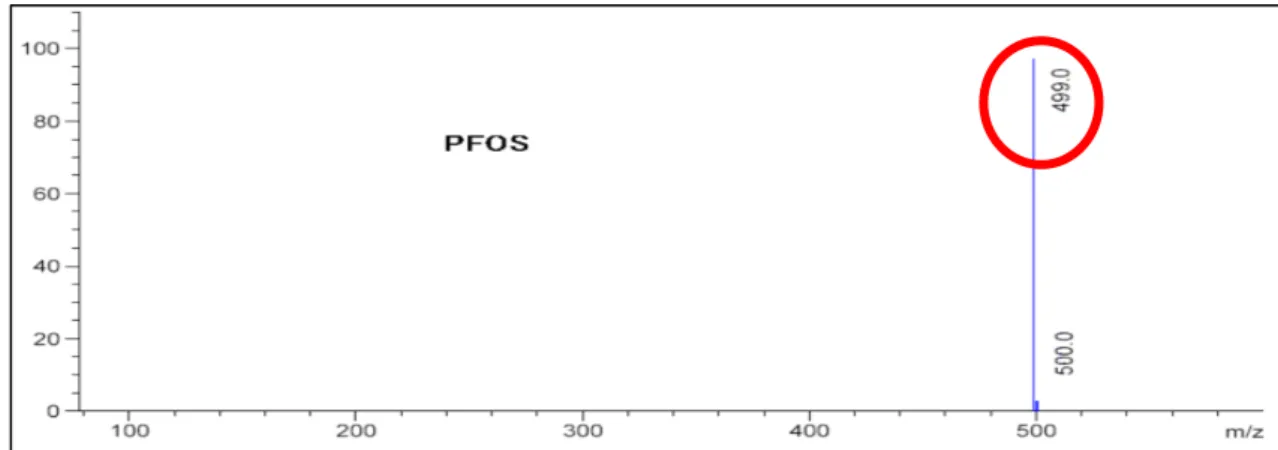
図4-1 PFOS マススペクトル(MS 及び MS/MS)
-MS2 (498.94) CE (-78): 10 MCA scans from Sample 1 (TuneSampleName) of PFOS_Final... Max. 6.4e6 cps.
80 85 90 95 100 105 110 115 120 125 130 m/z, amu 5.0e5 1.0e6 1.5e6 2.0e6 2.5e6 3.0e6 3.5e6 4.0e6 4.5e6 5.0e6 5.5e6 6.0e6 6.4e6 98.9 129.9 82.9 84.9 PFOS プレカーサーイオン m/z=499 79.9
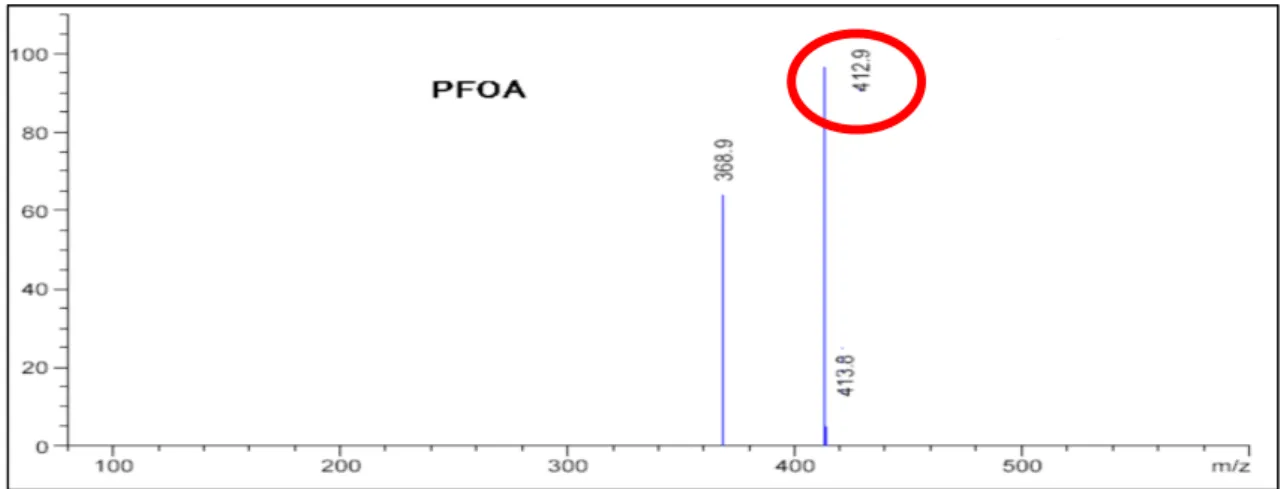
図4-2 PFOA マススペクトル(MS 及び MS/MS)
-MS2 (412.86) CE (-34): 10 MCA scans from Sample 1 (TuneSampleName) of PFOA_Final... Max. 5.6e7 cps.
120 130 140 150 160 170 180 190 200 210 220 230 240 250 260 270 280 290 300 310 320 330 340 350 360 370 m/z, amu 5.0e6 1.0e7 1.5e7 2.0e7 2.5e7 3.0e7 3.5e7 4.0e7 4.5e7 5.0e7 5.5e7 168.9 218.9 118.9 368.9 PFOA プレカーサーイオン m/z=413
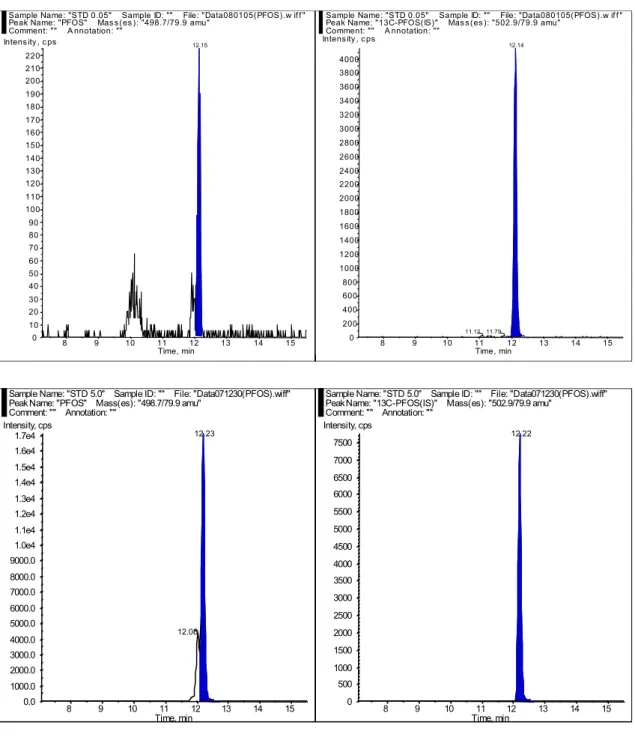
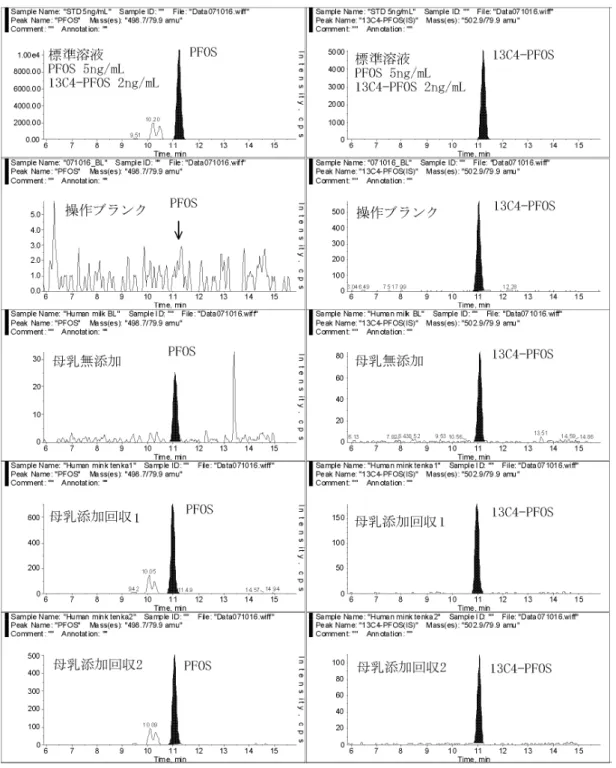
図5 PFOS 標準品(上段:0.05 ng/mL 下段:5.0 ng/mL) クロマトグラム
Sample Name: "STD 0.05" Sample ID: "" File: "Data080105(PFOS).w if f " Peak Name: "PFOS" Mas s (es ): "498.7/79.9 amu"
Comment: "" A nnotation: "" 8 9 10 11 12 13 14 15 Time, min 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180 190 200 210 220 Intens ity , c ps 12.15
Sample Name: "STD 0.05" Sample ID: "" File: "Data080105(PFOS).w if f " Peak Name: "13C-PFOS(IS)" Mas s (es ): "502.9/79.9 amu"
Comment: "" A nnotation: "" 8 9 10 11 12 13 14 15 Time, min 0 200 400 600 800 1000 1200 1400 1600 1800 2000 2200 2400 2600 2800 3000 3200 3400 3600 3800 4000 Intens ity , c ps 12.14 11.79 11.12
Sample Name: "STD 5.0" Sample ID: "" File: "Data071230(PFOS).wiff" Peak Name: "PFOS" Mass(es): "498.7/79.9 amu"
Comment: "" Annotation: "" 8 9 10 11 12 13 14 15 Time, min 0.0 1000.0 2000.0 3000.0 4000.0 5000.0 6000.0 7000.0 8000.0 9000.0 1.0e4 1.1e4 1.2e4 1.3e4 1.4e4 1.5e4 1.6e4 1.7e4 Intensity, cps 12.23 12.06
Sample Name: "STD 5.0" Sample ID: "" File: "Data071230(PFOS).wiff" Peak Name: "13C-PFOS(IS)" Mass(es): "502.9/79.9 amu"
Comment: "" Annotation: "" 8 9 10 11 12 13 14 15 Time, min 0 500 1000 1500 2000 2500 3000 3500 4000 4500 5000 5500 6000 6500 7000 7500 Intensity, cps 12.22
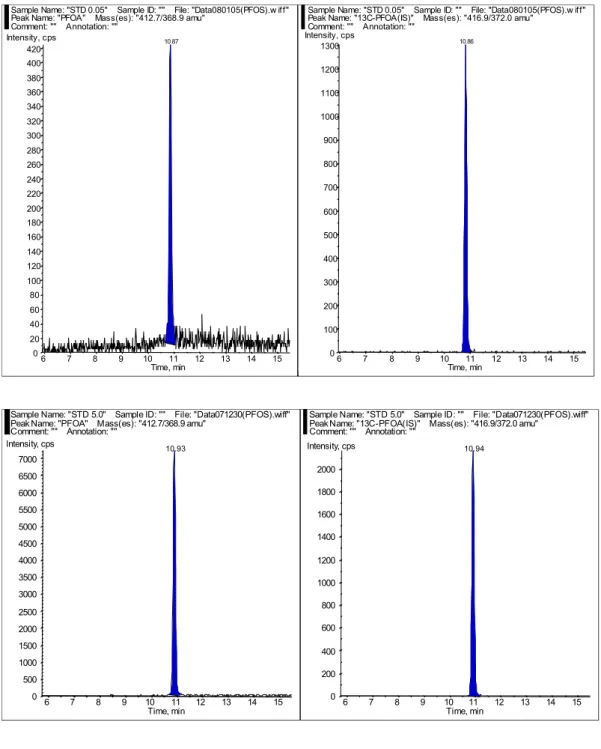
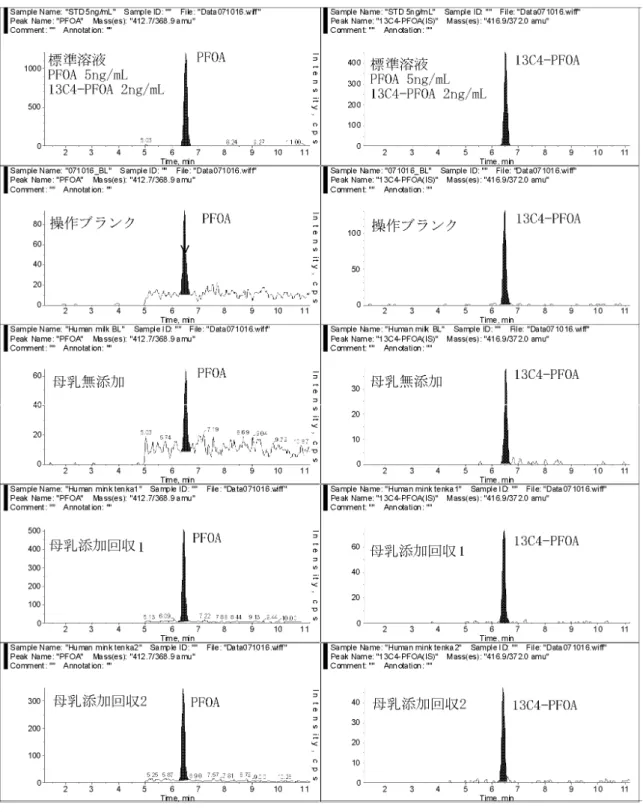
図6 PFOA 標準品(上段:0.05 ng/mL 下段:5.0 ng/mL) クロマトグラム
Sample Name: "STD 0.05" Sample ID: "" File: "Data080105(PFOS).w iff" Peak Name: "PFOA" Mass(es): "412.7/368.9 amu"
Comment: "" Annotation: "" 6 7 8 9 10 11 12 13 14 15 Time, min 0 20 40 60 80 100 120 140 160 180 200 220 240 260 280 300 320 340 360 380 400 420 Intensity, cps 10.87
Sample Name: "STD 0.05" Sample ID: "" File: "Data080105(PFOS).w iff" Peak Name: "13C-PFOA(IS)" Mass(es): "416.9/372.0 amu"
Comment: "" Annotation: "" 6 7 8 9 10 11 12 13 14 15 Time, min 0 100 200 300 400 500 600 700 800 900 1000 1100 1200 1300 Intensity, cps 10.86
Sample Name: "STD 5.0" Sample ID: "" File: "Data071230(PFOS).wiff" Peak Name: "PFOA" Mass(es): "412.7/368.9 amu"
Comment: "" Annotation: "" 6 7 8 9 10 11 12 13 14 15 Time, min 0 500 1000 1500 2000 2500 3000 3500 4000 4500 5000 5500 6000 6500 7000 Intensity, cps 10.93
Sample Name: "STD 5.0" Sample ID: "" File: "Data071230(PFOS).wiff" Peak Name: "13C-PFOA(IS)" Mass(es): "416.9/372.0 amu"
Comment: "" Annotation: "" 6 7 8 9 10 11 12 13 14 15 Time, min 0 200 400 600 800 1000 1200 1400 1600 1800 2000 Intensity, cps 10.94
[固相カートリッジからの溶出液の検討] マトリックスが無い状態では、PFOS/PFOA はメタノールのみの溶出でも問題が 無かった。図10 にサロゲート物質(13C4-PFOS、13C4-PFOA:50 ng/mL)を用いた 固相カートリッジからの溶出検討結果を示す) しかしながら、実際の母乳を用いた検討では、メタノール溶出で、13C 安定同位 体の回収率はPFOS が 60~90%程度、PFOA が 45~80%程度であった。 2%アンモニア/MeOH 溶出では、PFOA/PFOA ともにバラツキが少なく、平均 80% 以上の回収であった。 図10 固相カートリッジからの溶出検討結果 [添加回収実験結果] 母乳への標準物質添加回収実験結果を表4 に示す。 表4 添加回収実験結果 試料 母乳 全血
PFOS PFOA PFOS PFOA
試料量:g 3 3 3 3 添加量:ng 1.5 1.5 1.5 1.0 設定濃度:ng/g 0.5 0.5 0.5 0.33 注入濃度:ng/g 0.75 0.75 0.75 0.5 試行回数 5 5 5 5 回収率:% 97-110 平均:104 72-87 平均:80 71-96 平均:82 63-90 平均:80 CV:% 5.2 8.0 16 17 なお母乳・臍帯血・血液には、サロゲート物質(13C4-PFOS、13C4-PFOA:50 ng/mL)
[LC 条件の検討結果] 分析初期条件における移動相の安定化時間の長短によっても PFOA のブランク 値は異なってくる。LC 条件において、特に初期のアセトニトリル溶媒の割合が低 い場合、かなり大きな PFOA ピークが確認される。出来るだけ感度を損なわず、 ブランクを下げるためは、移動相のグラジュエント条件を工夫する必要がある。 一例としてLC 条件 1~4(図 11~14)を記載した。 結果は、 1. 移動相 B のアセトニトリルの初期割合を 35%~40%程度にすることで、LC 装置や移動相等に含まれるPFOA のカラムヘッド面に濃縮される PFOA 量は 低減される。 2. 移動相の急激な濃度勾配条件では、PFOS のピーク分離が不十分となる。 3. PFOA の溶出する時間における有機溶媒割合により、感度が大きく異なる。 先に示したLC 条件で PFOA ブランクが高く検出される場合は、事項に示す 4 例 を参考に、上記の点を留意しながら、LC 条件の変更が必要である。なお、どうし ても改善されない場合は、移動相条件をアイソクラテックで行うとよい。
<LC 分析条件-1>
移動相 A:10 mM 酢酸アンモニウム溶液 B:アセトニトリル
標準品濃度0 ng/mL のクロマトグラム
XIC of -MRM (4 pairs): 498.7/79.9 amu from Sample 9 (MeOH-BL) of Dat... Max. 16.0 cps.
5 10 15 20 Time, min 0 5 10 15 In te n. ..
Acq. File: Data080313.wiff Sample Name: MeOH-BL Sample Number: N/A
XIC of -MRM (4 pairs): 502.9/79.9 amu from Sample 9 (MeOH-BL) of D... Max. 1.9e4 cps.
5 10 15 20 Time, min 0.0 5000.0 1.0e4 1.5e4 1.9e4 In te n. .. 13.13 Acq. File: Data080313.wiff Sample Name: MeOH-BL
Sample Number: N/A
XIC of -MRM (4 pairs): 412.7/368.9 amu from Sample 9 (MeOH-BL) of ... Max. 456.0 cps.
5 10 15 20 Time, min 0 20 40 In te n. ..
Acq. File: Data080313.wiff Sample Name: MeOH-BL Sample Number: N/A
XIC of -MRM (4 pairs): 416.9/372.0 amu from Sample 9 (MeOH-BL) of ... Max. 444.0 cps.
5 10 15 20 Time, min 0 200 400 In te n. .. 8.83 Acq. File: Data080313.wiff Sample Name: MeOH-BL
Sample Number: N/A
PFOA
13C4-PFOA 13C4-PFOS PFOS
<LC 分析条件-2> 移動相 A:10 mM 酢酸アンモニウム溶液 B:アセトニトリル 標準品濃度0 ng/mL のクロマトグラム 図12 LC 条件違いによる PFOS/PFOA のブランク確認-2 PFOA 13C4-PFOA 13C4-PFOS PFOS
<LC 分析条件-3> 移動相 A:10 mM 酢酸アンモニウム溶液 B:アセトニトリル 標準品濃度0 ng/mL のクロマトグラム PFOA 13C4-PFOA 13C4-PFOS PFOS
<LC 分析条件-4> 移動相 A:10 mM 酢酸アンモニウム溶液 B:アセトニトリル 標準品濃度0 ng/mL のクロマトグラム 図14 LC 条件違いによる PFOS/PFOA のブランク確認-4 PFOA 13C4-PFOA 13C4-PFOS PFOS
【評価】
本法により、母乳及び臍帯血・血液試料中の 0.01~0.02 ng/g レベルに存在する
PFOS 及び PFOA の定量が可能である。
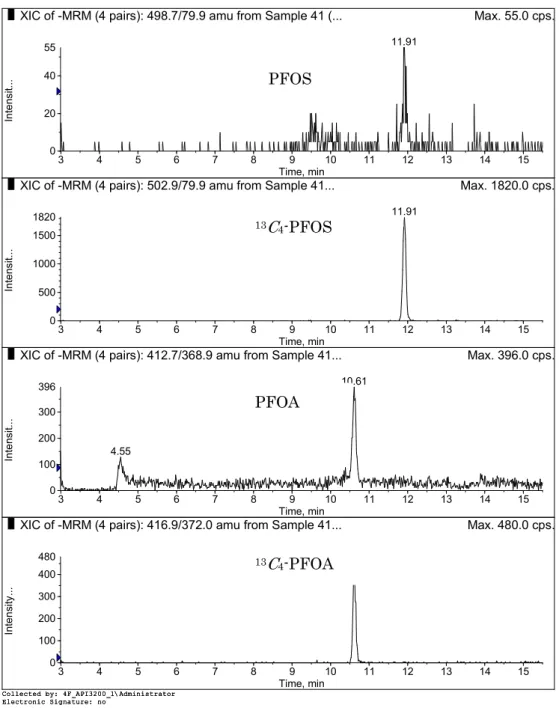
参考までに、母乳及び血液(全血)試料のクロマトグラムを以下に示す。
図15 母乳試料の PFOS/PFOA のクロマトグラム
XIC of -MRM (4 pairs): 498.7/79.9 amu from Sample 41 (... Max. 55.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 20 40 55 In te ns it. .. 11.91 Printing Time: 11:04:38 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no
Operator: Administrator
XIC of -MRM (4 pairs): 502.9/79.9 amu from Sample 41... Max. 1820.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 500 1000 1500 1820 In te ns it. .. 11.91 Printing Time: 11:04:38 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no
Operator: Administrator
XIC of -MRM (4 pairs): 412.7/368.9 amu from Sample 41... Max. 396.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 100 200 300 396 In te ns it. .. 10.61 4.55 Printing Time: 11:04:38 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no
Operator: Administrator
XIC of -MRM (4 pairs): 416.9/372.0 amu from Sample 41... Max. 480.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 100 200 300 400 480 In te n si ty ... 10.61 Printing Time: 11:04:38 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no Operator: Administrator PFOA 13C4-PFOA 13C4-PFOS PFOS
図16 血液(全血)試料の PFOS/PFOA のクロマトグラム 【担当者氏名・連絡先】 担当 株式会社島津テクノリサーチ 住所 〒604-8436 京都市中京区西ノ京三条坊町 2-13 TEL:075-811-3182 FAX:075-811-3278 担当者 青野さや香 [email protected] 大井悦雅 [email protected]
XIC of -MRM (4 pairs): 498.7/79.9 amu from Sample 50... Max. 7160.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 2000 4000 6000 7160 In te n si t. .. 12.20 12.02 10.24 14.62 Printing Time: 11:10:58 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no
Operator: Administrator
XIC of -MRM (4 pairs): 502.9/79.9 amu from Sample 50... Max. 1820.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 500 1000 1500 1820 In te n si t. .. 12.20 Printing Time: 11:10:58 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no
Operator: Administrator
XIC of -MRM (4 pairs): 412.7/368.9 amu from Sample 50... Max. 620.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 200 400 600 In te n si t. .. 10.94 Printing Time: 11:10:58 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no
Operator: Administrator
XIC of -MRM (4 pairs): 416.9/372.0 amu from Sample 50... Max. 316.0 cps.
3 4 5 6 7 8 9 10 11 12 13 14 15 Time, min 0 100 200 300 In te n si ty .. . 10.94 Printing Time: 11:10:58 AM
Printing Date: Tuesday, August 19, 2008
Collected by: 4F_API3200_1\Administrator Electronic Signature: no Operator: Administrator PFOA 13C4-PFOA 13C4-PFOS PFOS
Perfluorooctanesulfonic acid (PFOS) Perfluorooctanoic acid (PFOA)
This method provides procedure for the determination of PFOS/PFOA in breast milk, maternal blood and cord blood sample by liquid chromatography/tandem quadrupole mass
spectrometry (LC/MS/MS). A breast milk and blood sample spiked 13C4-PFOS and
13C
4-PFOA as surrogate is added 1% formic acid. And then, it is extracted with ultrasonic
extraction for 5 minutes. And liquid layer is passed through an Oasis HLB cartridge. It is washed 10 mL of water, and washed 5 mL of 40% methanol / water. The extract is eluted with 5 mL of 2% ammonia water / methanol. After the eluted solution is concentrate to 2 mL under a gentle nitrogen stream and analyze with LC/MS/MS. The analytes are determined in the SRM mode as the precursor/product ion pair of m/z 498.7/79.9 for PFOS
and m/z 502.9/79.9 for 13C4-PFOS and m/z 412.7/368.8 for PFOA and m/z 416.9/372.0 for
13C
4-PFOA. The method detection limit (MDL) is PFOS (milk) 0.0087 ng/g, PFOS
(blood) 0.0082 ng/g, PFOA (milk) 0.014 ng/g, PFOA (blood) 0.010 ng/g, and the method
quantification limit (MQL) is PFOS (milk) 0.034 ng/g, PFOS (blood) 0.032 ng/g, PFOA (milk) 0.053 ng/g, PFOA (blood) 0.039 ng/g. The average of recoveries (N=5) of PFOS/PFOA in a breast milk and blood containing 0.33-0.5 ng/g is 80-104%. The relative standard deviation is 1.4%.
Sample 3g
13C
4-PFOS・13C4-PFOS:2ng add.
1%- formic acid 12 mL
2%ammonia water / methanol 5mL
Extract Oasis HLB Cartridge
(with methanol 10 mL、watar 10mL conditioning) Washing 1. water 10mL 2. 40%water / methanol Elute Nitrogen purge → 2ml LC-MS/MS ESI(Negative)
物質名 分析法フローチャート 備考 Perfluorooctane sulfonic acid (PFOS) Perfluorooctanoic acid (PFOA) 装置: API-3200 LC/MS/MS ESI 負イオン <PFOS> Q1/Q3→ 498.7/79.9 13C 4-surrogate Q1/Q3→ 502.9-79.9 <PFOA> Q1/Q3→ 412.7/368.8 13C 4-surrogate Q1/Q3→ 416.9/372.0 カラム Inertsil ODS-SP 2.1×150 mm (5 µm) 検出下限(MDL) PFOS 0.0082 ~ 0.0087 ng/g PFOA 0.010~0.014 ng/g 1%ギ酸水溶液 12 mL パージ 2 mL まで Oasis HLB カートリッジ ミリQ水 10 mL 前捨て 40%メタノール 5 mL 前捨て 2%アンモニア水/メタノール 5 mL で溶出 超音波抽出 5 分間 LC-MS/MS 試料 3g ESI(Negative) サロゲート:2ng 添加 1%-ギ酸 12mL
![表 3 測定方法の検出下限 (MDL) 及び定量下限 (MQL) の算出(全血) [全血] 13 C 4 安定同位体を用いて検討 対象物質名 13 C 4 -PFOS 13 C 4 -PFOA 試料量 (g) 3 3 標準品添加量 (ng) 0.1 0.1 試料換算濃度 (ng/g) 0.033 0.033 最終液量 (mL) 2 2 注入濃度 (ng/mL) 0.05 0.05 装置注入量 (µL) 10 10 操作ブランク平均(ng/g) ① 0 0 無添加平均(ng/g) ②](https://thumb-ap.123doks.com/thumbv2/123deta/8694694.957193/10.892.140.771.227.861/用い対象CPFOSCPFOA試料量標準品添濃度装置注入µLブランク②.webp)