1
(別添様式)
未承認薬・適応外薬の要望に対する企業見解
1.要望内容に関連する事項
会社名
ファイザー株式会社
要 望 さ れ
た医薬品
要望番号
Ⅱ-72
成
分
名
( 一 般 名 )
① 注射液:クリンダマイシンリン酸エステル
② カプセル:クリンダマイシン塩酸塩
販
売
名
① ダラシン S 注射液 300mg、同 600mg
② ダラシンカプセル 75mg、同 150mg
未承認薬・適応
外薬の分類
( 該 当 す る も の に チェックする。)未承認薬
適応外薬
要望内容
効 能 ・ 効 果
( 要 望 さ れ た 効 能・効果について記 載する。)トキソプラズ脳炎を含む重症トキソプラズマ症
の治療および再発予防
用 法 ・ 用 量
( 要 望 さ れ た 用 法・用量について記 載する。)1 回 600mg を 1 日 4 回点滴静注あるいは経口投
与する。
備
考
( 該 当 す る 場 合 は チェックする。) 小児に関する要望 (特記事項等)現 在 の 国
内 の 開 発
状況
現在開発中 治験実施中 承認審査中 現在開発していない 承認済み 国内開発中止 国内開発なし (特記事項等)企 業 と し
て の 開 発
の意思
あり なし(開発が困難とする場合、その特段の理由)
項6 で記載したとおり,米国 CDC ガイドラインおよび本邦 熱帯病治療薬 研究班ガイドライン(寄生虫症薬物治療の手引き)において,AIDS 患者, 免疫不全の患者のトキソプラズマ症の治療には,標準治療としてpyrimethamine+ sulfadiazine+ロイコボリンの併用,または pyrimethamine+ クリンダマイシン+ロイコボリンの併用治療を推奨している。しかしなが
2 ら,本邦において primethamine は承認されておらず,sulfadiazine は承認が 得られているものの,トキソプラズマ脳炎を含む重症トキソプラズマ症の治 療および再発予防に対する適応は得られていない。したがって,ダラシン S 注射液およびカプセルの要望効能・効果に対する開発を進めるにあたり, primethamine および sulfadiazine の両薬剤についても,開発の意思が得られ る必要があると考える。
「 医 療 上
の 必 要 性
に 係 る 基
準 」 へ の
該当性
( 該 当 す る も の に チ ェ ッ ク し 、 分 類 し た 根 拠 に つ い て 記 載する。)1.適応疾病の重篤性
ア 生命に重大な影響がある疾患(致死的な疾患) イ 病気の進行が不可逆的で、日常生活に著しい影響を及ぼす疾患 ウ その他日常生活に著しい影響を及ぼす疾患 エ 上記の基準に該当しない (上記に分類した根拠) AIDS 患者やリンパ球増殖性症候群のために免疫抑制療法を受けている 患者において,血清学的に Toxoplasma gondii 陽性である場合には,トキ ソプラズマ脳症を発症するリスクが極めて高く,治療を行わなければ急 速に致死的となることがある。 以上のことから,適応疾病の重篤性はアに該当すると考える。2.医療上の有用性
ア 既存の療法が国内にない イ 欧米等の臨床試験において有効性・安全性等が既存の療法と比 べて明らかに優れている ウ 欧米等において標準的療法に位置づけられており、国内外の医 療環境の違い等を踏まえても国内における有用性が期待できると考 エ 上記の基準に該当しない (上記に分類した根拠) トキソプラズマ脳炎に対する治療薬として国内外の教科書およびガイド ラインで推奨されているスルファジアジン,ピリメサミンおよびロイコ ボリンもしくはクリンダマイシン,ピリメサミンおよびロイコボリンの 三剤併用療法は,いずれもトキソプラズマ脳炎を含む重症トキソプラズ マ症の治療および再発予防に対する適応を国内では有していない。 以上のことから,医療上の有用性はアに該当すると考える。備考
以下、タイトルが網かけされた項目は、学会等より提出された要望書又は見解
に補足等がある場合にのみ記載。
3
2.要望内容に係る欧米での承認等の状況
欧米等 6 か
国での承認
状況
(該当国にチ ェックし、該 当国の承認内 容を記載す る。)米国
英国
独国
仏国
加国
豪州
〔欧米等 6 か国での承認内容〕
欧米各国での承認内容(要望内容に関連する箇所に下線) 米国 販売名(企業名) 承認なし 効能・効果 用法・用量 備考 英国 販売名(企業名) 承認なし 効能・効果 用法・用量 備考 独国 販売名(企業名) 承認なし 効能・効果 用法・用量 備考 仏国 販売名(企業名) 承認なし 効能・効果 用法・用量 備考 加国 販売名(企業名) 承認なし 効能・効果 用法・用量 備考 豪州 販売名(企業名) 承認なし 効能・効果 用法・用量 備考欧米等 6 か
国での標準
的使用状況
(欧米等 6 か 国で要望内容 に関する承認 がない適応外 薬についての み、該当国に チェックし、 該当国の標準 的使用内容を 記載する。)米国
英国
独国
仏国
加国
豪州
〔欧米等 6 か国での標準的使用内容〕
欧米各国での標準的使用内容(要望内容に関連する箇所に下線) 米国 ガイドライ ン名Guidelines for Prevention and Treatment of
Opportunistic Infections in HIV-Infected Adults and Adolescents, Recommendations from CDC, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America.
効能・効果 (または効能・ 効果に関連のあ
4 る記載箇所) 用法・用量 (または用法・ 用量に関連のあ る記載箇所) 148p ガイドライン の根拠論文
要望 1. Katlama C, De Wit S, O’Doherty E, et al. Pyrimethamine-clindamycin vs.
pyrimethamine-sulfadiazine as acute and long-term therapy for toxoplasmic encephalitis in patients with AIDS. Clin Infect Dis 1996;22(2):268-75.
要望 2. Dannemann B, McCutchan JA, Israelski D, et al. Treatment of toxoplasmic
encephalitis in patients with AIDS. a randomized trial comparing pyrimethamine plus clindamycin to pyrimethamine plus sulfadiazine. Ann Intern Med 1992;116(1):33-43.
要望 3. Leport C, Raffi F, Matheron S, et al. Treatment of central nervous system toxoplasmosis with pyrimethamine/sulfadiazine combination in 35 patients with the acquired immunodeficiency
syndrome: efficacy of long-term continuous therapy. Am J Med 1988;84:94-100.
要望 4. Luft BJ, Hafner R, Korzun AH, et al. Toxoplasmic encephalitis in patients with the acquired immunodeficiency syndrome. N Engl J Med 1993;329(14):995-1000. 備考 英国 ガイドライ ン名 不明 効能・効果 (または効能・ 効果に関連のあ る記載箇所) 用法・用量 (または用法・ 用量に関連のあ る記載箇所) ガイドライン の根拠論文 備考 独国 ガイドライ ン名 不明 効能・効果
5 (または効能・ 効果に関連のあ る記載箇所) 用法・用量 (または用法・ 用量に関連のあ る記載箇所) ガイドライン の根拠論文 備考 仏国 ガイドライ ン名 不明 効能・効果 (または効能・ 効果に関連のあ る記載箇所) 用法・用量 (または用法・ 用量に関連のあ る記載箇所) ガイドライン の根拠論文 備考 加国 ガイドライ ン名 不明 効能・効果 (または効 能・効果に関連 のある記載箇 所) 用法・用量 (または用 法・用量に関連 のある記載箇 所) ガイドライ ンの根拠論 文 備考 豪州 ガイドライ ン名 不明 効能・効果 (または効
6 能・効果に関連 のある記載箇 所) 用法・用量 (または用 法・用量に関連 のある記載箇 所) ガイドライ ンの根拠論 文 備考
3.要望内容に係る国内外の公表文献・成書等について
(1)無作為化比較試験、薬物動態試験等に係る公表文献としての報告状況
<海外における臨床試験等>1)データベース:Medline(Ovid 版)1946-present & In-Process. 検索式:
1 ((Toxoplasmic encephalitis or encephalopathy) and (Dalacin or clindamycin)).af. 2 limit 1 to randomized controlled trial.
検索時期:2011 年 11 月 28 日.
検索結果:トキソプラズ脳炎を含むトキソプラズマ症を対象とした無作為化比較試験等 (Randomized Controlled Trial)は 6 報であった。
海外における臨床試験の概要: 海外における臨床試験に係る公表文献の報告状況は,これらの文献検索で得られた 6 報要 望1~3, 企 業1~3と学会要望書において引用された文献 1 報要 望4を加え 7 報により評価し た。これらの論文において,HIV 患者におけるトキソプラズ脳炎を対象とし経口 pyrimethamine+経口クリンダマイシン併用投与,あるいは経口 pyrimethamine+静注クリン ダマイシン併用投与した場合,クリンダマイシンは有効性を示すことを確認した。 下記に示す Katlama C et al. (1996)要 望1の文献は,CDC(米国)ガイドラインで引用 された根拠論文である。その要旨は,AIDS 患者におけるトキソプラズ脳炎の治療の第 1 選択薬は pyrimethamine+sulfadiazine+ロイコボリンの併用であるが,その代替療法として 急性療法の投与量:pyrimethamine+クリンダマイシン(2.4g/日経口,分 4)または sulfadiazine +ロイコボリンの併用を 6 週間,維持療法の投与量:pyrimethamine+クリンダマイシン(1,2 g/日経口,分 4)または sulfadiazine +ロイコボリンを長期間併用投与した。 pyrimethamine+sulfadiazine の代替療法として,pyrimethamine+クリンダマイシンの併用は 有効であり,急性療法期の副作用として,皮疹(3%),下痢(8%)が認められた。 文献,(発行年), 臨床試験 Katlama C et al. (1996)要 望1 無作為化比較試験 対象 トキソプラズマ脳炎,対象患者数:299 例,HIV 陽性,平均年齢は P+C 群;34±9 歳,P+S 群;33±8 歳
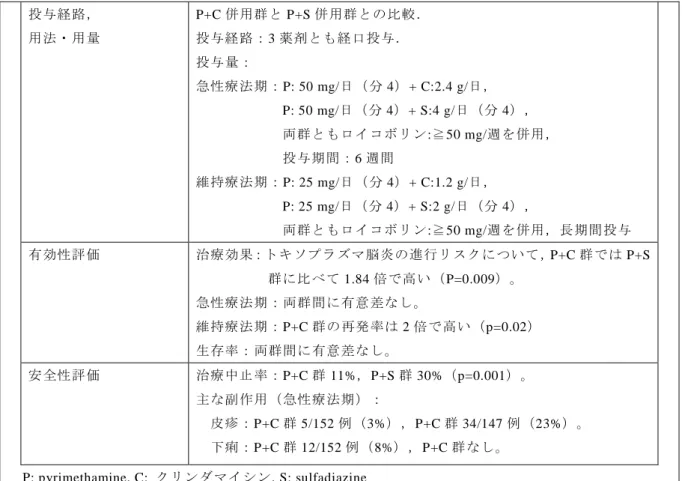
7 投与経路, 用法・用量 P+C 併用群と P+S 併用群との比較. 投与経路:3 薬剤とも経口投与. 投与量: 急性療法期:P: 50 mg/日(分 4)+ C:2.4 g/日, P: 50 mg/日(分 4)+ S:4 g/日(分 4), 両群ともロイコボリン:≧50 mg/週を併用, 投与期間:6 週間 維持療法期:P: 25 mg/日(分 4)+ C:1.2 g/日, P: 25 mg/日(分 4)+ S:2 g/日(分 4), 両群ともロイコボリン:≧50 mg/週を併用,長期間投与 有効性評価 治療効果:トキソプラズマ脳炎の進行リスクについて,P+C 群では P+S 群に比べて 1.84 倍で高い(P=0.009)。 急性療法期:両群間に有意差なし。 維持療法期:P+C 群の再発率は 2 倍で高い(p=0.02) 生存率:両群間に有意差なし。 安全性評価 治療中止率:P+C 群 11%,P+S 群 30%(p=0.001)。 主な副作用(急性療法期): 皮疹:P+C 群 5/152 例(3%),P+C 群 34/147 例(23%)。 下痢:P+C 群 12/152 例(8%),P+C 群なし。 P: pyrimethamine, C: クリンダマイシン, S: sulfadiazine
<クリンダマイシン経口剤/注射剤の Core Data Sheet(弊社) における記載状況, Version 5.0, 11-May-2011CDS>
表 1 に示す 5 報企 業2,4-7の文献はクリンダマイシン(経口剤/注射剤)Core Data Sheet の
トキソプラズ脳炎に対するクリンダマイシン治療の根拠論文である。クリンダマイシンは pyrimethamine,葉酸(ロイコボリン)と共に併用投与され,その投与量は 1,200~4,800 mg/ 日の範囲であり,5 報中 2 報企 業-2,6では 2,400 mg/日(分 4)を経口または静脈内投与した。 トキソプラズ脳炎に対するクリンダマイシン併用治療について,その有効性(臨床的・神 経学的評価,頭部 CT/MRI 所見)および安全性が報告されている。 表 1.AIDS 患者におけるトキソプラズ脳炎に対するクリンダマイシン併用治療 文献 (発行 年) 対象疾患 併用薬, 用法・用量 有効性 評価 安全性 評価
8 <日本における臨床試験等>
データベース:医中誌 WEB,1983~2011(全年)
検索式:((トキソプラズマ脳炎/AL or (トキソプラズマ症/TH or トキソプラズマ症/AL)) and ((Clindamycin/TH or ダラシン/AL) or (Clindamycin/TH or clindamycin/AL)) 検索結果:33 報見出された。トキソプラズ脳炎を含むトキソプラズマ症を対象とした無 企業 4 (1988) トキソプラ ズマ脳炎, AIDS, 29-64 歳,15 例 一次治療 P+C(iv)1,200 mg 6 時間 毎,900 mg 6 または 8 時間 毎 再発予防 P+C(po)300~900 mg 6 時間毎, 900 mg 8 時間毎 臨床的効果 および頭部 CT 所見:改 善 11/15 例 C 投与 15 例中 12 例で発現した副作 用の内訳. 下痢 4 例,皮疹 5 例,可逆的顆粒球減 少症 1 例,悪心・嘔 吐・下痢1例,腹 痛・下痢 1 例 企業 2 (1991) 無作為化 試験 ト キ ソ プ ラ ズ マ 脳 炎 , AIDS,148 例 一 次 治 療 お よ び 維 持 治 療:P+C(po/iv)2,400 mg/ 日(維持:1,200 mg/日), または S+葉酸 神経学的効果:回復ま たは改善 77%(114/148 例) 148 例 中 の 副 作 用 発現例数, 皮疹:52 例,発熱: 31 例,下痢:17 例, 悪心:12 例,その 他:21 例 企業 5 (1991) レトロス ペク ティブ ト キ ソ プ ラ ズ マ 脳 炎 , AIDS, 14 例, 23-39 歳,骨 髄 抑 制 *, ア レルギー**, 一次治療: P+C(po)600-900 mg, 8 時 間毎+葉酸, 6-8 週間 維持治療: P+C(po)300 mg 6 時間毎 または 450 mg 8 時間毎+葉 酸,平均 7.7 ヵ月間 P+C: 臨 床 症 状 : 著 効 10/14 例 , 神 経 学 的 症 状:著効 8/14 例 C に 関 連 し た 副 作 用 ( 2/14 例) ; 重 度 の 悪 心 ・ 嘔 吐 1 例 , 重 度 の 下 痢 1 例(偽膜性大腸炎と の関連なし) 企業 6 (1991) 中 枢 神 経 系 急 性 ト キ ソ プラズマ症, AIDS, 51 例 3 剤併用: P+C(po)2,400 mg/日 (po/iv)+ Spiramycin + 葉 酸を 3 週間投与 2 剤併用: P+C(po/iv)2,400 mg/日+ 葉酸を 3 週間投与 生存率は 3 剤,2 剤併用 ともに 92%.脳病巣お よ び 神 経 学 的 症 状 の 寛 解:3 剤,2 剤併用とも に 80%. Spiramycin を 投 与 す る ベ ネ フ ィ ッ ト はない P+C, 51 例 中 の 副 作用発現率は, 貧血 12%,白血球減 少 25%,血 小板 減 少 症 20%, アレ ル ギー皮膚反応 20%, 胃腸障害 33% 企業 7 (1991) 中 枢 神 経 系 急 性 ト キ ソ プラズマ症, AIDS, 8 例, 22-51 歳 一次治療および維持治療: P+C(po)1,200-2,400 mg/ 日 分 4 sulfadiazine アレルギー 患者 6 例中 4 例が臨 床・CT/MRI 所見ともに 改善 C 高用量(2,400 mg)では全例で下 痢が発現したが,減 量(1,200 mg)によ り消失
P: pyrimethamine, C: クリンダマイシン, S: sulfadiazine, po: 経口投与, iv: 静注
*P+S の標準療法では骨髄抑制のためトキソプラズマ脳炎の治療ができない.**サルファ薬に重度 のアレルギー反応を示す患者.
9
作為化比較試験(Randomized Controlled Trial)の文献は認められなかったが,症例報告 は 15 報について検討した(小児科,眼科疾患領域の論文は除外)。 表 2 に示す通り,宿主の免疫機能の低下に伴って発症するトキソプラズマ症の治療にク リンダマイシンは pyrimethamine との併用,pyrimethamine/sulfadiazine の合剤と併用投与 された。クリンダマイシンの投与経路は経口または点滴静注であり,投与量は 1,600~ 2,400 mg/日の分割投与であった。これらの治療により,臨床症状および頭部 CT/MRI 所見 は全般的に改善したと評価された。副作用として,皮疹,骨髄抑制が報告されている。 表 2. トキソプラズ脳炎を含む重症トキソプラズマ症の治療企 業 8~19 文献,(発 行年) 対象疾患 併用薬, 用法・用量 有効性 評価 安全性 評価 企業 8 (2009), 症例報告 トキソプラズマ脳炎,HIV 抗体陽性, 29 歳,男性(イ ンドネシア国籍) P+S の合剤(ファンシ ダールⓇ)+ C を併用 頭部 CT 所見:改善 記載なし 企業 9 (2007), 症例報告 トキソプラズマ脳炎,HIV 陽性,64 歳,男性 P+C 併用 P(po)+C:2,400 mg/ 日(iv) 病巣縮小 記載なし 企業 10 (2009), 症例報告 非 AIDS トキソプラズマ 脳炎,62 歳,男性 P+C 併用 投与期間:10 週間 頭部 MRI 所見で病 変はほぼ消失 記載なし 企業 11 (2005), 症例報告 シクロスポリン単剤投与 中に発現したトキソプラ ズマ脳炎, 44 歳,女性 S+P+C 併用 S+P (po),C:1,600 mg/ 日(iv) 加療 9 日目,頭部 MRI 所見で病変は 縮小 皮疹,骨髄 抑制 企業 12 (2005), 症例報告 トキソプラズマ感染に関 連した多発性筋炎,60 歳, 女性 P+S の合剤(ファンシ ダールⓇ)+ C を併用 解熱,その後副腎皮 質ステロイド po で 筋症状は回復 記載なし 企業 13 (1999), 症例報告 トキソプラズマ脳炎,HIV 陽性,31 歳,男性(ブラ ジル人) 3 剤併用 P +C:1,800 mg +S 併用 頭部 MRI 所見で病 変の縮小(第 16 病 日).13 ヵ月後に死 亡. 骨髄抑制, 汎血球減 少(S の中 止により 回復) 企業 14 (1997), 症例報告 トキソプラズマ脳膿瘍, HIV 陽性,35 歳,女性(タ イ人) S, P 合剤+葉酸+C:1800 mg を併用 頭痛は軽減,脳膿瘍 は軽快.C 単剤投与 は無効 骨髄抑制 (SP 合剤) 企業 15 (2006), 症例報告 トキソプラズマ脳炎,HIV 陽性,44 歳,男性 ST 合剤 (sulfamethoxazole / trimetoprim を投与した が,薬疹のため中止.C (注射剤)2,400 mg +P+Lv に変更 頭部 MRI 所見,意 識障害は改善 薬疹(ST 合剤)
10 企業 16 (2007), 症例報告 トキソプラズマ脳症, SLE*,免疫不全,39 歳, 女性 P+C 軽快傾向 記載なし 企業 17 (2006), 症例報告 脳トキソプラズマ症, AIDS S+C 視野欠損,軽度の認 知症を認めるが自 宅療養まで回復 記載なし 企業 18 (2002), 症例報告 トキソプラズマ脳症,HIV 感染,45 歳,男性(ガー ナ人) P+C 併用 麻痺は徐々に消失. 頭部 CT, MRI 所見 で病変は著明に改 善.後日,間質性肺 炎を認め,呼吸不全 のため死亡. 記載なし 企業 19 (1999), 症例報告 トキソプラズマ脳症, AIDS, 46 歳,男性 P+S+C;900 mg/日 併用 頭部 CT 所見で病変 は縮小,全身状態良 好 記載なし
P: pyrimethamine, C: クリンダマイシン, S: sulfadiazine, Lv: ロイコボリン, po: 経口投与, iv: 静注 SLE*: systemic lupus erythematosus
(2)Peer-reviewed journal の総説、メタ・アナリシス等の報告状況
1)総説:トキソプラズマ症の治療企業 -20,21 トキソプラズマの治療は 2 剤の組合せ治療が基本である。 1)pyrimethamine+sulfadiazine いずれも葉酸代謝拮抗剤であり,トキソプラズマ治療の標準治療薬である。Pyrimethamine 50~75 mg と sulfadiazine 4g 分 4 にロイコボリン 10~50 mg を加えて治療する。副作用は骨 髄抑制が最も重要であり,アレルギー反応として発熱,発疹などがみられる場合もある。 消化器症状も少なくない。 2)pyrimethamine+クリンダマイシン pyrimethamine+クリンダマイシンは pyrimethamine+sulfadiazine と同等の臨床効果が報告 されており,白血球減少の頻度が低く,HIV 感染者にも使用しやすい組合わせである。ま たクリンダマイシンが点滴投与できることも,意識障害が認められやすいトキソプラズマ 脳炎では使用しやすい理由の一つである。Pyrimethamine 50~75 mg とクリンダマイシン 600 ~800 mg を 1 日 4 回(6 時間ごと)投与する。ロイコボリンのレスキュ投与はこの場合も 必要である。副作用はやはり骨髄抑制やアレルギー反応に注意が必要で,クリンダマイシ ンは,急速点滴による血圧低下や,偽膜性腸炎の発症などに注意する必要がある。 2)メタ・アナリシス企 業-22 トキソプラズマ脳炎の治療法比較(Cochrane analysis) 評価対象は無作為化二重盲検試験であり,選択基準に適合した試験は Danneman et al 1992 および Katlama et al 1996 が実施した pyrimethamine+sulfadiazine (P+S) と11 pyrimethamine+clindamycin (P+C) との比較試験,Torre et al 1998 の pyrimethamine+sulfadiazine (P+S)と trimethoprim-sulfamethoxazole (TMP-SMX)との比較であ った。 これらのエビデンスを検討した結果,トキソプラズマ脳炎に対してどの治療法も優位性 を示すことはできなかった(各治療法間で有意差なし)。
(3)教科書等への標準的治療としての記載状況
<海外における教科書等>1)Harrison's Principles of Internal Medicine 17th
Edition 1305-11要 望5 AIDS 患者に対しては急性トキソプラズマ症の治療を優先する。免疫不全の患者におい て,未治療の場合はトキソプラズマ症で急速に死に至る。 トキソプラズマ脳炎の患者には,pyrimethamine と sulfadiazine にロイコボリンを加え た併用療法は有効である。sulfadiazine の代わりにクリンダマイシンを用いることも可能 である。
2)Mandell: Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases, 7th ed.企 業23 免疫不全患者における急性トキソプラズマ脳炎の治療指針 薬剤 用法・用量 標準治療 pyrimethamine 初日;200 mg 経口,以降 50 (<60 kg)~75 (>60 kg) mg 経口, 1 日 1 回 葉酸(ロイコボリン)* + sulfadiazine(推奨) 10~20 mg 経口, 静注, または 筋注 1 日1回 ( 50 mg まで) 1000 (<60 kg) ~1500 (>60 kg) mg 経口 6 時間毎 または クリンダマイシン 600 mg 経口または静注 (1200 mg 静注まで) 6 時間毎 *葉酸の投与量は血液像に基づき増減する。1 日あたり 50 mg まで <日本における教科書等> 1)新臨床内科学第 9 版 >> 第 10 章 感染症・寄生虫疾患 >> 原虫性疾患 >> 3.トキソ プラズマ症企 業-24 トキソプラズマ症の治療 免疫機能不全宿主の脳炎は無治療で予後絶対不良,適切な治療薬の開始により,臨床症 状は速やかに改善する。第 1 選択薬は sulfadiazine+pyrimethamine(+葉酸)であるが,サル ファ薬アレルギー患者ではクリンダマイシン+pyrimethamine が有効である。
(4)学会又は組織等の診療ガイドラインへの記載状況
<海外におけるガイドライン等>Guidelines for Prevention and Treatment of Opportunistic Infections in HIV-Infected Adults and Adolescents, Recommendations from CDC, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America. 要 望6
12 トキソプラズマ脳炎の治療 第1選択としてpyrimethamine+sulfadiazine+ロイコボリン(AI)の併用投与で治療し, この治療が無効または忍容できない場合には pyrimethamine+クリンダマイシン+ロイコ ボリン(AI)で治療する。 <日本におけるガイドライン等> 寄生虫症薬物治療の手引き – 2010- 改訂第 7.0 版,熱帯病治療薬研究班企 業25 免疫不全者では体内に潜伏感染していたトキソプラズマが再活性化し、臓器障害を引き 起こす(再燃)。例えばトキソプラズマ IgG 抗体陽性の HIV 感染者では CD4 細胞数が 100/mm3以下に低下すると、予防投与を受けていない場合、約30%の確率でトキソプラ ズマの再燃が見られる。また HIV 感染症以外で免疫不全状態にある患者が脈絡網膜炎、 肺炎、ARDS やショックを伴う多臓器障害を示すこともある。 薬剤 投与量 治療期間 トキソプ ラズマ脳 炎 (AIDS 患 者) <標準治療> pyrimethamine 初日 200mg/日,分 2,その後 50~75mg/日 症状軽快後 4~6 週 ロイコボリン 10~20mg/日(最大 50mg/日) pyrimethamine 中止後 1 週まで継続 sulfadiazine または 4.0~6.0g/日,分 4 クリンダマイシン 2,400mg/日,分 4(注射は最大 4,800mg/日)
(5)要望内容に係る本邦での臨床試験成績及び臨床使用実態(上記(1)以
外)について
1)
(6)上記の(1)から(5)を踏まえた要望の妥当性について
トキソプラズマ脳炎を含むトキソプラズマ症に対するクリンダマイシン(経口剤,注射 剤)の使用実態について,海外および国内の公表文献,教科書,ガイドライン等により調 査 し た 。 ク リ ン ダ マ イ シ ン ( 経 口 剤 , 注 射 剤 ) は , ト キ ソ プ ラ ズ マ 脳 炎 に 対 し て pyrimethamine +クリンダマイシン+ロイコボリンで併用使用,HIV 患者に高頻度でおきる サルファ剤アレルギーなど sulfadiazine が使用できない場合の代替療法として必要であ り,「未承認薬・適応外薬の要望」の記載は下記の理由により妥当であると考えられた。 <要望効能・効果について> 米国 CDC ガイドライン要 望-6および本邦 熱帯病治療薬研究班ガイドライン(寄生虫症薬 物治療の手引き企 業25)において,AIDS 患者,免疫不全の患者のトキソプラズマ症の治療 には,pyrimethamine+sulfadiazine+ロイコボリンの併用投与で治療し,この治療が無効また は忍容できない場合には pyrimethamine+クリンダマイシン+ロイコボリンで治療を推奨 している。国内外の教科書(Harrison要 望5,Mandell企 業23,新臨床内科学企 業24 )において も,同様の記載がありサルファ薬アレルギー患者ではクリンダマイシン+pyrimethamine+13 ロイコボリンの併用投与を推奨している。
文献検索の結果,無作為化比較試験等要 望1~3,企 業1~3
6 報,およびクリンダマイシン経口 剤/注射剤の Core Data Sheet に記載されている文献企 業2,4,5,6,7
5 報の論文は,AIDS 患者のト キソプラズマ脳炎を含むトキソプラズマ症の治療および再発予防にクリンダマイシン+ pyrimethamine+ロイコボリンの併用した場合の有効性と安全性を示している。本邦では, トキソプラズマ症の治療にクリンダマイシンを使用した,無作為化比較試験等は見当らな かったが,症例報告 12 報が見出されクリンダマイシンの有効性が報告されている企 業8~19。 以上のことから,要望の効能・効果は妥当であると考える。 <要望用法・用量について> ガ イ ド ラ イ ン や 教 科 書 に 記 載 さ れ て い る ト キ ソ プ ラ ズ マ 症 の ク リ ン ダ マ イ シ ン の 用 法・用量について,クリンダマイシン+pyrimethamine+ロイコボリンの併用する場合,本 邦ガイドラインでは 2,400mg/日,分 4(注射は最大 4,800mg/日)企 業 25,海外の教科書 (Mandell)では 600 mg 経口または静注(1,200 mg 静注まで)6 時間毎企 業23とされている。 外国人健康成人 9 例にクリンダマイシンリン酸エステル 600 mg を 6 時間ごとに 5 回, 25 分かけて点滴静注したときに得られた PK パラメータ平均値を用い,クリンダマイシン リン酸エステル 600 mg を 1 時間かけて点滴静注したときの血清中濃度推移を推定した。 その結果,点滴終了時に得られた最高血清中濃度(Cmax)は,8.14 µg/mL と推定され, 日本人健康成人(n=4)および日本人呼吸器疾患患者(n=3)で得られた 10.5 µg/mL およ び 8.1 µg/mL と同様であった。さらにトラフ値(投与開始後 6 時間値)は 1.22 µg/mL と推 定され,日本人健康成人および患者の平均血清中濃度(それぞれ 1.4 および 1.2 µg/mL, ただし日本人患者については投与開始後 7 時間値)と同様の値であった。したがって,ク リンダマイシンの薬物動態は日本人と外国人で同様であると考えられる。日本人における トキソプラズマ脳炎を含むトキソプラズマ症を対象とした,ピリメタミンなどとクリンダ マイシンを併用投与した無作為化比較試験の報告はない。しかし,クリンダマイシンの薬 物動態は日本人と外国人で同様であると考えられるため,外国で実施された臨床試験要 望1 ~3, 企 業1~3の結果を参考に出来ると考えられる。 また,要望されている用法・用量は,国内の別効能の承認用量の範囲であり,日本人に おける安全性は確立している。 以上のことから,要望の用法・用量は妥当であると考える。 <臨床的位置づけについて> トキソプラズマ症は,トキソプラズマ原虫 Toxoplasma gondii の寄生による感染症で, 日本人の成人の 20%に感染している。一度感染すると慢性持続感染となり,潜伏状態が 維持される。免疫能の正常な宿主では不顕性か軽度な熱性疾患を発症するが,免疫不全の 状態にある患者への感染では髄膜脳炎,心筋炎,肺炎,網脈絡膜炎などに発展することが ある。トキソプラズマ脳炎は不顕性感染していた患者が,AIDS などにより免疫抑制状態 (後天性免疫不全)に陥った際に発症する重篤な疾患である。AIDS 患者のうちトキソプ ラズマに対する抗体陽性者の 30~50%で髄膜炎や壊死性脳炎を発症するといわれている 企 業26。また,トキソプラズマ脳症は AIDS の 指標疾患である。感染症発生動向調査 IASR 2008 年 6 月によると,トキソプラズマ脳症の年別 AIDS 指標疾患発症数は 1999 年 2 人, 2001 年 9 人,2003 年 9 人,2005 年 16 人,2007 年 16 人であり,わが国では HIV 感染者, AIDS 患者の報告数はいずれも増加傾向が続いている。
14 このように,AIDS 患者やリンパ球増殖性症候群のために免疫抑制療法を受けている患 者において,血清学的に T. gondii 陽性である場合には,トキソプラズマ脳炎を発症する リスクが極めて高く,治療を行わなければ急速に致死的となるにもかかわらず,本邦では トキソプラズマ脳炎が適応症とされている薬剤はない。 国内外の教科書およびガイドラインにおいて,トキソプラズマ脳炎の治療には, pyrimethamine+sulfadiazine+ロイコボリン,または pyrimethamine+クリンダマイシン+ロイ コボリンが推奨されている。pyrimethamine+クリンダマイシン+ロイコボリンは pyrimethamine+sulfadiazine+ロイコボリンと同等の臨床効果が報告されており,クリンダマ イシンの併用投与は白血球減少の頻度が低く,HIV 感染者にも使用しやすい組み合わせ で,点滴静脈内投与もできる企 業-20ため,医療上の有用性および必要性は高いと考えられ る。しかしながら,トキソプラズマ脳炎に対するクリンダマイシン治療の臨床的位置づけ は,限られた臨床報告では明確にできないため,学会の要望と米国 CDC ガイドラインに順 守し,クリンダマイシンを第二選択薬(Sulfadiazine が使えなかった患者のみ)として 使用されることが妥当であると考える。したがって,本邦におけるトキソプラズマ脳炎罹 患者は非常に少ないため,今回の文献調査でのエビデンスの集積には限界があるが,外国 での臨床試験および使用実績を踏まえた有効性および,今まで他の疾患で使用されてきた 実績を踏まえた安全性を考慮したうえで,早急に医療の現場に提供できるように環境を整 える必要があると考えられる。
4.実施すべき試験の種類とその方法案
1)
収集された国内外のエビデンスは日本人における有効性と安全性を説明していると 考える。よって,新たな試験の実施は不要と考える。5.備考
<その他>
1)なし
6.参考文献一覧
1)学会要望書-参考文献 <海外における無作為化比較試験>;米国 CDC ガイドラインの根拠論文 要望 1 Katlama C, De Wit S, O’Doherty E, et al. Pyrimethamine-clindamycin vs.pyrimethamine-sulfadiazine as acute and long-term therapy for toxoplasmic encephalitis in patients with AIDS. Clin Infect Dis 1996;22(2):268-75.
要望 2 Dannemann B, McCutchan JA, Israelski D, et al. Treatment of toxoplasmic encephalitis in patients with AIDS. a randomized trial comparing pyrimethamine plus clindamycin to pyrimethamine plus sulfadiazine. Ann Intern Med 1992;116(1):33-43.
要望 3 Leport C, Raffi F, Matheron S, et al. Treatment of central nervous system toxoplasmosis with pyrimethamine/sulfadiazine combination in 35 patients with the acquired
immunodeficiency syndrome: efficacy of long-term continuous therapy. Am J Med 1988;84:94-100.
要望 4 Luft BJ, Hafner R, Korzun AH, et al. Toxoplasmic encephalitis in patients with the acquired immunodeficiency syndrome. N Engl J Med 1993;329(14):995-1000.
15 <海外における教科書>
要望 5 Kasper LH. 207 Toxoplasma infections. In: Harrison's Principles of Internal Medicine 17th Edition. 1305-11.
<海外におけるガイドライン>
要望 6 Kaplan JE. Benson C. Holmes KH, et al. Guidelines for prevention and treatment of opportunistic infections in HIV-infected adults and adolescents: recommendations from CDC, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America. Recommendations & Reports. 58(RR-4):1-207; quiz CE1-4, 2009 Apr 10.
2)企業-参考文献
<海外における無作為化比較試験>
企業 1 Jacobson MA, Besch CL, Child C, et al. Toxicity of clindamycin as prophylaxis for AIDS-associated toxoplasmic encephalitis. Lancet, 1992;339:333-4.
企業 2 Katlama C. Evaluation of the efficacy and safety of clindamycin plus pyrimethamine for induction and maintenance therapy of toxoplasmic encephalitis in AIDS. Eur J Clin Microbiol Infect Dis, 1991;10:189-91.
企業 3 Dannemann BR, McCutchan JA, Israelski DM, et al. Treatment of acute toxoplasmosis with intravenous clindamycin. The California Collaborative Treatment Group. Eur J Clin Microbiol Infect Dis, 1991;10:193-5.
企業 4 Danneman BR, Israelski DM, Remington JS. Treatment of Toxoplasmic Encephalitis with Intravenous Clindamycin. Arch Intern Med, 1988;148:2477-82.
企業 5 Foppa CU, Bini T, Gregis G, et al. A Retrospective Study of Primary and Maintenance Therapy of Toxoplasmic Encephalitis with Oral Clindamycin and Pyrimethamine. Eur J Clin Microbial Infect Dis, 1991;10:187-9.
企業 6 Ruf B, Pohle HD. Role of Clindamycin in the Treatment of Acute Toxoplasmosis of the Central Nervous System. Eur J Clin Microbiol Infect Dis, 1991;10:183-6.
企業 7 Rolston KVI. Treatment of Acute Toxoplasmosis with Oral Clindamycin. Eur J Clin Microbiol Infect Dis, 1991;10:181-3.
<国内における症例報告>
企業 8 加藤 博子, 安藤 哲朗, 土方 晴浩.救急外来に頭痛で初診した AIDS 関連トキソ プラズマ脳症の 1 例. Journal of Japanese Congress on Neurological Emergencies, 2009;21:76-8.
企業 9 Naito T, Kudo N, Hattori M, et al. Toxoplasma Encephalitis in a HIV-infected Patient. Gen Med, 2007;8:29-30. 企業 10 加藤 哲朗, 佐藤 文哉, 坂本 光男, 他. ステロイド投与中の慢性腎不全患者に発 症し,サイトメガロウイルス網膜炎を併発した非 AIDS トキソプラズマ脳炎の 1 例. 感染症学雑誌, 2009;83(5):534-7. 企業 11 中村 正史,永井 真貴子,志賀 裕正,他.ベーチェット病に対するシクロスポ リン単剤投与中にトキソプラズマ脳炎を合併した 1 例.臨床神経学,2005;45 (2) :105 -10.
16
企業 12 朝山 真哉, 中村 聖香, 三宅 浩介, 他.トキソプラズマ感染症との関連が疑われ た多発性筋炎の一例. 臨床神経学, 2005;45(2):188.
企業 13 内海 英貴, 磯田 淳 , 登田 久子, 他. トキソプラズマ脳炎を初発症状として発 症した AIDS の 1 例. Kitakanto Med J, 1999;49(2):127-30.
企業 14 小河原 一恵, 片山 薫, 朝比奈 正人, 他. AIDS 関連トキソプラズマ脳腫瘍の治 療経験. 第 15 回日本神経治療学会総会(1997.6), 71. 企業 15 前田 卓哉. トキソプラズマ症. 化学療法の領域, 2006;22(8):1244-8. 企業 16 稲次 洋平, 鈴木 秀和, 西郷 和真,他. SLE 患者が, 微細な神経症状を来たし画像 上は著明な脳浮腫病変が散在したトキソプラズマ脳症の 1 例. Neuroinfection, 2007;12(2):190. 企業 17 三木 淳, 腰原 啓史, 田畑 賢一, 他. 脳腫瘍が疑われて病理組織診断により診断 された脳トキソプラズマ症の 1 例. 新潟医学会雑誌,2006;120(12):705. 企業 18 大田 黒滋, 古庄 憲浩, 鍋島 茂樹, 他.トキソプラズマ脳症を発症し,経過中,播種 性ヒストプラズマ症を合併した後天性免疫不全症候群の一例. 感染症学雑誌, 2002; 76(臨増):142. 企業 19 堀部 尚弘, 高橋 隆, 遠藤 一博, 他. AIDS に併発したトキソプラズマ脳症に対し pyrimethamine, sulfadiazine, clindamycin 併用療法が著効した一例. 感染症学雑誌, 1999; 73(臨増):90.
<Peer-reviewed journal の総説、メタ・アナリシス等>
企業 20 安岡 彰, 岡 慎一. 日和見感染症の治療. 臨床と微生物, 1997;24 (Suppl.):641-8. 企業 21 味澤 篤.トキソプラズマ症. 日本エイズ学会誌, 2004:6(1):22-23.
企業 22 Dedicoat M, Livesley N. Management of toxoplasmic encephalitis inHIV-infected adults (with an emphasis on resource-poor settings). Cochrane Database of Systematic Reviews 2006, Issue 3. Art. No.: CD005420. DOI: 10.1002/14651858.CD005420.pub2.
<教科書等への標準的治療>
企業 23 Montoya JG, Boothroyd JC, Kovacs JA. 279 Toxoplasma gondii. In: Mandell: Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases, 7th ed. 3495-526. 企業 24 増田 剛太. 第 10 章 感染症・寄生虫疾患, 原虫性疾患 3.トキソプラズマ症. In: 高 久 史麿, 尾形 悦郎, 黒川 清, 矢崎 義雄(監修). 新臨床内科学第 9 版.医学書 院. <国内におけるガイドライン> 企業 25 中村 ふくみ.熱帯病治療薬研究班. 1.原虫症 9.トキソプラズマ症. 寄生虫治療 の手引き- 2010- 改訂第 7.0 版,2010:25-8. <その他> 企業 26 大前 比呂思,遠藤 卓郎.原虫・寄生虫類を原因とする急性脳炎.Infectious Agents Suveillance Report, 2007, 28: 345-6. http://idsc.nih.go.jp/iasr/28/334/dj3344.html