研究報告
新規腎機能マーカーのシスタチン C を応用した硫酸アルベカシンの Therapeutic drug monitoring に関する臨床薬学的研究
大塚 尚
【目 的】
腎機能の指標には腎糸球体濾過量(glomerular filtration rate: GFR)が用いられ
る。GFR は一定時間に糸球体を濾過される量であり GFR は ml/min で表される。 これは言い換えると単位時間当たりに排泄される薬物量を血漿量に換算したも のとなる。すなわち 1 分間にその量の血漿に含まれる薬剤が完全に除去される ことを表す。このように腎排泄型の薬剤はそのクリアランスが腎機能に依存す るため、腎機能に応じた適切な薬物投与設計には GFR の把握が必要となる。 通常、GFR の推定法としては、血清クレアチニン値から算出する Cockcroft and Gault 式が汎用されてきた。しかし、血清クレアチニン値は、主に筋組織 で産生されるために年齢や性差の影響を受け、さらに一部は尿細管分泌を受け るため、高齢者や軽中程度の腎機能障害者に対し腎機能を適切に評価できない
問題が挙げられる。また、Cockcroft and Gault 式は外国人母集団であることや、
現在日本で血清クレアチニン値の測定法の主流である酵素法ではなく、jaffe 法 で血清クレアチニン値が測定されていることなども問題である。近年日本腎臓
学会は酵素法を用いて計測された血清クレアチニン値と日本人母集団とを用い
て GFR の推定式を報告している(eGFR 式)。この式は非常に優れた式であり、 日常診療でも簡便に使用できるが、クレアチニン依存の式であり、高齢者で寝
たきりの患者などは正確に腎機能を評価することはこの式をもってしても難し い。 一方で、近年腎機能の指標として内因性腎機能マーカーであるシスタチン C の評価法が開発され、2005 年 10 月より新しく保険適応が認められた。シスタ チン C は、クレアチニンとは異なり血液中からの排出が完全に糸球体濾過に依 存するため、糖尿病性腎症や高血圧性腎症などの早期腎機能障害の優れた診断 マーカーとして臨床でもその有用性が証明されている。血清クレアチニン値は、 濃度が GFR < 40 mL/min/1.73m2程度まで低下しないと上昇しないのに対して、 血清シスタチン C 濃度は GFR が 70 mL/min/1.73m2程度まで低下すると上昇す るため、早期の腎機能マーカーとして有用であることが報告されている。また、 近年のメタ解析により、シスタチン C はクレアチニンと比較して腎機能の指標 として優れていることが証明されている。 シスタチン C は 122 のアミノ酸からなる 13kDa の低分子蛋白で、cysteine
protease inhibitor のひとつである。全身の有核細胞に発現しており、house-keeping
gene をコードしているため、炎症などの細胞外の影響を受けにくく、年齢によ らず産生量も一定である。また、細胞外に分泌されたシスタチン C は血中の蛋 白と結合せず、free 体として存在しており、糸球体で濾過される。濾過後はほ とんどが近位尿細管で再吸収され、アミノ酸に分解されるため、血中には戻ら ない。このため、シスタチン C の血中濃度は GFR に依存している。したがっ て、シスタチンCはクレアチニンと比較して性差や年齢の影響を受けにくい。 今後は、さらに TDM や薬物投与設計の領域においてもその応用とエビデンス の構築が望まれている。事実、近年になりシスタチン C の投与設計への適応の
エビデンスが蓄積されてきている。最近種々の研究において、血清シスタチン C 値から GFR を推定し、ジゴキシン、トポテカン、カルボプラチン、アミカシ ン、バンコマイシンなどの薬剤の投与設計における臨床上の有効性の報告も成 されている。一方で、尿細管分泌を受ける薬剤ではクレアチニンの方が予測精 度が高いとの報告もあり、尿細管分泌の影響が大きい薬剤ではシスタチン C の 有用性は明確になってない。 治療効果と安全性のさらなる向上を望むには、投与前段階から薬物投与設計 を行う初回投与設計が必要となり、またその精度向上が重要となる。初回投与 法の推定方法としては、様々なノモグラムや population mean 法が応用され、同 じ抗 MRSA 薬である塩酸バンコマイシン(VCM)では簡便なノモグラムの報 告も多い。一方、硫酸アルベカシンではこれまでノモグラムの報告はなく、
1-compartment model 解析手法である Sawchuk-Zaske 法を用い、その解析結果に
よる経験的投与設計が行われてきたが、population dynamics 理論が一般的にな るにつれ、population mean 法が広く用いられるようになった。しかし、VCM 初 回投与法の血中濃度の予測精度を評価した報告がいくつかなされているが、 population mean 法を用いた硫酸アルベカシン初回投与設計の予測精度に関する 報告はほとんどみられない。さらにこれまでシスタチン C を腎排泄型薬剤の硫 酸アルベカシンの初回投与設計に応用した報告はない。また血清シスタチン C 値による GFR 推定式は複数報告がある。 そこで、本研究では、新規腎機能マーカーのシスタチン C による GFR 推算 式を応用したアルベカシン初回投与設計に関する臨床薬学的研究を行った。 【方法・結果】
糖尿性腎症や高血圧性腎症などの早期腎機能障害に対して優れた新規診断マ ーカーであるシスタチン C に注目し、この新規腎機能評価物質を糸球体濾過率 (GFR)の指標として硫酸アルベカシン動態解析に組み込み、至適初回投与設計 法の確立を検討した。対象患者は松山市民病院および愛媛大学医学部附属病院 にて、MRSA 感染症で硫酸アルベカシンが投与され TDM が施行された患者 95 名とした。血清検体は、定常状態到達後と推定される投与開始から 3 日以上経 過した後に、peak 値(Cmax)と trough 値の 2 ポイントで採血し、血清 ABK 濃 度と血清シスタチン C 値を測定した。そして血清クレアチニン値
(Cockcroft-Gault equation) と血清シスタチン C 値から推定された GFR に基づ
いた population mean 法を用い、血清アルベカシン濃度の予測精度を評価した。 血清シスタチン C 値からの GFR 推定には、Hoek、Grubb’s および Sjöström 式 を用いた。なお、population mean 法による予測の偏りおよび正確性は、Sheiner らの方法を用いて mean prediction error (ME)、the mean absolute error (MAE)、 そして the root mean squared prediction error (RMSE)を計算することで評価 した。ME、MAE および RMSE がより小さければ、偏りが小さく、より正確 な結果を示す。ME、MAE および RMSE の各 95% C.I.が”0”を含まない場合は 予測性能に有意差があると判定した。 ME = 1/n (予測値–計算値) MAE = 1/n |予測値–計算値| RMSE = [1/n (予測値–計算値) 2]1/2
Σ
i=1nΣ
i=1nΣ
i=1nΣ
i=1nΣ
i=1nΣ
i=1nCockcroft and Gault 式: クレアチニンクリアランス (CLcr, mL/min) = (140 - 年齢 (years)) × 体重 (kg) / ( 72 ×[血清クレアチニン] (mg/dL) ) × (0.85) [女性] Hoek 式: GFR (mL/min/1.73m2) = -4.32 + 80.35 / [血清シスタチン C] (mg/L) Sjöström 式: GFR (mL/min/1.73m2) =124 / [血清シスタチン C] (mg/L) – 22.3 Grubb 式: GFR (mL/min/1.73m2) = 86.49 × [血清シスタチン C] -1.686 (mg/L) × (0.948) [女性] GFR 値は ml/min/1.73m2 で表記されているため、Dubois-Dubois 式により算出 した BSA により補正した。 Dubois-Dubois 式: BSA (m2) = 0.007184 × 身長(cm)0.725 × 体重(kg)0.425 Hoek、Grubb 及び Sjöström 式を用いて初回投与設計を行った場合の血中ア ルベカシン濃度の予測性を比較検討した結果、GFR の推定にシスタチン C を 用いた場合には、いずれの推定式においてもクレアチニンと比較して peak 値 ならびに trough 値において血中 ABK 濃度の予測性(ME、MAE)が向上したが、
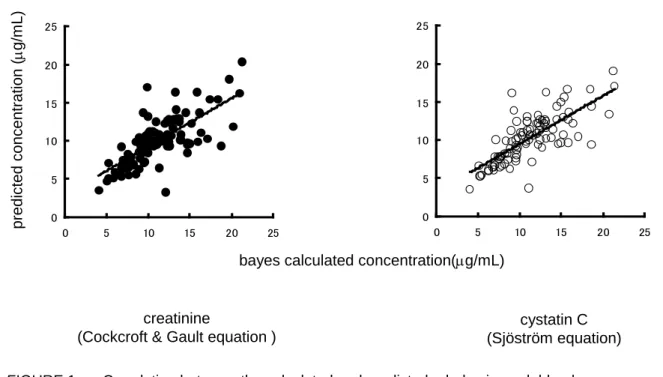
Sjöström 式のみが有意差を持って予測精度が向上していた(ΔMAE)。
FIGURE 1. Correlation between the calculated and predicted arbekacin peak blood
concentrations using the estimated GFR based on the creatinine and cystatin C concentrations.
The GFR values were estimated based on the serum creatinine (Cockcroft-Gault equation) and cystatin C (Sjöström equation) concentrations (n=95). Closed circles: creatinine, y = 0.63x + 2.92 (r2=0.53, P<0.0001), Open circle:
0 5 10 15 20 25 0 5 10 15 20 25 p re d ic te d c on c e n tra ti o n ( µg /mL ) 0 5 10 15 20 25 0 5 10 15 20 25 creatinine
(Cockcroft & Gault equation )
cystatin C (Sjöström equation) bayes calculated concentration(µg/mL)
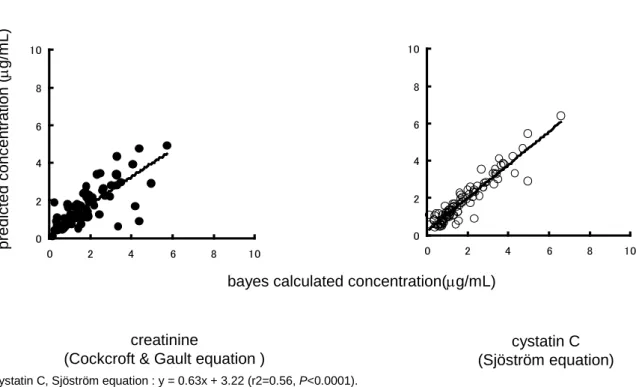
cystatin C, Sjöström equation : y = 0.63x + 3.22 (r2=0.56, P<0.0001).
FIGURE 2. Correlation between the calculated and predicted arbekacin trough blood
concentrations using the estimated GFR based on the creatinine and cystatin C concentrations.
The GFR values were estimated based on the serum creatinine (Cockcroft-Gault equation) and cystatin C (Sjöström, Hoek and Grubb equation) concentrations (n=95). Closed circles: creatinine, y=0.72x + 0.38 (r2=0.64, P<0.0001), Open circle: cystatin C, Sjöström equation : y=0.88x + 0.25 (r2=0.89, P<0.0001).
0 2 4 6 8 10 0 2 4 6 8 10 0 2 4 6 8 10 0 2 4 6 8 10 p re d ic te d c on c e n tra ti o n ( µg /mL ) creatinine
(Cockcroft & Gault equation )
cystatin C (Sjöström equation) bayes calculated concentration(µg/mL)
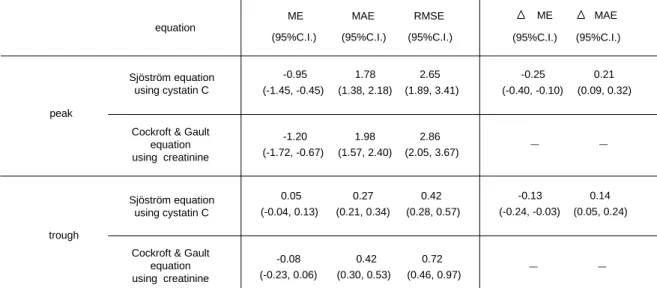
TABLE 1. The bias and accurate of prediction and predictability the peak and trough blood concentrations of arbekacin based on the estimated GFR using the creatinine and cystatin C concentrations.
The GFR values were estimated based on the serum creatinine (Cockcroft-Gault equation) and cystatin C (Sjöström equation) concentrations (n=95). ME:mean prediction error, MAE: mean absolute error, RMSE: root mean squared prediction error, 95% C.I.: 95% confidence interval. ΔME:ME of creatinine - ME of cystatin C, ΔMAE: MAE of creatinine - MAE of cystatin C.
ME MAE RMSE
(95%C.I.) (95%C.I.) (95%C.I.)
Sjöström equation using cystatin C
-0.95 1.78 2.65
(-1.45, -0.45) (1.38, 2.18) (1.89, 3.41)
Cockroft & Gault equation using creatinine equation -1.20 1.98 2.86 (-1.72, -0.67) (1.57, 2.40) (2.05, 3.67) Δ ME Δ MAE (95%C.I.) (95%C.I.) -0.25 0.21 (-0.40, -0.10) (0.09, 0.32) - - 0.05 0.27 0.42 (-0.04, 0.13) (0.21, 0.34) (0.28, 0.57) -0.08 0.42 0.72 (-0.23, 0.06) (0.30, 0.53) (0.46, 0.97) Sjöström equation using cystatin C
Cockroft & Gault equation using creatinine -0.13 0.14 (-0.24, -0.03) (0.05, 0.24) - - peak trough
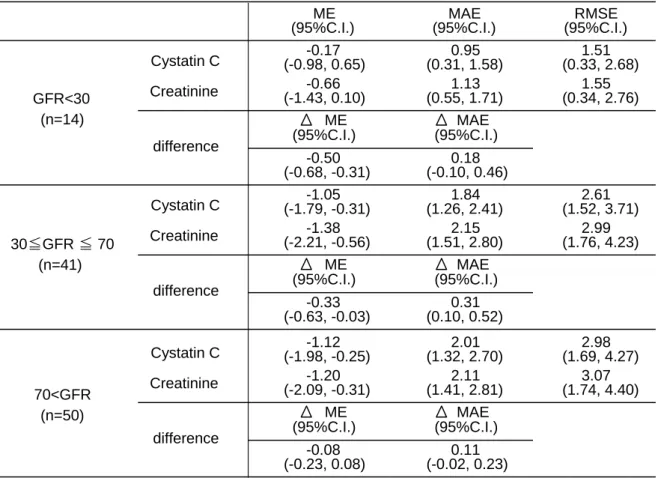
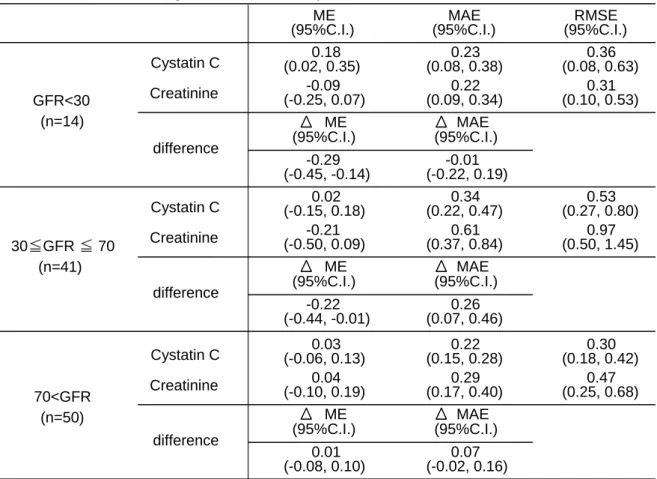
続いて 3 つの患者群(通常~軽度腎障害(GFR > 70 mL/min)、中程度腎障害(30 ≦ GFR ≦ 70 mL/min)、重度腎障害(GFR < 30 mL/min))に分けての検討を行 った。その結果、各群における血清アルベカシン濃度の予測性能の比較結果は、 peak 、trough 濃度ともに中程度腎障害においてクレアチニンでは予測値が負 に傾いていたが(ME)、シスタチン C ではその傾きが有意に改善された(ΔMA)。 また、予測の正確性の指標となるΔMAE も有意に小さい値を示しており、シス タチン C を用いることで予測精度が有意に向上した。しかしながら、通常~軽 度と重度腎障害患者群においては予測の正確性の有意な向上は認められなかっ た。(Table2,3)
TABLE 2. The relative predictive efficacy of the arbekacin peak blood concentrations based on the estimated GFR using the creatinine and cystatin C concentrations.
ME:mean prediction error, MAE: mean absolute error, RMSE: root mean squared prediction error, 95% C.I.: 95% confidence interval . ΔME: ME of creatinine - ME of cystatin C, ΔMAE: MAE of creatinine - MAE of cystatin C.
Cystatin C Creatinine
Δ ME Δ MAE difference (95%C.I.) (95%C.I.) GFR<30
30≦GFR ≦ 70
70<GFR
ME MAE RMSE
(95%C.I.) (95%C.I.) (95%C.I.) -0.17 (-0.98, 0.65) -0.66 (-1.43, 0.10) -0.50 (-0.68, -0.31) (n=14) (n=41) (n=50) 0.95 (0.31, 1.58) 1.13 (0.55, 1.71) 0.18 (-0.10, 0.46) 1.51 (0.33, 2.68) 1.55 (0.34, 2.76) Cystatin C Creatinine Δ ME Δ MAE difference (95%C.I.) (95%C.I.)
-1.05 (-1.79, -0.31) -1.38 (-2.21, -0.56) -0.33 (-0.63, -0.03) 1.84 (1.26, 2.41) 2.15 (1.51, 2.80) 0.31 (0.10, 0.52) 2.61 (1.52, 3.71) 2.99 (1.76, 4.23) Cystatin C Creatinine Δ ME Δ MAE difference (95%C.I.) (95%C.I.)
-1.12 (-1.98, -0.25) -1.20 (-2.09, -0.31) -0.08 (-0.23, 0.08) 2.01 (1.32, 2.70) 2.11 (1.41, 2.81) 0.11 (-0.02, 0.23) 2.98 (1.69, 4.27) 3.07 (1.74, 4.40)
TABLE 3. The relative predictive efficacy of the arbekacin trough blood concentrations based on the estimated GFR using the creatinine and cystatin C concentrations.
ME:mean prediction error, MAE: mean absolute error, RMSE: root mean squared prediction error, 95% C.I.: 95% confidence interval . ΔME: ME of creatinine - ME of cystatin C, ΔMAE: MAE of creatinine - MAE of cystatin C.
Cystatin C Creatinine
Δ ME Δ MAE difference (95%C.I.) (95%C.I.) GFR<30
30≦GFR ≦ 70
70<GFR
ME MAE RMSE
(95%C.I.) (95%C.I.) (95%C.I.) 0.18 (0.02, 0.35) -0.09 (-0.25, 0.07) -0.29 (-0.45, -0.14) (n=14) (n=41) (n=50) 0.23 (0.08, 0.38) 0.22 (0.09, 0.34) -0.01 (-0.22, 0.19) 0.36 (0.08, 0.63) 0.31 (0.10, 0.53) Cystatin C Creatinine Δ ME Δ MAE difference (95%C.I.) (95%C.I.)
0.02 (-0.15, 0.18) -0.21 (-0.50, 0.09) -0.22 (-0.44, -0.01) 0.34 (0.22, 0.47) 0.61 (0.37, 0.84) 0.26 (0.07, 0.46) 0.53 (0.27, 0.80) 0.97 (0.50, 1.45) Cystatin C Creatinine Δ ME Δ MAE difference (95%C.I.) (95%C.I.)
0.03 (-0.06, 0.13) 0.04 (-0.10, 0.19) 0.01 (-0.08, 0.10) 0.22 (0.15, 0.28) 0.29 (0.17, 0.40) 0.07 (-0.02, 0.16) 0.30 (0.18, 0.42) 0.47 (0.25, 0.68)
【考 察】 硫酸アルベカシンは濃度依存的に殺菌作用を示し、副作用である腎障害は能動 的な尿細管上皮細胞への取り込みの機序によるため、臨床において硫酸アルベ カシンを適切に使用するためには TDM を用いて患者個々の治療を実践するこ とが必要となる。さらに、治療効果と安全性を高めるには、投与前段階から薬 物投与設計を行う初回投与設計の精度向上が重要となる。また、硫酸アルベカ シンは分布容積が約 20%と水溶性が高く、腎排泄型の薬剤であることから、適 切な投与設計を行う上で高齢患者や軽度腎機能障害患者の腎機能の正確な評価 が重要となる。そこでそれらの患者群において、非常に感度が優れた GFR マ ーカーであることが示されているシスタチン C の ABK 初回投与設計への応用 を検討した。シスタチン C の血清アルベカシン濃度の予測精度 (ΔMAE)は peak 、trough 値ともに優れている傾向にあったが、唯一シスタチン C を用い た GFR 推定式の中でも Sjöström 式のみが有意差を持って peak、trough 値と もに予測精度が優れていた。更に、通常~軽度(GFR > 70 mL/min)、中程度(30 ≦ GFR ≦ 70 mL/min)および重度腎障害患者(GFR < 30 mL/min)群間におい て血清アルベカシン濃度の予測可能性を比較した結果、血清シスタチン C 値に 基づいた予測の偏り(ME)は、中程度および重度腎障害患者において、血清クレ アチニン値の予測よりも特に小さいことが示された。加えて血清シスタチン C 値を用いた予測の正確性(MAE)は、中程度腎障害患者において、血清クレアチ ニン値を用いたものよりも特に優れていた。これは、シスタチン C がクレアチ ニンと比較し、中程度腎障害患者において硫酸アルベカシンの初回投与設計の より精度の高い指標となることを示している。
【結 論】 以上の研究の結果より、今回我々はシスタチン C を用いたアルベカシン初回 投与設計法の有用性を立証した。また我々は、同じ抗 MRSA 薬であり腎排泄型 薬剤でもあるバンコマイシンの投与設計においてもシスタチン C の有用性を立 証しており、今後は他の種々の腎排泄型薬剤の薬剤投与設計に臨床応用展開す ることでより薬剤の適正使用に寄与できるものと思われる。 【追 記】 CKD 診療ガイド 2012(日本腎臓学会編)において日本人母集団を用いたシ スタチン C による GFR 推算式が報告された。
男性:eGFRcys(ml/min/1.73m2)=(104×Cys-C-1.019×0.996年齢(歳))-8
女性:eGFRcys(ml/min/1.73m2)=(104×Cys-C-1.019×0.996年齢(歳)×0.929)-8
※18 歳以上、国際的な標準物質に基づく測定値を用いる。
今後日本人母集団を用いたシスタチン C による GFR 推算式を用いて、TDM や薬物投与設計の領域への応用とエビデンスの構築が望まれる。