Sofia Influenza A+B FIA 1 / 32ページ Sofia および Sofia 2 でご使用ください。 CLIA 複雑度: 直接鼻スワブ、鼻咽頭スワブ、および鼻咽頭吸引/洗 浄検体については waived(免除) CLIA 複雑度: 輸送用培地に溶出した鼻咽頭スワブおよび鼻咽頭吸 引/洗浄検体については Moderate(中等度) 体外診断用
本テストをCLIA waivedの設定で実施する場合は、Certificate of Waiver(免除の証明書)が必要です。本テスト はまた、複雑度がmoderate(中等度)とhigh(高度)の検査を実施する検査機関によっても使用することができます。 Certificate of Waiver(免除の証明書)を取得するには、州の保健局にご連絡ください。CLIA waiverに関する詳細情 報は、メディケア・メディケイドサービスセンターのウェブサイト(www.cms.hhs.gov/CLIA)または州の保健局から入手でき ます。
指示に従わなかったり、本テストシステムの指示に修正を加えると、テストがwaivedの分類の要求基準を満たさない結 果となります。
使用目的
Sofia Influenza A +B FIA は、免疫蛍光法を用いて、症状のある患者の鼻拭い液、鼻咽頭拭い液、鼻咽頭 吸引物/洗浄液の新鮮または輸送検体液中のインフルエンザ A 型およびインフルエンザ B 型ウイルス 核タンパク抗原を検出します。この定性検査は、急性 A 型インフルエンザと B 型インフルエンザによ るウイルス感染の迅速鑑別診断の補助としての使用を目的とします。本テストは、C 型インフルエン ザ抗原の検出用ではありません。陰性の検査結果は推定であるため、ウイルス培養または FDA 認可 A 型および B 型インフルエンザ分子アッセイによって結果を確認することが推奨されます。陰性結果は、 インフルエンザウイルスの感染を除外するものではなく、治療やその他の管理に関する決断のための 唯一の根拠として使用するべきではありません。本テストは、専門家による検査室での使用向けです。 Sofia Influenza A+B FIAは、SofiaまたはSofia 2で使用できます。
A型およびB型インフルエンザに対するパーフォーマンス特性は、「アップデート:インフルエンザの活動状態--米国、 2010~2011シーズン、および2011~2012インフルエンザワクチンの組成」と題するCDCからの罹患率と死亡率週報に基 づき、A型インフルエンザウイルス/California/7/2009(2009 H1N1)、A型インフルエンザウイルス/Perth/16/2009 (H3N2)、 およびB型インフルエンザウイルス/Brisbane/60/2008(ビクトリア系統) が流行中の最も優勢なインフルエンザウイルスであ った、2011年の2月から3月の間に立証されました。 パーフォーマンス特性は、新たに出現するその他のウイルスに対しては ばらつきがあります。 公衆衛生当局により推奨される現行の臨床ならびに疫学的スクリーニング基準に基づき、新型インフルエンザウイルス による感染が疑われる場合は、新型病原性インフルエンザウイルスに対する適切な感染予防措置を講じて検体を採 取して、検査のために州または地元の衛生局に送付してください。 検体を受領し、培養するBSL 3+施設が利用でき ない限り、このような症例では、ウイルスの培養を試みないでください。
Sofia Influenza A+B FIA 2 / 32ページ
概要と説明
インフルエンザウイルスは、極めて感染性の高い、気道の急性ウイルス性感染症の原因病原体です。 インフルエンザウイルスは、免疫学的に多様な、1本鎖RNAウイルスです。インフルエンザウイルスには、A型、B型、C型 の3つのタイプがあります。 A型ウイルスは、最も一般的で、最も重篤な流行に関連しています。B型ウイルスによる病状 は、一般的にA型よりも軽症です。C型ウイルスは、ヒトでは大きな流行と関連したことはかつてありません。A型とB型ウ イルスの両方が同時に流行する可能性はありますが、通常は特定のシーズン中では1つの型が優勢です。1 米国では毎年、平均して人口の5~20%がインフルエンザを罹患します。インフルエンザの合併症のために入院する人 は20万人を超え、約3万6千人がインフルエンザに関連する原因で死亡しています。年齢が65歳以上の成人、幼い小 児、そして特定の健康状態を有する人など、人によっては、インフルエンザによる重篤な合併症を生じるリスクが高くな ります。2テストの原理
Sofia Influenza A+B FIAは、Sofiaと Sofia 2で使用される免疫蛍光技術によって、インフルエンザウイルスの核タンパク 質を検出します。本テストでは、A型インフルエンザとB型インフルエンザの抗原の鑑別検出が可能です。
患者検体を試薬チューブに入れると、この間に検体中のウイルス粒子が破壊されて、内部のウイルス核タンパク質が 露出します。破壊後、検体をテストカセットの検体ウェル中に分注します。検体は、検体ウェルから、様々な独特の化 学的な環境を含むテストストリップを通って移動します。インフルエンザのウイルス抗原が存在していると、検体が特定 の場所にトラップされます。
注: ユーザーの選択に応じて、テストカセットは、自動時間測定(WALK AWAYモード)のためにSofia またはSofia 2の 内部に入れるか、あるいは手動時間測定(READ NOWモード)のためにカウンターかベンチトップの上に静置してから、 Sofia またはSofia 2中に入れてスキャンします。 Sofia とSofia 2は、テストストリップをスキャンして、メソッド固有のアルゴリズムを使用して結果を処理することにより、 蛍光シグナルを測定します。Sofia とSofia 2は、画面にテスト結果(陽性、陰性、または無効)を表示します。
キットに同梱の試薬と資材
25-
テストキット:
個別包装されたテストカセット (25 個): マウスモノクローナル抗 A 型インフルエンザ抗体および抗 B 型インフルエン ザ抗体 試薬チューブ(25 本): 界面活性剤と還元剤を含む凍結乾燥バッファー 試薬液(25 本): 食塩水入りアンプル 滅菌鼻スワブ(25 本) 小型で透明の 120 µL 容量固定ピペット(25 本) 大型でピンク色の 250 µL 容量固定ピペット(25 本) A 型インフルエンザおよび B 型インフルエンザ陽性コントロールスワブ(1 本): スワブは、非感染性組換え A 型イン フルエンザと B 型インフルエンザ抗原でコートされています。 陰性コントロールスワブ(1 本): スワブは、熱不活性化された、非感染性 Streptococcus C(ストレプトコッカス・コンス テラータス)抗原でコートされています。 添付文書(1 部) クイック・リファレンスガイド(1 部) QC カード(キットボックスに同梱) プリンター用紙(1 枚)
Sofia Influenza A+B FIA 3 / 32ページ
キットに同梱されていない資材
タイマーまたは腕時計 Sofia または Sofia 2 検体容器 検体採取用滅菌生理食塩水 鼻咽頭吸引物または鼻咽頭洗浄液採取用装置 ナイロンフロック加工(植毛加工)鼻咽頭スワブ キャリブレーションカセット(Sofia インストールパッケージまたは Sofia 2 に同梱)警告および使用上の注意
体外診断用 ボックス外側に印刷されている使用期限を過ぎたキット内容物は使用しないでください。 患者検体と使用済みキット内容物の採取/回収、取り扱い、保管、ならびに廃棄には適切な予防措置を講じて ください。3 患者検体の取り扱い時には、ニトリル、ラテックス(またはこれに相当する)手袋の使用を推奨します。3 使用済みのテストカセット、容量固定ピペット、試薬チューブ、溶液、またはコントロールスワブを再使用してはなり ません。 テストカセットをすぐに使用するための準備が整うまでは、絶対にテストカセットのホイルパウチを開封して、周囲環 境に曝してはなりません。 破損した、または落としたテストカセットや資材は、使用しないで、廃棄してください。 試薬液は、食塩水(生理食塩水)を含んでいます。試薬液が皮膚や眼に接触した場合は、大量の水で洗い流 してください。 正確な結果を得るためには、添付文書に記載の指示に必ず従ってください。 キャリブレーションカセットは、使用していないときは、保管用パウチ(備品)に入れて保管してください。 検体の採取、保管、輸送が不十分または不適切な場合は、誤った検査結果が生じる可能性があります。 検体採取と取り扱い手順は、特別のトレーニングとガイダンスを必要とします。 正確な結果を得るためには、本添付文書で推奨するウイルス輸送用培地(VTM)を使用してください。 鼻スワブ検体を採取する際には、本キットに同梱の鼻スワブを使用してください。 鼻咽頭スワブ検体を採取する際には、ナイロンフロック加工(植毛加工)鼻咽頭スワブを使用してください。 テストの手順に従って、適切な容量固定ピペットを使用してください: すべての検体タイプについて、患者検体をテストカセットに加えるためには、小型で透明の 120 µL 容量固定ピ ペットのみを使用してください。 吸引物/洗浄またはウイルス輸送用培地のテスト手順で、患者検体を検体採取容器から試薬チューブに移 す際には、大型でピンク色の 250 µL 容量固定ピペットのみを使用してください。 試薬チューブからテストカセットの検体ウェル中に直に検体を注いではなりません。テストカセットに検体を加える際 には、小型で透明の 120 µL 容量固定ピペット(備品)を使用してください。 正確な結果を得るためには、血液が混じっていたり、過度に粘り気のあることがはっきり目視できる検体を使用し てはなりません。 テストカセットのバーコードの上に書き込まないでください。このバーコードは、実行されているテストのタイプを識別す るために Sofia と Sofia 2 によって使用され、同じ Sofia または Sofia 2 によるテストカセットの 2 回目の読み出しを 防ぐために、個々のテストカセットを識別します。 公衆衛生当局により推奨される現行の臨床ならびに疫学的スクリーニング基準に基づき、新型の A 型インフルエ ンザウイルスによる感染が疑われる場合は、新型病原性インフルエンザウイルスに対する適切な感染予防策を講 じて検体を採取して、検査のために州または地元の衛生局に送付してください。検体を受領し、培養する BSL 3+ 施設が利用できない限り、このような症例では、ウイルスの培養を試みないでください。
Sofia Influenza A+B FIA 4 / 32ページ 本テストは、鳥インフルエンザ A 型サブタイプ H5N1 ウイルスを含む培養鳥インフルエンザウイルスを検出することが 示されていますが、H5N1 やその他の鳥インフルエンザウイルスに感染した人からの検体についての本テストのパーフ ォーマンス特性は分かっていません。 検出用の試薬は蛍光化合物であるため、テストストリップの上に目視できる結果は生じません。結果の判読には、 Sofia または Sofia 2 を使用しなければなりません。 正確な結果を得るためには、開封してむきだしになっているテストカセットは、ラミナーフローフードの中や強く換気さ れている場所では使用しないでください。 テストは、適度に換気されている場所で行ってください。 容器や未使用の内容物は、連邦、州、および地域の規制基準に従って廃棄してください。 本キットの内容物を取り扱う際には、適切な保護衣、保護手袋、保護眼鏡、保護面を着用してください。 取り扱い後は、よく手を洗ってください。 ハザードシンボル、本キットに同梱のコンポーネントに関する安全性、取り扱いおよび廃棄に関する追加情報につ いては、quidel.com に掲載されている安全性データシート(SDS)をご参照ください。
キットの保管と安定性
本キットは、直射日光を避け、室温 [15°C~30°C(59°F~86°F)] で保管してください。キットの内容物は、外側ボック スに印刷されている使用期限までは安定です。凍結しないでください。品質管理
SofiaまたはSofia 2ならびにテストカセットには、3つのタイプの品質管理があります: Sofiaキャリブレーションチェック手順、 内蔵式プロシージャーコントロール、外部コントロール。
Sofia
キャリブレーションチェック
注: これは「キャリブレーションチェック」の手順です。 キャリブレーションチェック手順は、30日ごとに実施する必要があります。Sofiaでは、ユーザーにキャリブレーションチェック 手順の完了を促すリマインダーを設定できます。 キャリブレーションチェックは、特定のキャリブレーションカセットを使用して、Sofiaの光学と計算システムを点検する必須 機能です。このキャリブレーションカセットはSofiaインストールパッケージに同梱されています。キャリブレーションチェック手 順に関する詳細は、Sofiaユーザーマニュアルを参照してください。 重要: 光への曝露から保護するため、使用していないときは、キャリブレーションカセットは、必ず保管用パウチ(備品) に入れて保管してください。 1. Sofia のキャリブレーションをチェックするには、メインメニューから キャリブレーションを選びます。 2. メッセージが表示されたら、Sofia にキャリブレーションカセットを 入れてから、引き出しを閉じます。Sofia は、2 分以内に、自 動的にキャリブレーションチェックを実行します。ユーザーは何も 入力する必要はありません。Sofia Influenza A+B FIA 5 / 32ページ Sofiaは、いつキャリブレーションチェックが完了したかを表示します。OKを押して、メインメニューに戻ります。 注: キャリブレーションチェックに合格しなかった場合は、施設監督者に通知するか、あるいはQuidelのテクニカルサポー トにご連絡ください。月曜日~金曜日、午前7時~午後5時(太平洋標準時)、電話:800.874.1517(米国内) 858.552.1100(米国以外)、ファックス:858.455.4960、カスタマサービス:[email protected]、テクニカルサ ポート: [email protected]、または最寄りの代理店までご連絡ください。
Sofia 2 キャリブレーションチェック
キャリブレーションチェック手順は、30日ごとに実施する必要があります。Sofia 2では、ユーザーにキャリブレーションチェッ ク手順の完了を促すリマインダーを設定できます。 キャリブレーションチェックは、特定のキャリブレーションカセットを使用して、Sofia 2の光学と計算システムを点検する必 須機能です。このキャリブレーションカセットは、Sofia 2に同梱されています。キャリブレーションチェック手順に関する詳細 は、Sofia 2ユーザーマニュアルを参照してください。 重要: 光への曝露から保護するため、使用していないときは、キャリブレーションカセットは、必ず保管用パウチ(備品) に入れて保管してください。 1. Sofia 2 のキャリブレーションをチェックするには、メインメニ ュー)からキャリブレーションを実行を選びます。 2. メッセージが表示されたら、Sofia 2 にキャリブレーションカセ ットを入れてから、引き出しを閉じます。Sofia 2 は、 1 分以内に、自動的にキャリブレーションチェックを実行し ます。ユーザーは何も入力する必要はありません。 Sofia 2は、いつキャリブレーションチェックが完了したかを表示します。 を選択して、テストの実行画面に戻ります。 注: キャリブレーションチェックに合格しなかった場合は、施設監督者に通知するか、あるいはQuidelのテクニカルサポー トにご連絡ください。月曜日~金曜日の午前7時~午後5時(太平洋標準時)、 電話:800.874.1517(米国内) 858.552.1100(米国以外)、ファックス:858.455.4960、カスタマサービス:[email protected]、テクニカルサ ポート: [email protected]、または最寄りの代理店までご連絡ください。内蔵式プロシージャーコントロール
内蔵式プロシージャーコントロールSofia Influenza A+B FIAは、内蔵式プロ シージャーコントロール機能を備えています。Sofia またはSofia 2でテストを実行するときは毎回、プロシージャーコントロ ールゾーンがSofia またはSofia 2 によってスキャンされ、その結果がSofiaまたはSofia 2 の画面に表示されます。 日常管理については、メーカーは、各日に検査した最初の検体について、これらの内蔵式プロシージャーコントロールの結 果を記録しておくことを推奨しています。この記録は、各テスト結果をSofiaまたはSofia 2中に自動的にログ記録します。Sofia Influenza A+B FIA 6 / 32ページ プロシージャーコントロールから得られた有効な結果は、テストが正常にフローし、テストカセットの機能的完全性が維 持されていることを実証します。プロシージャーコントロールは、テストカセットが15分間現像された後、Sofiaまたは Sofia 2によって分析されます。テストが正常にフローしなかった場合は、SofiaまたはSofia 2は、結果が無効であったこと を示します。これが生じた場合、手順を見直して、新しい患者検体と新しいテストカセットを使用して、もう一度テスト を実施してください。
外部品質管理
外部コントロールはまた、試薬と検査手順が正しく実行されたことを確認するためにも使用できます。 Quidelは、陽性と陰性の外部コントロールを実行することを推奨します: トレーニングを受けていないオペレータそれぞれにつき 1 回 キットの配送品を新しく受領する度毎に 1 回 – 配送で受領したそれぞれの異なるロットを検査するという前提 貴施設の施設内品質管理手順によりさらに必要であると見なされる場合、ならびに、国、州、および連邦の 規制基準または認定要件に準拠する場合 ユーザーは、まずSofiaまたはSofia 2のメインメニューで、QCを実行を選んでから、メッセージが表示されたら、(キットボッ クスに同梱されている)QCカードをスキャンしてください。このカードは、ロット番号と使用期限を含むそのキットロットに固 有の情報を提供します。
所望するモード(WALK AWAYまたはREAD NOW)を選んでから、外部コントロールスワブを実行してください。
例: この画面は、Sofia での無効結果
を表示しています。
例: この画面は、Sofia 2 での無効結
果を表示しています。
Sofia Influenza A+B FIA 7 / 32ページ 陽性と陰性の外部コントロールスワブはキットに同梱されています。本添付文書またはクイックリファレンスガイドに記載 のスワブ検査手順を使用して、検査してください。インフルエンザの陽性コントロールスワブは、A型インフルエンザとB型イ ンフルエンザ両方の抗原を含んでいます。必ず陽性コントロールスワブを最初に実行してから、陰性コントロールスワブ を検査してください。 QCランを完了したら、それぞれの結果は、陽性コントロールと陰性コントロールについて、Sofiaでは合格) または不合格、Sofia 2では または として表示されます。 いずれかのQCテストの結果が不合格の場合は、患者のテストを実施したり、患者のテスト結果を報告しないでください。 患者検体の検査を行う前に、もう一度テストを行うか、あるいはQuidelのテクニカルサポートに連絡してください。 もし 陽性と陰性コントロールが不合格だった場合は、新しい陽性と陰性コントロールで2回目のテストを行ってください。 一方のコントロールのみが不合格の場合は、ユーザーには、陽性と陰性コントロールの両方についてもう一度テストを 行うか、あるいは不合格だったコントロールのみについてもう一度テストを行うオプションがあります。 以前に合格したコン トロールのテストをスキップするには、Sofiaの画面で、「スキップ」を選ぶか、あるいはSofia 2の画面で を選ぶことがで きます。QC の結果は、スキップしたコントロールのテストには、Sofiaでは「不明」、Sofia 2では、 と表示されます。 外部コントロールスワブの追加注文をご希望の場合は、Quidelカスタマサポートに連絡して、別個に取り寄せることがで きます[800.874.1517 (米国内)または858.552.1100]。
検体採取および取扱方法
検体採取
鼻スワブ検体
キットに同梱の鼻スワブを使用してください。 鼻スワブ検体を採取するには、肉眼検査で最も分泌物が多い鼻孔の中にスワブ(キットに同梱)を注意深く挿入しま す。静かに回転させて、鼻甲介 [鼻孔中1インチ(2.54 cm)未満] の高さで抵抗が感じられるまで、スワブを押し込みま す。スワブを鼻腔壁に対して数回回転させてから、鼻孔から取り出します。
鼻咽頭スワブ検体
ナイロンフロック加工(植毛加工)鼻咽頭スワブを使用します。このスワブはキットに同梱されていません。 鼻咽頭スワブ検体を採取するには、肉眼検査で最も分泌物が多い鼻孔の中にスワブを注意深く挿入します。スワブ を静かに上咽頭の後方中に押し込んでいる間、鼻中隔底近くでスワブを保持します。スワブを数回回転させてから、 鼻咽頭から取り出します。
鼻咽頭吸引
/
洗浄検体
鼻咽頭吸引/洗浄検体を採取するには、貴医療機関のプロトコルに従ってください。手順で認められている最少量の 生理食塩水を使用すること。一方、貴医療機関がプロトコルを備えていない場合は、臨床医により使用される以下 の手順を考慮してください。 鼻咽頭吸引検体を採取するには:サクションするために、滅菌生理食塩水を数滴、鼻孔中に滴下します。鼻孔底に 沿って、口蓋と並行に、フレキシブルなプラスチックチューブを挿入します。鼻咽頭に入れた後、チューブを取り出しなが ら、分泌物を吸引します。最初の鼻孔から採取した分泌物の量では足りない場合は、もう一方の鼻孔について、この 手順を繰り返してください。 鼻咽頭洗浄検体を採取するには:小児の場合は、頭部を両親の胸に押しつけた状態で前を向かせて両親の膝に座 らせてもかまいません。シリンジまたは吸引用バルブを、被験者の体格と年齢に従って必要とされる最少量の生理食Sofia Influenza A+B FIA 8 / 32ページ 塩水で満たします。頭部を後ろに傾けながら、一方の鼻孔の中に生理食塩水を注入します。洗浄検体をシリンジま たはバルブ中に吸引してください。吸引した洗浄検体は、およそ1 cc程度になると思われます。
もう一つの選択肢としては、生理食塩水を滴下した後で、頭部を前に屈めて、生理食塩水を清潔な検体
採取容器中に流出させます。
検体の輸送と保管
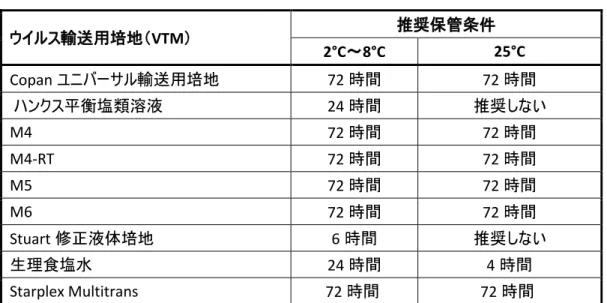
検体は、採取後できるだけ早く検査してください。ただし、検体を輸送する必要がある場合は、希釈するとテストの感 度が低下するため、検体をウイルス輸送用培地(VTM)で最小限希釈することを推奨します。可能な場合は常に、 患者検体を過度に希釈しないため、1 mL 以下とするのがベストです。表 1 に一覧するウイルス輸送用培地は、Quidel により試験され、Sofia Influenza A+B FIA と互換性があることが確認さ れています。 ただし、ウイルス輸送用培地のロット間のばらつきが、パーフォーマンスに影響を及ぼす可能性があります。 表 1 推奨ウイルス輸送用培地(VTM) ウイルス輸送用培地(VTM) 推奨保管条件 2°C~8°C 25°C Copan ユニバーサル輸送用培地 72 時間 72 時間 ハンクス平衡塩類溶液 24 時間 推奨しない M4 72 時間 72 時間 M4-RT 72 時間 72 時間 M5 72 時間 72 時間 M6 72 時間 72 時間 Stuart 修正液体培地 6 時間 推奨しない 生理食塩水 24 時間 4 時間 Starplex Multitrans 72 時間 72 時間 注: ウイルス輸送用培地(VTM)を使用する際には、検体を含む VTM を確実に室温まで温めることが重要です。 検体が冷たいと、正しくフローせず、誤った結果や無効な結果につながります。冷たい検体を室温に戻すには数分を 要します。
Sofia Influenza A+B FIA 9 / 32ページ
検査手順
すべての臨床検体(VTMに入れた検体を含む)は、本検査を開始する前に、室温でなければなりません。 使用期限: 使用前に、個別のテストパッケージまたは外側ボックスそれぞれに記載されている使用期限を確認してくだ さい。ラベルに記載の使用期限を過ぎたテストを使用してはなりません。 スワブテスト手順(鼻/鼻咽頭スワブ) 1. Sofia または Sofia 2 が所望するモードに設定されていることを確認します: WALK AWAY(ウオークアウェイ)または READ NOW(レディーナウ)。詳細情報については、「Sofia と Sofia 2 の使用方法」セクションを参照してください。 2. 試薬液を全部、試薬チューブ中に入れます。 試薬チューブを渦を巻くようにぐるぐる回して、内容物を溶かします。 3. 患者のスワブ検体を、試薬チューブの中に入れます。スワブ頭部を試薬チューブの底と 側面に押しつけながら、少なくとも 3 回転がすように動かします。 スワブを試薬チューブの中に 1 分間入れたままにしておきます。 スワブ頭部を試薬チューブの内面に押しつけて、転がすように動かしながら、スワブを取り 出します。使用済みのスワブは、バイオハザード廃棄物容器内に廃棄してください。 4. 試薬チューブから、患者検体を、小型で透明の 120 µL 容量固定ピペット(備品)に 満たします。 容量固定ピペットに患者検体を満たすには: a) トップバルブをしっかりと強く握ります。 b) バルブを握ったままで、ピペットチップを患者検体の中に入れます。 c) ピペットチップを患者検体中に入れたままで、バルブにかけた圧力をゆっくりと 緩めて、ピペットを満たします。 5. トップバルブをしっかりと強く握って、小型で透明の 120 µL 容量固定ピペットが空になる まで内容物を、テストカセットの検体ウェル中に注ぎます。オーバーフローバルブに残った 余分な液体は、そのまま残しておいてください。 注: 容量固定ピペットは、正しい容量の液性検体を採取して分注するように デザインされています。ピペットは、バイオハザード廃棄物容器内に廃棄してくだ さい。 注: 試薬チューブから検体を直に注いではなりません。小型で透明の 120 µL 容量固定ピペット(備品)を使用してください。 すぐに次のセクション「Sofia と Sofia 2 の使用方法」に進んで、検査を完了してください。 ゆっくり注ぎます 試薬チュ ーブ ねじって外します バルブ中 の試薬液 ここを強く握ります 120 uL の ピペット あふれ出た部分 患者の 検体 検体窓
Sofia Influenza A+B FIA 10 / 32ページ
鼻咽頭吸引/洗浄検体またはウイルス輸送用培地に入れた検体の検査手順
1. Sofia または Sofia 2 が所望するモードに設定されていることを確認します: WALK AWAY または READ NOW。詳細情報については、「Sofia と Sofia 2 の使 用方法」セクションを参照してください。また、次に進む前に、液性検体が室温で あることを確認してください。 2. 試薬液を全部、試薬チューブ中に入れます。試薬チューブを渦を巻くようにぐるぐる回 して、内容物を溶かします。 3. 検体採取容器またはテストチューブから、患者検体を、大型でピンク色の 250 µL 容量 固定ピペット (備品)に満たします。 容量固定ピペットに検体を満たすには: a) トップバルブをしっかりと強く握ります。 b) バルブを握ったままで、ピペットチップを患者検体の中に入れます。 c) ピペットチップを患者検体中に入れたままで、バルブにかけた圧力をゆっく りと緩めて、ピペットを満たします。 注: 正確な結果を得るためには、検体採取容器から、患者検体を、大型で ピンク色の250 µL容量固定ピペット に満たす際に、粘液様物質を避けてくだ さい。 4. トップバルブをしっかりと強く握って、大型でピンク色の 250L 容量固定ピペットが空 になるまで内容物を、 試薬チューブ中に注ぎます。オーバーフローバルブに残った余 分な液体は、そのまま残しておいてください。 注: 検体を試薬チューブに加えたら、検体をテストカセットに移す前に、勢いよく混 和してください。 注: 容量固定ピペットは、正しい容量の液性検体を採取して分注するようにデザイ ンされています。ピペットは、バイオハザード廃棄物容器内に廃棄してください。 5. バルブにかけた圧力をゆっくり緩めて、小型で透明の 120 µL 容量固定ピペットに、試薬 チューブから、患者検体を満たします。 ゆっくり注ぎます 試薬チュ ーブ ねじって外します バルブ中 の試薬液 ここを強く握 ります 120 uL の ピペット あふれ出た部分 患者の 検体 ここを強く握 ります 250 uL の ピペット 試薬チュ ーブ ここを強く 握ります 120 uL の ピペット あふれ出た部分 患者の 検体
Sofia Influenza A+B FIA 11 / 32ページ 6. トップバルブをしっかりと強く握って、小型で透明の 120L 容量固定ピペットが空になるま で内容物を、テストカセットの検体ウェル中に注ぎます。オーバーフローバルブに残った余 分な液体は、そのまま残しておいてください。ピペットは、バイオハザード廃棄物容器内に 廃棄してください。 注: 試薬チューブから検体を直に注いではなりません。小型で透明の 120 µL 容量固 定ピペット(備品)を使用してください。 7. すぐに次のセクション「Sofia と Sofia 2 の使用方法」に進んで、検査を完了してください。
Sofia とSofia 2の使用方法
WALK AWAY/READ NOW
モード
操作手順については、SofiaまたはSofia 2のユーザーマニュアルを参照してください。
SofiaとSofia 2は、2つの異なるモード(WALK AWAYとREAD NOW)に設定できます。各モードについての手順を以下に 説明します。
WALK AWAYモード
WALK AWAYモードでは、直ちに、テストカセットを、SofiaまたはSofia 2の中に入れます。SofiaとSofia 2では、進行時間 が異なる場合があります。 Sofia – Sofiaでは、検査の進行時間が自動的に計測されて、15分でその結果が表示されます。 Sofia 2 – Sofia 2は、検査進行中に定期的にテストカセットをスキャンします。 陽性結果は、3分から15分の間に 表示されます。 陰性結果は、15分経過した時点で表示されます。
READ NOWモード
極めて重要: SofiaまたはSofia 2中に入れる前に、完全に15分間、テストを進行させてください。 まず、テストカセットをカウンターまたはベンチトップの上に 15 分間静置し(Sofia または Sofia 2 の外部)、この進行ステッ プの時間を手動で測定します。次に、テストカセットを、Sofia または Sofia 2 の中に入れます。 READ NOW モードでは、 Sofia と Sofia 2 は、1 分以内にスキャンして検査結果を表示します。注: 15 分間の推奨進行時間後、さらに 15 分間は、結果は安定のまま保たれます。バッチ検査に関するヒント
作業量に応じて、バッチ検査を容易にするためにいくつかのオプションがあります。1本以上の試薬チューブに試薬液を 加えて、キャップを閉じてから、検体を加える前に、最長12時間まで、活性を失うことなく、室温(RT)でベンチの上で保 存することができます。 もう一つの選択肢としては、試薬液を加えてから、試薬チューブの中でスワブまたは液性検体を処理し、スワブを取り 出した後(該当する場合)、チューブのキャップを閉じて、検査前に最長12時間まで、活性を失うことなく、RTで静置し ておくことができます。 極めて重要: すぐ使用するための準備が整うまでは、絶対にホイルパウチを開封して、テストカセットを周囲環境に曝し てはなりません。Sofia による検査実施
1. バーコードスキャナーを使用するか、あるいはキーパッドを使用して手入力により、ユーザーID を入力します。 注:間違ったバーコードを誤ってスキャンした場合には、Sofiaのキーパッド上の矢印ボタンを使用して、そのフィールドを もう一度ハイライトし直します。それから、正しいバーコードをもう一度スキャンするだけで、前のバーコードが正しいバー コードで上書きされます。 検体窓Sofia Influenza A+B FIA 12 / 32ページ
2. バーコードスキャナーを使用するか、あるいはキーパッドで手入力により、患者 ID または発注番号を入力します。
3. 検査開始を押すと、Sofia の引き出しが自動的に開きます。
4. 正しい進行モード(WALK AWAY または READ NOW)が 選択されていることを確認します。準備が整った患者のテ ストカセットを、Sofia の引き出しの中に入れてから、引き 出しを閉じます。 5. Sofia は自動的に起動して、下の例に示すように、進行 状況を表示します。WALK AWAY モードでは、約 15 分で 検査結果が画面に表示されます。READ NOW モードで は、1 分以内にで検査結果が画面に表示されます。「結 果の判読」セクションを参照してください。
Sofia Influenza A+B FIA 13 / 32ページ
Sofia を用いる結果の判読
検査が完了すると、Sofiaの画面に結果が表示されます。このオプションが選択されると、本体のプリンターで結果が自 動的に印刷されます。蛍光である検査ラインは、肉眼では見ることができません。 Sofia画面は、手順コントロールの結果については「有効または無効」として表示し、A型インフルエンザとB型インフルエ ンザについてはどちらも、陽性または陰性結果を表示します。手順コントロールが「無効の場合は、新しい患者検体と 新しいテストカセットで検査をやり直してください。 陽性結果:例: この画面は、B 型インフルエンザについての有効な陽性
結果を示しています。
注: 陽性結果は、その他の病原体による同時感染を除外
するものではありません。
例: この画面は、WALK AWAY モード実行されてい
る検査の残り時間が 12 分 13 秒であることを示して
います。Sofia は、15 分後に、結果を読み取って表
示します。
例: この画面は、A 型インフルエンザについての有効な陽
性結果を示しています。
注: 陽性結果は、その他の病原体による同時感染を除
外するものではありません。
Sofia Influenza A+B FIA 14 / 32ページ 陰性結果: 無効結果:
例: この画面は、A 型インフルエンザと B 型インフルエンザに
ついての有効な陰性結果を示しています。
注: 陰性結果は、インフルエンザウイルスの感染を除外する
ものではありません。陰性の検査結果は、ウイルス培養また
は FDA 認可 A 型および B 型インフルエンザ分子アッセイに
よって確認することを推奨します。
例: この画面は、無効な結果を示しています。
無効結果: 検査が無効の場合、新しい患者検体と新
しい テストカセットを使用して、新しい検査を実施する
必要があります。
例: この画面は、A 型インフルエンザと B 型インフルエンザにつ
いての有効な陽性結果を示しています。
注: 陽性結果は、その他の病原体による同時感染を除外した り、A型インフルエンザのサブタイプを特定することはありません。 注: A型インフルエンザとB型インフルエンザの同時感染はめったに ありません。Sofia Influenza A+B FIAが「二重陽性」である臨床検 体(A型インフルエンザとB型インフルエンザ陽性)は、再検査する 必要があります。A型インフルエンザとB型インフルエンザの「二重陽 性」の結果を繰り返す場合は、結果を報告する前に、ウイルス培 養またはFDA認可A型およびB型インフルエンザ分子アッセイによっ て結果を確認することを推奨します。Sofia Influenza A+B FIA 15 / 32ページ
SOFIA 2 による検査実施
1. 本体のバーコードスキャナーを使用するか、あるいは画面に表示されているキーパッドで手入力により、ユーザーID を入力します。 注:間違ったバーコードを誤ってスキャンした場合、そのフィールドを選択して、もう一度ハイライトします。それから、 正しいバーコードをもう一度スキャンするだけで、前のバーコードが正しいバーコードで上書きされます。2. バーコードスキャナーを使用するか、あるいは画面に表示されているキーパッドで手入力により、患者 ID と
発注番号(該当する場合)を入力します。
3. 正しい進行モード(WALK AWAY または READ NOW)が選択されていることを確認します。 を押して、 Sofia 2 の引き出しを開けます。
Sofia Influenza A+B FIA 16 / 32ページ 4. 準備が整ったテストカセットを、Sofia 2 の引き出しの中に入れてから、引き出しを閉じます。
5. Sofia 2 は、自動的に起動して、下の例に示すように、進行状況を表示します。WALK AWAY モードでは、3 分から 15 分のあいだに検査結果が画面に表示されます。READ NOW モードでは、1 分以内にで検査結果が画面に表示 されます。「Sofia 2 を用いる結果の判読」セクションを参照してください。
Sofia 2 を用いる結果の判読
検査が完了すると、Sofia 2の画面に結果が表示されます。蛍光である検査ラインは、肉眼では見ることができません。 Sofia 2画面は、手順コントロールの結果については または として表示し、A型インフルエンザとB型インフルエンザ両 方について、 または 結果を表示します。手順コントロールが の場合は、新しい患者検体と新しいテストカセット で検査をやり直してください。プリンターが接続されている場合は、検査結果が画面に表示されているあいだに、印刷ア イコンを選択することによって、結果を手動で印刷することができます。 陽性結果:例: この画面は、A 型インフルエンザについ
ての有効な陽性結果を示しています。
注: 陽性結果は、その他の病原体による
同時感染を除外するものではありません。
例: この画面は、WALK AWAY モード実行され
ている検査の残り時間が 12 分 34 秒であること
を示しています。Sofia 2 は、3 分から 15 分のあ
いだに、
結果を読み取って表示します。
Sofia Influenza A+B FIA 17 / 32ページ 陰性結果:
例: この画面は、A 型インフルエンザと B 型インフ
ルエンザについての有効な陰性結果を示してい
ます。
注: 陰性結果は、インフルエンザウイルスの感染
を除外するものではありません。陰性の検査結
果は、ウイルス培養または FDA 認可 A 型および
B 型インフルエンザ分子アッセイによって確認する
ことを推奨します。
例: この画面は、A 型インフルエンザと B 型イン
フルエンザについての有効な陽性結果を示して
います。
注: 陽性結果は、その他の病原体による同時感 染を除外したり、A型インフルエンザのサブタイプを 特定することはありません。 注: A型インフルエンザとB型インフルエンザの同時 感染はめったにありません。Sofia Influenza A+B FIAが「二重陽性」である臨床検体(A型インフルエ ンザとB型インフルエンザ陽性)は、再検査する必要 があります。A型インフルエンザとB型インフルエンザの 「二重陽性」の結果を繰り返す場合は、結果を報 告する前に、ウイルス培養またはFDA認可A型およ びB型インフルエンザ分子アッセイによって結果を確 認することを推奨します。例: この画面は、B 型インフルエンザについて
の有効な陽性結果を示しています。
注: 陽性結果は、その他の病原体による同
時感染を除外するものではありません。
Sofia Influenza A+B FIA 18 / 32ページ 無効結果:
制限事項
本キットの内容物は、鼻スワブ、鼻咽頭スワブ、ならびに鼻咽頭吸引/洗浄検体から、A 型と B 型のインフルエンザ ウイルス抗原の定性的検出に使用します。 本検査は、A 型と B 型インフルエンザの生(生きている)ウイルスと生育不能なウイルス両方を検出します。検査パ ーフォーマンスは、検体中のウイルス(抗原)の量によって左右されるため、同一検体で実施されたウイルス培養の 結果と相関する場合もしない場合もあります。 鼻咽頭吸引/洗浄検体についての Sofia Influenza A+B FIA の臨床成績は、22 歳以上の患者においては確立さ れていないため、幼少患者で得られた臨床成績と一貫しない可能性があります。 検体中の抗原の量が本テストの検出下限を下回る場合、あるいは検体の採取や輸送が不適切な場合には、 陰性結果が生じることがあります。 検査手順の遵守を怠ると、検査パーフォーマンスに悪影響が及んだり、検査結果が無効になったり、あるいはその 両方が生じる可能性があります。 検査結果は、医師が入手できるその他の臨床データと併せて評価される必要があります。 陽性結果は、その他の病原体による同時感染を除外するものではありません。 陽性結果は、A 型インフルエンザウイルスの特定のサブタイプを識別しません。 陰性結果は、インフルエンザ以外のウイルスや細菌による感染を除外するものではありません。 小児は、成人と比べて、より多量に、かつ長期間ウイルスを放出する傾向があります。したがって、成人からの検 査検体はしばしば、小児からの検査検体よりも、感度が低くなります。 陽性と陰性の予測値は、有病率によって大きく左右されます。有病率が高い流行のピーク時には、偽陰性の検 査結果がより生じやすくなります。有病率が中程度から低くインフルエンザの活動が低い期間中には、偽陽性の 検査結果がより生じやすくなります。 A 型インフルエンザワクチンの鼻腔内投与を受けた人では、ワクチン接種後最長 3 日までは、検査が陽性結果を 示すことがあります。 モノクローナル抗体は、対象エピトープ領域で微小なアミノ酸変化しか受けなかった A 型インフルエンザウイルス対 する感度が低かったり、検出できないことがあります。 A 型インフルエンザウイルスの特定のサブタイプとウイルス株の識別が必要な場合は、州または地元の公衆衛生当 局に相談して、追加検査を行う必要があります。 全血の混入が 4% v/v を超える検体、あるいはムチンの混入が 0.5% v/v を超える検体では、本テストの判定に干 渉が生じることがあります。 血液が混じっていたり、過度に粘り気のあることがはっきり目視できる検体は使用しな いでください。 本テストのパーフォーマンスは、呼吸器感染の兆候や症状のない患者に対する使用については評価されていま せん。
例: この画面は、無効な結果を示しています。
無効結果: 検査が無効の場合、新しい患者
検体と新しいテストカセットを使用して、新しい
検査を実施する必要があります。
Sofia Influenza A+B FIA 19 / 32ページ
推定値
インフルエンザの季節的流行は、北半球と南半球双方において世界的に生じ、毎冬病気の蔓延の原因となっていま す。インフルエンザの年ごとの平均発病率は、100人あたり26~33例です。 このうち入院が必要となるリスクがあるのは、 感染した極めて幼少な患者と高齢な患者のうちほぼ300人に1人です。1976年から2006年まで30年間にわたり、米国 においてインフルエンザに関連して死亡した人は、低く見積もって約3千人、高く見積もって約4万9千人の範囲と推定 されています。2死亡の90%は、年齢65歳以上の人に生じました。4インフルエンザの大流行は、1918年、1957年、 1968年、2009年に発生しました。1918年の大流行の結果、世界中で推定4千万人から5千万人の人が死亡しまし た。2011年に実施されたSofia Influenza A+B FIAの臨床試験中に参照検査(ウイルス培養)により観察された有病率 は、A型インフルエンザが15%、B型インフルエンザが13%でした。パーフォーマンス特性
以下の試験は、Sofia Influenza A+B FIA と Sofia で実施されました。
細胞培養と比較する、
Sofia Influenza A+B FIA
のパーフォーマンス
Sofia Influenza A+B FIAをSofia で使用した場合のパーフォーマンスが、米国において2011年の2月から3月のあいだに、 多施設共同臨床フィールド試験で、直接蛍光アッセイ(DFA)によって、ウイルス細胞培養法と比較されました。 この試験は、米国の様々な地域の17ヵ所の著名な専門医療機関とCLIA waived検査施設(協同)の医療従事者に より実施されました。この多施設共同、ポイント・オブ・ケア(POC)フィールド試験では、2,066人の患者それぞれから、 鼻スワブ検体が2本、あるいは鼻咽頭スワブまたは鼻咽頭吸引/洗浄検体が2本採取されました。671人から1対 (両方の鼻孔から)の鼻スワブ検体が採取され、734人から1対(両方の鼻孔から)の鼻咽頭スワブ検体が採取され、 661人から鼻咽頭吸引/洗浄検体が採取されました。すべての臨床検体は、症候性患者から採取されました: 6歳未 満 74%、6~21歳 22%、22~59歳 4%、60歳以上 1%。53%が男性で、47%が女性でした。
この臨床試験中に、合計2,047の前向き臨床検体が、Sofia Influenza A+B FIAを使用して検査され、有効な結果が 得られました。これらの結果は、表2~6に記載されています。無効率は、0.9%(19/2066)で、95% CI: 0.6%-1.4%でし た。再検査のために新しい患者検体が採取されなかったため、無効結果は、表2~6から除外されています。
1本の鼻スワブまたは鼻咽頭スワブ、あるいは鼻咽頭吸引/洗浄検体の一部分についての現地検査が、医師のオ フィスまたは病院の検査施設で、Sofia Influenza A+B FIAを使用して、医療従事者によって実施されました。すべて の検体は、新しく採取してから、検査されました。残りの検体は、培養用としてウイルス輸送用培地に入れました。 Sofia Influenza A+B FIAと培養の比較において、1対(両方の鼻孔から)の鼻スワブ検体または1対(両方の鼻孔から) の鼻咽頭吸引/洗浄検体が、検査順序に関してランダム化されました。ウイルス細胞培養は、検査施設の施設内臨 床検査室で実施、または48時間以内に培養するために、検体をアイスパックに載せて、中央検査機関まで、凍結し ないで翌日便で輸送されました。結果は、表2~6に表示されています。
表 2
Sofia Influenza A+B FIA 結果と培養結果の比較(鼻スワブを使用した場合) (全年齢グループ)
A 型 B 型
培養 感度 = 124/138 = 90% 培養 感度 = 100/112 = 89%
陽性 陰性 (95% C.I. 84%-94%) 陽性 陰性 (95% C.I. 82%-94%)
Sofia 陽性 124 27 特異度 = 500/527 = 95% Sofia 陽性 100 23 特異度 = 530/553 = 96%
Sofia 陰性 14 500 (95% C.I. 93%-96%) Sofia 陰性 12 530 (95% C.I. 94%-97%)
Sofia Influenza A+B FIA 20 / 32ページ 表 3
Sofia Influenza A+B FIA 結果と培養結果の比較(鼻咽頭スワブを使用した場合) (全年齢グループ)
A 型 B 型
培養 感度 = 100/103 = 97% 培養 感度 = 101/112 = 90%
陽性 陰性 (95% C.I. 91%-99%) 陽性 陰性 (95% C.I. 83%-95%)
Sofia 陽性 100 34 特異度 = 596/630 = 95% Sofia 陽性 101 19 特異度 = 602/621 = 97%
Sofia 陰性 3 596 (95% C.I. 93%-96%) Sofia 陰性 11 602 (95% C.I. 95%-98%)
表 4
Sofia Influenza A+B FIA 結果と培養結果の比較(鼻咽頭吸引/洗浄を使用した場合) (全年齢グループ) A 型 B 型 培養 感度 = 68/69 = 99% 培養 感度 = 46/52 = 88% 陽性 陰性 (95% C.I. 91%-100%) 陽 性 陰性 (95% C.I. 77%-95%) Sofia 陽性 68 26 特異度 = 554/580 = 96% Sofia 陽性 46 22 特異度 = 575/597 = 96%
Sofia 陰性 1 554 (95% C.I. 93%-97%) Sofia 陰性 6 575 (95% C.I. 94%-98%)
表 5 A 型インフルエンザについての、年齢グループ別による検体タイプの、培養と比較するパーフォーマンス 鼻スワブ 鼻咽頭スワブ 鼻咽頭吸引/洗浄 感度 特異度 感度 特異度 感度 特異度 全年齢 90%(124/138) (95%CI=84%-94%) 95%(500/527) (95%CI=93%-96%) 97%(100/103) (95%CI=91%-99%) 95%(596/630) (95%CI=93%-96%) 99%(68/69) (95%CI=91%-100%) 96%(554/580) (95%CI=93%-97%) 6 歳未満 95%(62/65) (95%CI=87%-99%) 95%(210/221) (95%CI=91%-97%) 97%(61/63) (95%CI=89%-100%) 94%(444/470) (95%CI=92%-96%) 99%(68/69) (95%CI=91%-100%) 95% (544/570) (95%CI=93%-97%) 6~21 歳 87%(46/53) (95%CI=75%-94%) 95%(193/204) (95%CI=91%-97%) 97%(35/36) (95%CI=85%-100%) 94%(136/144) (95%CI=89%-97%) 該当なし(0/0) 100%(10/10) (95%CI=68%-100%) 22~59 歳 78%(14/18) (95%CI=54%-92%) 96%(82/85) (95%CI=90%-99%) 100%(4/4) (95%CI=45%-100%) 100%(15/15) (95%CI=76%-100%) 該当なし(0/0) 該当なし(0/0) 60 歳以上 100%(2/2) (95%CI=29%-100%) 88%(15/17) (95%CI=64%-98%) 該当なし(0/0) 100%(1/1) (95%CI=17%-100%) 該当なし(0/0) 該当なし(0/0)
Sofia Influenza A+B FIA 21 / 32ページ 表 6 B 型インフルエンザについての、年齢グループ別による検体タイプの、培養と比較するパーフォーマンス 鼻スワブ 鼻咽頭スワブ 鼻咽頭吸引/洗浄 感度 特異度 感度 特異度 感度 特異度 全年齢 89%(100/112) (95%CI=82%-94%) 96%(530/553) (95%CI=94%-97% 90%(101/112) (95%CI=83%-95%) 97%(602/621) (95%CI=95%-98%) 88%(46/52) (95%CI=77%-95%) 96%(575/597) (95%CI=94%-98%) 6 歳未満 90%(35/39) (95%CI=76%-97%) 96%(238/247) (95%CI=93%-98%) 87%(54/62) (95%CI=76%-94%) 97%(455/471) (95%CI=95%-98%) 87%(39/45) (95%CI=73%-94%) 96%(572/594) (95%CI=94%-98%) 6~21 歳 92%(56/61) (95%CI=82%-97%) 95%(187/196) (95%CI=91%-98%) 94%(45/48) (95%CI=83%-98%) 98%(130/132) (95%CI=94%-100%) 100%(7/7) (95%CI=60%-100%) 100%(3/3) (95%CI=38%-100%) 22~59 歳 73%(8/11) (95%CI=43%-91%) 97%(89/92) (95%CI=90%-99%) 100%(2/2) (95%CI=29%-100%) 94%(16/17) (95%CI=71%-100%) 該当なし(0/0) 該当なし(0/0) 60 歳以上 100%(1/1) (95%CI=17%-100%) 89%(16/18) (95%CI=66%-98%) 該当なし(0/0) 100%(1/1) (95%CI=17%-100%) 該当なし(0/0) 該当なし(0/0)
再現性試験
Sofia Influenza A+B FIAをSofiaで使用した場合の再現性は、3ヵ所の異なる検査機関(そのうちの1ヵ所はQuidel)で 評価されました。各検査機関で2人のオペレータが別々に、A型インフルエンザとB型インフルエンザの弱陰性から中等 度の陽性の範囲にわたる負の臨床行列として作製された、コード化された、考案による一連の検体を検査しました。 検査は、およそ2週間に及ぶ期間に、日を改めて5回実施されました。検査機関間の一致率(表7)は、陰性検体に ついては94%-100%、陽性検体については98%-100%でした。
表 7
Sofia Influenza A+B 再現性試験(Sofia で使用した場合) 検査機関間の一致率
検査機関 陰性 (ウイルスなし) A 型イ ンフルエンザ 強陰性(C5) A 型イ ンフルエンザ 弱陽性(C95) A 型イ ンフルエンザ 中等度陽性 (C3X) B 型イ ンフルエンザ 強陰性(C5) B 型イ ンフルエンザ 弱陽性(C95) B 型イ ンフルエンザ 中等度陽性 (C3X) 1 30/30 29/30 30/30 30/30 28/30 29/30 30/30 2 30/30 29/30 30/30 30/30 30/30 29/30 30/30 3 30/30 30/30 30/30 30/30 27/30 30/30 30/30 合計 90/90 88/90 90/90 90/90 85/90 88/90 90/90 予測結果 についての 総合一致 率(%) (95% CI) 100% (95%-100%) 98% (92%-100%) 100% (95%-100%) 100% (95%-100%) 94% (87%-98%) 98% (92%-100%) 100% (95%-100%)
Sofia Influenza A+B FIA 22 / 32ページ
検出下限
Sofia Influenza A+B FIAをSofiaで使用した場合の検出下限(LOD)は、合計7株のヒトインフルエンザウイルス ー直接 検体についてA型インフルエンザ(2株)とB型インフルエンザ(2株)、VTMに溶出した検体についてA型インフルエンザ (2株)とB型インフルエンザ(2株)ー を使用して算出されました(表8)。 表 10 A 型および B 型インフルエンザのヒト分離株を用いた検出下限 ウイルス株 ウイルスタイプ サブタイプ 最小検出濃度 (TCID50/mL) A/California/07/2009 A 2009 H1N1 202 A/Hong Kong/8/68 A H3N2 105 B/Allen/45 B 40 B/Malaysia/2506/04 B 24 輸送用培地に入れた検体 ウイルス株 ウイルスタイプ サブタイプ 最小検出濃度 (TCID50/mL) A/New Jersey/8/76 A H1N1 M5 2460 UTM 1645 A/Port Chalmers/1/73 A H3N2 M5 1482 UTM 1446 B/Allen/45 B M5 5 UTM 4.6 B/Florida/07/2004 B M5 40 UTM 35 TCID50濃度は、Reed-Muench(リード・ミュンヒ)の方法またはRowe(ロウ)によるELISA法によって測定され ました。
分析的反応性
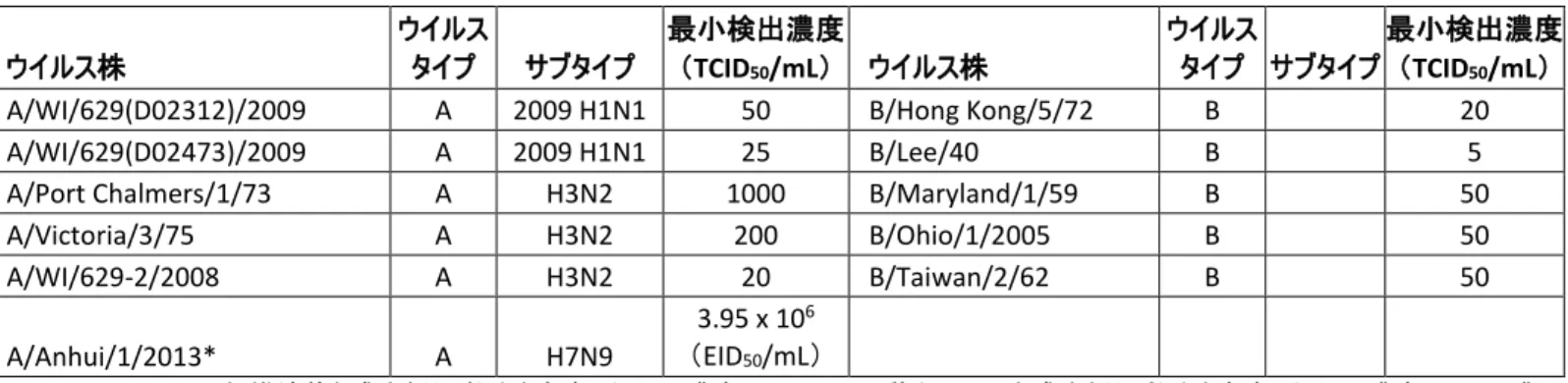
21株のA型インフルエンザウイルスと9株のB型インフルエンザウイルスから成る合計30株のヒトインフルエンザウイルスを用 いて、Sofia Influenza A+B FIAをSofiaで使用した場合の分析的反応性が確認されました(表9)。表9 A型およびB型インフルエンザのヒト分離株を用いた分析的反応性 ウイルス株 ウイルス タイプ サブタイプ 最小検出濃度 (TCID50/mL) ウイルス株 ウイルス タイプ サブタイプ 最小検出濃度 (TCID50/mL)
A/Fort Monmouth/1/47 A H1N1 50 A/Wisconsin/67/05 A H3N2 20
A/New Caledonia/20/1999 A H1N1 200 A2/Aichi/2/68 A H3N2 1.25
A/New Jersey/8/76 A H1N1 500 A/Anhui/01/2005 A H5N1 5
A/NWS/33 A H1N1 0.63 A/GWT/LA/169GW/88 A H10N7 20
A/Puerto Rico/8/34 A H1N1 100 A/Shearwater/
Australia2576/79 A H15N9 10 A/Solomon Islands/3/06 A H1N1 0.31 A/Taiwan/42/06 A H1N1 200 B/Brisbane/60/2008 B 10 A/WI/629-9/2008 A H1N1 200 B/Florida/04/2006 B 250 A1/Denver/1/57 A H1N1 20 B/Florida/07/2004 B 500 Influenza/Mexico/4108/2009 A 2009 H1N1 200 B/GL/1739/54 B 2000
Sofia Influenza A+B FIA 23 / 32ページ ウイルス株 ウイルス タイプ サブタイプ 最小検出濃度 (TCID50/mL) ウイルス株 ウイルス タイプ サブタイプ 最小検出濃度 (TCID50/mL)
A/WI/629(D02312)/2009 A 2009 H1N1 50 B/Hong Kong/5/72 B 20
A/WI/629(D02473)/2009 A 2009 H1N1 25 B/Lee/40 B 5
A/Port Chalmers/1/73 A H3N2 1000 B/Maryland/1/59 B 50
A/Victoria/3/75 A H3N2 200 B/Ohio/1/2005 B 50
A/WI/629-2/2008 A H3N2 20 B/Taiwan/2/62 B 50
A/Anhui/1/2013* A H7N9
3.95 x 106
(EID50/mL)
TCID50/mL = 50%の組織培養を感染させる能力を有するウイルス濃度。 EID50/mL = 鶏卵の 50%を感染させる能力を有するウイルス濃度。TCID50濃
度と EID50濃度は、Reed-Muench(リード・ミュンヒ)の方法によって測定されました。
* 本テストは、陽性ヒト呼吸器検体から培養された H7N9 ウイルスを検出することが示されていますが、H7N9 インフルエンザウイルスに陽性の臨床検体 についての本デバイスのパーフォーマンス特性は、確認されていません。Sofia Influenza A+B FIA は、A 型インフルエンザウイルスと B 型インフルエンザウイ ルスを区別することが可能ですが、インフルエンザのサブタイプを鑑別することはできません。
分析的反応性は、鳥から分離された 12 株のインフルエンザウイルス(A 型)を用いてさらに評価されました。The Sofia Influenza A+B FIA は、検査された全株を検出しました(表 10)。
表 10 鳥インフルエンザ(A 型)の異なる分離株を用いた分析的反応性 ウイルス株* ウイルスタイプ サブタイプ 最小検出濃度 (TCID50/mL) A/Mallard/NY6750/78 A H2N2 100 A/Mallard/OH/338/86 A H4N8 50 A/Mallard/WI/34/75 A H5N2 100 A/Chicken/CA/431/00 A H6N2 50 A/Chicken/NJ/15086-3/94 A H7N3 5 A/Blue Winged Teal/LA/B174/86 A H8N4 10 A/Chicken/NJ/122210/97 A H9N2 10 A/Chicken/NJ/15906-9/96 A H11N9 50 A/Duck/LA/188D/87 A H12N5 50 A/Gull/MD/704/77 A H13N6 0.625 A/Mallard/GurjevRussia/262/82 A H14N5 20 A/Shorebird/DE/172/2006 A H16N3 2 * ヒト病原体として出現する A 型インフルエンザウイルスのサブタイプについてのパーフォーマンス特 性は、確認されていません。
分析的特異性
交差反応
Sofia Influenza A+B FIAをSofiaで使用した場合が、合計18株の細菌と真菌微生物ならびに16のインフルエンザウイル ス以外の分離株について評価されました。細菌と真菌の分離株は、2x106 cfu/mLの濃度で評価されました。ウイルス
分離株は、2x105 TCID
50/mLの濃度で評価されました。下の表11 に一覧する微生物やインフルエンザ以外のウイルス
のいずれも、本検査においていかなる交差反応の兆候も示しませんでした。また、検体フローとコントロールラインの出 現にも影響はありませんでした。
Sofia Influenza A+B FIA 24 / 32ページ 表 11 分析特異性と交差反応 微生物/インフルエンザ以外のウイルス 濃度* A 型インフルエン ザ結果 B 型インフルエン ザ結果
Bordetella pertussis(百日咳菌) 2x106 cfu/mL 陰性 陰性
Canidida albicans(カンジダ・アルビカンス) 2x106 cfu/mL 陰性 陰性
Chlamydia trachomatis(トラコーマ病原体) 2x106 cfu/mL 陰性 陰性
Corynebacterium diphtheriae(ジフテリア菌) 2x106 cfu/mL 陰性 陰性
Escherichia coli(大腸菌) 2x106 cfu/mL 陰性 陰性
Haemophilus influenzae(インフルエンザ菌) 2x106 cfu/mL 陰性 陰性
Lactobacillus plantarum(ラクトバチラス・プランタルム) 2x106 cfu/mL 陰性 陰性
Legionella pneumophila(レジオネラ・ニューモフィラ) 2x106 cfu/mL 陰性 陰性
Moraxella catarrhalis(カタル球菌) 2x106 cfu/mL 陰性 陰性
Mycobacterium tuberculosis(avirulent)[結核菌 (非病原性)] 2x106 cfu/mL 陰性 陰性
Mycoplasma pneumoniae(肺炎マイコプラズマ) 2x106 cfu/mL 陰性 陰性
Neisseria meningitidis(髄膜炎菌) 2x106 cfu/mL 陰性 陰性
Neisseria subflava(ナイセリア‐サブフラバ) 2x106 cfu/mL 陰性 陰性
Pseudomonas aeruginosa(緑膿菌) 2x106 cfu/mL 陰性 陰性
Staphylococcus epidermidis(表皮ブドウ球菌) 2x106 cfu/mL 陰性 陰性
Streptococcus pneumoniae(肺炎連鎖球菌) 2x106 cfu/mL 陰性 陰性
Streptococcus pyogenes(化膿性連鎖球菌) 2x106 cfu/mL 陰性 陰性
Streptococcus salivarius(ストレプトコッカス・サリバリウス) 2x106 cfu/mL 陰性 陰性
Adenovirus type 1(1 型アデノウイルス) 2x105 TCID
50/mL 陰性 陰性
Adenovirus type 7(7 型アデノウイルス) 2x105 TCID
50/mL 陰性 陰性
Human coronavirus(OC43)[ヒトコロナウイルス(OC43)] 2x105 TCID
50/mL 陰性 陰性
Human coronavirus(229E)[ヒトコロナウイルス(229E)] 2x105 TCID50/mL 陰性 陰性
Human coxsackievirus(ヒトコクサッキーウイルス) 2x105 TCID
50/mL 陰性 陰性
Cytomegalovirus(サイトメガロウイルス) 2x105 TCID
50/mL 陰性 陰性
Epstein Barr Virus(エプスタイン・バーウイルス) 2x105 TCID
50/mL 陰性 陰性
Human parainfluenza type 1(ヒトパラインフルエンザウイルス 1
型) 2x105 TCID
50/mL 陰性 陰性
Human parainfluenza type 2(ヒトパラインフルエンザウイルス 2
型) 2x105 TCID
50/mL 陰性 陰性
Human parainfluenza type 3(ヒトパラインフルエンザウイルス 3
型) 2x105 TCID
50/mL 陰性 陰性
Measles(麻疹) 2x105 TCID
50/mL 陰性 陰性
Human metapneumovirus(ヒトメタニューモウイルス) 2x105 TCID
50/mL 陰性 陰性
Mumps virus(ムンプスウイルス) 2x105 TCID
50/mL 陰性 陰性
Respiratory syncytial virus type A(呼吸器多核体ウイルス A
型) 2x105 TCID
50/mL 陰性 陰性
Respiratory syncytial virus type B(呼吸器多核体ウイルス B
型) 2x105 TCID