水溶性シッフ塩基へのマージングゾーン誘導体化/逆相分配高速液体クロマトグラフィーによるn-アルキルアミン類の分離定量
6
0
0
全文
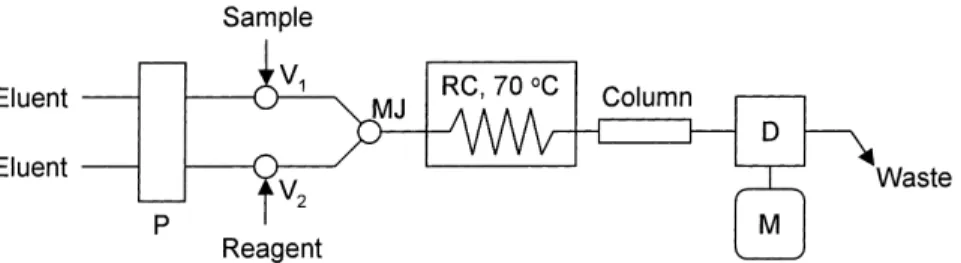
(2) 724. BUNSEKI. Vol. 53 (2004). KAGAKU. Fig. 1 Merging zone derivatization - RP-HPLC system for the determination of n -alkylamines as SAS- and SPAHNA- Schiff bases P : double plunger pump ; V1 and V2 : six way valves with loop ; MJ : mixing joint ; RC : reaction coil (5 m); Column : TSK-GEL ODS-80TMCTR (4.6 mm i.d.× 100 mm), D : UV-Vis detector, M : Monitor. 及び 4-(4-スルホフェニルアゾ)-1-ヒドロキシ-2-ナフトアル デヒド(SPAHNA)を開発した. 13)∼16). .これら誘導体化試. 薬を用いるプレキャピラリー誘導体化により,n -アルキル アミン類は対応する水溶性シッフ塩基に変換され,比較的 短い反応時間,分析時間及び十分な感度が得られた.本研 究では,上記誘導体化試薬をオンライン誘導体化試薬とし て 用 い る 逆 相 分 配 高 速 液 体 ク ロ マ ト グ ラ フ ィ ー ( RPFig. 2. HPLC)について検討した.試料溶液は流路にゾーンとし. Structure of labeling reagents. て注入され,もう一方の流路に注入された試薬溶液とオン ラインで混合されて,水溶性シッフ塩基を生成する.アル キル鎖長の異なる 4 種類の n -アルキルアミンは 5 m,70℃. ミルアミン : AmA,n -ヘキシルアミン : HxA,n -ヘプチル. の反応コイル中で定量的に誘導体化された.諸条件の最適. アミン : HpA,n -オクチルアミン : OcA),イオン対試薬. 化により,オンライン誘導体化を含む 1 試料当たりの分. + − として用いた臭化テトラエチルアンモニウム(TEA Br ). 析時間は SAS,SPAHNA を用いた場合それぞれ 25 分,18. は東京化成工業製のものを用いた.. 分であり,検出感度も十分であった.. 2. 実 験. 2・1 装 置. 溶離液に用いるメタノールは和光純薬製 HPLC 級のも のを用いた.溶離液の pH 緩衝液は和光純薬製特級リン酸 二水素カリウムとリン酸水素二ナトリウムを蒸留水に溶解 して混合したもの(0.1 M,pH 7.5)を用いた.. オンライン誘導体化を含む RP-HPLC システムを Fig. 1 に示す.送液ポンプはサヌキ工業製ダブルプランジャーポ ンプ(DM2M-1026)を,逆相カラムは東ソー製 TSKgel ODS-80TMCTR(内径 4.6 mm,カラム長 100 mm)を,検. 2・3. n -アルキルアミン類のオンライン SAS シッフ塩基. 誘導体化における標準操作 溶離液には 50%(v/v)リン酸緩衝液(10 mM,pH 7.5). 出器は横河製 LC100 紫外可視吸光検出器を用い,クロマ. と 50%(v/v)メタノールを含むものを用い,イオン対試. トモニター(日本フィルコン製)を用いてクロマトグラム. + − 薬として 2 mM TEA Br を添加して用いた.ダブルプラ. を記録した.試料溶液注入,試薬溶液注入にそれぞれ六方. ンジャーポンプを用いて 2 つのキャリヤー流れとし,一. バルブを用い,Y 型のミキシングジョイントで 2 つの流れ. 方の流れにループインジェクターを用いて n -アルキルア. を混合した.配管はすべてテフロン製のもの(内径 0.5. ミンのメタノール溶液の 100 µl を注入した.もう一方の. mm)を用いた.反応コイルは水浴中に浸し,アドバンテ. キャリヤー流れには SAS 水溶液(8 mM)の 100 µl を試料. ック東洋製 MTU-1 を用いて温度を制御した.. 溶液注入と同時に注入した.誘導体化反応が十分進行する ように全流量を 0.5 ml min. 2・2. 試 薬. に設定して,Y 型ジョイント. により両液を混合し,70℃ に設定された長さ 5 m の反応. 誘導体化試薬として用いた SAS 及び SPAHNA は前報に より合成したもの. −1. 13)16). を用いた.それらの構造を Fig. 2 に. 示す.分析対象物質として用いたアルキルアミン類(n -ア. コイル中でオンライン誘導体化した.注入から 10 分経過 以降,迅速な溶離のために総流量を 1.0 ml min 250 nm で吸光検出した.. −1. として,.
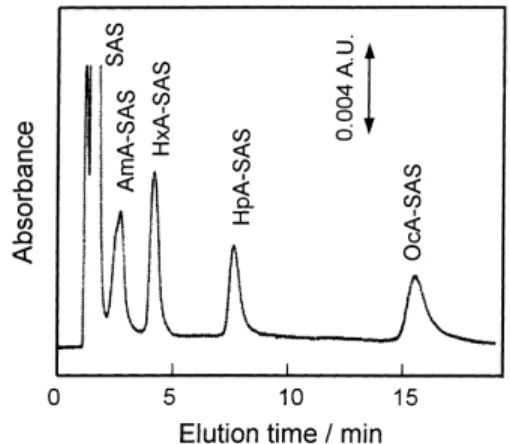
(3) 報 文 高柳,DRIOUICH,澤井,LI,大島,本水 : 水溶性シッフ塩基への RP-HPLC による n-アルキルアミン類の分離定量. Fig. 3 Effect of TEA+ Br− concentrations on retention factor of SAS-Schiff bases Eluent : 10 mM phosphate buffer (pH 7.5) - methanol (5 : 5 v/v)+0∼ 16 mM TEA+ Br−. Sample solution : 50 µM of each n -alkylamine SAS Schiff base. Chromatographic conditions : flow rate, 0.7 ml min−1 ; injection volume 20 µl ; detection wavelength, 250 nm. □, SAS ; ◇, n -amylamine ; ○, n -hexylamine ; △, n heptylamine ; ■, n -octylamine. 725. Fig. 4 Typical chromatogram for pre-column derivatized SAS-Schiff bases Eluent : 10 mM phosphate buffer (pH 7.5) - methanol (5 : 5 v/v)+ 2 mM TEA+ Br− . Sample solution : 50 µM of each n -alkylamine SAS-Schiff base. Chromatographic conditions : flow rate, 0.7 ml min−1 ; injection volume 20 µl ; detection wavelength, 250 nm. あり,アルキル鎖の長いものほど顕著であった.そこで, . 溶離時間の短縮とシグナル形状の改善を目的として TEA. +. . 2・4. n -アルキルアミン類のオンライン SPAHNA シッフ. Br − を 1 ∼ 16 mM の範囲で溶離液に添加して検討した . . + − (Fig. 3).TEA Br 濃度の増加に伴い溶離時間を短縮で. 塩基誘導体化による標準操作. . 溶離液には 30%(v/v)リン酸緩衝液(10 mM,pH 7.5) と 70%(v/v)メタノールを含むものを用い,イオン対試 +. は短いアルキル鎖長のシッフ塩基で SAS との分離が悪く . −. . + − き,シグナル形状も改善されたが,高濃度の TEA Br で. . 薬として 2 mM TEA Br を添加して用いた.前項と同じ. + − なるために,TEA Br 濃度として 2 mM を設定した.ク. く 2 つのキャリヤー流れに n -アルキルアミンのメタノー. ロマトグラムの例を Fig. 4 に示す.. ル溶液(20 µl)と SPAHNA 水溶液(15 mM,100 µl)を. SPAHNA を誘導体化試薬として用いた場合の HPLC 分. 同時に注入した.反応コイル長,反応条件,流量など,検. 離も,上記の条件で検討した.SPAHNA は疎水性が高く. 出波長を 420 nm とした以外は前項と同じ条件とした.. ODS カラムに強く保持されたため,溶離液のメタノール . 3 3・1. . + − 分率は 70%(v/v)とした.TEA Br 濃度の 2 mM で 4 種. 結果と考察. 類の n -アルキルアミン-シッフ塩基のベースライン分離と. n -ア ル キ ル ア ミ ン 類 の プ レ カ ラ ム 誘 導 体 化 と. 14 分以内での迅速な溶離が可能となった.. HPLC 分離特性 オンライン誘導体化−RP-HPLC の検討に先立ち,プレ カラム誘導体化した水溶性シッフ塩基のカラム分離特性に ついて検討した.Driouich らの報告. 13)∼15). で,40%(v/v). 3・2. SAS を用いた n -アルキルアミン類の水溶性シッフ. 塩基へのオンライン誘導体化と HPLC 分離 Fig. 1 の HPLC システムを用いる n -アルキルアミン類. 以上のエタノールを含む水溶液では,SAS により誘導体化. のオンライン誘導体化について,2 m の反応コイルと. された n -アルキルアミン−シッフ塩基は pH 7.0 ∼ 8.6 の範. 40℃ の温度条件で検討した.なお,試料溶液,試薬溶液. 囲で安定であることを見いだした.そこで,50%(v/v)メ. の注入ループから Y 型ミキシングジョイントまでのチュ. タノールを含む水溶液中で,4 種類の n -アルキルアミン. ーブの長さは,ゾーンの広がりを抑えるためできるだけ短. (それぞれ 50 µM)に誘導体化試薬(SAS あるいは SPAH-. くした.0.1 mM の n -アミルアミン(AmA)を含む試料溶. NA,2 mM)を添加して 40℃ で 20 分間,誘導体化反応. 液(100 µl)と 0.5 mM の SAS を含む試薬溶液(100 µl). を行った.反応生成物を 50%(v/v)リン酸緩衝液(10. を同時に注入したところ,AmA-シッフ塩基に対応する小. mM,pH 7.5)− 50%(v/v)メタノールを溶離液とする一流. さなシグナルが得られた.SAS 濃度の増加,注入体積の増. 路の RP-HPLC で分離検出した.. 加ではシグナル高さは改善はされず,他のアルキルアミン. SAS を誘導体化試薬として用いた場合,上記の条件では 長い溶離時間を必要とし,得られたシグナルもブロードで. でも同様の結果であった. 反応コイル長を 5 m,反応温度を 70℃ として,SAS 濃.
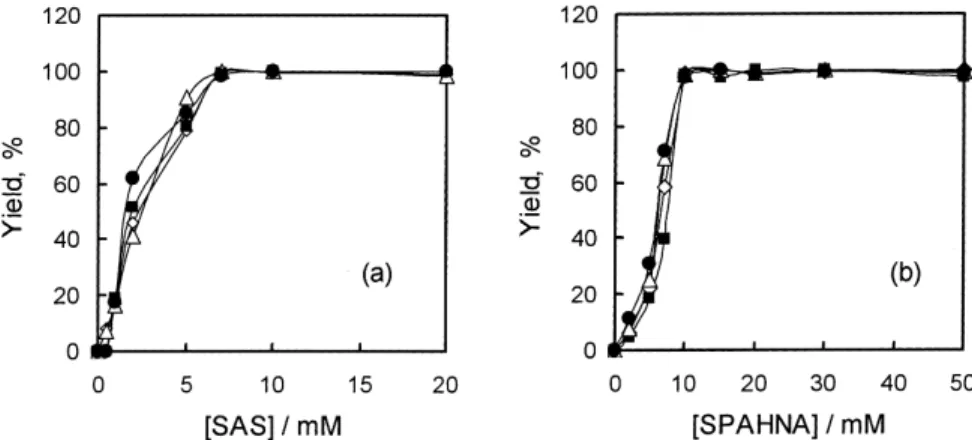
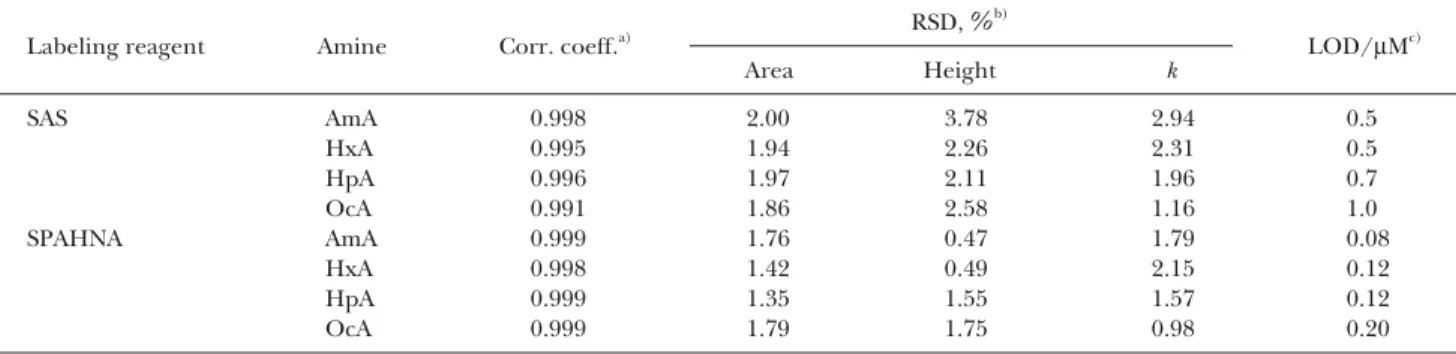
(4) 726. BUNSEKI. Vol. 53 (2004). KAGAKU. Fig. 5 Effect of concentrations of labeling reagent on the yield of on-line derivatization reaction +. Eluent : 10 mM phosphate buffer (pH 7.5) - methanol (5 : 5 v/v)+ 2 mM TEA Br−. Sample solution : 10 µM n -alkylamines. Reaction coil : 5 m, 70℃. Total flow rate : 0.5 ml min− 1 (0 ∼ 10 min), 1.0 ml min− 1 (10 ∼ 30 min). Labeling reagent : (a), SAS ; (b), SPAHNA. Injection volume : sample, 100 µl (for SAS) or 20 µl (for SPAHNA); reagent, 100 µl. Detection wavelength : 250 nm (for SAS) or 420 nm (for SPAHNA). ◇, n -amylamine ; ■, n -hexylamine ; △, n -heptylamine ; ●, n-octylamine. 度 0 ∼ 20 mM の範囲で誘導体化について再検討したとこ ろ,効率的に誘導体化できることが分かった.Fig. 5( a) に示すように,4 種類の 10 µM n -アルキルアミンに対して 十分な感度が得られ,SAS 濃度 8 mM 以上で最大感度が得 られた.高濃度の SAS は AmA-シッフ塩基とシグナルが重 なるので,反応コイル中での反応時間について,流量を変 化させて検討した. 分析対象物質であるアルキルアミンと SAS が反応コイ . ル中で十分混合するように,最初の総流量を 0.5 ml min. −1. として 10 分間流し,その後,迅速に溶離できるように総 . 流量を 1.0 ml min. −1. とした.4 種類の n -アルキルアミン. のクロマトグラムの例を Fig. 6 に示す. 3・3. SPAHNA を用いた n -アルキルアミン類の水溶性シ. ッフ塩基へのオンライン誘導体化と HPLC 分離 SPAHNA を用いるオンライン誘導体化についても同様 に検討した.溶離液中のメタノール分率を 70%(v/v)と. Fig. 6 Typical chromatogram for n -alkylamines as SAS-Schiff bases by on-line derivatization Eluent : 10 mM phosphate buffer (pH 7.5) - methanol (5 : 5 v/v)+ 2 mM TEA+ Br−. Sample solution : 10 µM of each n -alkylamine. Reagent solution : 8 mM SAS. Reaction coil : 5 m, 70℃. Total flow rate : 0.5 ml min−1 (0 ∼ 10 min), 1.0 ml min−1 (10 ∼ 30 min). Injection volume : sample, 100 µl ; reagent, 100 µl. Detection wavelength : 250 nm. して 10 mM リン酸緩衝液を用い,0 ∼ 50 mM の SPAHNA 濃度で検討した.10 µM の n -アルキルアミンを 100 µl 注 入した場合,上記濃度範囲で定量的な反応を得ることがで. 3・4. オンライン誘導体化 RP-HPLC による分析性能. きなかった.このことから,SPAHNA が SAS よりも反応. 2 種類の誘導体化試薬を用い,n -アルキルアミン濃度. 速度が遅いことで説明できる.反応率を高めるために,試. 5 ∼ 50 µM の範囲で検量線を作成したところ,相関係数. 料溶液の注入体積を 20 µl とした場合,Fig. 5(b)に示す. 0.991 以上の良好な直線性が得られた(Table 1).また,. とおり SPAHNA 濃度 15 mM 以上で最大感度が得られた.. Table 1 に示すように,ピーク高さ,ピーク面積,リテン. クロマトグラムの例を Fig. 7 に示す.. ションファクターの再現性は SAS を用いた場合 1.16 ∼ 3.78%,SPAHNA を用いた場合は 0.47 ∼ 2.15% と良好な 結果が得られた.n -アルキルアミンに対する検出限界は,.
(5) 報 文 高柳,DRIOUICH,澤井,LI,大島,本水 : 水溶性シッフ塩基への RP-HPLC による n-アルキルアミン類の分離定量. 727. Table 1 Calibration data, reproducibility, and limits of detection by the on-line derivatization methods Labeling reagent. Amine. SAS. AmA HxA HpA OcA AmA HxA HpA OcA. SPAHNA. RSD, %b). Corr. coeff.a) 0.998 0.995 0.996 0.991 0.999 0.998 0.999 0.999. LOD/µMc). Area. Height. k. 2.00 1.94 1.97 1.86 1.76 1.42 1.35 1.79. 3.78 2.26 2.11 2.58 0.47 0.49 1.55 1.75. 2.94 2.31 1.96 1.16 1.79 2.15 1.57 0.98. 0.5 0.5 0.7 1.0 0.08 0.12 0.12 0.20. a) Concentration range : 5∼ 50 µM ; b) Values analyzed with 8 measurements ; c) Values at S /N = 3. NA では 0.08 ∼ 0.20 µM が得られた.ワイン中のアルキル アミン濃度として mg l. −1. レベル(10 µM レベル)が報告. 17). されており ,実際の分析法として十分な感度を有してい ることが示された. 本研究の一部は,日本学術振興会科学研究費補助金(一般研 究(B)No. 13440220)により行われた.. 文 献. Fig. 7 Typical chromatogram for n -alkylamines as SPAHNA-Schiff bases by on-line derivatization Eluent : 10 mM phosphate buffer (pH 7.5) - methanol (3 : 7 v/v)+ 2 mM TEA+ Br− . Sample solution : 5 µM of each n -alkylamine. Reagent solution : 15 mM SPAHNA. Reaction coil : 5 m, 70℃ . Total flow rate : 0.5 ml min−1 (0 ∼ 10 min), 1.0 ml min−1 (10 ∼ 30 min). Injection volume : sample, 20 µl ; reagent, 100 µl. Detection wavelength : 420 nm. どちらの試薬ともキャピラリー電気泳動法により得られた 結果. 13)16). よりも低い検出限界であった.SAS と SPAHNA. を比較すると,SPAHNA は短い分析時間と高感度,高再 現性が得られる点で優れた試薬である.. 4. 結 語. 2 種類の水溶性誘導体化試薬を用い,n -アルキルアミン の水溶性シッフ塩基へのオンライン誘導体化をマージング ゾーン法により行った.誘導体化反応とカラム分離/検出 を含む分析時間は SAS,SPAHNA についてそれぞれ 25 分, 18 分であり,検出感度も SAS では 0.5 ∼ 1.0 µM,SPAH-. 1) P. Simon, C. Lemacon : Anal. Chem., 59, 480 (1987). 2) A. Sevillano-Cabeza, Y. Moliner-Martinez, C. MolinsLegua, P. Campíns-Falcó : Anal. Bioanal. Chem., 376, 918 (2003). 3) J. Krol, P. G. Alden, J. Morawski, P. E. Jackson : J. Chromatogr., 626, 165 (1992). 4) M. Maruyama, T. Nagayoshi : J. Chromatogr., 594, 159 (1992). 5) J. Ruzicka, E. H. Hansen : “Flow Injection Analysis”, (1998), (The Library of Congress, USA). 6) J. Ruzicka : Anal. Chim. Acta, 190, 155 (1986). 7) Y. Saito, M. Kawazoe, K. Jinno : Analyst, 125, 807 (2000). 8) D. F. Evans, P. H. Misse : J. Chem. Soc. Dalton Trans., 1985, 1451. 9) D. F. Evans, P. H. Misse : J. Chem. Soc. Dalton Trans., 1987, 1279. 10) M. Botsivali, D. F. Evans, P. H. Misse, M. W. Upton : J. Chem. Soc. Dalton Trans., 1985, 1147. 11) K. J. Berry, F. Moya, K. S. Murray, A. M. B. Van Den Bergen, B. O. West : J. Chem. Soc. Dalton Trans., 1982, 109. 12) S. R. Sandler, W. Karo : “Organic Functional Group Preparation”, (1986), (Academic Press, New York). 13) R. Driouich, T. Takayanagi, M. Oshima, S. Motomizu : J. Chromatogr. A, 934, 95 (2001). 14) R. Driouich, T. Takayanagi, M. Oshima, S. Motomizu : Anal. Sci., 17, a343 (2001). 15) R. Driouich, T. Takayanagi, M. Oshima, S. Motomizu : J. Pharm. Biomed. Anal., 30, 1523 (2003). 16) R. Driouich, T. Takayanagi, M. Oshima, S. Motomizu : Electrophoresis, in Press. 17) K. K. Ngim, S. E. Ebeler, M. E. Lew, D. G. Crosby, J. W. Wong : J. Agr. Food Chem., 48, 3311 (2000)..
(6) 728. BUNSEKI. KAGAKU. Vol. 53 (2004). 要 旨 n -アルキルアミン類の分離定量法として,陰イオン性アルデヒドを誘導体化試薬として用いる吸光検出− 逆相分配高速液体クロマトグラフィーを検討した.誘導体化試薬としては,サリチルアルデヒド-5-スルホン 酸イオン(SAS)と 4-(4-スルホフェニルアゾ)-1-ヒドロキシ-2-ナフトアルデヒド(SPAHNA)を用いた.n アルキルアミンを含む試料溶液と試薬溶液はそれぞれの流路に同時に注入され,マージングゾーン法により オンラインで混合され,5 m,70℃ の反応コイル中で水溶性シッフ塩基へと誘導体化された.生成した水溶 性シッフ塩基は逆相カラムにより分離され,吸光検出された.オンライン誘導体化とカラム分離/検出を含 む分析時間は,SAS を用いた場合 25 分,SPAHNA を用いた場合は 18 分であった.アルキルアミン類に対 する検量線は 0 ∼ 50 µM の範囲で良好な直線性が得られ,検出限界は,SAS を用いた場合 0.5 ∼ 1.0 µM, SPAHNA を用いた場合は 0.08∼0.20 µM であった..
(7)
図
関連したドキュメント
生殖毒性分類根拠 NITEのGHS分類に基づく。 特定標的臓器毒性 特定標的臓器毒性単回ばく露 単回ばく露 単回ばく露分類根拠
色で陰性化した菌体の中に核様体だけが塩基性色素に
UVBVisスペクトルおよびCDスペクトル を測定し、Dabs-AAの水溶液中での会へ ロ
引火性液体 : 区分4 眼に対する重篤な損傷性/ : 区分2B 眼刺激性 警告 眼刺激 可燃性液体
図 21 のように 3 種類の立体異性体が存在する。まずジアステレオマー(幾何異 性体)である cis 体と trans 体があるが、上下の cis
定性分析のみ 1 検体あたり約 3~6 万円 定性及び定量分析 1 検体あたり約 4~10 万円
(F)ハロゲン化誘導体、スルホン化誘導体、ニトロ化誘導体、ニトロソ化誘導体 及びこれらの複合誘導体並びに 29.11 項、29.12 項、29.14 項、
3.8 ブラベンダービスコグラフィー ブラベンダービスコグラフを用い、乾燥した試料を 450ml の水で測 定容器に流し込み、液温が