平成
28 年度経済産業省委託事業
平成28年度化学物質安全対策(ナノ材料気管内投与試験
法等の国際標準化に関する調査)
調査報告書
平成29
年3月
国立研究開発法人産業技術総合研究所
目次
1.概要 ··· 3 2.気管内投与試験方法のラボ間比較試験の実施 ··· 4 2.1 試験の実施体制 ··· 4 2.2 試験の概要 ··· 4 2.3 手技や条件の共通化、及び条件の記録 ··· 6 2.4 酸化ニッケル(NiO)の肺内分布の確認 ··· 8 2.4.1 NiO の試料調製とキャラクタリゼーション ··· 8 2.4.2 NiO の定量方法 ··· 11 2.4.3 試験結果と解析 ··· 12 2.5 酸化ニッケル(NiO)の炎症反応の確認 ··· 18 2.5.1 試料調製とキャラクタリゼーション ··· 18 2.5.2 試験結果と解析(気管支肺胞洗浄液BALF 検査) ··· 19 2.5.3 試験結果と解析(病理組織学的検査) ··· 30 2.6 単層カーボンナノチューブ(SWCNT)の肺内分布の確認 ··· 37 2.6.1 SWCNT の試料調製とキャラクタリゼーション ··· 37 2.6.2 SWCNT の定量方法 ··· 39 2.6.3 試験結果と解析 ··· 40 2.7 多層カーボンナノチューブ(MWCNT)の肺内分布の確認 ··· 46 2.7.1 MWCNT の試料調製とキャラクタリゼーション ··· 46 2.7.2 MWCNT の定量方法 ··· 48 2.7.3 試験結果と解析 ··· 49 2.8 ラボ間比較試験のまとめ ··· 55 3.気管内投与試験方法の手順書の改良 ··· 56 4.気管内投与試験及び同等性判断基準に関するOECD/WPMN への発信 ··· 57 4.1 OECD/WPMN に対するガイダンス文書作成提案 ··· 57 4.2 OECD GD 39(吸入毒性試験に関するガイダンス)に対する意見表明 ··· 59 4.3 その他 ··· 61 4.3.1 リスク解析学会でのMETI ナノ安全 PJ 成果の発表 ··· 61 4.3.2 グルーピングとリードアクロスに関するOECD 専門家会合 ··· 61 5.気管内投与試験方法と同等性判断に関する情報収集 ··· 63 5.1 文献からの情報 ··· 63 5.1.1 気管内投与試験方法に関連した情報 ··· 635.2 METI ナノ安全 PJ の情報整理と再解析 ··· 68 5.2.1 吸入暴露試験での肺負荷量の個体差 ··· 68 5.2.2 肺負荷量とBALF データの関係 ··· 69 5.2.3 気管内投与試験における炎症反応の肺内分布 ··· 73 6.全体会議の開催と関係機関の情報共有 ··· 74 Appendix 1:試験方法の共通化 ··· 75 Appendix 2:試験条件・測定データの記録フォーマット ··· 82 Appendix 3:気管内投与試験の標準的手順書試案_ver.2 ··· 91
1.概要 ナノ材料の安全性評価手法である気管内投与試験方法と同等性判断基準の国際標準化に関する 活動を行った。具体的には、以下の通りである。 経済産業省「ナノ材料の安全・安心確保のための国際先導的安全性評価技術の開発」プロジェ クト(平成23 年度から 27 年度)(以降「METI ナノ安全 PJ」)で開発された気管内投与試験方法 について、5 つの動物試験機関によるラボ間比較試験を実施した。そこでは、粒子状の酸化金属 ナノ材料として酸化ニッケル(NiO)ナノ材料、2 種類の形状の異なるカーボンナノチューブ(CNT) として単層カーボンナノチューブ(SWCNT)と多層カーボンナノチューブ(MWCNT)を用い、 肺内分布の確認(3 材料)と炎症反応の確認(1 材料:NiO)を行った。そのために、それぞれの ナノ材料について、試料調製、キャラクタリゼーション、気管内投与試験、肺組織中ナノ材料分 析、気管支肺胞洗浄液検査(NiO のみ)、肺の病理組織学的検査(NiO のみ)等を実施した。 得られた知見に基づいて気管内投与方法に関する議論を行い、METI ナノ安全 PJ の成果物であ る「手順書 ラットを用いたナノ材料の気管内投与試験の標準的手法」(以降「手順書」)の改良 を行った。 気管内投与試験方法及び同等性判断基準に関する成果の発信としては、OECD WPMN(ナノ材 料作業部会)の第 16 回会合、ナノ材料の吸入毒性のテストガイドライン・ガイダンスに関する 専門家会合、リスク解析学会2016 年会に参加して、ガイダンス作成提案、意見表明、成果発信を 行った。 また、上記の検討及び成果発信において参照するための情報として、文献等の情報収集に加え て、METI ナノ安全 PJ で得られた知見の精査とデータ解析を実施した。 なお、本事業の推進にあたり、関係機関による全体会合を3 回実施した(第 1 回:2016 年 5 月 2 日、第 2 回:2016 年 12 月 5 日、第 3 回:2017 年 2 月 6 日)。
2.気管内投与試験方法のラボ間比較試験の実施 2.1 試験の実施体制 気管内投与試験のラボ間比較試験は、当該試験方法の経験を有する下記の5 機関において実施 した。 ・独立行政法人労働者健康安全機構日本バイオアッセイ研究センター(「バイオ」) ・一般財団法人化学物質評価研究機構(「CERI」) ・学校法人産業医科大学(「産業医大」) ・公益財団法人食品農医薬品安全性評価センター(「安評センター」) ・株式会社DIMS 医科学研究所(「DIMS」) 国立研究開発法人産業技術総合研究所(「産総研」)は、全体取りまとめ、投与に供する分散液 の調製とキャラクタリゼーション(NiO)、肺及び気管中のナノ材料分析(SWCNT と MWCNT)、 データの解析を担当した。被験試料のうち 2 種類の CNT に関しては、本事業の外部から下記の 2機関の協力を得た。 ・昭和電工株式会社(実施計画書「CNT_A に関する協力者」として) 協力内容: MWCNT の分散液の供給(試料調製とキャラクタリゼーション) ・単層CNT 融合新素材研究開発機構(実施計画書「CNT_B に関する協力者」として) 協力内容: SWCNT の分散液の供給(試料調製とキャラクタリゼーション) 肺及び気管中のSWCNT 分析 2.2 試験の概要 気管内投与試験は、METI ナノ安全 PJ の成果物である手順書に基づき、また、適宜、同じく METI ナノ安全 PJ の成果物である「気管内投与試験法を初期有害性情報取得の目的で用いる際のデー タ解釈上の留意点」「ナノ材料有害性の同等性判断評価のための試料調製とキャラクタリゼーシ ョンに関する技術解説書」を参照した。 試験設計は、実施計画書(仕様書)に記載された内容としたが、具体的な指示がされていなか った被験材料、投与用量、BALF 検査と病理組織学的検査に供する肺葉(右か左か)、BALF 検査 での測定項目としての蛋白かアルブミンかについては、実施機関との協議により決定した。用量 については、同様のナノ材料の過去の試験データに基づいて、下記の考え方に基づいて決定した。 肺内分布の確認(1用量:NiO、SWCNT、MWCNT) 分析の観点から高めの用量が望ましいが、顕著な有害性は生じない用量 炎症反応の確認(3用量:NiO) 高用量:影響あり、中用量:若干の影響、低用量:無影響となることを想定 試験内容の概要を表2.2-1 に示す。
表2.2-1 試験概要のまとめ
肺内分布の確認 炎症反応の確認
被験 材料
NiO ナ ノ 材 料 (US3352:US Research Nanomaterials 社):有害性既知の酸化金属 ナノ材料1材料(粒子状)として SWCNT(ZEONANO SG101:日本ゼオン株 式会社)とMWCNT(VGCF®-H:昭和電工 株式会社):性状の異なるカーボンナノチ ューブ2材料として
NiO ナ ノ 材 料 (US3352:US Research Nanomaterials 社):有害性既知の酸化金属 ナノ材料1材料(肺内分布の確認で使用し た材料)として 動物 雄SD ラット 8 週 同左 群構成 対照群(溶媒):各1 匹 1 用量:各 5 匹 対照群(溶媒):各5 匹 3 用量(公比 3):各 5 匹 用量 NiO:0.67 mg/kg SWCNT:1 mg/kg MWCNT:0.4 mg/kg NiO:0.2, 0.67, 2.0 mg/kg 投与 単回投与(イソフルラン麻酔下) 同左 観察 時期 投与後3 日 同左 観察 項目 肺の葉別(5 葉)及び気管の負荷量 BALF 検査(右肺) 総細胞、好中球比率、好中球数、LDH、 総蛋白 病理組織検査(左肺) 各機関で気管内投与する分散液の状態をなるべく揃えるため、一括で調製・発送された分散液 をほぼ同時期に気管内投与することとした。試験は2期に分けて実施し、下記の日程であった。 NiO、SWCNT の肺内分布の確認、NiO の炎症反応の確認 分散液の各機関への発送:2016 年 7 月 27 日 気管内投与試験: 2016 年 7 月 29 日:安評センター、DIMS 2016 年 8 月 1 日:バイオ、CERI、産業医大 MWCNT の肺内分布の確認 分散液の各機関への発送:2016 年 9 月 21 日 気管内投与試験: 2016 年 9 月 23 日:CERI、安評センター、DIMS 2016 年 9 月 26 日:バイオ、産業医大 なお、動物試験は、動物愛護の観点から、関連する各種法令・基準・指針等を遵守するととも に、気管内投与試験を実施する各機関における動物実験委員会等での審査・承認を経て実施した。
2.3 手技や条件の共通化、及び条件の記録 本事業では、各機関において、基本的に「手順書 ラットを用いたナノ材料の気管内投与試験 の標準的手法」に準じた試験を実施することとしたが、実際に試験を実施するにあたっては、手 技の詳細や条件を具体的に設定する必要がある。 手順書において共通化が望ましいとされている事項や、本事業の目的(=気管内投与試験方法 のラボ間比較)に照らして共通化が望ましい事項については、追加的に機関間の共通化を実施し た。また、手順書において試験実施機関の裁量とされている事項や、手順書に記載のない事項に ついては、各機関が通常行う手技や条件で実施することとし、その中で、試験結果を左右するか もしれない事項、及び通常の試験で記録することが一般的である事項については記録を残すこと とした。 表 2.3-1 に動物の準備と飼育環境について、表 2.3-2 に気管内投与のやり方について、表 2.3-3 に投与後の観察についての、手技や条件の共通化、及び条件の記録について整理した。なお、試 験条件や測定データの記録フォーマットは共通化した(Appendix 2) 表2.3-1 手技や条件の共通化、及び条件の記録:動物の準備と飼育環境 共通化の項目 内容 動物(ラット) 系統(SD)週齢(投与時8週齢)性(雄)の共通化に加えて、ブリーダーと 繁殖場まで統一することとし、一括で発注することとした(日本チャールズ リバー・厚木飼育センター)。 飼育環境 温度、湿度、換気回数、明暗サイクル、ケージの種類・サイズ、ケージあた り匹数※、飼料・飲料水の種類及び給仕・給水方法を記録することとした。 ※ 可能であれば1匹/ケージとするが、各機関の状況によって難しい場合 は、複数匹でもよいこととした。 表2.3-2 手技や条件の共通化、及び条件の記録:気管内投与のやり方 共通化の項目 内容 投与分散液の扱い 一括で供給し、取り扱いの方法等を共通化した(Appendix 1-A)。 投与器具 各機関が通常用いている器具として、共通化はしないこととした。 経口ゾンデ:3機関、スプレーヤー:2機関 器具の通過前後の粒径分布と濃度の確認を行うこととした。 投与時麻酔 イソフルラン吸入麻酔に統一した。条件(濃度、流量、時間、用いた装置な ど)を記録することとした。 投与時体位(保 定) 手順書に書かれている範囲で各機関の裁量とする。ただし詳細を記録するこ ととした。 投与器具挿入方法 及び位置 手順書に書かれている範囲で各機関の裁量とする。ただし詳細を記録するこ ととした。 投与液量 1 mL/kg 体重とした。 投与速度 手順書に書かれている範囲で各機関の裁量とする。ただし、動物への投与の 様子を動画で撮影することとした。 投与回数 1回の投与とした。 投与手順 手順書中の例示の書き方を参考に、実施した手順の詳細を記録することとし た。
表2.3-3 手技や条件の共通化、及び条件の記録:投与後の観察 共通化の項目 内容 一般観察 手順書に書かれている範囲で各機関の裁量とする。ただし詳細を記録するこ ととした。 解剖時麻酔 イソフルラン吸入麻酔に統一した。条件(濃度、流量、時間、用いた装置な ど)を記録することとした。 解剖、試料重量測 定 一連の流れを手順としてまとめて共有化した(Appendix 1-B, C)。 試料の送付の方法 と容器 用いる容器や条件等について共通化した(Appendix 1-A)。 病理組織学的検査 標本作成方法については、各機関の方法とするが、一連の流れを共有するこ ととした(Appendix 1-D)。また、所見と用語の共通化のため、METI ナノ安 全 PJ で実施された病理ピアレビューの報告書を回覧するとともに、結果の 入力フォーマットを作成することとした。 BALF 採取方法 右肺から採取することとした。各機関の方法で良いが、洗浄の強度としては ややマイルドな条件とすることとした。参考とするため右肺からのBALF 採 取方法を確立して例として共有した(Appendix 1-E)。
2.4 酸化ニッケル(NiO)の肺内分布の確認
2.4.1 NiO の試料調製とキャラクタリゼーション
各機関で投与に用いるNiO 分散液を調製し、そのキャラクラタリゼーション項目について確認
を行った。
NiO 分散液の調製は、NiO ナノ材料として US3352(US Research Nanomaterials, Inc., TX, USA)
を2 g 取り、50 mL の超純水中で 2 時間超音波に掛け(5510J-MT; Branson Ultrasonics Co., Danbury,
CT, USA)、その後 1000 g 20ºC で 30 分遠心した(CF16RXII and T15A41; Hitachi Koki Co., Ltd., Tokyo, Japan)。上澄液を 40 mL 採取して調製原液とした。200°C で乾燥させた(ON-300S; Asone Co., Osaka, Japan)後に重量を計測して(AUW220D; Shimadzu Co., Kyoto, Japan)、調製原液濃度を
求め、調製原液を超純水で希釈し、濃度を 0.67 mg/mL とした分散液を動物試験用に 5 機関へ供
与した。
1 次粒子径については、同じロットの原料について電子顕微鏡(S4800, Hitachi High-Technologies
Co., Tokyo, Japan)観察により計測したデータ(METI ナノ安全 PJ による)があり、20±8 nm で
ある(図2.4-1)。ガス吸着法により得られる比表面積についても同様に、51 m2/g の原料であり、
球形を仮定して一次粒径を推定すると18 nm となる。
動的光散乱(DLS; Zetasizer nano-ZS; Malvern Instruments Ltd., Worcestershire, UK)を用いて測定
した二次粒径は、個数平均で 47 nm であった。光散乱電気泳動法により同じ DLS 装置で測定し たゼータ電位は、23 mV であった。 表2.4-1 NiO 粉体と分散液のキャラクタリゼーション(US3352) 項目 値 測定方法 【粉体】 不純物 純度99.98+% カタログ値 1次粒子径 18 nm 20±8 nm 17.7nm カタログ値 TEM で 500 個計測の平均±SD 球形を仮定したBET 表面積からの換算粒径 密度 6.72 カタログ値 比表面積 50.5 m2/g BET 法・METI ナノ安全 PJ 報告値 【分散液】 媒体 超純水 NiO 濃度 0.72±0.01 mg/mL 酸分解後、ICP-MS 分析 2次粒子径 47 nm(試料調製直後) 53 nm(6 日後再分散)
動的光散乱 DLS(Zetasizer nano-ZS; Malvern
Instruments Ltd.)にて計測(個数基準平均径)
ゼータ電位 23 mV(試料調製直後)
27 mV(6 日後再分散)
光散乱電気泳動法(Zetasizer nano-ZS; Malvern
Instruments Ltd.)にて計測
電子顕微鏡像 図2.4-1 走査型電子顕微鏡(SEM)前プロジェクト報
告像
図2.4-1 US3352 の電子顕微鏡像(一次粒径) 各機関で使用するゾンデを用いて通過前後の投与液の粒径とゼータ電位に変化がないかの確認 を行った結果を図2.4-2 及び図 2.4-3 に示す。その結果、各機関のどのゾンデを用いても粒径やゼ ータ電位に大きな変化を引き起こすことはないことが確認された。 図2.4-2 ゾンデ通過前後の NiO 分散液の粒径(動的光散乱法による測定結果) 0 50 100 150 200 250 300 平均粒径 [nm ] 原液 バイオゾンデ CERIゾンデ 産業医大ゾンデ 安評ゾンデ DIMSゾンデ 原液 (2回目) 0.22 mg/mL mg/mL0.67 mg/mL2.0 mg/mL0.22 mg/mL0.67 mg/mL2.0 個数平均粒径 Z平均粒径 0 5 10 15 20 25 30 35 ゼー タ 電 位 [mV ] 原液(1回目) バイオゾンデ CERIゾンデ 産業医大ゾンデ 安評ゾンデ DIMSゾンデ 原液(2回目) 0.22 mg/mL 0.67 mg/mL mg/mL2.0
また、光学顕微鏡(ECLIPSE Ni-E; Nikon)を用いて、調製時及び各機関でのゾンデ通過後の投
与液を撮影した結果(図2.4-4)、ゾンデを通して投与する際に明らかな凝集が進んではいないこ
とが確認された。
2.4.2 NiO の定量方法
肺及び気管の試料は、左肺と右肺後葉については1.5 mL の 0.01M トリス塩酸・0.01M EDTA・
0.5%SDS の混合水溶液と 0.2 mL のプロテアーゼ K を追加し、右肺前葉・中葉・副葉・気管につ
いては0.7 mL の 0.01M トリス塩酸・0.01M EDTA・0.5%SDS の混合水溶液と 0.1mL のプロテアー
ゼK を追加し、それぞれ 45~50ºC で数時間超音波に掛けて(ASU6D, ASONE Co.)肺を分解して
均一な溶液を作成した。分散液約 0.02 mL もしくは肺分解液約 0.2 mL もしくは気管分解液全量 を秤取し、1 mL の硝酸と 0.2 mL の硫酸を追加して、220℃20 分のマイクロ波分解を行った。5% 硝酸になるように100 倍の希釈を行い、ICP-MS(ELEMENT XR; Thermofisher)により分析した。 超純水および左肺の分解液をそれぞれN=5 で分析し、測定された Ni を全て NiO だったとして ブランク値を求めたところ、それぞれ0.000062±0.000056 μg/mL および 0.043±0.056 μg/g であ った。10σを定量限界とすると、分散液と肺試料の定量限界は 0.00056μg/mL および 0.56μg/g と なり、本研究の目的に十分な分析の感度を有していることが確認された。 分散液中や臓器中の NiO の分析が共存物質の干渉を受けないかを確認するために、Ni 標準液 やNiO 分散液を肺試料等に一定量添加して分析する添加回収試験を行った。その結果、添加回収 率は総じて 90%以上であり(表 2.4-2)、臓器中の NiO を問題なく分析できることが確認された。 本分析法を用いて、動物試験に供与した分散液の濃度をN=3 で分析したところ、0.72±0.01 mg/mL と分析された。 表2.4-2 Ni 標準液及び NiO 分散液の添加回収試験結果 添加対象 添加液 回収率 [%] サンプル 数 Mean SD Blank (純水の酸処理試料) Ni 標準液 300ppb 104% 1.5% N=6 99.9% 2.3% N=6 101% 2.1% N=6 Blank (純水の酸処理試料) Ni 標準液 400ppb 101% 0.42% N=5 左肺 (酵素処理試料) 100% 0.15% N=5 US3352 分散液 (1.99 mg/mL) 91.9% 1.1% N=5 Blank (純水の酸処理試料) US3352 分散液 (1.99 mg/mL) 96.0% 1.1% N=5 左肺 (酵素処理試料) 96.1% 3.7% N=5 左肺 (酵素処理試料) US3352 分散液 (0.67 mg/mL) 94.6% 1.3% N=3
2.4.3 試験結果と解析 図2.4-5 から図 2.4-15 に、機関ごとの各葉の投与量に対する負荷量の割合を示す。図 2.4-5 から 図 2.4-9 は機関ごとに集計したグラフであり、図 2.4-10 から図 2.4-15 は葉ごとに集計したグラフ であり、どちらも同じデータをプロットしている。図中の黒点は各ラットのデータ、赤点は5 匹 のラットデータの平均値、青色バーは平均値±1 標準偏差を示す。図より、機関別の葉の分布は おおまかには同じ傾向であったものの、Lab A は後葉と左葉への分配比率がやや大きく、Lab B は 左葉への分配比率がやや大きいことが見て取れる。なお、表 2.4-3 に各機関の各葉の投与量に対 する負荷量の割合の平均値と標準偏差を示す。 図2.4-5 Lab A の投与量に対する各葉の負荷量の割合 図2.4-6 Lab B の投与量に対する各葉の負荷量の割合 Lab A 副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6
Lab B
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6図2.4-7 Lab C の投与量に対する各葉の負荷量の割合 図2.4-8 Lab D の投与量に対する各葉の負荷量の割合 図2.4-9 Lab E の投与量に対する各葉の負荷量の割合
Lab C
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6Lab D
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6Lab E
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6図2.4-10 各機関の投与量に対する前葉の負荷量の割合 図2.4-11 各機関の投与量に対する中葉の負荷量の割合 図2.4-12 各機関の投与量に対する副葉の負荷量の割合
前葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
中葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
副葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
図2.4-13 各機関の投与量に対する後葉の負荷量の割合 図2.4-14 各機関の投与量に対する左葉の負荷量の割合 図2.4-15 各機関の投与量に対する気管の負荷量の割合
後葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
左葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
気管
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
表2.4-3 各機関の各葉の投与量に対する負荷量の割合の平均値と標準偏差(単位はすべて%) Lab A Lab B Lab C Lab D Lab E
前葉 平均値 9.19 6.67 5.99 8.62 8.44 標準偏差 8.06 3.38 0.956 2.18 0.997 中葉 平均値 5.66 4.33 4.21 6.44 6.29 標準偏差 1.26 5.55 0.898 2.81 1.40 副葉 平均値 9.35 7.91 5.68 6.81 7.95 標準偏差 2.63 5.49 0.550 2.77 2.53 後葉 平均値 28.2 14.5 21.0 14.6 15.5 標準偏差 7.99 7.37 2.35 3.86 3.72 左葉 平均値 37.6 42.7 19.9 21.6 24.4 標準偏差 9.04 4.01 1.22 4.96 4.74 気管 平均値 0.143 0.327 0.0938 0.943 0.589 標準偏差 0.128 0.198 0.0661 0.171 0.402 次に、ラットごとに投与量に対する肺負荷量の総量の割合を計算し、図 2.4-16 及び表 2.4-4 に 示した。図中の黒点は各ラットのデータ、赤点は5 匹のラットデータの平均値、青色バーは平均
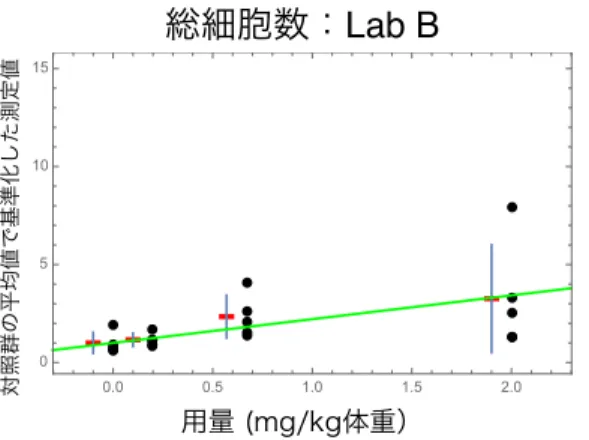
値±1 標準偏差を示す。LabB, Lab D, Lab E では他のラットに比べやや少ないラットもあることが 見て取れる。
図2.4-16 各機関の投与量に対する肺負荷量の総量の割合
表 2.4-4 各機関の肺負荷量の総量の投与量に対する割合の平均値と標準偏差(単位はすべて%)
Lab A Lab B Lab C Lab D Lab E
平均値 90.2 76.4 56.8 59.0 63.2
標準偏差 4.68 13.2 2.20 7.31 5.00
気管内投与試験のラボ間比較を定量的に行うために、ISO 5725-2:1994 (Accuracy (trueness and
precision) of measurement methods and results -- Part 2: Basic method for the determination of
repeatability and reproducibility of a standard measurement method) を参考に、左肺の負荷量の投与量 に対する割合と右肺の負荷量(前葉、中葉、副葉、後葉の負荷量の合計)の投与量に対する割 合の精度を算出した。ここで、病理組織学的検査を左葉で、気管支肺胞洗浄液BALF 検査を右 肺でそれぞれ行っため、左肺と右肺それぞれに着目するものとした。なお、ラットごとに右肺
肺の総量
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.2 0.4 0.6 0.8 1.0
の負荷量の総量の投与量に対する割合を計算し、図2.4-17 と表 2.4-5 に示した。図中の黒点は各
ラットのデータ、赤点は5 匹のラットデータの平均値、青色バーは平均値±1 標準偏差を示す。
図2.4-17 各機関の投与量に対する右肺負荷量の総量の割合
表2.4-5 各機関の右肺負荷量の総量の投与量に対する割合の平均値と標準偏差(単位はすべて%)
Lab A Lab B Lab C Lab D Lab E
平均値 52.4 33.4 36.9 36.4 38.1 標準偏差 11.6 13.0 2.48 7.76 6.01 ISO 5725-2 に規定されている検定方法により、各機関の分散及び各機関の平均値に統計的外 れ値がないことが確認された。そのため、得られた全てのデータを用いて、左肺負荷量の投与 量に対する割合と右肺負荷量の投与量に対する割合の精度をそれぞれ算出した。その結果を表 2.4-6 に示す。 表2.4-6 NiO の左肺負荷量及び右肺負荷量の投与量に対する割合の精度(単位はすべて%) 一般平均 併行標準偏差 再現標準偏差 左肺負荷量の投与量に対する割合 29.2 5.41 11.3 右肺負荷量の投与量に対する割合 39.5 9.00 11.0 最後に、ラボ間差の有無を定量的に確認するために、併行分散と室間分散(再現分散—併行分 散)の比の検定を左肺負荷量の投与量に対する割合と右肺負荷量の投与量に対する割合のそれ ぞれについて行った。その結果、左肺負荷量の投与量に対する割合については、有意水準片側 5%で「ラボ間差がある」との結論が導かれた。一方、右肺負荷量の投与量に対する割合につい ては、有意片側水準5%で「ラボ間差があるとは言えない」との結論が導かれた。
右肺の総量
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.2 0.4 0.6 0.8 1.0
2.5 酸化ニッケル(NiO)の炎症反応の確認
2.5.1 NiO の試料調製とキャラクタリゼーション
NiO の肺内分布の確認(2.4節)に合わせて調製を行い、濃度を 0.22 mg/mL、0.67 mg/mL、
2.0 mg/mL に希釈した分散液を動物試験用に 5 機関へ供与した。キャラクタリゼーションの結果
は表2.5-1 に示した。
動的光散乱(DLS;Zetasizer nano-ZS; Malvern Instruments Ltd., Worcestershire, UK)を用いて測定
した二次粒径は、個数平均で90 nm(0.22 mg/mL)、47 nm(0.67 mg/mL)、60 nm(2.0 mg/mL)で あった。同じDLS 装置で光散乱電気泳動法により測定したゼータ電位は、20 mV(0.22 mg/mL)、 23 mV(0.67 mg/mL)、30 mV(2.0 mg/mL)であった。 2.4.2節に示した分析法を用いて、動物試験に供与した分散液の濃度をN=3 で分析したと ころ、3 濃度の分散液はそれぞれ 0.23±0.004 mg/mL、0.72±0.01 mg/mL、2.1±0.05 mg/mL と分析 された。 表2.5-1 NiO 粉体と分散液のキャラクタリゼーション(US3352) 項目 値 測定方法 【粉体】 不純物 純度99.98+% カタログ値 1次粒子径 18 nm 20±8 nm 17.7nm カタログ値 TEM で 500 個計測の平均±SD 球形を仮定したBET 表面積からの換算粒径 密度 6.72 カタログ値 比表面積 50.5 m2/g BET 法 【分散液】 媒体 超純水 NiO 濃度 0.22 mg/mL : 0.23±0.004 mg/mL 0.67 mg/mL: 0.72±0.01 mg/mL 2.0 mg/mL: 2.1±0.05 mg/mL 酸分解後、ICP-MS 分析 2次粒子径 0.22 mg/mL 90 nm(試料調製直後) 76 nm(6 日後再分散) 0.67 mg/mL 47 nm(試料調製直後) 53 nm(6 日後再分散) 2.0 mg/mL 60 nm(試料調製直後) 60 nm(6 日後再分散)
動的光散乱 DLS(Zetasizer nano-ZS; Malvern
Instruments Ltd.)にて計測(個数基準平均径)
ゼータ電位 23 mV(試料調製直後)
27 mV(6 日後再分散)
光散乱電気泳動法(Zetasizer nano-ZS; Malvern
Instruments Ltd.)にて計測 電 子 顕 微 鏡 像 図2.4-1 走査型電子顕微鏡(SEM):METI ナノ安全 PJ 報告像 等電位点 12.5 以上 METI ナノ安全 PJ 報告値
2.5.2 試験結果と解析(気管支肺胞洗浄液BALF 検査)
はじめに、各機関のデータを相互に比較可能にするために、報告値を検査項目ごと機関ごとに 対照群の平均値で基準化した。そして、対照群の平均値に対しての倍率に着目し、報告値の解析
を進めた。基準化に用いた値を表2.5-2 に示す。
表2.5-2 データの基準化に用いた対照群の平均値の一覧
Lab A Lab B Lab C Lab D Lab E
総細胞数 (cells/μL) 184 140 84.26 268 492 好中球比率 (%) 0.734 0.34 0.60 0.80 16.38 好中球数 (cells/μL) 3.8 (個/500) 0.64 0.76 2 78
LDH (U/L) 35.6 (mg/dL) 61.4 180.64 (U/L) (U/L) 57.8 (U/L) 38.6
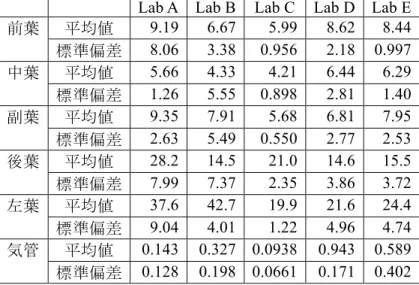
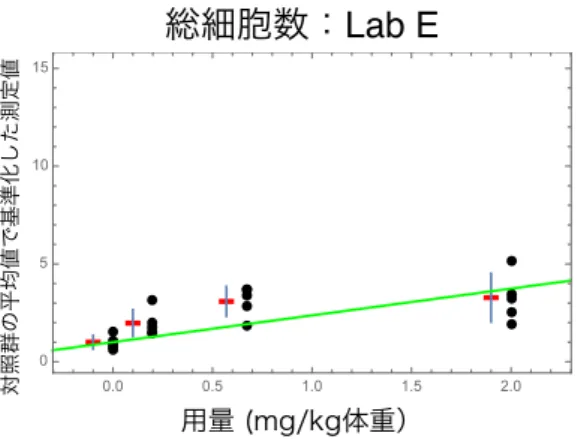
総蛋白 (μg/ml) 77.8 9.42 71.50 90.4 8.34 図2.5-1 から図 2.5-5 に総細胞数の結果を示す。図中の黒点は各ラットの報告値を対照群の平均 値で基準化したデータ、赤点は5 匹のラットデータの平均値、青色バーは平均値±1 標準偏差を 示す。また、緑色の直線は、切片を1 に固定した回帰モデルを黒点で示すデータに当てはめた際 の回帰直線を表す。 図2.5-1 Lab A の総細胞数の報告値を対照群の平均値で基準化したデータのグラフ
総細胞数:Lab A
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15図2.5-2 Lab B の総細胞数の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-3 Lab C の総細胞数の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-4 Lab D の総細胞数の報告値を対照群の平均値で基準化したデータのグラフ
総細胞数:Lab B
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15総細胞数:Lab C
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15総細胞数:Lab D
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15図2.5-5 Lab E の総細胞数の報告値を対照群の平均値で基準化したデータのグラフ 図 2.5-6 から図 2.5-10 に好中球比率の結果を示す。図中の黒点は各ラットの報告値を対照群の 平均値で基準化したデータ、赤点は5 匹のラットデータの平均値、青色バーは平均値±1 標準偏 差を示す。また、緑色の直線は、切片を1 に固定した回帰モデルを黒点で示すデータに当てはめ た際の回帰直線を表す。 図2.5-6 Lab A の好中球比率の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-7 Lab B の好中球比率の報告値を対照群の平均値で基準化したデータのグラフ
総細胞数:Lab E
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15好中球比率:Lab A
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 50 100 150 200好中球比率:Lab B
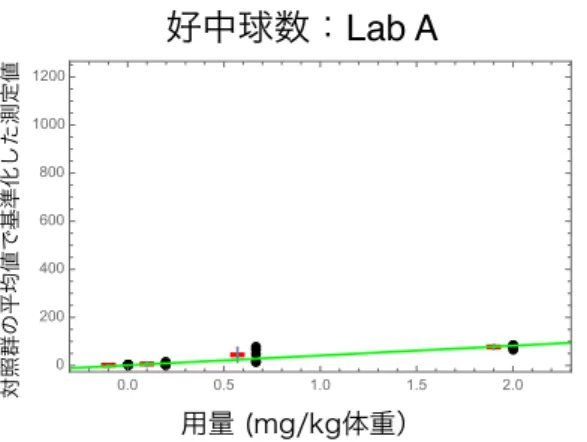
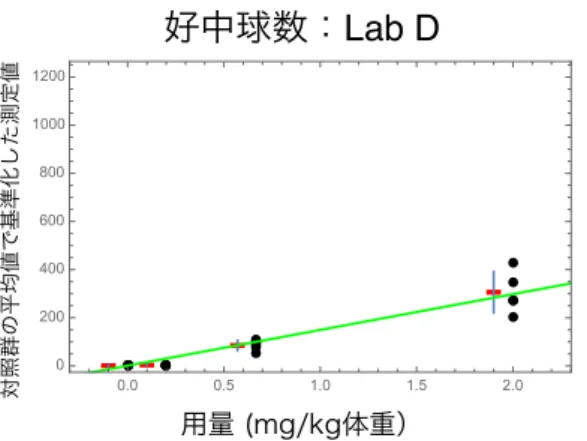
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 50 100 150 200図2.5-8 Lab C の好中球比率の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-9 Lab D の好中球比率の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-10 Lab E の好中球比率の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-11 から図 2.5-15 に好中球数の結果を示す。図中の黒点は各ラットの報告値を対照群の平 均値で基準化したデータ、赤点は 5 匹のラットデータの平均値、青色バーは平均値±1 標準偏差 を示す。また、緑色の直線は、切片を1 に固定した回帰モデルを黒点で示すデータに当てはめた 際の回帰直線を表す。
好中球比率:Lab C
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 50 100 150 200好中球比率:Lab D
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 50 100 150 200好中球比率:Lab E
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 50 100 150 200図2.5-11 Lab A の好中球数の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-12 Lab B の好中球数の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-13 Lab C の好中球数の報告値を対照群の平均値で基準化したデータのグラフ
好中球数:Lab A
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 200 400 600 800 1000 1200好中球数:Lab B
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 200 400 600 800 1000 1200好中球数:Lab C
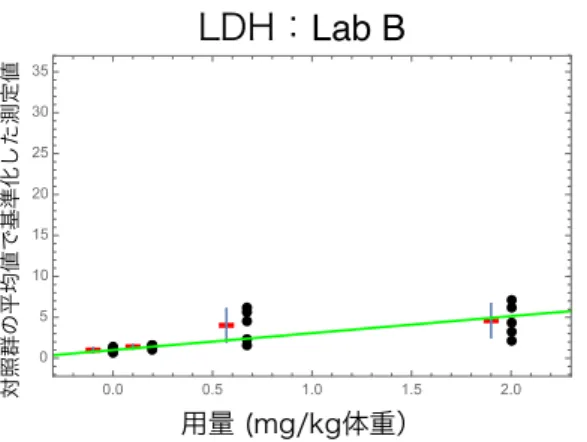
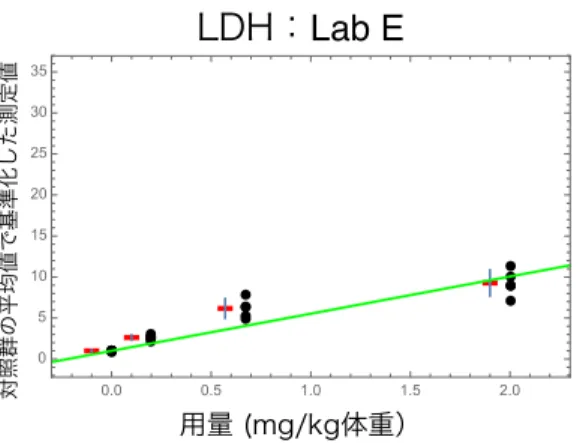
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 200 400 600 800 1000 1200図2.5-14 Lab D の好中球数の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-15 Lab E の好中球数の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-16 から図 2.5-20 に LDH の結果を示す。図中の黒点は各ラットの報告値を対照群の平均 値で基準化したデータ、赤点は5 匹のラットデータの平均値、青色バーは平均値±1 標準偏差を 示す。また、緑色の直線は、切片を1 に固定した回帰モデルを黒点で示すデータに当てはめた際 の回帰直線を表す。 図2.5-16 Lab A の LDH の報告値を対照群の平均値で基準化したデータのグラフ
好中球数:Lab D
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 200 400 600 800 1000 1200好中球数:Lab E
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 200 400 600 800 1000 1200LDH:Lab A
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15 20 25 30 35図2.5-17 Lab B の LDH の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-18 Lab C の LDH の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-19 Lab D の LDH の報告値を対照群の平均値で基準化したデータのグラフ
LDH:Lab B
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15 20 25 30 35LDH:Lab C
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15 20 25 30 35LDH:Lab D
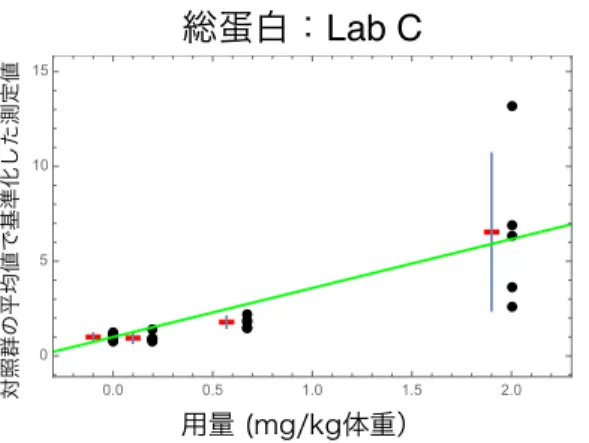
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15 20 25 30 35図2.5-20 Lab E の LDH の報告値を対照群の平均値で基準化したデータのグラフ 図2.5-21 から図 2.5-25 に総蛋白の結果を示す。図中の黒点は各ラットの報告値を対照群の平均 値で基準化したデータ、赤点は5 匹のラットデータの平均値、青色バーは平均値±1 標準偏差を 示す。また、緑色の直線は、切片を1 に固定した回帰モデルを黒点で示すデータに当てはめた際 の回帰直線を表す。 図4.5-21 Lab A の総蛋白の報告値を対照群の平均値で基準化したデータのグラフ 図4.5-22 Lab B の総蛋白の報告値を対照群の平均値で基準化したデータのグラフ 用量 (mg/kg体重)
LDH:Lab E
対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15 20 25 30 35総蛋白:Lab A
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15総蛋白:Lab B
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15図4.5-23 Lab C の総蛋白の報告値を対照群の平均値で基準化したデータのグラフ 図4.5-24 Lab D の総蛋白の報告値を対照群の平均値で基準化したデータのグラフ 図4.5-25 Lab E の総蛋白の報告値を対照群の平均値で基準化したデータのグラフ 表2.5-3 から表 2.5-7 に、総細胞数、好中球比率、好中球数、LDH、総蛋白、それぞれの回帰 係数の平均値及び95%信頼上限、95%信頼下限を示す。すべての機関のすべての観察項目につ いて、回帰係数の95%信頼区間は 0 をまたいでいない。そのため、帰無仮説「回帰直線の傾き が0 である」は、すべての機関のすべての観察項目について有意水準 5%で棄却されることとな る。よって、すべての機関のすべての観察項目について、正の用量反応関係が観察されたと結 論づけられる。
総蛋白:Lab C
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15総蛋白:Lab D
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15総蛋白:Lab E
用量 (mg/kg体重) 対照群の平均値で基準化した測定値 0.0 0.5 1.0 1.5 2.0 0 5 10 15表2.5-3 各機関の総細胞数における回帰係数の平均値及び 95%信頼上限と 95%信頼下限 機関 平均値 信頼上限 信頼下限 Lab A 1.33 1.63 1.04 Lab B 1.21 1.84 0.59 Lab C 3.69 5.12 2.26 Lab D 1.71 2.03 1.40 Lab E 1.37 1.84 0.90 表2.5-4 各機関の好中球比率における回帰係数の平均値及び 95%信頼上限と 95%信頼下限 機関 平均値 信頼上限 信頼下限 Lab A 42.11 49.95 34.26 Lab B 77.08 96.05 58.10 Lab C 26.96 33.79 20.13 Lab D 34.10 39.85 28.35 Lab E 1.39 1.71 1.06 表2.5-5 各機関の好中数における回帰係数の平均値及び 95%信頼上限と 95%信頼下限 機関 平均値 信頼上限 信頼下限 Lab A 40.64 48.21 33.06 Lab B 203.97 298.89 109.06 Lab C 150.34 208.89 91.80 Lab D 148.56 167.84 129.29 Lab E 6.27 8.14 4.39 表2.5-6 各機関の LDH における回帰係数の平均値及び 95%信頼上限と 95%信頼下限 機関 平均値 信頼上限 信頼下限 Lab A 4.60 5.13 4.07 Lab B 2.07 2.78 1.36 Lab C 6.70 8.68 4.72 Lab D 3.74 4.12 3.35 Lab E 4.53 5.21 3.85 表2.5-7 各機関の総蛋白における回帰係数の平均値及び 95%信頼上限と 95%信頼下限 機関 平均値 信頼上限 信頼下限 Lab A 2.26 2.84 1.67 Lab B 1.61 2.17 1.06 Lab C 2.58 3.47 1.70 Lab D 2.66 3.02 2.30 Lab E 2.04 2.44 1.63
次に参考までに、米国環境保護庁 (US EPA) が開発し無償で公開している Benchmark Dose Software (BMDS) 2.6 を利用し、気管支肺胞洗浄液 BALF 検査のデータから各機関の各観察項目
について動物試験におけるNOEL に相当すると考えられている Benchmark dose (BMD) と BMD
の安全側の信頼下限値であるBenchmark dose lower confidence limit (BMDL) を算出した。表 2.5-8
表2.5-8 各機関の総細胞数における BMD と BMDL 機関 BMD BMDL Lab A 0.137 0.059 Lab B 0.673 0.169 Lab C 0.520 0.148 Lab D 0.620 0.235 Lab E 0.162 0.042 表2.5-9 各機関の好中球比率における BMD と BMDL 機関 BMD BMDL Lab A 0.320 0.133 Lab B 0.392 0.180 Lab C 0.921 0.413 Lab D 0.311 0.156 Lab E 0.312 0.166 表2.5-10 各機関の好中球数における BMD と BMDL 機関 BMD BMDL Lab A 0.320 0.133 Lab B 0.666 0.236 Lab C 0.910 0.383 Lab D 0.492 0.212 Lab E 0.313 0.128 表2.5-11 各機関の LDH における BMD と BMDL 機関 BMD BMDL Lab A 0.186 0.090 Lab B 0.325 0.146 Lab C 0.883 0.360 Lab D 0.254 0.113 Lab E 0.123 0.058 表2.5-12 各機関の総蛋白における BMD と BMDL 機関 BMD BMDL Lab A 0.298 0.117 Lab B 0.357 0.123 Lab C 0.731 0.436 Lab D 0.311 0.134 Lab E 0.161 0.080
2.5.3 試験結果と解析(病理組織学的検査) 病理組織学的検査の結果を図示するために、各所見に付されたグレード「−,±, +, ++, +++」 をそれぞれスコア「0, 1, 2, 3, 4」に対応させ、5 値データに変換した。図 2.5-26 から図 2.5-44 に、 各所見の各用量について、ラット5 匹のスコアの平均値を機関別に青点で示す。 図2.5-26 所見「被験物質の沈着:肺胞マクロファージ内」の機関別用量別スコアの平均値 図2.5-27 所見「被験物質の沈着:肺胞腔内(非貪食)」の機関別用量別スコアの平均値 図2.5-28 所見「被験物質の沈着:肺胞壁内(非貪食)」の機関別用量別スコアの平均値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 被験物質の沈着:肺胞マクロファージ内
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 被験物質の沈着:肺胞腔内(非貪食)
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 被験物質の沈着:肺胞壁内(非貪食)
図2.5-29 所見「被験物質の沈着:気管支周囲リンパ組織内(貪食)」の 機関別用量別スコアの平均値
図2.5-30 所見「被験物質の沈着:気管支周囲リンパ組織内(非貪食)」の
機関別用量別スコアの平均値
図2.5-31 所見「肺胞マクロファージ:増加」の機関別用量別スコアの平均値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 被験物質の沈着:気管支周囲リンパ組織内(貪食)
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 被験物質の沈着:気管支周囲リンパ組織内(非貪食)
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肺胞マクロファージ:増加
図2.5-32 所見「肺胞マクロファージ:変性/壊死」の機関別用量別スコアの平均値
図2.5-33 所見「炎症細胞浸潤:肺胞腔/肺胞壁」の機関別用量別スコアの平均値
図2.5-34 所見「炎症細胞浸潤:気管支周囲」の機関別用量別スコアの平均値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肺胞マクロファージ:変性/壊死
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 炎症細胞浸潤:肺胞腔/肺胞壁
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 炎症細胞浸潤:気管支周囲
図2.5-35 所見「炎症細胞浸潤:血管周囲」の機関別用量別スコアの平均値
図2.5-36 所見「II 型肺胞上皮細胞の増生」の機関別用量別スコアの平均値
図2.5-37 所見「肺胞壁の線維化」の機関別用量別スコアの平均値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 炎症細胞浸潤:血管周囲
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 II型肺胞上皮細胞の増生
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肺胞壁の線維化
図2.5-38 所見「肺胸膜の線維化」の機関別用量別スコアの平均値
図2.5-39 所見「肉芽形成」の機関別用量別スコアの平均値
図2.5-40 所見「肉芽形成:気管支周囲リンパ組織」の機関別用量別スコアの平均値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肺胸膜の線維化
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肉芽形成
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肉芽形成:気管支周囲リンパ組織
図2.5-41 所見「出血」の機関別用量別スコアの平均値
図2.5-42 所見「肺胞蛋白症」の機関別用量別スコアの平均値
図2.5-43 所見「気管支上皮:変性/変死」の機関別用量別スコアの平均値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 出血
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 肺胞蛋白症
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 気管支上皮:変性/壊死
図2.5-44 所見「気管支上皮:増生」の機関別用量別スコアの平均値 次に、機関ごと所見ごとに、用量反応関係が認められるかを確認するために、ヨンキーの傾向 検定を行った。この検定は、スコアが単調増加であることを前提に、対立仮説を「対照群≦低用 量群≦中用量群≦高用量群」とする傾向検定である。また、データを順位データとして扱うノン パラメトリックな方法である。表2.5-13 に帰無仮説を「用量依存性がない」とした際の P 値の一 覧を示した。表中において「NA」は 5 匹のラットすべてにおいて該当所見が観察されなかったこ とを示す。また、有意水準 5%で有意であった箇所は赤く塗りつぶしている。表 2.5-13 より、用 量反応関係の有無は、すべての所見において4 機関以上は揃っていることがわかる。 表2.5-13 各機関の各所見におけるヨンキーの傾向検定の P 値
Lab A Lab B Lab C Lab D Lab E
0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 0 1 2 3 4 0.0 0.5 1.0 1.5 2.0 用量 (mg/kg体重) 病理所見スコアの平均値 気管支上皮:増生
Lab A Lab B Lab C Lab D Lab E
( ) 0.0020 0.0000 0.0000 0.0000 0.0000 I 0.0010 0.0000 NA 0.0000 0.0000 I NA NA NA NA NA / I NA NA NA NA NA / I NA NA NA NA NA ( ) 0.0000 0.0000 0.0000 0.0000 0.0000 ( ) 0.0010 NA NA NA NA 0.0000 0.0000 0.0000 0.0000 0.0000 0.0000 0.0000 0.0000 0.0000 0.3320 0.0000 0.0030 0.0000 0.0000 0.1270 : 0.0260 0.0070 0.0170 0.0000 0.0000 NA NA NA 0.0260 NA NA NA NA NA NA NA NA NA NA 0.0260 / NA NA NA NA NA NA 0.3270 NA 0.2800 NA 0.0900 NA NA NA NA 0.0900 NA NA NA 0.0000 0.0000 0.0000 0.0000 0.0000 0.0000
2.6 単層カーボンナノチューブ(SWCNT)の肺内分布の確認 2.6.1 SWCNT の試料調製とキャラクタリゼーション 技術研究組合単層CNT 融合新材料研究開発機構(TASC)により実施された NEDO プロジェク ト「ナノ炭素材料及びその応用製品の排出・暴露評価技術の確立」(平成26 年度から 28 年度)の 成果である「ナノ炭素材料の安全性試験総合手順書」(技術研究組合単層CNT 融合新材料研究開 発機構(TASC)、産業技術総合研究所 2017)に示されている方法に従い、超音波処理及び遠心分 離を用いて、ZEONANO SG101(日本ゼオン株式会社)の分散液を 1.0 mg/mL で調製した。 調製したSWCNT 分散液を 20 倍・50 倍・100 倍希釈して、凝集径(球形を仮定)及びゼータ電 位を、2.4.1節と同じDLS 装置により測定したところ、191 nm、185 nm、180 nm、及び、-38.4 mV、-32.1 mV、-15.7 mV であった。TEM により撮影した分散液中の SWCNT を図 2.6-1 に示 す。このTEM の画像から SWCNT の径及び長さを求めた結果を図 2.6-2、表 2.6-1 に示す。 図2.6-1 SWCNT 分散液の TEM 画像 図2.6-2 分散液中の SWCNT の長さ及び幅の分布
表2.6-1 SWCNT 粉体と分散液のキャラクタリゼーション(ZEONANO SG101) 項目 値 測定方法 【粉体】 不純物 Fe 0.011%, Al 0.0015% NEDO プロジェクト報告値 1次粒子径 平均繊径:19 nm 平均繊維長:283 nm TEM で 500 個計測の平均±SD 比表面積 1000 m2/g 以上(未開口) カタログ値 【分散液】 媒体 BSA 水溶液 SWCNT 濃度 0.97±0.02 mg/mL 酸分解後、ICP-MS 分析 2次粒子径 20 倍希釈 191 nm(試料調製直後) 190 nm(8 日後再分散) 50 倍希釈 185 nm(試料調製直後) 181 nm(8 日後再分散) 100 倍希釈 180 nm(試料調製直後)
動的光散乱 DLS(Zetasizer nano-ZS; Malvern
Instruments Ltd.)にて計測(個数基準平均径) ゼータ電位 20 倍希釈 -38 mV(試料調製直後) -40 mV(8 日後再分散) 50 倍希釈 -32 mV(試料調製直後) -31 mV(8 日後再分散) 100 倍希釈 -16 mV(試料調製直後)
光散乱電気泳動法(Zetasizer nano-ZS; Malvern
Instruments Ltd.)にて計測 電子顕微鏡像 図2.6-1 透過型電子顕微鏡(TEM) また、2.4.1節と同じ光学顕微鏡を用いて、調製時及び各機関でのゾンデ通過後の投与液を 撮影した結果(図2.6-3)、ゾンデを通して投与する際に明らかな凝集が進んではいないことが確 認された。 図2.6-3 SWCNT 分散液の光学顕微鏡像の一例(左:調製後、右:バイオ投与時ゾンデ通過
後) 各機関で使用するゾンデを用いて通過前後の投与液の粒径とゼータ電位に変化がないかの確認 を行った結果を図2.6-4 及び図 2.6-5 に示す。その結果、各機関のどのゾンデを用いても粒径やゼ ータ電位に大きな変化を引き起こすことはないことが確認された。 図2.6-4 ゾンデ通過前後の SWCNT 分散液の粒径(動的光散乱法による測定結果) 図2.6-5 ゾンデ通過前後の SWCNT 分散液のゼータ電位(光散乱電気泳動法による測定結果) 2.6.2 SWCNT の定量方法 基本的には、「ナノ炭素材料の安全性試験総合手順書」(技術研究組合単層 CNT 融合新材料研 究開発機構(TASC)、産業技術総合研究所 2017)に準じて、肺や気管の酵素分解後に紫外領域 (700nm~800nm)の吸光度を測定する方法で SWCNT 濃度の分析を行った。ただし、これまで 左肺のみや全肺での測定例しかないため、右肺各葉や気管に対して同様の手法が適用可能かどう か、必要な酵素量がどの程度かについての検討をし、十分に肺の分解が進み700nm~800nm の吸 光度のバックグラウンド値が十分に低くなる条件を確立して分析を実施した。N=5 で測定した調 製原液濃度は、0.97±0.02 mg/mL であった。 0 50 100 150 200 250 300 平均粒径 [nm ] 原液 バイオゾンデ CERIゾンデ 産業医大ゾンデ 安評ゾンデ DIMSゾンデ 原液 (2回目) 2.0 mg/mL mg/mL2.0 個数平均粒径 Z平均粒径 -30 -25 -20 -15 -10 -5 0 ゼー タ 電 位 [m V] バイオゾンデ CERIゾンデ 産業医大ゾンデ 安評ゾンデ DIMSゾンデ 原液 2.0 mg/mL
2.6.3 試験結果と解析 図2.6-6 から図 2.6-16 に、機関ごとの各葉の投与量に対する負荷量の割合を示す。図 2.6-6 から 図2.6-10 は機関ごとに集計したグラフで、図 2.6-11 から図 2.6-16 は葉ごとに集計したグラフであ り、どちらも同じデータをプロットしている。図中の黒点は各ラットのデータ、赤点は5 匹のラ ットデータの平均値、青色バーは平均値±1 標準偏差を示す。図より、機関別の葉の分布はおお まかには同じ傾向であったものの、Lab C は、左葉への分配比率がやや大きいことが見て取れる。 なお、表2.6-2 に各機関の各葉の投与量の割合に対する負荷量の平均値と標準偏差を示す。 図2.6-6 Lab A の投与量に対する各葉の負荷量の割合 図2.6-7 Lab B の投与量に対する各葉の負荷量の割合 図2.6-8 Lab C の投与量に対する各葉の負荷量の割合
Lab A
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6Lab B
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6Lab C
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6図2.6-9 Lab D の投与量に対する各葉の負荷量の割合 図2.6-10 Lab E の投与量に対する各葉の負荷量の割合 図2.6-11 各機関の投与量に対する前葉の負荷量の割合
Lab D
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6Lab E
副葉 前葉 中葉 後葉 左葉 気管 負荷量の割合(対投与量) 0.0 0.1 0.2 0.3 0.4 0.5 0.6前葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
図2.6-12 各機関の投与量に対する中葉の負荷量の割合 図2.6-13 各機関の投与量に対する副葉の負荷量の割合 図2.6-14 各機関の投与量に対する後葉の負荷量の割合
中葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
副葉
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
後葉
Lab A負荷量の割合(対投与量) 0.0 Lab B Lab C Lab D Lab E 0.1 0.2 0.3 0.4 0.5 0.6
図2.6-15 各機関の投与量に対する左葉の負荷量の割合
図2.6-16 各機関の投与量に対する気管の負荷量の割合
左葉
Lab A
負荷量の割合(対投与量)
Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
気管
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.1 0.2 0.3 0.4 0.5 0.6
表2.6-2 各機関の各葉の投与量に対する負荷量の割合の平均値と標準偏差(単位はすべて%) Lab A Lab B Lab C Lab D Lab E
前葉 平均値 9.62 8.72 4.73 10.8 9.94 標準偏差 4.13 5.13 1.77 6.35 3.20 中葉 平均値 8.24 7.63 2.79 3.65 7.63 標準偏差 2.57 4.17 1.81 2.92 2.59 副葉 平均値 10.5 10.3 5.22 5.39 11.3 標準偏差 3.43 4.76 2.70 4.23 4.33 後葉 平均値 24.5 25.4 16.3 20.5 25.7 標準偏差 4.60 10.9 5.59 12.1 7.10 左葉 平均値 32.4 30.5 46.4 28.1 27.18 標準偏差 7.90 10.1 6.75 12.8 13.1 気管 平均値 0.0430 0.868 0.313 0.391 0.561 標準偏差 0.0515 1.76 0.107 0.243 0.623 次に、ラットごとに肺負荷量の総量の投与量に対する割合を計算し、図 2.6-17 及び表 2.6-3 に 示した。図中の黒点は各ラットのデータ、赤点は5 匹のラットデータの平均値、青色バーは平均 値±1 標準偏差を示す。LabB と Lab D では他のラットに比べ極端に少ないラットもあることが見 て取れる。 図2.6-17 各機関の投与量に対する肺負荷量の総量の割合 表 2.6-3 各機関の肺負荷量の総量の投与量に対する割合の平均値と標準偏差(単位はすべて%)
Lab A Lab B Lab C Lab D Lab E
平均値 85.2 83.5 75.7 68.8 82.3
標準偏差 7.24 17.6 3.25 26.8 8.18
気管内投与試験のラボ間比較を定量的に行うために、ISO 5725-2:1994 (Accuracy (trueness and
precision) of measurement methods and results -- Part 2: Basic method for the determination of
repeatability and reproducibility of a standard measurement method) を参考に、左肺の負荷量の投与量 に対する割合と右肺の負荷量(前葉、中葉、副葉、後葉の負荷量の合計)の投与量に対する割 合の精度を算出した。ここで、病理組織学的検査を左葉で、気管支肺胞洗浄液BALF 検査を右 肺でそれぞれ行うため、左肺と右肺それぞれに着目するものとした。なお、ラットごとに右肺
肺の総量
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.2 0.4 0.6 0.8 1.0
の負荷量の総量の投与量に対する割合を計算し、図2.6-18 と表 2.6-4 に示した。図中の黒点は各
ラットのデータ、赤点は5 匹のラットデータの平均値、青色バーは平均値±1 標準偏差を示す。
図2.6-18 各機関の投与量に対する右肺負荷量の総量の割合
表2.6-4 各機関の右肺負荷量の総量の投与量に対する割合の平均値と標準偏差(単位はすべて%)
Lab A Lab B Lab C Lab D Lab E
平均値 52.8 52.1 29.0 40.3 54.6 標準偏差 5.95 10.4 8.26 16.7 15.3 ISO 5725-2 に規定されている検定方法に従い各機関の分散及び各機関の平均値に統計的外れ 値がないことが確認された。そのため、得られた全てのデータを用いて、左肺負荷量の投与量 に対する割合と右肺負荷量の投与量に対する割合の精度をそれぞれ算出した。その結果を表 2.6-5 に示す。 表 2.6-5 SWCNT の左肺負荷量及び右肺負荷量の投与量に対する割合の精度(単位はすべて%) 一般平均 併行標準偏差 再現標準偏差 左肺負荷量の投与量に対する割合 32.9 10.4 12.2 右肺負荷量の投与量に対する割合 45.7 12.0 15.3 最後に、ラボ間差の有無を定量的に確認するために、併行分散と室間分散(再現分散—併行分 散)の比の検定を左肺負荷量の投与量に対する割合と右肺負荷量の投与量に対する割合のそれぞ れについて行った。その結果、左肺負荷量の投与量に対する割合、右肺負荷量の投与量に対する 割合、どちらの場合も有意水準片側5%で、「ラボ間差があるとは言えない」との結論が導かれた。
右肺の総量
Lab A 負荷量の割合(対投与量)Lab B Lab C Lab D Lab E 0.0 0.2 0.4 0.6 0.8 1.0
46 2.7 多層カーボンナノチューブ(MWCNT)の肺内分布の確認 2.7.1 MWCNT の試料調製とキャラクタリゼーション ラボ間比較試験に供するMWCNT 分散液の調製・キャラクタリゼーション・供給は、昭和電工株 式会社により行われた。 分散液は、VGCF®-H 粉体(昭和電工株式会社製)を原料とし、十分な分散性を得るため、バ ス型超音波洗浄機、プローブ型超音波発生機、湿式分散装置を用いて調製された。 表 2.7-1 に、MWCNT(VGCF®-H)粉体及び分散液のキャラクタリゼーションデータを示す。 表2.7-1 MWCNT 粉体と分散液のキャラクタリゼーション(VGCF®-H) 項目 値 測定方法 【粉体】 不純物 Fe (9ppm)、他 (ND) 蛍光X 線法 1次粒子径 平均繊径: 177 nm 平均繊維長:5.2 µm 走査型電子顕微鏡(SEM):200 本の計測の数 平均値 比表面積 14 m2/g BET 法 【分散液】 媒体(分散剤の種 類と濃度) 0.3% Kolliphor®P188 (0.3% PluronicF68 と同等品) /Saline MWCNT 濃度 0.4 mg/mL 分光光度計測器(日本分光(株)紫外可視近 赤外分光光度計 V-670):波長 600-800 nm の 平均吸光度による検量線に基づく 2次粒子径 587 nm(試料調製直後) 592 nm(6 日後再分散) DLS:ゼータ電位・粒径・分子量測定システ ム(大塚電子(株)ELSZ-2000ZS) ゼータ電位 -2.2 mV(試料調製直後) 0.4 mV(6 日後再分散) ゼータ電位・粒径・分子量測定システム(大 塚電子(株)ELSZ-2000ZS) 電子顕微鏡像 図2.7-1 走査型電子顕微鏡(日本電子(株)JSM7000F) 図2.7-1 分散液中の MWCNT(昭和電工(株)VGCF®-H)の電子顕微鏡像 2. 分散液の特性に関する (1) 濃度測定 分散液の濃度は、分光光度計測器(日本分光(株) 紫外可視近赤外分光光度計 V-670)によっ て測定した。濃度既知の VGCF®-H 分散液を調製し、波長 600~800nm における平均吸光度から VGCF®-H 濃度と懸濁液の吸光度との関係(検量線)を求めた。調製後の分散液の吸光度を測定し、 該検量線を用いて最終的な濃度を決定した。 (2) 粒⼦形状(⼀次粒⼦:SEM) 走査型電子顕微鏡(日本電子(株) 電界放出型走査電子顕微鏡 JSM7000F)を用いて、一次 粒子を観察した。試料前処理として、分散液を純水で 100 倍に希釈、孔径 0.2μm のメンブレンフィ ルタでろ過捕集、風乾後に表面を Os で蒸着した。写真の通り、互いに独立した繊維を確認した。 (3) 粒度分布(⼆次粒⼦:ルミサイザー) 粒度分布・分散安定性分析装置(日本ルフト(株) LUMiSizer)で粒度分布に関する特性評価を 実施した。分散液を 4 倍に希釈して測定した。 下記に、調製直後と、冷凍保存 6 日後に解凍、再分散処理を実施した分散液のルミサイザーによ る特性評価結果を示した。結果のとおり、再分散処理を行うことで、調製直後の分散性を再現できて いることを確認した。 試料調製直後: メジアン径 0.77μm (n=4) (0.76~0.79μm)
また、2.4.1節と同じ光学顕微鏡を用いて、調製時及び各機関でのゾンデ通過後の投与液 を撮影した結果(図2.7-2)、ゾンデを通して投与する際に明らかな凝集が進んではいないことが 確認された。 図2.7-2 MWCNT 分散液の光学顕微鏡像の一例(左:調製後、右:バイオ投与時ゾンデ通過 後) 100μm 100μm
![図 2.4-1 US3352 の電子顕微鏡像(一次粒径) 各機関で使用するゾンデを用いて通過前後の投与液の粒径とゼータ電位に変化がないかの確認 を行った結果を図 2.4-2 及び図 2.4-3 に示す。その結果、各機関のどのゾンデを用いても粒径やゼ ータ電位に大きな変化を引き起こすことはないことが確認された。 図 2.4-2 ゾンデ通過前後の NiO 分散液の粒径(動的光散乱法による測定結果)050100150200250300平均粒径[nm]原液バイオゾンデCERIゾンデ産業医大ゾンデ安評ゾンデDI](https://thumb-ap.123doks.com/thumbv2/123deta/8574492.934042/10.892.220.675.129.356/ゾンデ引き起こす粒径動によるバイオゾンデCERIゾンデゾンデゾンデDI.webp)