白血病委 員会
B前 駆細胞 型急性 リンパ性 白血病 の治療
渡 辺 新
中通総合病院小児科
Treatment of Childhood Acute Lymphoblastic Leukemia with B-Cell Precursor Phenotype
Arata WATANABE
Department of Pediatrics, Nakadori General Hospital
Abstract Although more than 80% of children with acute lymphoblastic leukemia of the B-cell precursor phenotype (BCP-ALL) has been cured by the 4 groups' clinical study in Japan, the remaining 20% of patients underwent some events including induction failure, relapse, secondary cancer and also suffered from late complication. Japanese Pediatric Leukemia/ Lymphoma Study Group (JPLSG) was organized in 2003 and the JPLSG protocols have been al-ready started for three distinct and rare types of ALL, including mature B-ALL, infant ALL and Ph+ALL. We are just planning to start JPLSG T-cell ALL protocol in 2009. For the purpose of finding the standard treatment of BCR-ALL in Japan, central nervous system leukemia directed treatment is important to avoid pre-symptomatic cranial radiother-apy. Then, for the best cure by the best treatment, it is importanr that risk-directed stratification also contain not only age and WBC count at onset, but also genetic subtype of BCP-ALL, early response to treatment and introduction of selected antileukemic drugs being tested in clinical trials.
要 旨 小 児 急 性 リ ンパ 性 白血 病(ALL)の8割 以 上 はB前 駆 細 胞 型(BCP-ALL)で あ り,本 邦 で は4グ ル ー プ に よ る多 施 設 共 同 研 究 に よ り治 癒 率 は 向上 した が,約20%の 児 に,寛 解 導 入 不 能,再 発,2次 が ん が 生 じて い る こ と と,晩 期 合 併 症 が 問 題 とな っ て い る.2003年 に結 成 さ れ た 日本 小 児 白血 病 リ ンパ 腫 研 究 グ
ル ー プ(JPLSG)に よ りB-ALL,乳 児ALL,Ph+ALLの 全 国 共 通 臨 床 試 験 が始 ま り,2009年 に はT-ALLの 統 一 治 療 研 究 が 開 始 さ れ る.BCP-ALL治 療 に お い て,よ りよ い 治 療 に よ る,よ り よ い治 癒 を 目指 す た め に 重 要 な こ と は,予 防 的頭 蓋 照 射 の全 廃 を 見 据 え た中 枢 神 経 系 白血 病 の予 防法 導 入 と,従 来 の年 齢 ・白血 球 数 に よ る層 別 化 に加 え て,白 血 病 細 胞 の染 色 体 ・遺 伝 子 異 常 と治 療 反 応 性 に基 づ い た 新 た な層 別 化 と,新 規 開 発 薬 剤 を 導 入 した至 適 治 療 法 選 択 が重 要 とな る.
Key words: acute lymphoblastic leukemia, B-cell precursor phenotype, central nervous system leukemia, mini-mal residual disease, clofarabine
I. は じ め に
小 児 急 性 リ ンパ 性 白 血 病(ALL)は,わ が 国 で 年 間 約 600例 が 発 症 し て お り,そ の う ちT細 胞 型 と 成 熟B細 胞 型 を 除 い たB前 駆 細 胞 型ALL(B- cell precursor ALL: BCP-ALL)は 年 間 約500例 前 後 発 症 す る と 推 定 さ れ, 国 内 で は CCLSG, TCCSG, KYCCSG, JACLSの4グ ル ー プ を 中心 に 多施 設 共 同 治 療 研 究 が 施 行 され て きて お り, 国 内外 の 臨 床 研 究 に お い てBCP-ALLで は年 代 と と も に 治 療 成 績 の 改 善 傾 向 が認 め られ,90年 代 の 臨 床 研 究 に お い て は80%近 い無 病 生 存 率(EFS)が 達 成 さ れ て い る がB),逆 に い え ば 依 然 と して20%以 上 の 患 児 に お い て 寛 解 導 入 不 能 ・再 発 ・2次 が ん ・死 亡 と い ったeventが 生 じ,一 部 の 症 例 で は多 剤 耐 性 か ら治 療 抵 抗 性 とな っ て い る こ とに な る.こ の背 景 に は リス ク因 子 に基 づ い た層 別 化 に よ り治 療 戦 略 を立 て て い く場 合,メ ソ ト レキ セ ー ト (MTX) (1953年 発 売), 6-メ ル カ プ トプ リ ン (6MP) (1953年 発売), ビ ンク リス チ ン(VCR) (1963年 発 売), シ タ ラ ビ ン(AraC)(1969年 発 売)と, BCP- ALLに 汎 別 刷 請 求 先: 〒010- 8577秋 田市 南 通 み そ の 町3-15 中 通 総 合 病 院 小 児 科 渡 辺 新
Reprint requests to Arata Watanabe, Department of Pediatrics, Nakadori General Hospital, 3-15, Misono-cho, Minamidori, Akita, 010-8577 Japan
NHL03, Ph+ALLO4, MLLO3)が 開 始 さ れ,診 断 ・治 療 の 標 準 化 が 図 ら れ て き て い る.ま た,難 治 性T細 胞 性 ALL (TIALL)にnelarabine (ア ラ ノ ンGR)が 認 可 され た こ と を受 けて,JPLSGのT-ALLの 全 国 共 通 臨 床 試 験 が 開 始 され る運 び と な って い る.本 稿 で はBCP-ALLに 関 して も っ と も新 しい リス ク因 子 に基 づ く層 別 化 と治 療 選 択 の現 況 に つ い て 概 説 す る と と も に,新 規 薬 剤 の 臨 床 的 意 義 に つ い て も考 察 す る. II. BCP-ALLに お け る リ ス ク 因 子 に 基 づ く 層 別 化 の 基 本 的 考 え 方 本 邦 に お け るCCLSGの 多 施 設 共 同 研 究 は1981年 の ALL811研 究 か ら 始 ま っ て い る が,同 じ 年 の1月 か ら Dana-Farber Cancer Institute(DFCI)グ ル ー プ は 次 の よ う な 考 え に 基 づ い てprotocol 81―-0lを 開 始 し て い る4).す な わ ち,1973∼1980年 に お け る 治 療 経 験 を 踏 ま え て, 患 児 をstandard risk (SR)とhigh risk (HR)の2群 に 層 別 化 し,SR群 で は 治 療 関 連 毒 性 を 減 ら しつ つ 最 大 の 治 療 効 果 を 得 る こ と を 目 標 と し た.一 方,HR群 で は 再 発 を 防 ぐ た め の 治 療 強 化 が 優 先 さ れ,そ れ に 伴 う 治 療 関 連 毒 性 は 容 認 す る と い う,き わ め て 明 確 な 戦 略 を 打 ち 出 し た.SR群 は 年 齢2∼9歳 で あ っ て,1)白 血 球 数20,000/ μ1以 上,2)T細 胞 性,3)縦 隔 腫 瘤,4)中 枢 神 経 系 浸 潤,の4つ の 特 徴 を1つ も 認 め な い 群 と し,SR群 の 基 準 を 満 た さ な い 群 をHR群 と し て,治 療 戦 略 の 骨 子 は HD-MTX/ ADRIVCR/ PSLの4剤 に よ る 寛 解 導 入 と,そ れ に 引 き 続 い て 行 う週1回 のintensive L-asparaginasether-apyで あ っ た.Median follow-up35ヵ 月 と や や 短 い も の
の,SR群 の4年event-free-survival (4y-EFS):8 6±4%, HR群 の4y-EFS: 71±4%と,最 新 研 究 と 比 べ て も 見 劣 り し な い 成 績 を 報 告 し て い る が,こ の 「治 療 関 連 毒 性 の 容 認 」 に 関 して は,心 筋 障 害 と 脳 腫 瘍 を 中 心 と し た 二 次 が ん な ど の 晩 期 合 併 症 の 発 病 率 は 追 跡 期 間 が 長 く な る ほ BCP-ALLに お け る 初 発 時 の 年 齢 と 白 血 球 数 の 予 後 因 子 と し て の 重 要 性 はT-ALLに 比 べ よ り 大 き い も の が あ り7),リ ス ク 因 子 の 共 通 化 に 向 け てCTEP/NCI(ロ ー マ/ NCI)ワ ー ク シ ョ ッ プ で 提 案 さ れ た リ ス ク 基 準 で は,白 血 球 数5万 未 満 か っ1.00∼9.99歳 をSR,そ れ 以 外 を
HRに 分 類 し,米 国CCG, POG, DFCI, St. Jude小 児 研
究 病 院 のBCP-ALL症 例 解 析 か ら,SR群(患 者 比 率68
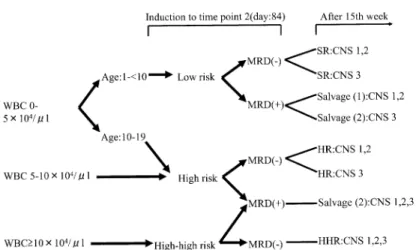
%): 4y-EFS80.3%,HR群: 4y- EFS 63.9%と し て い る8). 現 在,多 く の 臨 床 研 究 で は,初 診 時 デ ー タ と し て1) TEL-AML1,2) hyperdiploidy (染 色 体 数50以 上),3) BCR-ABL, 4) MLL融 合 遺 伝 子,5)3種 のtrisomy (4, 10,17),6)中 枢 神 経 系 白 血 病 の 有 無(CNS1, 2, 3), 7) 睾 丸 浸 潤 の 有 無 の7点 を 加 え,さ ら に 治 療 反 応 性(BFM グ ル ー プ で は 早 期 プ レ ド ニ ゾ ロ ン 反 応 性 とday33: BM お よ びday 78: BMのPCR法 に よ る MRD9), CCG/ POG: COGで はday 8: BMとdayl5: BMの 芽 球 比 率 お よ び day29: BMのFCM法 に よ るMRD10)を み る こ と で,予 後 が き わ め て 良 好 な 群 と,き わ め て 不 良 な 群 を 抽 出 し, と く に7EL週 雌Jを 有 す る 群 は 独 立 し た 予 後 良 好 群 と し た 前 方 視 的 研 究 が 行 わ れ て き て い る11). 抗 原 受 容 体 遺 伝 子 再 構 成 を 利 用 し た 微 小 腫 瘍 残 存 (MRD)定 量 法 の 開 発 は,個 々 のALL患 児 の 白 血 病 細 胞 の 化 学 療 法 反 応 性 に 合 わ せ た 新 た な 層 別 化 に 結 び っ け ら れ て き て い る.ド イ ツBFMグ ル ー プ は,T細 胞 受 容 体(TCR)γ,δ 鎖,免 疫 グ ロ ブ リ ン遺 伝 子 κ 鎖(Igk), お よ びTAL1遺 伝 子 再 構 成 を 指 標 と し,治 療 開 始 後,5, 12, 22∼25, 28∼33, 70, 80週,2年 目,3年 目 に 骨 髄 MRD定 量 を 行 い,す べ て の 測 定 時 点 に お い てMRDが 独 立 し た 予 後 因 子 と な る こ と を 証 明 し た12). Fig.1に 小 児 が ん 白 血 病 研 究 グ ル ー プ(CCLSG の ALL 2004 protocolに お け る,初 発 時 デ ー タ と 第15週 の MRDに 基 づ い た2段 階 の 層 別 化 と 治 療 プ ロ ト コ ー ル を 示 し た.対 象 は 乳 児ALLを 含 ま な い1歳 以 上19歳 未 満
の未 治 療ALLで,プ レ ドニ ゾ ロ ン単 独7日 間 先 行 投 与 期 間 中 に 成 熟B細 胞 性ALLお よ び,t(9;22)ま た は βCR.AβL融 合 遺 伝 子 を 有 す る こ とが 判 明 した もの は含 ま ず,初 発 時 の 年 齢 と 白血 球 数 で 標 準 危 険 群( SR群: 白 血 球0∼5万 か っ 年 齢1∼10歳),高 危 険 群( HR群: 白 血 球5∼10万 ま た は 年 齢10∼19歳),超 高 危 険 群 (HHR群:白 血 球10万 以 上)の3群 に 分 け る.次 に 中 枢 神 経 系 浸 潤 に 関 してCNSI(髄 液 赤 血 球 数 が10/μ1未 満 で細 胞 診 が 陰 性),CNS2(髄 液 赤 血 球 数 が10/μ1未 満 で 白 血 球 数 が54/μ1未満 か つ 細 胞 診 が 陽 性),CNS3(髄 液 赤 血 球 数 が10/μ1未 満 で 白血 球 数 が5/μ1以 上 か っ 細 胞 診 が 陽 性)の3群 に 分 類 し,髄 液 赤 血 球 数10/μ1以 上 で はtraumatic lumbar punctureと して 末 梢 血 の 赤 血 球 ・白 血 球 の 比 率 で 補 正 し た.CNS1 とCNS2は 第15週 ま で の 髄 注 回 数 が 違 う だ けで 第15週 以 降 は同 じ レ ジ メ ン と し,CNS3に は頭 蓋 照 射 を行 うた め別 レ ジ メ ンと した. MRD量 は,TCR, Igk遺 伝 子 再 構 成 を 指 標 と し,寛 解 時 の 骨 髄DNAと 初 診 時 のDNAを,健 常 人 の 白 血 球 DNAで 段 階 希 釈 し た もの を症 例(ク ロ ー ン)特 異 的 プ ライ マ ーを 用 い て増 幅 し,両 者 を比 較 す る こ とで 判 定 す る.第15週 以 降 の 治 療 レ ジメ ン決 定 の た め のMRD定 量 は初 回 完 全 寛 解 判 定 時 の骨 髄(ポ イ ン ト1)と,第 13 週 の 骨 髄(ポ イ ン ト2)の2点 で 行 い,こ れ ま で の Intemational BMF Group,CCLSGの 研 究 結 果 に基 づ き, 定 量 結 果10-3以 上 を 陽 性:MRD (+)と した7).図 に示 す よ う に2段 階 の層 別 化 後 に第15週 以 降 の 治 療 レ ジ メ ンが 決 定 され,MRD陰 性 群 に はSR, HR, HHRの レジ メ ン治 療 が 行 わ れ,CNS3お よ びHHR群 に頭 蓋 照 射 が 導 入 さ れ る.MRD陽 性 群 に は,よ り強 い 強 化 療 法 を 組 み 込 ん だSalvage (1)お よ びSalvage (2)が 行 わ れ,予 定 ど お り 研 究 継 続 中 で あ る. III. 小 児ALLに よ く み ら れ る 染 色 体 ・ 遺 伝 子 異 常 と 臨 床 的 特 徴(Table 1, 2) BCP-ALLで 多 く認 め ら れ る 染 色 体 異 常 に,染 色 体 数 50以 上 の 高2倍 体,t(12;21) (pl2-13;q22)に よ り 生 じ る ETV6I-CBFA2 (TEL-AM乙J),4番 ・10番 ・17番 染 色 体 の trisomy が あ り,こ れ ら は い ず れ も1∼10歳 に 多 く,代 謝 拮 抗 剤 を 基 本 に し た 化 学 療 法 で5y- EFSが85∼ 90%と 推 定 さ れ る 予 後 良 好 群 で あ る13).ま た,t(1;19)(q21; q23) に よ り生 じ るE2A-PBX1はPre-B cell型ALLで み ら れ, 中 枢 神 経 系 浸 潤 を 起 こ し や す い こ と が 知 ら れ て い た が, 最 近 の 強 化 さ れ た 化 学 療 法 を 行 う こ と で 小 児 で は 予 後 良 好 群 に 含 ま れ る も の の,成 人ALLで は 依 然 と し て 予 後 不 良 で あ る14).最 近 報 告 さ れ た 小 児ALLの 約2%に FISH法 で 認 め ら れ る21番 染 色 体 内 のAML1遺 伝 子 の 増 幅(intrachromosomal amplifiation) もPre-B型 ALL
に 多 く,予 後 不 良 で あ る こ と が 報 告 さ れ て い る15).一 方, t(4;11) (q21;q23)お よ び 他 の11q23に よ るMLL変 異 は 乳 児 ・若 年 成 人 に 認 め ら れ た 場 合 に 予 後 不 良 と な り16), t(9;22) (q34;qll)に よ り 生 じ るBCR-ABLは 白 血 球5万 以 上 ま た は10歳 以 上 のNCI-HR群 で 予 後 不 良 と な り, 染 色 体 ・遺 伝 子 異 常 と年 齢 と の 関 係 が 認 め ら れ て い る17). BCP-ALLとTIALLを 比 較 す る と,早 期 治 療 反 応 不 良 は 共 通 の 予 後 不 良 因 子 で あ る が,NCI-HR群 は BCP- ALL で の み 予 後 不 良 と な る(Table2). IV. 治 療 レ ジ メ ン BCP-ALLに 対 す る 多 く の 代 表 的 な 治 療 レ ジ メ ン は, 1)寛 解 導 入 相,2)中 枢 神 経 系 白 血 病 予 防 相,3)中 間
維 持 療 法 相,4)再 寛 解 導 入 相,5)連 続 維 持 療 法 相,の 5相 か ら成 り立 って い る.NCI-SR/HRに よ る リス ク分 類 に 基 づ い て 最 近 の 治 療 研 究 で は,SR群 はVCR/L-asp+ steroidの3剤,HR群 は こ れ にanthracyclineを 加 え た4 剤 で 初 回 寛 解 導 入 を 開 始 され る こ とが 多 く,寛 解 導 入 に 用 い られ る レ ジメ ン と同 じ内 容 で再 寛 解 導 入 相 が組 み 入 れ られ る こ と が 多 い18).半 減 期 が長 い こ と と中 枢 神 経 系 へ の到 達 率 の 高 い点 か らデ キ サ メ サ ゾ ンの プ レ ドニ ゾ ロ ンに対 す る優 位 性 の報 告 は 多 いが 投 与 量 設 定 に ば らっ き が あ り19-20),ランダ ム 化 比 較 試 験 に よ る検 討 が 進 ん で い る.ま た,L-asparaginase製 剤 の 優 劣 が 報 告 さ れ て い る が,至 適 投 与 量 が 投 与 さ れ る こ とで 各 薬 剤 の優 劣 は少 な くな る可 能 性 が 指 摘 さ れ て い る21).寛 解 導 入 後 の 強 化 療 法 の 目 的 は 薬 剤 耐 性 化 した 白 血 病 細 胞 の 排 除 で あ り, MTX大 量 療 法+6MPな ど が 行 わ れ るが,MTXの 指 摘 投 与 量 はALLの 遺 伝 子 型/表 現 型 と個 々 の 患 児 の薬 物 代 謝 に よ り変 わ っ て くる.す な わ ち,SR群 で はMTX量 と して1∼29/m2が ほ とん ど の患 児 に と っ て 至 適 量 と な る が,HR群 やT-ALLで は5g/m2と い っ た 高 用 量 が 必 要 と な り,33.6g/m2と い っ た超 大 量 は不 要 だ が,ロ イ コ ボ リ ン に よ る救 済 の タ イ ミ ン グ と投 与 量 も重 要 と な る22).BCP-ALLで は維 持 療 法 相 を 含 む2∼2.5年 の 治 療 期 間 が行 わ れ る が,お そ ら く2/3の 児 が1年 で 治 癒 して い る と して も,そ れ らの児 を 抽 出 で き る手 段 が な い現 状 で は全 員 に 維 持 療 法 を 行 う必 要 が あ り23),代 表 的 な レ ジ メ ン と して は6MP連 日 内 服 とMTX週1回 内服 が 行 わ れ る こ とが 多 い.
V. 中 枢 神 経 系 指 向 性 治 療(Table 3) 中 枢 神 経 系 再 発 予 防 はBCP-ALLの 治 癒 率 向 上 に と っ て き わ め て 重 要 で あ る が,予 防 的 頭 蓋 照 射(pre-symptomatic cranial radiotherapy: pCRT)後 に は2次 が ん, 認 知 障 害,内 分 泌 障 害,成 長 障 害 と い った重 篤 な 晩 期 障 害 を生 じ る た め24),照 射 量 の 削 減 が試 み られ て きた が, 12Gyに 減 量 したpcRT後 に も15年 の 追 跡 調 査 で1.7% (95%CI 0.1∼3.4)で2次 が ん が 認 め られ て い る こ と な ど か ら25),近 年 の 小 児ALLに 対 す る 臨 床 プ ロ トコ ー ル に お け るpCRT対 象 群 は2∼20%に 抑 え られ て き て お り, pCRTの 全 廃 か ら髄 注 療 法 へ の 変 更 が進 ん で きて い る26). 現 行 の プ ロ トコ ー ル で 照 射 対 象 と さ れ る の は,T―ALL, BCP-ALLで 白血 球 数10万 以 上,MRD高 値,予 後 不 良 染 色 体 異 常,お よ びCNS3な ど で あ る が,2歳 未 満 児 へ の 照 射 は避 け るか 減 量 され る こ とが 多 く,CNS3も 含 め て pCRTを 全 廃 した 臨 床 研 究 も少 な か らず進 行 して きて い る(Table3).こ れ を 担 保 す る理 論 と して,照 射 後 の2 次 が ん の発 生 率 が20年 後 に20.9%に 達 し,と くに2次 性 脳 腫 瘍 の 死 亡 率 が き わ め て 高 い こ と お よ び,髄 注 療 法 を 強 化 す る こ と の有 効 性 と,中 枢 神 経 系 単 独 再 発 後 に初 め て照 射 を 行 っ た群 の治 癒 率 が 高 い こ とな どか ら,頭 蓋 照 射 は 中 枢 神 経 系 再 発 後 に備 え て控 え て お くべ き だ とい う意 見 が 上 が っ て き て い る.pCRTで 注 意 す べ き は 18∼24Gyの 頭 蓋 照 射 に よ り,通 常 は照 射 時 に 遮 蔽 さ れ て い な い 甲状 腺 に,散 乱 放 射 線 と して13∼132 cGyが か か って しま い,2次 が ん と して の 甲 状 腺 癌 が 生 じ る可 能 性 が 指 摘 さ れ て い る こ と で あ り,甲 状 腺 癌 は小 児ALL 治 療 後 の2次 が ん の10%弱 を 占め て い る こ と で あ る27). こ の散 乱 放 射 線 被 爆 量 は報 告 さ れ て い る被 爆 甲 状 腺 癌 の 閾 値:200cGyを 下 回 るが28),か っ て 行 わ れ た 頭 部 白癬 に対 す る10cGyの 少 量 照 射 後 に も若 年 小 児 で は2次 発 癌 の報 告 が み られ る こ と な どか ら,厳 重 な 甲 状 腺 遮 蔽 に 加 え,や は り予 防 的 頭 蓋 照 射 の 全 廃 を可 能 に す る方 法 が 求 め られ る こ と に な る.ま た,最 近 の報 告 で は,抗 白血 病 薬 の薬 物 代 謝 に 関連 す る蛋 白質 を コー ドす る遺 伝 子 多 型 と中 枢 神 経 系 再 発 頻 度 との 関 連 性 が示 唆 され て お り, MTX耐 性 と 関 連 す る ビ タ ミ ンD受 容 体 遺 伝 子 の 多 型 や29),イ ン タ ー ロ イ キ ン15の 発 現 過 多 と発 症 時 の 中 枢 神 経 系 浸 潤 との 関連 が報 告 され て お り30),将来 の オ ー ダ ー メイ ド治 療 に お け る個 別 の至 適 中 枢 神 経 系 白血 病 予 防 法 選 択 の手 が か り とな って い く こ とが 期 待 で き る.
上 の 群 と し た た め,通 常 は 高2倍 体 と 共 存 し な い7EL-AML1は 融 合 遺 伝 子 陽 性 群 の 比 率 はLR群 で152例 中7 名(5%)と 低 く, SR群470名 中173名 (37%), PR 群 304名 中64名 (21%),全 体 で926名 中244名 (26%) で あ っ た.LR群 とSR群 に はanthracycline, epipodophy-lotoxin,ア ル キ ル 化 剤 が ま っ た く 入 らず,pCRTも 行 わ な い 治 療 プ ロ ト コ ー ル が 施 行 さ れ た.観 察 期 間7.8年 で 5y- EFSはTEL- AML1群 で86±2 %, germline TEL群 で 72± 2% (p< 0.0001), NCI- SR群 に お い てTEL- AML1群 は 有 意 に 予 後 が よ く(5y-EFs, 88± 3%vs . 78±2%: p= 0.0011), NCI- HR群 で も有 意 に 予 後 良 好(5y- EFs , 81± 5%vs.62±3%:p)= 0.0032)で あ っ た (Fig.2).ま た, day 15: BMでM1 marrowで あ っ た 群 を 早 期 治 療 反 応 良 好 群 と す る と,予 想 ど お りTEL辺 雌J群 に お け る 早 期 治 療 反 応 良 好 群 は 有 意 に 予 後 が よ く(5y-EFS, 87±2% vs. 71± 12%: p= 0.043), germline TEL群 で も 早 期 治 療 反 応 不 良 群 は 有 意 に 予 後 良 好(5y-EFs, 75±2%vs . 56± 6%:ρ=0.0032)で あ っ た.さ ら に 早 期 治 療 反 応 良 好 群
に お い て もTEL- AML1群 はgermline TEL群 と 比 べ て 有 意 に 予 後 良 好(5y- EFS, 87± 2%vs. 75± 2%: p= 0.0001) で あ っ た.注 目 す べ き 点 は,TEL-AM1群 で は 診 断 か ら 5年 以 上 経 っ て か ら 生 じ るlateeventが198名 中4名 (2%)で あ っ た の に 対 し,germlineTEL群 で は467名 中 19名(4%)と 多 か っ た 点 で あ る.多 変 量 解 析 で もTEL-AMLJ融 合 遺 伝 子 を 認 め な い こ と が 独 立 し た 予 後 不 良 因 子(p=0.0002)と な り,ま た,同 様 の 報 告 は 他 施 設 か ら も 報 告 さ れ て い る.し た が っ て,TEL- AML融 合 遺 伝 子 陽 性 か っ 早 期 治 療 反 応 良 好 群 は,現 在 の 代 謝 拮 抗 剤 を 中 心 と し た 晩 期 障 害 の 少 な い 治 療 が 推 奨 さ れ る. VII. 治 療 新 規 薬 剤 の 導 入(Table 4) BCP-ALLの 普 遍 的 な 原 因 が 未 解 明 で あ る 以 上,普 遍 的 な タ ー ゲ ッ ト治 療 の 開 発 は 困 難 で あ る が,新 し い 機 序 C の 抗 白 血 病 剤 や 分 子 標 的 療 法 薬 は 近 年,続 々 と 開 発 さ れ っ っ あ る(Table4) .抗CD22抗 体 で あ るepratuzumab や ubiquitin proteasome pathway の 阻 害 薬 で あ る bortezomibは,現 在,COG の 再 発ALL program( COG AALLO7Pl)で 第II相 臨 床 試 験 が 進 行 中 で あ る が,BCP一
Fig. 2 Event-free survival (EFS) estimates of patients treated on ALinC 16 and their relation to TEL gene status (A) EFS estimates of patients with TEL rearrangements (R-TEL) compared with those of patients with germline TEL (G-TEL). (B) EFS estimates of patients with National Cancer Institute (NCI) standrad-risk ALL shown in relation to TEL status. (C) EFS estimates of pa-tients with NCI high-risk ALL shown in relation to TEL status.31)
ALLに も っ と も 期 待 さ れ て い る 新 薬 と し て はclofarabine が 挙 げ ら れ る32).Clofarabineはnudarabineと cladribine の 両 方 の 特 徴 を も っ 新 し い ア デ ノ シ ン ア ナ ロ グ で,ara― CTPの 集 積 を 強 化 し っ っ,epipodophylotoxin,ア ル キ ル 化 剤 に よ っ て 生 じ たDNA損 傷 の 回 復 を 阻 害 す る こ と が 期 待 さ れ,clofarabine: 30mg/m2× 5days+ etoposide: 100 mg/m2×5days+ cyclophosphamide: 440mg/m2×5days の 併 用 療 法 が 初 回 寛 解 導 入 不 能 例 や 再 発 後 の 難 治 例 に 試 み ら れ て い る(CLO21800205)33). VIII. お わ り に Clofarabineを は じ め,Table 4に 挙 げ た 新 規 薬 剤 の 多 く は 欧 米 で は 認 可 さ れ た に も か か わ ら ず,本 邦 で は 未 承 認 薬 が ほ と ん ど で あ り,nelarabineが 難 治 性T-ALLに 承 認 さ れ た 以 外 は,発 売 の め ど す ら た っ て い な い 薬 剤 が 多 い こ と は,き わ め て 憂 慮 す べ き 状 況 で あ る と い わ ざ る を え な い.小 児 のBCP-ALLは 近 年,フ ォ ロ ー ア ッ プ 期 間 が20∼30年 を 超 え て き て,晩 期 合 併 症 が 大 き く取 り 上 げ ら れ て き て い る が34,35),小 児 で はBCP-ALLを 治 癒 さ せ た 後,60年 以 上 の 余 生 が あ り,そ のQOLは 今 後 も 問 わ れ 続 け て い く こ と に な る.よ り よ い 治 療 と よ り よ い 治 癒 は す べ て の 患 児 ・家 族 の 望 み で あ り,旧 来 の 治 療 薬 の 組 み 合 わ せ に よ るQOL向 上 に は 限 界 が あ る こ と を 踏 ま え,新 薬 の 承 認 を 含 め た 治 療 法 の さ ら な る 改 善 が 期 待 さ れ る. 引 用 文 献
1) Pui CH, Relling MV, Downing JR : Acute lymphoblastic leukemia. N Engl J Med 350: 1535-1548, 2004 2) Moorman AV, Harison CJ, Buck GA, et al: Karyotype
is an independent prognostic factor in adult acute lymphoblastic leukemia (ALL): Analysis of cytogenetic data from patients treated on the Medical Research Council (MRC) UKALL XII/Eastern Cooperating Oncology Group (ECOG) 2993 trial. Blood 109: 3189-3197, 2007
3) Nachman JB, Heerema NA, Sather H, et al: Outcome of treatment in children with hypodiploid acute lympho-blastic leukemia. Blood 110: 1112-1115, 2007 4) Clavell LA, Gelber RD, Cohen HJ, et al: Four-agent
in-duction and intensive asparaginase therapy for treatment of childhood acute lymphoblastic leukemia. N Engl J Med 315: 657-663, 1986
5) Anja Moricke, Alfred Roiter, Martin Zimmermann, et al: Risk-ajusted therapy of acute lymphoblastic leukemia can decrease treatment burden and improve survival: Treatment results of 2169 unselected pediatric and ado-lescent patients enrolled in the trial ALL-BFM 95. Blood
111: 4477-4489, 2008
6) Watanabe A, Katano N, Kikuta A, et al: *Strategy of cu-mulative dose reduction of drugs with late effects, using
escalating dose of anti-metabolites with or without mega-dose chemotherapy plus autologous peripheral blood stem cell rescue for treatment of childhood acute lymphoblastic leukemia: Children's Cancer and Leukemia Study Group of Japan (CCLSG), CCLSG
lymphoblastic leukemia: A Children's Oncology Group. J Clin Oncol 26: 2186-2191, 2008
11) Romana SP, Mauchauffe M, Le Coniat M, et al: The t(12;21) of acute lymphoblastic leukemia results in a tel-AML1 gene fusion. Blood 85: 3662-3670, 1995 12) Okamoto T, Yokota S, Katano N, et al: Minimal residual
disease in early phase of chemotherapy reflect poor out-come in children with acute lymphoblastic leukemia: A retrospective study by the Children's Cancer and Leukemia Study Group in Japan. Leuk Lymphoma 43: 1001-1006, 2002
13) Pui CH: Childhood Leukemias 16 Acute Lymphoblastic Leukemia. Cambridge University Press 439-472 , 2006 14) Landau H, Lamanna N: Clinical manifestations and
treat-ment of newly diagnosed acute lymphoblastic leukemia in adults. Curr Hematol Malig Rep 1: 171-179, 2006 15) Moorman AV, Richards SM, Robinson HM, et al:
Prognosis of children with acute lymphoblastic leukemia (ALL) and intrachromosomal amplification of chromo-some 21 (iAMP21). Blood 109: 2327-2330, 2007 16) Pui CH, Gaynon PS, Boyett JM, et al: Outcome of
treat-ment in childhood acute lymphoblastic leukemia with re-arrangements of 11q23 chromosomal region. Lancet 359: 1909-1915, 2002
17) Schultz KR, Pullen DJ, Sather HN, et al: Risk- and re-sponse-based classification of childhood B precursor acute lymphoblastic leukemia: A combined analysis of prognostic markers from the Pediatric Oncology Group (POG) and Children's Cancer Group (CCG). Blood 109: 926-935, 2007
18) Pui CH, Robinson LL, Look AT: Acute lymphoblastic leukemia. Lancet 371: 1030-1043, 2008
19) Mitchell CD, Richards SM, Kinsey SE, et al: Benefit of dexamethasone compared with prednisolone for child-hood acute lymphoblastic leukemia: Results of the UK Medical Research Council ALL97 randomized trial. Br J Haematolo 129: 734-745, 2005
20) Bostrom BC, Sensel MR, Sather HN, et al: Dexametha-sone versus predniDexametha-sone and daily oral versus weekly in-travenous mercaptopurine for patients with standard-risk acute lymphoblastic leukemia: A report from the
(CCG-1942). Pediatr Blood Cancer 49: 250-255, 2007 24) Geenen MM, Cardous-Ubbink MC, Kremer LCM et al:
Medical assessment of adverse health outcomes in long-term survivors of childhood cancer. JAMA 297: 2705-2715, 2007
25) Pui CH, Howard S: Current management and challenges of malignant disease in CNS in paediatric leukemia. Lancet Oncol 9: 1-12, 2008
26) Vilmer E, Suciu S, Ferster A, et al: Long-term results of three randomized trials (58831, 58832, 58881) in child-hood acute lymphoblastic leukemia: A CLCG-EORTC report. Leukemia 14: 2257-2266, 2000
27) Perel Y, Leverger G, Carrere A, et al: Second thyroid neplasms after prophylactic cranial irradiation for acute lymphoblastic leukemia. Am J Hematol 59: 91-94 , 1988 28) Tucker MA, Morris Jones PH, Boice JD Jr, et al: Therapeutic radiation at a young age is linked to sec-ondary thyroid cancer. Cancer Res 51: 2885-2888 , 1991 29) Rocha JCC, Cheng C, Liu W, et al: Pharmacogenetics of outcome in children with acute lymphoblastic leukemia. Blood 105: 4752-4758, 2005
30) Cario G, Izraeli S, Teichert A, et al: High interleukin-15 expression characterized childhood acute lymphoblastic leukemia with involvement of the CNS. J Clin Oncol 25: 4752-4758, 2005
31) van Dongen JJ, Seriu T, Panzer-Grumayer , et al: Prognostic value of minimal residual disease in acute lymphoblastic leukemia in childhood. Lancet 352:
1731-1738, 1998
32) Conrey SJ: New agents in the treatment of childhood leukemias and myelodysplastic syndrome. Curr Oncol Rep 7: 399-405, 2005
33) Hayes MP: Briefing package for pediatric oncology sub-committee (ODCA) meeting, 20 October 2005: Product , Clofarabine, ClolarTM. P1-23: 2005
34) Mody R, Li S, Dover DC, et al: Twenty-five-year follow-up among survivor of childhood acute lymphoblastic leukemia: A report from the Childhood Cancer Survival Study. Blood 111: 5515-5523, 2008 35) Oeffinger KC, Meriens AC, Sklar CA, et al: Chronic
health conditions in adult survivors of childhood cancer . N Engl J Med 355: 1572-1582, 2006