東京理科大学Ⅰ部化学研究部 2016 年度秋輪講書
ウリ科植物における
アルコール分解酵素含有量の比較
2016 年火曜班 Eguchi,N.(1K),Kikuchi,E.(1OK),Taketomi,H.(1K),Naradate,M.(1K),Fukushima,M.(1K), Sugawara,A.(2C),Tanaka,M.(2K),Baba,H.(2K),Sato,M.(2K) 1. 背景 大学の部活やサークル活動の一環として,また職場の仲間と親睦を深めるために, など我々は日常の様々な場面で飲酒をする機会がある.しかし,日本人のおよそ半 数がアルコール分解酵素であるアセトアルデヒドデヒドロゲナーゼ(以下,ALDH)が 低活性型もしくは非活性型であり,生まれつきお酒に弱いか全く飲めない体質であ ると言われており,肝機能を高めたり二日酔いを軽減したりする製品は需要が高く, 特にウコンやシジミを初めとする肝機能を高めるとされる食品が多く含まれた製品 が販売されている. そのような製品がある一方,キュウリはお酒と共に摂取すると二日酔いが軽減で きるといわれている.果実に含まれるアルコール分解酵素であるアルコールデヒド ロゲナーゼ(以下,ADH),ALDH が体内でアルコールおよびアセトアルデヒドを分解 することによって二日酔いの軽減に関与するものと考えられる.胃や肝臓に多くの アルコール分解酵素が存在することによりアルコールを効率的に分解することがで きる. 他にアルコール分解酵素を持つことが分かっているキュウリと同じウリ科植物と してヘチマ,ニガウリ,トウガン,シロウリがある1)が,その他のウリ科植物につい ては分かっていない.他のウリ科植物としてはスイカやメロンなど身近な果実も多 いため,ヘチマやニガウリに比べて飲酒の際に摂取しやすくお酒に弱い人たちの一 助となると思われる.また,ウリ科植物の果実を用いた新しい健康食品の開発に役 に立つことも考えられる. よって本実験では他の様々なウリ科植物を用いて,アルコール分解酵素を発見し, その活性を評価することにした. 2. 目的 各種ウリ科植物に含まれるアルコール分解酵素ADH,ALDH の活性の有無,及び 活性の評価をする.3. 原理 3.1. アルコール分解酵素1) ADH は,アルコール代謝の律速酵素である.ADH による反応は,可逆的で,還元 型ニコチンアミドアデニンジヌクレオチド(以下,NAD)を特異的な酵素として利用 し,①式で表せる. C2H5OH+NAD+ ⇄ CH3CHO+NADH+H+ ① エタノール代謝により生成したアセトアルデヒドは ALDH によって分解される. ALDH は②式に従い,アセトアルデヒドを酢酸に不可逆的に酸化する.
CH3CHO+H2O+NAD+ →CH3COOH+NADH+H+ ②
一般にADH 及び ALDH 活性が高いほど,アルコールは効率的に分解される. よって本実験では生成された NADH の濃度を吸光度測定により測定することで ADH 及び ALDH 活性を調べ,アルコール分解効果を評価する. 3.2. 紫外可視分光光度計(UV-vis) 3.2.1. ランベルト-ベールの法則2) この法則は,紫外可視吸光度測定法,原子吸光光度法,蛍光光度法,赤外吸収 スペクトル測定法,旋光度測定法と,多くの分光分析法にあてはまる重要な法則 である.入射光の強度(I0)と透過光の強度(I)の比を透過度(t)といい,それを%で表 したものを透過率(T)という.吸光度(A)とは,透過度の逆数の常用対数である. 透過度の値が減少すると,吸光度の値は増加する.透過度が1 のとき,吸光度は 0 であり,透過度が 0.1 のとき吸光度は 1 になる. t=Io/I ③ T= t×100= Io/I×100 ④ A=log Io/I ⑤ ランベルト-ベールの法則は,吸光度は層長の長さに比例するというランベル トの法則と,吸光度は試料の濃度に比例するというベールの法則を合体させたも のである.層長(l)と濃度(c)との積に定数であるモル吸光定数 ε,または比吸光度 E を乗じたものが,吸光度(A)になる.
A=εcl ⑥ A=Ecl ⑦ 3.2.2. 紫外可視吸光度測定法3) 基本構成は,光源→分光部→試料部→測光部,記録部である.特定波長の光を, 試料中の分子に照射してどのくらい吸収されたかを調べる装置になっている.光 源は通例,紫外線(200~400 nm)を出すためには重水素放電管を使用し,可視光線 (400~800 nm)を出すためにはタングステンランプやハロゲンタングステンラン プを使用する.分光部はプリズムや回折格子が利用されることが多い.簡易的に フィルターを使ったものは光電光度計と呼ばれ,取り出す波長が幅広く精密な測 定には不向きである.試料は通常,1 cm×1 cm の角型の二面が透明の容器に入れ る.また,ガラスは紫外線を通さないため,紫外線での測定の場合,石英製のセ ルを使用しなければならない.測光部で光強度を光電子増倍管で電気強度に変換 して,コンピュータで処理し吸光スペクトルを製作する. 4. 実験 4.1. 試薬 ・エタノール4) ethanol 分子式:C2H5OH 分子量:46.07 融点:-114.5℃ 沸点:78.325℃ 引火点:13℃ 危険性:引火性 用途:基質 無色,特有の芳香を有する揮発性の液体で可燃性.水,ジエチルエーテルな どと任意の割合で混和.
・ニコチンアミドアデニンジヌクレオチド5)
nicotinamide adenine dinucleotide 分子式:C21H27N7O14P2 分子量:663.43 融点:160℃ 沸点:無 引火点:不燃性 危険性:無 用途:反応溶液中の補酵素 白色粉末.吸湿性.水に易溶.一般に酸化型ニコチンアミドアデニンジヌク レオチド(以下,NADH)は酸性で比較的安定.アルカリ性で不安定.NAD はこ の逆. 多くの脱水素酵素の補酵素として,生体酸化還元系で水素原子伝達をする. ・グリシン6) glycine 分子式:NH2CH2COOH 分量:75.07 融点:232-236℃(分解) 沸点:無 引火点:不燃性 危険性:無 用途:緩衝溶液 水に易溶,ピリジンやエタノールに微溶,ほかの有機溶媒に不溶. ・水酸化ナトリウム7) sodium hydroxide 分子式:NaOH 分子量:40.0 融点:318℃ 沸点:1388℃ 引火点:不燃性 危険性:腐食性 用途:緩衝溶液 常温では無色,斜方晶系固体.潮解性を示す.溶解に伴い発熱する.
・ピラゾール8) pyrazole 分子式:C3H4N2 分子量:68.08 融点:67-70℃ 沸点:186-188℃ 引火点:不燃性 危険性:無 用途:反応溶液中ADH 阻害剤 ピリジン様臭のある針状晶またはプリズム晶.水,エタノール,エーテル, ベンゼンに易溶.水溶液は中性.pKa=2.5.
・EDTA(エチレンジアミン四酢酸)9) ethylenediaminetetraacetic acid
分子式:C10H16N2O8 分子量:292.24 融点:250℃(分解) 沸点:無 引火点:不燃性 危険性:刺激性 用途:反応溶液中キレート剤 白色結晶性粉末.水に微溶,有機溶媒には不溶.二ナトリウム塩は水に易溶. 窒素,酸素配位の五座ないし六座配位子として働き,多くの金属イオンときわ めて安定な金属キレート化合物をつくる.このとき,金属とEDTA が結合する モル比は常に1:1 である.金属間で選択性が小さい. ・ピロリン酸ナトリウム(二リン酸ナトリウム十水和物)10)
sodium diphosphate decahydrate 組成式:Na4P2O7・10H2O 分子量:446.06 融点:79℃ 沸点:94℃(分解) 引火点:不燃性 危険性:有害(経口),皮膚刺激 用途:緩衝溶液 白色粉末.水に可溶で,アルカリ性を呈する.水溶液は煮沸により次第に加 水分解してNa2HPO4を生じる.十水和物は単斜晶系晶.
・アセトアルデヒド11) acetaldehyde 分子式:C2H4O 分子量:44.05 融点:-123℃ 沸点:20.2℃ 引火点:-38℃ 危険性:引火性,発がん性,有害(経口,経皮,蒸気吸入) 用途:基質 特有の刺激臭を有する液体.水,エタノール,エーテルなどと任意に混和. 重合しやすく,低温で塩化水素を作用させれば重合度の高いメタアルデヒドと なる. ・塩酸12) hydrochloric acid 化学式:HCl 分子量:36.46 沸点:100℃ 危険性:金属腐食性,皮膚腐食性/刺激性,目に対する重篤な損傷性,呼吸器 感作性,特定標的臓器毒性(単回暴露),特定標的臓器毒性(反復暴露), 水生環境有毒性(急性) 用途:酵素の酸耐性評価のため 塩化水素の水溶液.実験室では NaCl に硫酸を加え,加熱して発生した塩化 水素ガスを水に溶かして得られる.多くの金属と反応して水素を発生し,塩化 物をつくる.気密容器に入れ保存する. ・各種ウリ科植物 キュウリ,カボチャ,メロン,スイカ,ズッキーニ 4.2. 器具 ホームミキサー,ビーカー,遠心分離機,フィルター,液体窒素,コニカルビー カー,ホールピペット,マイクロピペッター,ヨーグルトメーカー(恒温槽として 用いる),俎板,包丁
4.3. 実験操作 4.3.1. ADH 活性測定 (1) 各種ウリ科植物の果実20 g を予め冷却し,冷やしたイオン交換水(以下,冷 水)80 cm3を加えてミキサーで粉砕した.その後,遠心分離(10000 rpm,30 分)を行った.その後,上清を吸引濾過して得られた濾液をウリ科植物果実エ キスとした. (2) 希釈した果実エキス0.1 cm3および反応溶液(終濃度で 2.4 mmol dm-3 NAD を 含む0.1 mol dm-3グリシン-NaOH 緩衝液,pH10)1.8 cm3を混和し,25℃で 3 分間プレインキュベートした. (3) 基質(660 mmol dm-3エタノール溶液)を加える前の溶液をブランク,基質 0.1 cm3を加えたものをサンプルとして,分光光度計を用いて 340 nm の吸光度 を測定した. 4.3.2. ALDH 活性測定 (1) 4.3.1.(1)と同様にウリ科植物果実エキスを作製した. (2) 希釈した果実エキス0.1 cm3および基質以外の反応溶液(終濃度で 4 mmol dm
-3NAD,0.1mmol dm-3ピラゾール及び1 mmol dm-3 EDTA を含む 32 mmol dm -3ピロリン酸ナトリウム緩衝液,pH8)0.8 cm3を混和し,37℃で 3 分間プレイ ンキュベートした. (3) 基質(80 mmol dm-3アルデヒド溶液)を加える前の溶液をブランク,基質 0.05 cm3を加えた溶液をサンプルとして,分光光度計を用いて 340 nm の吸光度 を測定した. 4.3.3. 酸耐性評価 (1) 1 mol dm-3塩酸を果実エキスに添加(添加した体積については後述)し,20 分 間温置したものを酸処理溶液とした. (2) 未処理のウリ科植物果実エキスに対する酸処理溶液の残存活性により,酸耐 性を評価した. 4.4. NADH 水溶液の検量線の作成 (1) 3 種類の異なる濃度(0.107,0.092,0.046 mmol dm-3)の NADH 水溶液(以下, NADHaq)を作製し,吸光度測定をした. (2) 同量のイオン交換水の吸光度測定を行い,ブランクとした.
4.5. 夏休み以降の実験操作の変更点 前期の実験では,実験を 2 週に分けて行っていたため果実エキスの保存のため に瞬間冷却を行っていたが,夏休み中の実験から,1 日で果実エキスの作製から吸 光度測定までを終えられるように計画を変更したため,瞬間冷却を行わずにその まま反応溶液,基質との混和および吸光度測定の操作を行った. また,前期の実験では4.3.1.ADH 活性測定,ならびに 4.3.2.ALDH 活性測定 の(1)の操作において吸引ろ過に Sterifilip-GP(吸引ろ過用の滅菌済みフィルター付 きの容器)を使用していたが,夏休み以降は Sterifilip-GP を使用できなかったため サンプルの汚染を防ぐために吸引ろ過の操作も行わず,遠心分離後の上清を果実 エキスとして用いた. 5. 実験結果 5.1. ADH 活性測定 時間と吸光度の変化をTable 5.1.1.にまとめた. 果実名の後の数字は,4.3.1.ADH 活性測定(2)における希釈倍率を表している. また,希釈倍率が1(希釈を行っていない)のサンプルに関しては瞬間冷却を行っ ていないサンプルである. Table 5.1.1.ADH 活性測定における吸光度変化 時間/min. ブランク 30 45 60 カボチャ10 0.412 0.420 0.438 0.447 カボチャ5 0.091 0.148 0.156 0.188 カボチャ1 0.263 0.338 0.361 0.376 カボチャ1 0.431 0.511 0.527 0.540 スイカ10 0.192 0.153 0.148 0.193 スイカ1 0.093 0.221 0.274 0.320 ズッキーニ10 0.147 0.151 0.151 0.173 メロン5 0.063 0.216 0.375 0.363 キュウリ1 0.412 0.557 0.577 0.602 よって,どのサンプルも 60 分まで吸光度が上昇しているため,60 分での吸光 度からブランクの値を引いた値を吸光度変化量とするとTable 5.1.2 のようになる.
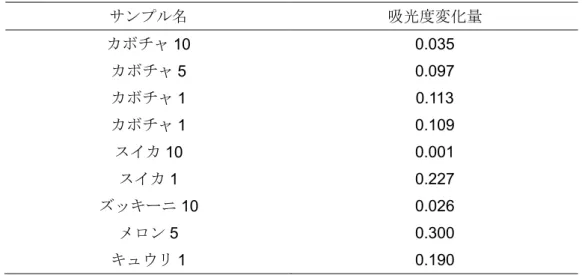
Table 5.1.2 ADH 活性測定での吸光度変化量 サンプル名 吸光度変化量 カボチャ10 0.035 カボチャ5 0.097 カボチャ1 0.113 カボチャ1 0.109 スイカ10 0.001 スイカ1 0.227 ズッキーニ10 0.026 メロン5 0.300 キュウリ1 0.190 5.2. ALDH 活性測定 5.1.ADH 活性測定と同様に時間と吸光度の変化を Table 5.2.1.にまとめた. Table 5.2.1.ALDH 活性測定における吸光度変化 時間/min. ブランク 30 45 60 カボチャ10 0.143 0.283 0.261 0.159 カボチャ5 0.088 0.171 0.162 0.163 カボチャ1 0.555 0.543 0.541 0.537 カボチャ1 0.289 0.282 0.282 0.282 スイカ10 0.057 0.066 0.064 0.063 スイカ1 0.103 0.105 0.101 0.098 ズッキーニ10 0.066 0.071 0.064 0.061 メロン5 0.072 0.157 0.140 0.144 メロン1 0.235 0.236 0.235 0.236 キュウリ10 0.119 0.131 0.128 0.139 キュウリ1 0.485 0.476 0.474 0.472 ALDH 活性測定においては 30-60 分までほとんど吸光度の変化が見られない. よって 30 分での値からブランクの値を引いたものを吸光度変化量とすると Table 5.2.2.のようになる.
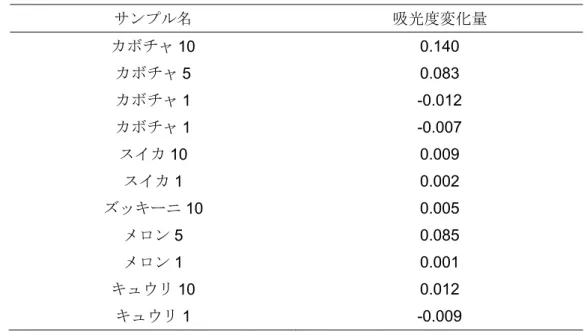
Table 5.2.2 ALDH 活性測定での吸光度変化量 サンプル名 吸光度変化量 カボチャ10 0.140 カボチャ5 0.083 カボチャ1 -0.012 カボチャ1 -0.007 スイカ10 0.009 スイカ1 0.002 ズッキーニ10 0.005 メロン5 0.085 メロン1 0.001 キュウリ10 0.012 キュウリ1 -0.009 5.3. 酸耐性評価 5.1.,5.2.と同様に酸処理溶液の残存活性について Table 5.3.1.にまとめた. Table 5.3.1.酸処理溶液の ADH 活性測定における吸光度変化 時間/min. ブランク 30 45 60 カボチャ 0.093 0.088 0.088 0.090 メロン 0.079 0.078 0.078 0.078 キュウリ 0.183 0.184 0.184 0.185 なお酸耐性評価において,Table 5.1.1.のサンプルのうちカボチャとメロンは果実 エキスと1 mol dm-3塩酸が体積比1:9,キュウリは 1:1 で混合している. 60 分の値からブランクの値を引いたものを吸光度変化量とし,Table 5.3.2.にまと めた. Table 5.3.2 酸処理溶液の ADH 活性測定での吸光度変化量 サンプル名 吸光度変化量 カボチャ -0.003 メロン -0.001 キュウリ 0.002
5.4. NADH の検量線の作成 4.4.(1)よりそれぞれの溶液の吸光度をブランク処理した値を Table 5.4.1.にま とめた. Table 5.4.1. NADHaq の吸光度 濃度/mmol dm-3 吸光度 0.107 0.655 0.094 0.570 0.047 0.302 以上より,検量線はFig. 5.4.1.のようになった. この検量線を用いて,酵素の分解反応により生成したNADH の濃度を求める. 5.1.ADH 活性測定,Table 5.1.2 .から求めた NADH 濃度を Table 5.4.2.に示す.
Table 5.4.2 ADH 活性測定での NADH 濃度
サンプル名 NADH 濃度/µmol dm-3 カボチャ10 4.919×10 カボチャ5 7.515×10 カボチャ1 1.779×10 カボチャ1 1.713×10 y = 6.0586x + 0.0052 R² = 0.9992 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0 0.02 0.04 0.06 0.08 0.1 0.12 吸光度 /ABS 濃度/mmol dm-3
Fig. 5.4.1.
NADHaqの検量線
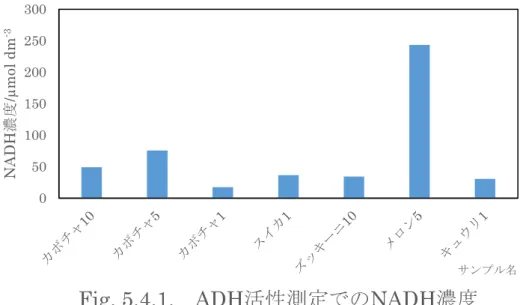
スイカ1 3.661×10 ズッキーニ10 3.433×10 メロン5 2.433×102 キュウリ1 3.050×10 Table 5.4.2.を棒グラフの形にまとめたものが Fig. 5.4.1.である. なお,カボチャ 1 に関してはほとんど同様の値となったため,平均を取ってい る.
同様に5.2.ALDH 活性測定,Table 5.2.2.より NADH 濃度は Table 5.4.3 のよう になる.
Table 5.4.3. ALDH 活性測定での NADH 濃度 サンプル名 NADH 濃度/µmol dm-3 カボチャ10 2.225×102 カボチャ5 6.421×10 カボチャ1 - 2.839 カボチャ1 -2.014 スイカ10 6.272 スイカ1 -5.282×10-1 ズッキーニ10 -3.301×10-1 メロン5 6.586×10 メロン1 -6.932×10-1 0 50 100 150 200 250 300 N AD H 濃度 /µm ol dm -3 サンプル名
Fig. 5.4.1. ADH活性測定でのNADH濃度
キュウリ10 1.122×10
キュウリ1 -2.343
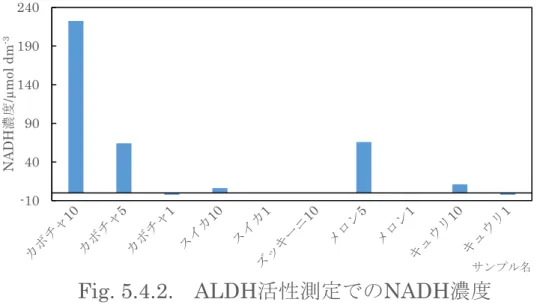
Table 5.4.3.の結果を Fig. 5.4.2.にまとめた.
なお,Fig. 5.4.2.と同様にカボチャ 1 に関しては 2 サンプルの平均を取った.
5.3.酸耐性評価,Table 5.3.2.より酸処理溶液の ADH 活性測定における NADH 濃度を求めTable 5.4.4.にまとめた.
Table 5.4.4 酸処理溶液の ADH 活性測定での NADH 濃度 サンプル名 NADH 濃度/µmol dm-3
カボチャ -1.353
メロン -1.023
キュウリ -0.5282
6. 考察
まず,ADH 活性測定に関して,5.4.NADHaq の検量線,Table5.4.2.より生成し た NADH の濃度を比較すると一番高い値となったサンプルはメロン 5 の 2.433× 102 µmol dm-3であった.ただし,同じ希釈倍率でもカボチャ1 では 0.66 µmol dm-3 の差が生じており,同種の果実を用いたサンプルでも,果実の収穫時期や果実の使 用部位によって含まれるアルコール分解酵素量に差が生じてしまう可能性が考えら れる.よって本実験においてメロンのサンプルから高い値が得られたからといって 一概にメロンに含まれるアルコール分解酵素量が多いとは言い難い. -10 40 90 140 190 240 NA D H 濃度 /µm ol dm -3 サンプル名
Fig. 5.4.2. ALDH活性測定でのNADH濃度
また,カボチャのサンプルに関してはNADH 濃度が.カボチャ 1<カボチャ 10< カボチャ5 となった.希釈濃度が大きくなると酵素量が少なくなり,NADH 濃度も 低くなると予想されるが,それと異なる結果となってしまった.カボチャ1 に関し ては4.5.夏休み以降の実験操作における変更点で述べた通り,瞬間冷却および遠心 分離後の吸引濾過を行っていないため、特に吸引濾過を行っていないことによる不 純物の混入などが考えられる. 次に,ALDH 活性測定に関しては希釈倍率が小さくなると NADH の生成量が少な くなっており濃度もNADH が生成したと言えるものはかなり少ない.また,サンプ ルによっては吸光度の値自体が ADH 活性測定に比べて小さいものも多い.希釈倍 率が小さくなると酵素量は増えるはずで,ALDH 活性が低下することは考えにくい. 本実験では時間の都合上,行うことが出来なかった 果実エキスの濃縮を行うこと でALDH 活性が確認される可能性がある. また,酸耐性評価についてカボチャ,メロン,キュウリの3 種について実験を行 ったが,どのサンプルにおいても残存活性は確認されなかった.スイカについては 実験を行った時期の都合上,入手が不可能であったため行うことが出来なかった. また,今回の酸耐性評価では予算の関係上,先行研究で用いられていた生体酵素 を含む人工胃液を作製できず1 mol dm-3塩酸を用いたため,実際のヒトの体内で同 じように残存活性が無くなるかどうかは不明である. ADH,ALDH 活性測定に多くの時間を割いてしまい,酸耐性評価のサンプル数を あまり確保できず,果実エキスと酸溶液の混合割合について最適なものを見つけら れなかった.また,実験で用いる試料果実の調達に関して大量の野菜果実の保存が 出来なかったために産地や収穫時期を統一したものを用意することができなかった. 希釈倍率の振り方と試料果実の調達方法を工夫することでより良い結果が得られる と思われる. 7. 結論 ウリ科植物であるキュウリ,カボチャ,スイカ,メロンについてアルコール分解 酵素 ADH が含まれていることが分かった.NADH の生成量で比較した場合,メロ ンの値が一番高い,という結果が得られた,しかし実際にどの果実に多く含まれて いるかについては産地や時期,旬など多くの要素によって影響を受ける可能性があ り,一概には言えないと考える. またALDH については活性が確認されないサンプルが多く,その原因の特定に至 らなかった.果実エキスの濃縮を行うことで活性が確認される可能性がある. また,酸耐性評価についても本実験では残存活性ゼロ,という結果になったが, 実際にヒトの体内で同様の結果が得られるか不明である.
8. 展望 同産地で収穫時期も同じころと見込まれる試料果実を大量に購入し,保存する方 法の確立,および人工胃液を用いた酸耐性評価を行うことによってより正確に果実 中の酵素活性について評価できると思われる. 参考文献 (1) 南方資源利用技術研究会,沖縄県産ウリ科植物に含まれるアルコール及びア ルデヒド分解酵素を利用した健康食品の開発, http://okinawa-repo.lib.u-ryukyu.ac.jp/bitstream/okinawa/14210/1/Vol21No1p17.pdf, 2016.2.26 取得 (2) 金子希代子,川原正博,神崎愷,小林茂樹,定金豊,馬渡健一,中込和哉,秋 澤俊史,『分析化学Ⅱ 機器分析編』,朝倉書店,2008,p112-116 (3) 中田宗隆,『なっとくする機器分析』,講談社,2007,p117-127 (4) 大木道則 他,『化学大辞典』,東京化学同人,第 7 刷 2003,p165 (5) 『化学大辞典』,p1013-1014 (6) 『化学大辞典』, p384 (7) 『化学大辞典』, p704 (8) 『化学大辞典』, p1174 (9) 『化学大辞典』, p172 (10)『化学大辞典』,p1038 (11)『化学大辞典』, p25 (12) 吉村壽次,『化学辞典 第 2 版』,森北出版,2009,p202 謝辞 春輪講にあたり,多くの意見をくださった先輩方,遠心分離および瞬間冷却の操作 に協力いただいた東京理科大学 理学部第一部 応用化学科 鳥越研究室の皆さま,夏 休み以降の実験において全面的にご協力いただいた東京理科大学 理学部第一部 教 養学科 武村研究室の深谷先輩に深く御礼申し上げます.