2018 年 6 月 8 日発行 2015‒2016 年度活動
【ダイジェスト版】
血管炎症候群の診療ガイドライン ( 2017 年改訂版)
Guidelines for Management of Vasculitis Syndrome ( JCS 2017 )
合同研究班参加学会・研究班
日本循環器学会 日本医学放射線学会 日本眼科学会 日本胸部外科学会 日本血管外科学会 日本小児科学会 日本心臓血管外科学会 日本心臓病学会
日本腎臓学会 日本病理学会 日本脈管学会 日本リウマチ学会 厚生労働省難治性疾患政策研究事業難治性血管炎に関する調査研究班
磯部 光章
榊原記念病院
東京医科歯科大学大学院循環制御内科学
班長
班員
石津 明洋
北海道大学大学院保健科学研究院 病態解析学
伊藤 秀一
横浜市立大学大学院医学研究科 発生成育小児医療学
有村 義宏
吉祥寺あさひ病院/杏林大学医学部 第一内科学腎臓・リウマチ膠原病内科
天野 宏一
埼玉医科大学総合医療センター リウマチ・膠原病内科
駒形 嘉紀
杏林大学医学部第一内科学 腎臓・リウマチ膠原病内科
小室 一成
東京大学医学部 循環器内科
小林 茂人
順天堂大学医学部附属 順天堂越谷病院内科
要 伸也
杏林大学医学部第一内科学 腎臓・リウマチ膠原病内科
種本 和雄
川崎医科大学 心臓血管外科
長谷川 均
愛媛大学大学院 血液・免疫・感染症内科学 東邦大学医療センター大橋病院高橋 啓
病理診断科
古森 公浩
名古屋大学大学院 血管外科
宮崎 龍彦
岐阜大学医学部附属病院 臨床病理部
宮田 哲郎
山王病院・山王メディカルセンター 血管病センター
藤元 昭一
宮崎大学医学部 血液・血管先端医療学講座
針谷 正祥
東京女子医科大学附属膠原病リウマチ痛風センター リウマチ性疾患薬剤疫学研究部門
和田 隆志
金沢大学医薬保健学総合研究科 腎臓内科学
吉田 晃敏
旭川医科大学 眼科
山田 秀裕
聖隷横浜病院 リウマチ・膠原病センター
協力員
大田 英揮
東北大学大学院医学系研究科 放射線診断学
岡崎 貴裕
聖マリアンナ医科大学 リウマチ ・ 膠原病 ・ アレルギー内科
内田 治仁
岡山大学大学院医歯薬学総合研究科 CKD・CVD地域連携包括医療学
井上 芳徳
てとあしの血管クリニック東京
木ノ内 玲子
旭川医科大学 医工連携総研講座・眼科
倉田 厚
東京医科大学 分子病理学分野
川上 民裕
聖マリアンナ医科大学 皮膚科
鬼丸 満穂
九州大学大学院医学研究院 病理病態学講座
目次
I.改訂にあたって ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥6 1. ガイドライン作成の背景 ‥‥‥‥‥‥‥‥‥‥‥‥6 2. 診療ガイドライン作成の方針 ‥‥‥‥‥‥‥‥‥‥6 2.1 対象疾患‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥6 2.2 診療ガイドラインの一般的な作成手法‥‥‥‥7 2.3 本診療ガイドラインの作成方法‥‥‥‥‥‥‥8
II.高安動脈炎 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥8 1. 疾患概念・疫学・細分類 ‥‥‥‥‥‥‥‥‥‥‥‥8 1.1 疾患概念‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥8 1.2 歴史的変遷‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥8 1.3 疫学‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥9 1.4 分類‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥9 2. 発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥9 2.1 遺伝的要因‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥9 2.2 環境要因‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥10 2.3 血管障害機序‥‥‥‥‥‥‥‥‥‥‥‥‥‥10 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥10 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥11 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥12 5.1 検査所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥12 5.2 画像所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥13 5.3 眼科検査‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥14
6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 15 6.1 診断基準‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 15 6.2 鑑別診断‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 15 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥16 7.1 ステロイド・免疫抑制薬‥‥‥‥‥‥‥‥‥ 16 7.2 生物学的製剤・抗血小板薬など‥‥‥‥‥‥ 18 7.3 観血的治療‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 19 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 20 9.小児の高安動脈炎 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥20
III.巨細胞性動脈炎 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥21
1.疾患概念・疫学・細分類 ‥‥‥‥‥‥‥‥‥‥‥ 21 1.1 疾患概念‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 21 1.2 疫学‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 21 1.3 細分類‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 21 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥21 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥21 3.1 罹患動脈‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 21 3.2 組織所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 22 3.3 鑑別診断ならびに類似疾患‥‥‥‥‥‥‥‥ 23 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 23 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 23 5.1 検査所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 23
(五十音順,構成員の所属は2017 年9月現在)
外部評価委員
重松 宏
国際医療福祉大学臨床医学研究センター 瀧原 圭子
キャンパスライフ健康支援センター大阪大学
木村 剛
京都大学大学院医学研究科 循環器内科学
尾崎 承一
聖マリアンナ医科大学
百村 伸一
自治医科大学附属さいたま医療センター 循環器内科
室原 豊明
名古屋大学大学院医学系研究科 循環器内科
重松 邦広
国際医療福祉大学三田病院 心臓血管センター血管外科
杉山 斉
岡山大学大学院医歯薬学総合研究科 血液浄化療法人材育成システム開発学
土橋 浩章
香川大学医学部 血液・免疫・呼吸器内科
吉藤 元
京都大学大学院医学研究科 内科学講座臨床免疫学
末松 栄一
独立行政法人国立病院機構 九州医療センター膠原病内科
岳野 光洋
日本医科大学大学院医学研究科 アレルギー膠原病内科学分野
中岡 良和
国立循環器病研究センター研究所 血管生理学部
渡部 芳子
川崎医科大学生理学1
佐田 憲映
岡山大学大学院医歯薬学総合研究科 腎・免疫・内分泌代謝内科学講座
杉原 毅彦
東京都健康長寿医療センター 膠原病・リウマチ科
堤野 みち
東京女子医科大学附属膠原病 リウマチ痛風センターリウマチ内科
前嶋 康浩
東京医科歯科大学大学院 医歯学総合研究科循環制御内科学
小菅 寿徳
つくば画像検査センター
末吉 英純
長崎大学大学院
医歯薬学総合研究科・放射線診断治療学
田村 直人
順天堂大学医学部 膠原病内科学講座
長坂 憲治
青梅市立総合病院 リウマチ膠原病科
5.2 画像所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥23 5.3 眼科検査‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥24 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥25 6.1 診断基準‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥25 6.2 診断にあたり注意すべき点‥‥‥‥‥‥‥‥25 6.3 大動脈病変の評価‥‥‥‥‥‥‥‥‥‥‥‥25 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥25 7.1 ステロイド・免疫抑制薬‥‥‥‥‥‥‥‥‥25 7.2 生物学的製剤・抗血小板薬など‥‥‥‥‥‥27 7.3 観血的治療‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥27 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥27
IV.バージャー病 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥28
1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥28 1.1 疾患概念‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥28 1.2 疫学‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥28 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥29 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥29 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥30 4.1 上下肢の虚血症状‥‥‥‥‥‥‥‥‥‥‥‥30 4.2 内臓動脈の罹患‥‥‥‥‥‥‥‥‥‥‥‥‥30 4.3 表在静脈炎‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥30 4.4 各症状の頻度‥‥‥‥‥‥‥‥‥‥‥‥‥‥30 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 5.1 身体診察‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 5.2 検査法‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 5.3 血管画像所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 5.4 血液学的検査‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 6.1 診断‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥31 6.2 鑑別すべき疾患‥‥‥‥‥‥‥‥‥‥‥‥‥31 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥33 7.1 保存的治療‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥33 7.2 外科治療‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥33 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥34 8.1 虚血肢の予後‥‥‥‥‥‥‥‥‥‥‥‥‥‥34 8.2 増悪因子・改善に寄与する因子‥‥‥‥‥‥34 8.3 非虚血肢の予後‥‥‥‥‥‥‥‥‥‥‥‥‥34 8.4 併存疾患ならびに生命予後‥‥‥‥‥‥‥‥34
V.結節性多発動脈炎 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥34 1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥34 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥34 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥35 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥35 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥35
6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 35 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥35 7.1 寛解導入療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 35 7.2 寛解維持療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 36 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 36
VI.顕微鏡的多発血管炎 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥37
1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 37 1.1 概念‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 37 1.2 疫学‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 37 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥37 2.1 遺伝因子‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥37 2.2 環境因子‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥37 2.3 病態‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥37 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥38 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥38 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 38 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 39 6.1 診断‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥39 6.2 鑑別診断の手順‥‥‥‥‥‥‥‥‥‥‥‥‥39 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥39 7.1 寛解導入療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥40 CQ1: ANCA関連血管炎の寛解導入治療では,
どのようなレジメンが有用か‥‥‥‥‥‥ 40 CQ2: 重症な腎障害を伴うANCA関連血管炎の 寛解導入治療で血漿交換は有用か‥‥‥‥ 40 7.2 寛解維持療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥41 CQ3: ANCA関連血管炎の寛解維持治療では,
どのようなレジメンが有用か‥‥‥‥‥‥ 41 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥42
VII.多発血管炎性肉芽腫症 ‥‥‥‥‥‥‥‥‥‥‥‥42 1.疾患概念・定義・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥42 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥42 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥42 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥43 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 43 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 43 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥43 7.1 寛解導入療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥43 CQ1: ANCA関連血管炎の寛解導入治療では,
どのようなレジメンが有用か‥‥‥‥‥‥ 43 CQ2: 重症な腎障害を伴うANCA関連血管炎の 寛解導入治療で血漿交換は有用か‥‥‥‥ 45 7.2 寛解維持療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥45 CQ3: ANCA関連血管炎の寛解維持治療では,
どのようなレジメンが有用か‥‥‥‥‥‥45 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥45
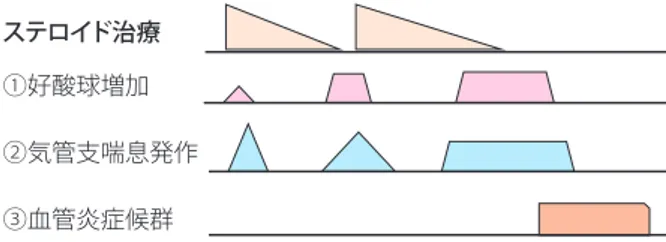
VIII.好酸球性多発血管炎性肉芽腫症 ‥‥‥‥‥‥‥‥45
1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥45 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥46 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥46 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥46 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥46 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥46 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥47 7.1 急性期‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥47 7.2 慢性期‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥48 7.3 寛解期‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥48 7.4 増悪期(再燃時) ‥‥‥‥‥‥‥‥‥‥‥‥48 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥48
IX.抗糸球体基底膜抗体病 ‥‥‥‥‥‥‥‥‥‥‥‥48 1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥48 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥48 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥49 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥49 5.検査所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥49 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥49 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥49 7.1 初期治療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥49 7.2 維持治療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥50 7.3 治療についての解説‥‥‥‥‥‥‥‥‥‥‥50 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥50
X.蕁麻疹様血管炎 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥50
1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥50 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥50 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥51 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥51 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥51 5.1 病理組織学的検査‥‥‥‥‥‥‥‥‥‥‥‥51 5.2 血清免疫学的検査所見‥‥‥‥‥‥‥‥‥‥51 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥51 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥51 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥52
XI.IgA血管炎(Henoch-Schönlein紫斑病) ‥‥‥‥‥52 1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥52 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53
4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53 4.1 皮膚症状‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53 4.2 関節症状‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53 4.3 消化器症状‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53 4.4 腎症状‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥53 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 53 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 53 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥54 7.1 腎外症状に対する治療‥‥‥‥‥‥‥‥‥‥54 7.2 腎炎を合併した場合‥‥‥‥‥‥‥‥‥‥‥54 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥55
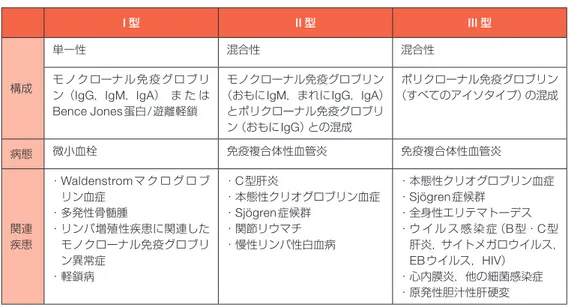
XII. クリオグロブリン血症性血管炎 ‥‥‥‥‥‥‥‥‥55 1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 55 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥55 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥55 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥55 5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 56 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥56 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥56 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥57
XIII. ベーチェット病 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58
1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 1.1 疾患概念‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 1.2 疫学‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 2.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 2.1 深部静脈血栓症‥‥‥‥‥‥‥‥‥‥‥‥‥58 2.2 動脈瘤・動脈閉塞‥‥‥‥‥‥‥‥‥‥‥‥58 2.3 肺動脈病変による症状‥‥‥‥‥‥‥‥‥‥58 3.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 3.1 検査所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 3.2 画像所見‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥58 4.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥59 4.1 診断‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥59 4.2 鑑別診断‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥59 5.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥59 5.1 薬物療法‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥59 5.2 外科手術と血管内治療‥‥‥‥‥‥‥‥‥‥60 6.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥60
XIV. 悪性関節リウマチ ‥‥‥‥‥‥‥‥‥‥‥‥‥‥61
1.疾患概念・疫学 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥61 2.発症機序 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥61 3.病理所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥61 4.症状 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥ 61
5.検査・画像所見 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥61 6.診断・診断基準 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥62 7.治療方針 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥62 8.予後 ‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥63
付表‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥64 文献‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥‥66
(無断転載を禁ずる)
略語一覧
3D-CT three-dimensional computed
tomography 三次元コンピュータ断層撮影
ABI ankle brachial index 足関節上腕血圧比
AAV ANCA-associated vasculitis ANCA関連血管炎 ACR American College of
Rheumatology 米国リウマチ学会
ADA adalimumab アダリムマブ
AKI acute kidney injury 急性腎障害
ANCA anti-neutrophil cytoplasmic
antibody 抗好中球細胞質抗体
AZA azathioprine アザチオプリン
bDMARDs biologic disease-modifying anti-rheumatic drugs 生物学的抗リウマチ薬 BVAS Birmingham Vasculitis Activity
Score バーミンガム血管炎活動性スコア
c-ANCA cytoplasmic anti-neutrophil
cytoplasmic antibody 細胞質型抗好中球細胞質抗体 CCr creatinine clearance クレアチニンクリアランス
CG cryoglobulin クリオグロブリン
CHCC Chapel Hill Consensus
Conference チャペルヒルコンセンサス会議
Cr creatinine クレアチニン
CT computed tomography コンピュータ断層撮影
CRP C-reactive protein C反応性蛋白
CyA cyclosporine シクロスポリン
CV cryoglobulinemic vasculitis クリオグロブリン血症性血管炎
CY cyclophosphamide シクロホスファミド
DMARDs disease-modifying anti-rheumatic drugs 抗リウマチ薬 EGPA eosinophilic granulomatosis with
polyangiitis 好酸球性多発血管炎性肉芽腫症
ESR erythrocyte sedimentation rate 赤血球沈降速度
ETN etanercept エタネルセプト
EULAR European League Against
Rheumatism 欧州リウマチ学会
EVG Elastica van Gieson エラスティカ・ファンギーソン
FDG fluorodeoxyglucose フルオロデオキシグルコース
GC glucocorticoid 糖質コルチコイド(副腎皮質ステロイド)
GCA giant cell arteritis 巨細胞性動脈炎
GBM glomerular basement membrane 糸球体基底膜 GFR glomerular filtration rate 糸球体濾過率 GPA granulomatosis with polyangiitis 多発血管炎性肉芽腫症
GLM golimumab ゴリムマブ
GRADE Grading of Recommendations, Assessment, Development and Evaluation
GWAS genome-wide association study ゲノムワイド関連研究
HBV hepatitis B virus B型肝炎ウイルス
HCV hepatitis C virus C型肝炎ウイルス
HE hematoxylin and eosin ヘマトキシリン・エオジン
HLA human leukocyte antigen ヒト白血球抗原 HUV hypocomplementemic urticarial
vasculitis 低補体血症性蕁麻疹様血管炎
HUVS hypocomplementemic urticarial
vasculitis syndrome 低補体血症性蕁麻疹様血管炎症候群
IFX infliximab インフリキシマブ
IL interleukin インターロイキン
IVCY intravenous cyclophosphamide シクロホスファミド間欠静注療法 IVIG intravenous high-dose
immunoglobulin 高用量ガンマグロブリン静注療法
LV-GCA large-vessel giant cell arteritis 大血管型巨細胞性動脈炎 MMF mycophenolate mofetil ミコフェノール酸モフェチル MPA microscopic polyangiitis 顕微鏡的多発血管炎
MPO myeloperoxidase ミエロペルオキシダーゼ
mPSL methylprednisolone メチルプレドニゾロン
MRA magnetic resonance angiography 核磁気共鳴血管造影 MRA malignant rheumatoid arthritis 悪性関節リウマチ MRI magnetic resonance imaging 核磁気共鳴画像法
MTX methotrexate メトトレキサート
MZR mizoribine ミゾリビン
NSAIDs non-steroidal anti-inflammatory
drugs 非ステロイド性抗炎症薬
PAN polyarteritis nodosa 結節性多発動脈炎
p-ANCA perinuclear anti-neutrophil
cytoplasmic antibody 核周囲型抗好中球細胞質抗体 PET positron emission tomography 陽電子放出断層撮影
PMR polymyalgia rheumatica リウマチ性多発筋痛症
PR3 proteinase 3 プロテイナーゼ3
PSL prednisolone プレドニゾロン
PSV primary systemic vasculitis 原発性全身性血管炎
RA rheumatoid arthritis 関節リウマチ
RCT randomized controlled trial ランダム化比較対照試験
RF rheumatoid factor リウマトイド因子
RLV renal-limited vasculitis 腎限局型血管炎 RPGN rapidly progressive
glomerulonephritis 急速進行性糸球体腎炎
RTX rituximab リツキシマブ
RV rheumatoid vasculitis リウマトイド血管炎
SLE systemic lupus erythematosus 全身性エリテマトーデス SNP single nucleotide polymorphism 一塩基多型
ST trimethoprim/sulfamethoxazole トリメトプリム・スルファメトキサゾール
TCZ tocilizumab トシリズマブ
TNF tumor necrosis factor 腫瘍壊死因子
略語一覧(続き)
I . 改訂にあたって
1.
ガイドライン作成の背景
血管炎は,血管自体に炎症を引き起こす疾患の総称であ る. 2012 年改定チャペルヒルコンセンサス会議( CHCC ) 分 類( CHCC2012 )の 正 式 な日本 語 名を
表11)に 示 す.
2007 年に日本循環器学会と厚生労働省難治性血管炎に関 する調査研究班が中心になり合同研究班を立ち上げ「血管 炎症候群のガイドライン」を発刊した
2).このたび,その後 の基礎・臨床研究の進歩をふまえ, 9 年ぶりに全面改訂版 である「血管炎症候群の診療ガイドライン 2017 年改訂版」
およびダイジェスト版を発刊することとなった.本ダイジェ スト版は,要点が簡潔に記載され日常診療に使いやすく工 夫されている.ぜひ診療にお役立てていただきたい.
2.
診療ガイドライン作成の方針
2.1
対象疾患
原発性血管炎は一般に, CHCC2012 (表
1)
1)を用いて表 記され,罹患血管サイズに基づいて,大型血管炎,中型血 管炎,小型血管炎に分類される.本診療ガイドラインでは,
大型血管炎として,高安動脈炎と巨細胞性動脈炎のほか,
バージャー病を対象疾患とした.中型血管炎では結節性多 発動脈炎,小型血管炎では抗好中球細胞質抗体( ANCA ) 関連血管炎である顕微鏡的多発血管炎( MPA ),多発血管 炎性肉芽腫症( GPA ),好酸球性多発血管炎性肉芽腫症
( EGPA ),免疫複合体性小型血管炎の抗 GBM 病,クリオ
I. 改訂にあたって
グロブリン血症性血管炎, IgA 血管炎,低補体血症性蕁麻
疹様血管炎を対象とした
1).中型血管炎である川崎病は,
ガイドライン利用者の診療領域を考慮し対象外とした.
CHCC2012 では上記のほか,多様な血管を侵す血管炎,
単一臓器血管炎,全身性疾患関連血管炎,推定病因を有 する血管炎が収載されているが
1),日常診療で遭遇する頻 度と診療上の重要度を考慮し,ベーチェット病およびリウ
表1 血管炎のカテゴリーと疾患CHCC2012原文1) 日本語訳
Large vessel vasculitis, LVV 大型血管炎
Takayasu arteritis, TAK 高安動脈炎*
Giant cell arteritis, GCA 巨細胞性動脈炎*
Medium vessel vasculitis, MVV 中型血管炎
Polyarteritis nodosa, PAN 結節性多発動脈炎*
Kawasaki disease, KD 川崎病
Small vessel vasculitis, SVV 小型血管炎
Antineutrophil cytoplasmic antibody (ANCA)-associated vasculitis, AAV 抗好中球細胞質抗体(ANCA)関連血管炎
Microscopic polyangiitis, MPA 顕微鏡的多発血管炎*
Granulomatosis with polyangiitis (Wegenerʼs), GPA 多発血管炎性肉芽腫症(Wegener肉芽腫症)*
Eosinophilic granulomatosis with polyangiitis (Churg-Strauss), EGPA 好酸球性多発血管炎性肉芽腫症(Churg-Strauss症候群)*
Immune complex SVV 免疫複合体性小型血管炎
Anti-glomerular basement membrane (anti-GBM) disease 抗糸球体基底膜抗体病(抗GBM病)*
Cryoglobulinemic vasculitis, CV クリオグロブリン血症性血管炎*
IgA vasculitis (Henoch-Schönlein), IgAV IgA血管炎(Henoch-Schönlein紫斑病)* Hypocomplementemic urticarial vasculitis, HUV (anti-C1q vasculitis) 低補体血症性蕁麻疹様血管炎(抗C1q血管炎)*
Variable vessel vasculitis, VVV 多様な血管を侵す血管炎
Behçetʼs disease, BD Behçet病*
Coganʼs syndrome, CS Cogan症候群
Single-organ vasculitis, SOV 単一臓器血管炎
Cutaneous leukocytoclastic angiitis 皮膚白血球破砕性血管炎
Cutaneous arteritis 皮膚動脈炎
Primary central nervous system vasculitis 原発性中枢神経系血管炎
Isolated aortitis 限局性大動脈炎
Vasculitis associated with systemic disease 全身性疾患関連血管炎
Lupus vasculitis ループス血管炎
Rheumatoid vasculitis リウマトイド血管炎*
Sarcoid vasculitis サルコイド血管炎
Vasculitis associated with probable etiology 推定病因を有する血管炎
Hepatitis C virus-associated cryoglobulinemic vasculitis C型肝炎ウイルス関連クリオグロブリン血症性血管炎*
Hepatitis B virus-associated vasculitis B型肝炎ウイルス関連血管炎
Syphilis-associated aortitis 梅毒関連大動脈炎
Drug-associated immune complex vasculitis 薬剤関連免疫複合体性血管炎
Drug-associated ANCA-associated vasculitis 薬剤関連ANCA関連血管炎
Cancer-associated vasculitis がん関連血管炎
*本ガイドラインで扱う疾患
(Jennette JC, et al. 2013 1)より)
マトイド血管炎を対象疾患とした.
2.2
診療ガイドラインの一般的な作成手法
診療ガイドラインの定義と作成方法は,時代とともに変
化している.世界保健機関( WHO )では,診療ガイドライ
ンを「診療と公衆衛生のための推奨を含む文書」と定義し ており
3),その作成法として GRADE システムを採用して いる.わが国の Minds ガイドラインセンターでは,診療ガ イドラインを「診療上の重要度の高い医療行為について,
エビデンスのシステマティックレビューとその総体評価,
益と害のバランスなどを考慮して,患者と医療者の意思決 定を支援するために最適と考えられる推奨を提示する文 書」と定義し,ガイドラインの作成法を公開している
4).
2.3
本診療ガイドラインの作成方法
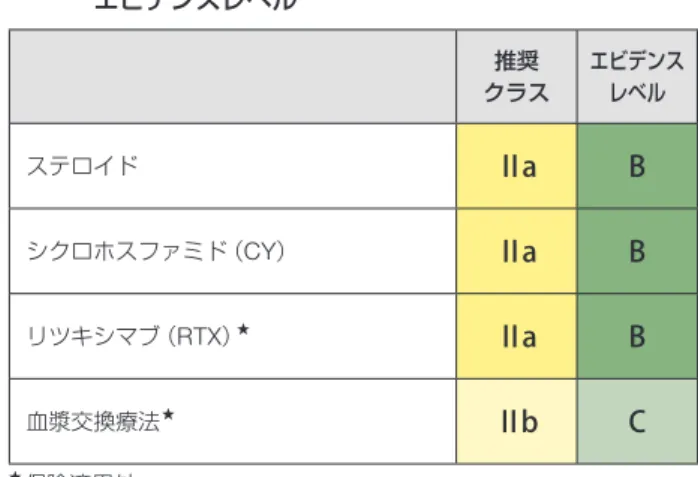
診療ガイドラインは GRADE システムあるいは Minds の 推奨する方法による作成が提唱されているが,希少性が高 い血管炎の各疾患に対してこれらの手法を完全に適用する ことはきわめて難しい.以上の点をふまえ,小型血管炎で ある MPA , GPA については GRADE システムに基づき推 奨を作成したが,それ以外の対象疾患に関しては,従来の 解説・レビュー形式を採用した.治療法の推奨度とエビデ ンスレベルについては,表
2,表
3の基準を用いた.
表2 推奨クラス分類 クラス I 実施すべきである
クラス IIa 実施は妥当である
クラス IIb 考慮してもよい
クラス III 無効または有害のため実施すべきではない
表3 エビデンスレベル
レベル A 複数のランダム化比較試験またはメタ解析から得られ たエビデンス
レベル B 単一のランダム化比較試験または非ランダム化研究か ら得られたエビデンス
レベル C 専門家の合意による意見
なってきており,予後は改善している
5, 6).
1.2歴史的変遷
高安右人は 1908 年に “奇異なる網膜中心血管の変化の 一例 ”として, 22 歳の女性を報告した(図
1)
7).橈骨動脈 の脈拍欠損が指摘されている. 1951 年,清水健太郎らは 25 例をまとめ,脈なし病( pulseless disease )と名付けて報 告した
8).上田英雄らは aortitis syndrome (大動脈炎症候 群)という病名を定着させた
9, 10).
1.
疾患概念・疫学・細分類
1.1
疾患概念
高安動脈炎は大動脈およびその基幹動脈,冠動脈,肺 動脈に生じる大血管炎である.主徴は全身の炎症,血管炎 による疼痛と血管狭窄・閉塞・拡張であり,炎症が鎮静化 した後も血流障害による各種臓器障害,動脈瘤が問題とな る.症状は多彩で,非特異的であるが,早期診断が可能と
II . 高安動脈炎
II. 高安動脈炎
1.3
疫学
1.3.1
年齢,性差,発生頻度
本疾患の登録は 6,000 人を超え,毎年の新規発症数は 300 人前後と推定される(図
2)
11).男女比は約 1 : 9 で,女 性における初発年齢は 20 歳前後にピークがある.症候が 多彩であるばかりか,非特異的な所見が多く,なお未診断 例が多いものと考えられる.
1.3.2
地域差
アジア,中近東での症例が多い.いずれの地域でも女性
に多い傾向がみられる.わが国および南米では頚動脈病変 が特徴的であるが,アジア諸国では腹部大動脈を主とした 病変による高血圧が多い.
1.4
分類
沼野らによる血管病変の分布による分類が用いられる
(図
3)
12-14).弓部の三分枝に病変を持つ例と,横隔膜下に
も病変を持つ例とに分けられる.血管造影の所見をもとに 分類したものであるが,血管内腔に著変がみられない部位 にも炎症性の肥厚が広範に認められることに留意すべきで ある
15).
2.
発症機序
遺伝的要因を背景に,感染などの環境要因がきっかけと なり,大動脈を主体とした弾性動脈が自己免疫機序により 破壊されると推定されている.
2.1
遺伝的要因
HLA-B*52 が本疾患の発症に関連することが報告され
ている
16, 17).加えて近年,発症感受性因子として IL12B 遺
伝子領域の遺伝子多型( single nucleotide polymorphism;
SNP )が同定された
18).
図1 高安右人博士と花環状吻合を示す眼底所見
(高安右人.1908 7)より)
図2 高安動脈炎の特定疾患医療受給証交付件数の推移
(難病情報センター 11)より)
件数
年 7000
6000 5000 4000 3000 2000 1000
01975 1980 1985 1990 1995 2000 2005 2010
2.2
環境要因
ウイルス感染の関与が推定されるが,誘因となるウイル スは同定されていない.
2.3
血管障害機序
T 細胞,マクロファージ, NK 細胞などの細胞がサイト カイン異常を伴って血管壁を障害すると考えられるが,そ の詳細なメカニズムは未解明である.
3.
病理所見
高安動脈炎は大型血管炎に分類され,大動脈とその主 要分枝動脈がしばしば侵襲される.肉眼的に罹患動脈は全 層が肥厚し,病変部では凹凸不整,斑状あるいは顆粒状の 内腔面を呈する.また,病変と病変の間にはしばしば健常 な部分が介在する(図
4).外膜には境界不明瞭な線維性 肥厚が目立つ.瘢痕期になると動脈壁は板状の石灰化を伴 い鉛管状を呈する(図
5)
19, 20).
組織学的に,初期には栄養血管( vasa vasorum )周囲へ の炎症細胞浸潤を伴った外膜の単核細胞浸潤が観察され,
中膜には梗塞性病変や断片化した弾性線維を貪食した多 核巨細胞を混ずる肉芽腫性動脈炎を呈する(図
6)
19-22).中 膜の外膜寄りに生じた炎症の結果,中膜弾性線維は虫食い 状に消失する.中膜,外膜には広範な線維化がもたらされ る一方,内膜にも細胞線維性肥厚が高度に生じ内腔狭窄に
至る(図
7)
19, 20).
瘢痕期には外膜は著しい線維化のために肥厚し,肥厚し た壁を有する vasa vasorum がしばしば観察される.動脈 内膜は進行性の線維性肥厚を示し,大動脈からの主要分 枝ではしばしば内腔狭窄に陥る.また,高度の線維化病変 が存在しても,病変の辺縁部で多核巨細胞を伴った活動性 炎症像が観察されることが多い
19).近年,早期診断,治療
図3 血管病変の分布による高安動脈炎の分類と頻度
(Hata A, et al. 1996 13),磯部光章.2014 14),Watanabe Y, et al. 2015 12)より)
Ⅰ型:大動脈弓分枝血管
Ⅱa型:上行大動脈.大動脈弓ならびにその分枝血管
Ⅱb型:Ⅱa病変+胸部下行大動脈
Ⅲ型:胸部下行大動脈,腹部大動脈,腎動脈
Ⅳ型:腹部大動脈,かつ/または,腎動脈
Ⅴ型:Ⅱb+Ⅳ型(上行大動脈.大動脈弓ならびにその分枝血管,胸 部下行大動脈に加え,腹部大動脈,かつ/または,腎動脈)
分類ごとの頻度
分類 頻度(%)
TypeⅠ 28.0 〜 35.9
TypeⅡa 9.4 〜 16.3
TypeⅡb 8.5 〜 16.6
TypeⅢ 0.9 〜 7.3
TypeⅣ 1.9 〜 5.9
TypeⅤ 25.8 〜 43.4
沼野らによる血管造影所見に基づく分類.上記のローマ数字および アルファベット小文字(Ⅰ,Ⅱa,Ⅱb,Ⅲ,Ⅳ,Ⅴ)に,冠動脈病 変ありの場合はC(+)を,肺動脈病変ありの場合はP(+)を付する.
Ⅰ Ⅱa Ⅱb Ⅲ Ⅳ Ⅴ 病変部位による分類 13)
図4 高安動脈炎の大動脈肉眼像1
弓部や腹部大動脈に褐色調,粗造な内腔面を呈する病変が認められ る.病変間には非病変部が介在しskip lesionを形成する.10代男性.
II. 高安動脈炎
の進歩による長期生存例の増加に伴い粥状動脈硬化症を
伴う症例や大動脈瘤,大動脈弁閉鎖不全などを伴う症例が 増加している.
樹皮状の内腔面を呈する大動脈は石灰化を伴った著明な線維性肥厚 を示す.50代女性.
図5 高安動脈炎の大動脈肉眼像2
外膜の広範な線維化とともに,外膜からの炎症により中膜外側が侵 襲され,中膜の梗塞巣を混ずる(⇨).病変には組織球,リンパ球と ともに多核巨細胞が出現し肉芽腫性炎症の像を呈する.巨細胞は弾 性線維を貪食する(➡).(左:HE染色,右:抗エラスチン抗体染色)
図6 高安動脈炎の大動脈組織所見
大動脈(左)・腕頭動脈(右)の組織所見.外膜の広範な線維化ととも に外膜からの炎症により,中膜外側を主とした弾性線維の虫食い状 消失が観察される.内膜肥厚は中膜傷害部に一致しており,弾性線 維の保たれた部位に内膜肥厚は生じていない.(EVG染色)
図7 高安動脈炎の組織所見
4.
症状
初発症状は,原因不明の発熱,全身倦怠感,頚部痛や さまざまな部位での疼痛,めまいなどで上気道炎と類似し た症状を認める(表
4)
12).その後,血管病変に起因する症 状を呈してくる.
表4 高安動脈炎の初発時にみられる主訴
有症率(%)
頭頚部症状 26.6
めまい 頭痛 失神発作 咬筋疲労 頚部痛
9.4 8.2 2.6 0.4 9.7
眼症状 3.3
失明 視力障害
0.1 2.7
上肢症状 17.3
脈なし
収縮期血圧左右差(≧10 mmHg)
易疲労感 冷感 しびれ感
4.9 3.9 4.6 1.7 3.6
心症状 11.1
息切れ 動悸 胸部圧迫感
4.4 2.1 1.5
呼吸器症状 6.7
血痰 呼吸困難
0.8 4.4
高血圧 3.9
下肢症状 # 3.6
体幹部の疼痛 * 15.9
全身症状 41.0
発熱 全身倦怠感 易疲労感
34.7 12.1 1.7 1,372例での報告
# 間欠性跛行,易疲労感,冷感,しびれ感,痛み
* 胸痛,背部痛,腹痛
(Watanabe Y, et al. 2015 12)より抜粋)
表6 高安動脈炎の合併症
有症率(%)
大動脈弁閉鎖不全 33.2
Grade I* Grade II* Grade III* Grade IV*
14.1 8.6 9.8 6.2
虚血性心疾患 10.6
眼症状 14.0
白内障 7.6
眼底所見 8.7
大動脈瘤 15.0
大動脈解離 1.9
腎障害 11.2
高血圧合併症 39.4
腎動脈狭窄 13.1
脳虚血発作 13.2
脳血栓 3.7
脳出血 0.9
1,372例での報告 * カラードップラー心エコーにより評価
(Watanabe Y, et al. 2015 12)より抜粋)
表5 高安動脈炎の臨床症状
有症率(%)
頭頚部症状 47.5
眼症状 14.3
上肢症状 66.4
心症状 37.8
呼吸器症状 10.8
高血圧 38.0
下肢間欠性跛行 9.5
全身症状 74.9
1,372例での報告
頭頚部症状 ... めまい,頭痛,失神発作,片麻痺,咬筋疲労 眼症状 ... 失明,視力障害,眼前暗黒感
上肢症状 ... 脈なし,収縮期血圧左右差(10 mmHg以上),易疲労 感,冷感,しびれ感
心症状 ... 息切れ,動悸,胸部圧迫感 呼吸器症状 ... 血痰,咳,呼吸困難 全身症状 ... 発熱,全身倦怠感,易疲労感
(Watanabe Y, et al. 2015 12)より抜粋)
下腿,とくに脛骨前面に皮疹(結節性紅斑)が多発することが多い.
図8 高安動脈炎でみられる皮疹(結節性紅斑)
他覚症状を含めると,左右上肢の血圧差や上肢の脈拍 が触知しないといった上肢乏血所見を認める症例が約 66 %ともっとも多い.ついでめまいや頭痛などの症状が約 48 %の症例で認められる.視力障害をもつ患者は約 14 %で 認められる.約 40 %の症例で高血圧を認める(表
5)
12).高 安動脈炎では下腿,とくに脛骨前面に皮疹(結節性紅斑)
が多発することが多い(図
8).
合併症として,大動脈弁閉鎖不全症,大動脈瘤,大動 脈解離,脳虚血発作,肺梗塞,狭心症,鎖骨下動脈盗流 症候群,異型大動脈縮窄症,腎血管高血圧症などがあげ られる(表
6)
12).表
6にみられるように,狭窄病変や拡張 病変に起因するものなど多彩であり,かつ,多発する傾向 にある.症状としては,無症状で経過する例から早期に 種々の症状を合併する症例まで多彩である.さらには炎症
性腸疾患や結節性紅斑,関節炎など自己免疫疾患に類す る症状が合併する.
5.
検査・画像所見
5.1
検査所見
高安動脈炎の診断に有用な特異的な血液・生化学検査
はないが,現時点では非特異的な炎症の指標である C 反
応性蛋白( CRP )と赤血球沈降速度( ESR )が本症の診断
にもっとも有用なバイオマーカーである.高安動脈炎は遺
伝的素因を示す場合があり,免疫制御に関わる HLA クラ
ス I 分子 ‒ B*52 や HLA ‒ B*67 との有意な関連があること
が知られているため
23, 24),これらが診断の補助として用い
II. 高安動脈炎
られる場合がある.
高安動脈炎の活動性の評価に有用な検査所見としては,
CRP と ESR のほかに,白血球数の上昇,貧血の進行,免 疫グロブリンや補体など免疫学的検査値の異常などがあげ られる.ことに, CRP は糖質コルチコイド( GC )治療を受 けた本症の患者の経過観察に有用であるが
25, 26),ヒト化抗 ヒト IL-6 受容体モノクローナル抗体であるトシリズマブ
( TCZ )の投与下では CRP を用いた高安動脈炎の活動性評 価に用いることができないことに留意しなければならない.
血清アミロイド A
27), Pentraxin-3 ( PTX3 )
28-30), IL-6
31), IL-18
32), sRAGE
33),可溶性 ICAM-1
34),マトリックスメ タロプロテアーゼ
35)なども高安動脈炎の活動性の評価に有 用であると報告されているが,これらのバイオマーカーは 実際の臨床の現場で高安動脈炎の診療に使用されるには 至っておらず, 2018 年の時点で保険が適用されていない.
5.2
画像所見
本疾患の初期評価には CT , MRI が推奨される(図
9) .
a. 胸部単純X線における下行大動脈辺縁の波状化
b. CT angiography(最大値投影法)における大動脈壁の石灰化
c. 頚動脈超音波における内膜-中膜複合体のびまん性・全周性肥厚
図9 高安動脈炎の画像所見
図10 高安動脈炎の造影CT画像
a. 単純CT b. 造影早期相CT c. 造影後期相CT
5.2.1
胸部単純 X 線
下行大動脈辺縁の波状化を認める(図
9a, 矢印).
5.2.2
CT
CT では,大血管や冠動脈,各臓器を評価する(図
9b).
初回時は 3 相撮影が望ましいが,再検時は被曝低減を考慮 する.単純 CT の動脈壁は,内腔より高濃度を示す(図
10a)
36).造影早期相 CT では内腔と壁の良好なコントラス トが得られる(図
10b).造影後期相 CT では,本疾患の早期 に大動脈壁の“ double ring-like pattern ”を認める(図
10c).
慢性期では,内腔の狭窄・拡張,壁の全周性石灰化(図
9b),側副血行路の発達を認める
37, 38).
5.2.3
MRI
造影 MR angiography では,内腔,壁肥厚,壁の造影剤 増強効果を評価する(図
11,
12)
15, 39, 40).非造影 MR angi-
上行大動脈の軽度拡張と弓部3分枝近位部の閉塞を認める.
図11 ガドリニウム造影MRA
a. 単純T1強調像.b. ガドリニウム造影T1強調像.左総頚動脈に壁 肥厚と造影剤増強効果を認める.
図12 高安動脈炎のMRI画像
ography でも大血管の形態評価は可能である.長期経過観 察には被曝のない MRI が望ましい
41).
5.2.4
血管造影
血管造影は,血管内治療や小血管,冠動脈などの評価 目的に用いられる
42).
5.2.5
超音波
高安動脈炎では,肥厚した総頚動脈壁の高輝度所見(マ カロニサイン)を認める(図
9c)
43, 44).
5.2.6
18
F-FDG PET / PET-CT
大血管壁への
18F-FDG 集積は診断に有用な所見である
(図
13)
45).
18F-FDG PET / PET-CT は, 2018 年 4 月より一 部の PET 施設では,他の検査で病変の局在または活動性
の判断がつかない大型血管炎患者を対象に,保険適用のも とでの検査が可能となった.
5.3
眼科検査
5.3.1
眼虚血による病態
高安動脈炎患者の 18 〜 30 %に霧視・視力低下,一過性 視力障害や眼痛などがみられ
46, 47),これらはおもに眼への 循環不全により生じる.高安網膜症(低灌流網膜症),虚血 性視神経症,虹彩新生血管などがあり,高安動脈炎 I , II , V 型(血管造影による沼野分類)
13)でみられる(図
3)
12-14). 高安網膜症では網膜血管の屈曲・蛇行,網膜静脈の拡張,
網膜毛細血管瘤,網膜出血,軟性白斑などが眼底で観察さ れる(図
14).網膜広汎に散在する毛細血管瘤と,眼虚血 が進行して起こる視神経乳頭部の花環状血管吻合は特徴 的な所見である(図
1)
7).眼底造影では腕 - 網膜循環時間の 延長,毛細血管の閉塞,毛細血管瘤,動静脈吻合などがみ られ,進行すると網膜や視神経乳頭に新生血管が認められ る(図
15).
5.3.2
高血圧による病態
腹部大動脈 / 腎動脈狭窄により高血圧を合併することが ある III , IV , V 型では,高血圧網膜症がみられることがあ る.眼底に網膜動脈の狭細,網膜浮腫,白斑,出血,視神 経乳頭浮腫を生じてくる.報告は少ないが,高血圧脈絡膜 症も生じることがある.
上行大動脈〜弓部3分枝に集積を認める.
図13 高安動脈炎の18F-FDG PET-CT画像
冠状断fusion画像 水平断fusion画像
II. 高安動脈炎
6.
診断・診断基準
6.1
診断基準
今回のガイドライン改訂にあたり,厚労省難治性血管炎研 究班・大型血管炎分科会において, 2008 年版ガイドライン
2)の高安動脈炎診断基準の骨子は変更せず,医学の進歩を反 映させて一部修正した新たな診断基準を作成した(表
7).
診断は,画像診断( CT , MRI ,超音波, PET-CT ,胸部 X 線,血管造影)を中心に行う.表
7のうち, A ) 1 項目以上の 症状と, B )大動脈とその第一次分枝の両方あるいはどちら かに,多発性またはびまん性の肥厚性病変,狭窄性病変(閉 塞を含む)あるいは拡張性病変(瘤を含む)のいずれかを認 め, C )鑑別疾患を除外できるものを高安動脈炎と診断する.
活動性がある大多数の症例で血液検査上の炎症所見の上 昇が認められ,診断の参考所見となるが,初診時に炎症所 見が正常である症例も存在し,また非活動性の症例は通常 炎症所見は認められないことに留意する.疫学的特徴(若年 女性に好発し,通常症状の発現が 40 歳以下)や, HLA-B*52 または HLA-B*67 の保有は,診断の参考所見とする.
なお
18F-FDG PET は, 2018 年 4 月より一部の PET 施設 では,他の検査で病変の局在または活動性の判断がつかな い大型血管炎患者を対象に,保険適用のもとでの検査が可 能となった.
6.2
鑑別診断
鑑別すべき疾患として①動脈硬化症,②先天性血管異常,
③炎症性腹部大動脈瘤,④感染性動脈瘤,⑤梅毒性中膜 炎,⑥巨細胞性動脈炎(側頭動脈炎),⑦血管型ベーチェッ ト病,⑧ IgG4 関連大動脈周囲炎があげられる.動脈硬化 症とは,発症年齢や罹患血管の分布である程度鑑別可能で ある.先天性血管異常としては mid-aortic syndrome がある が,大動脈の縮窄を認めるも壁は平滑である点から鑑別可 能である.炎症性腹部大動脈瘤は炎症を認め,水腎症を伴 うことが多く, CT で mantle sign が特徴である.感染性動 脈瘤は嚢状の動脈瘤を呈することが多く多発性のこともあ るが,瘤以外に病変がなく,その他の所見を参考にすれば 鑑別可能である.梅毒性中膜炎は,最近では経験すること
網膜静脈の拡張が著明で,網膜出血,軟性白斑がみられる.図14 高安動脈炎の眼底所見
網膜静脈の拡張と口径不同,毛細血管瘤がみられる.上方周辺部に は網膜新生血管が生じている.
図15 高安動脈炎のフルオレセイン眼底造影所見
は少ないが,血清学的・細菌学的に鑑別する.巨細胞性動 脈炎は高齢者に好発し,筋痛(リウマチ性多発筋痛症)をし ばしば合併する.血管型ベーチェット病は,嚢状の動脈瘤 をきたすことがあるが,その他の所見を参考にすれば鑑別 は可能である. IgG4 関連大動脈周囲炎は,血清 IgG4 濃度 や他臓器における IgG4 関連疾患病変から鑑別可能である.
7.
治療方針
表8
に高安動脈炎の治療に関する推奨を,
図16に高安 動脈炎の治療フローチャートを示す.
7.1
ステロイド・免疫抑制薬
7.1.1
ステロイド( glucocorticoids; GC )
a. 適応過去のコホート解析では,症例の
79
〜94
%6, 48-50)に,プ レドニゾロン(PSL
)が疾患活動性(Kerr
の基準50a)等で判 断する)を根拠に投与されていた.b. 初期量とその維持期間
国外の報告では PSL 1 mg/kg/ 日× 1 ヵ月
48, 50-52)などの用
表7 高安動脈炎の診断基準 A.症状
1. 全身症状:発熱,全身倦怠感,易疲労感,リンパ節腫脹(頚部),若年者の高血圧 (140/90 mmHg以上)
2. 疼痛:頚動脈痛(carotidynia),胸痛,背部痛,腰痛,肩痛,上肢痛,下肢痛
3. 眼症状:一過性又は持続性の視力障害,眼前明暗感,失明,眼底変化(低血圧眼底,高血圧眼底)
4. 頭頚部症状:頭痛,歯痛,顎跛行※a,めまい,難聴,耳鳴,失神発作,頚部血管雑音,片麻痺
5. 上肢症状:しびれ感,冷感,拳上困難,上肢跛行※b,上肢の脈拍及び血圧異常(橈骨動脈の脈拍減弱,消失,10 mmHg以上の血圧左右差),
脈圧の亢進(大動脈弁閉鎖不全症と関連する)
6. 下肢症状:しびれ感,冷感,脱力,下肢跛行,下肢の脈拍及び血圧異常(下肢動脈の拍動亢進あるいは減弱,血圧低下,上下肢血圧差※c)
7. 胸部症状:息切れ,動悸,呼吸困難,血痰,胸部圧迫感,狭心症状,不整脈,心雑音,背部血管雑音 8. 腹部症状:腹部血管雑音,潰瘍性大腸炎の合併
9. 皮膚症状:結節性紅斑
※a 咀嚼により痛みが生じるため間欠的に咀嚼すること
※b 上肢労作により痛みや脱力感が生じるため間欠的に労作すること
※c 「下肢が上肢より10〜30 mmHg高い」から外れる場合 B.検査所見
画像検査所見:大動脈とその第一次分枝※aの両方あるいはどちらかに検出される,多発性※bまたはびまん性の肥厚性病変※c,狭窄性病 変(閉塞を含む)※dあるいは拡張性病変(瘤を含む)※dの所見
※a 大動脈とその一次分枝とは,大動脈(上行,弓行,胸部下行,腹部下行),大動脈の一次分枝(冠動脈を含む),肺動脈とする.
※b 多発性とは,上記の2つ以上の動脈または部位,大動脈の2区域以上のいずれかである.
※c 肥厚性病変は,超音波(総頚動脈のマカロニサイン),造影CT,造影MRI(動脈壁全周性の造影効果),PET-CT(動脈壁全周性の FDG取り組み)で描出される.
※d 狭窄性病変,拡張性病変は,胸部X線(下行大動脈の波状化),CT angiography, MR angiography,心臓超音波検査(大動脈弁閉 鎖不全),血管造影で描出される.上行大動脈は拡張し,大動脈弁閉鎖不全を伴いやすい.慢性期には,CTにて動脈壁の全周性石 炭化,CT angiography, MR angiographyにて側副血行路の発達が描出される.
画像診断上の注意点:造影CTは造影後期相で撮影.CT angiographyは造影早期相で撮影,三次元画像処理を実施.血管造影は通常,
血管内治療,冠動脈・左室造影などを同時目的とする際に行う.
C.鑑別診断
動脈硬化症,先天性血管異常,炎症性腹部大動脈瘤,感染性動脈瘤,梅毒性中膜炎,巨細胞性動脈炎(側頭動脈炎),血管型ベーチェット病,
IgG4関連疾患
<診断のカテゴリー>
Definite: Aのうち1項目以上+ Bのいずれかを認め,Cを除外したもの.
(参考所見)
1.血液・生化学所見:赤沈亢進,CRP 高値,白血球増加,貧血 2.遺伝学的検査:HLA-B*52またはHLA-B*67保有
II. 高安動脈炎
法で使われている. 2008 年版ガイドラインでは PSL 20 〜
30 mg/ 日× 2 週と用量は少ないが「症例に応じて 60 mg/ 日 まで引き上げる」と付記されており,その用法で PSL 単独 の有効率は約 50 %であった
53).日本の 106 例の後ろ向きコ ホート
6)では,初期 PSL 量は 38.9 ± 14.6 mg/ 日であり,お よそ 0.5 〜 1 mg/kg/ 日に相当する.
c. ステロイドパルス療法(推奨クラス
IIb
,エビデンスレベ ルC
)緊急度の高い場合や難治例の再燃時に行われる52, 54, 55). d. 減量速度と維持量
PSL の減量は,寛解状態にあることを①症状,②血液炎 症マーカー,③画像所見で確認しつつ行う.日本の 106 例 の後ろ向きコホート研究
49)によると,再燃に寄与するもっ とも重要な因子は PSL 減量速度であり,減量速度が 1 ヵ月
表8 高安動脈炎の治療に関する推奨とエビデンスレベル 推奨
クラス エビデンス レベル
ステロイド
I B
ステロイドパルス療法
Ⅱb C
メトトレキサート(MTX)★
Ⅱa B
アザチオプリン(AZA)
Ⅱa B
シクロホスファミド(CY)
Ⅱb B
ミコフェノール酸モフェチル(MMF)★
Ⅱb B
タクロリムス(TAC)★
Ⅱb C
シクロスポリン(CyA)★
Ⅱb C
トシリズマブ(TCZ)
I B
TNF阻害薬 ★
Ⅱa B
抗血小板薬
Ⅱa B
血管バイパス手術
Ⅱa C
血管内治療
Ⅱb C
★保険適用外
あたり 1.2 mg より速いか遅いかで再燃率が有意に異なって いた. 2008 年版ガイドライン
56)のプロトコルでは, 2 週ご とに 5 mg ずつ 10 mg/ 日まで,以降は 2 週ごとに 2.5 mg ず つ維持量まで減量しているが,日本のコホート
6)における 再燃時 PSL 量が 13.3 ± 7.5 mg/ 日であったことを考慮し,
PSL 20 mg/ 日未満に達したら,きわめて慎重な減量速度 にすべきである.維持量は, PSL 5 〜 10 mg/ 日とするプロ トコルが多い
49, 52, 57).
e. GCフリー寛解
米国の
PSL
中止を目指すプロトコル51)で30
例中5
例(
17
%)がGC
フリー寛解を維持した.1975
年の日本の150
例の統計ではGC
離脱例は37.4
%であった56).f. 再燃時の増量
寛解導入治療をやり直すか,小幅な増量を行うかは,重 症度から判断する.
7.1.2
免疫抑制薬
a. メトトレキサート(MTX)(推奨クラス
IIa
,エビデンス レベルB
)(保険適用なし)米国のシングルアーム試験では, PSL 単独治療の効果が 不十分または再燃した例に, MTX ( 0.3 mg/kg/ 週から漸 増)と PSL ( 1 mg/kg/ 日から漸減)を投与し, 81 %が寛解し,
7 〜 18 ヵ月後に 50 %が寛解を維持した
58). MTX は高安動 脈炎にもっともよく使われてきた免疫抑制薬といえる.し かし,血管病変の進展を阻止できない可能性があることと,
無効または副作用で中止されることが少なくないことが問 題といえる
6, 50, 59).
b. アザチオプリン(AZA)(推奨クラス
IIa
,エビデンスレ ベルB
)(2011
年2
月23
日保険適用)インドのシングルアーム試験では,初発例に AZA ( 2 mg/
kg/ 日)と PSL ( 1 mg/kg/ 日から漸減)を併用投与し,全例 が寛解し 12 ヵ月後まで症状寛解を維持したが, 12 ヵ月後に 40 %で CRP または ESR が高値となっており,一部に血管 病変の進展例がみられた
57).各国のプロトコルにおける AZA の位置づけは高く, MTX の無効例に投与されること が多い.
c. シクロホスファミド(CY)(推奨クラス