日小 血 会 誌20 : 71-83, 2006
総
説
急性 白血病 にお ける微小残 存病変診 断 とその臨床応用
横 田 昇 平*1, 岡 本 朋 美*1, 鶴 澤 正 仁*2,3 *1京都 府 立 医科 大 学 血 液 ・腫 瘍 内 科, *2愛 知 医科 大 学 小 児 科, *3小 児 癌 白血 病 研 究 グル ープ(CCLSG)代 表 者Detection of Minimal Residual Disease and Its Clinical Application for Childhood Leukemia
Shohei YOKOTA,*1 Tomomi OKAMOTO*1 and Masahito TSURUSAWA*2,3
*1
Department of Hematology, Kyoto Prefectural University of Medicine
*2
Department of Pediatrics, Aichi Medical University
*3
Chairman of Japanese Children's Cancer and Leukemia Study Group
Abstract
More than 1012
tumor cells are present in a leukemia patient at diagnosis. They decrease in number along
with the chemotherapy and become undetectable by a microscope. Since the 80's several methods have been invented
to visualize the existence of minimal residual disease (MRD). The most useful MRD assays currently available are
polymerase chain reaction (PCR) amplification of fusion transcripts and rearranged T-cell receptor and
immunoglob-ulin genes, and flow cytometric (FCM) detection of aberrant immunophenotypes. Both PCR and FCM methods allow
detection of 1 leukemic cell in 10,000 normal cells in at least 90% of patients with acute lymphoblastic leukemia. A
number of clinical studies have elucidated that MRD assays are increasingly important in the clinical management of
patients with acute leukemia. Several studies in children and adult patients with acute lymphoblastic leukemia and
acute myeloid leukemia have shown a strong association between MRD and risk of relapse, irrespective of the
meth-odology used to detect residual disease. Those who are positive for bone marrow MRD have a bad prognosis either
after a standard protocol or the salvage therapy and stem cell transplantation for relapsed patients. These findings lead
to the idea of modifying the therapeutic regimen according to the amount of MRD. The international BFM group in
Europe and Japanese Children's Cancer and Leukemia Study Group (CCLSG) have started MRD-based protocol for
ALL children.
要 約 初 診 時 の 白血 病 患 者 体 内 に は1012個(約1kgに 相 当)も の 白血 病 細 胞 が 存 在 す る.急 性 白 血 病 で は,初 診 時 の 末 梢 血 白血 病 細 胞 数 な ど を も とに リス ク分 類 を行 い,こ れ に応 じた 治 療 プ ロ トコー ル を 設 定 す る,い わ ゆ るセ ッ ト療 法 が 一 般 的 で あ る.し か し,血 液 腫 瘍 で は固 形 腫 瘍 の よ う に画 像 診 断 等 で 残 存 す る腫 瘍 量 を測 定 す る こ とが 困 難 で あ る こ と か ら,再 発 しな い 限 り,一 度 定 め た プ ロ トコ ー ル を途 中 で 変 更 す る こ と な く,最 後 ま で 治 療 を 行 う こ とが 一 般 的 で あ った.寛 解 導 入 後 も体 内 に 存 在 す る微 小 残 存 病 変(MRD) を 診 断 す る手 段 と して,1980年 代 後 半 か ら分 子 生 物 学,免 疫 学 的 手 法 が 次 々 と開 発 さ れ た.と くにPCR法 は腫 瘍 細 胞 に あ って は正 常 の 造 血 細 胞 に は な い 遺 伝 子 の再 構 成 を 同 定 す る こ とで104∼106に1個 の 高 感 度 で MRDの 診 断 を可 能 に した.フ ィ ラデ ル フ ィア 染 色 体 のBCR/ABL遺 伝 子 再 構 成 を は じめ, 20種 類 もの 染 色 体 転 座 に伴 う遺 伝 子 の 再 構 成 がPCR増 幅 可 能 でMRD診 断 に 応 用 さ れ て い る.一 方,多 くの リ ンパ 系 腫 瘍 で は,免 疫 グ ロ ブ リ ンH鎖,T細 胞 受 容 体 δ.γ 鎖 遺 伝 子 が 単 ク ロー ン性 に再 構 成 して い る.再 構 成 の 結 合 部 塩 基 配 列 は ク ロ ー ン特 異 的 で あ り,こ れ をPCR増 幅 す る こ とでMRDの 診 断 が 行 わ れ て い る.ま た,白 血 球 分 化 抗 原 を モ ノ ク ロー ナ ル 抗 体 で 検 出す る細 胞 免 疫 学 的方 法 も2個 以上 の 抗 原 の パ ネル を マ ー カ ー と し, flow cytometry (FCM)を 利 用 す る こ とで,感 度 と特 異 性 を あ げ て い る.こ れ ら の方 法 を 利 用 して 多 施 設 共 同 臨 床 研 究 に お いて 治 療 経 過 の 定 時 に骨 髄 で のMRD定 量 を 行 い, MRDと 予 後 と の 関 連 を調 べ た結 果,治 療 早 期 のMRDと 予 後 と の 強 い相 関 が 明 らか に な った.ま た,再 発 例 に 対 す る治 療(salvage therapy)に お 2006年3月22日 受 理 別 刷 請 求 先:〒602-8566京 都 市 上 京 区 河 原 町広 小 路 上 る梶 井 町465京 都 府 立 医 科 大 学 血 液 ・腫 瘍 内 科 横 田昇 平Reprint requests to Shohei Yokota, Department of Hematology, Kyoto Prefectural University of Medicine, 465, Kajii-cho,
Kawaramachi-Hirokoji, Kamigyo-ku, Kyoto, 602-8566 Japan
い て も,早 期MRDと 予 後 の 関 連 が 認 め られ,再 発 例 に対 す る造 血 幹 細 胞 移 植 に お い て も,移 植 前 のMRD
は予 後 を 決 定 す る因 子 で あ る こ とが 報 告 され て い る.こ の よ う な知 見 を 得 て,MRD結 果 を 治 療 に応 用 す る
試 み が 始 ま って い る.早 期MRD量 に 基 づ い て,治 療 介 入 を 行 うプ ロ トコ ー ル は ドイ ッ を 中 心 と したBFM
グル ー プ や 日本 のCCLSGグ ル ー プ で2000年 か ら始 ま って い る.
Key words: minimal residual disease (MRD), flow cytometry (FCM), childhood leukemia
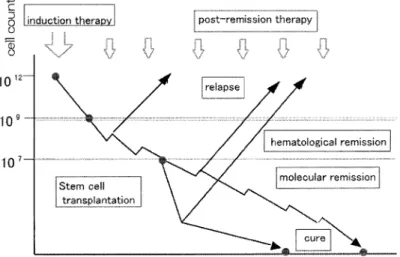
1. は じ め に 急 性 白血 病 患 者 の 体 内 に は,初 診 時 約1012個 の腫 瘍 細 胞 が存 在 す る.多 剤 併 用 の 強 力 な化 学 療 法 を施 す こ とで 白血 病 細 胞 は急 激 に 減 少 し,正 常 造 血 が 回 復 し,完 全 寛 解(complete remission, CR)に 至 る.し か しな が ら光 学 顕 微 鏡 で 骨 髄 中 に 白 血 病 細 胞 が み られ な くな る この 時 期 に も,体 内 に は最 大1010個 もの 腫 瘍 細 胞 が 残 存 して い る. こ れ に対 して,寛 解 後 療 法(地 固 め療 法,強 化 ・維 持 療 法)を 行 う こ と で 白血 病 細 胞 の再 増 殖 が 抑 制 さ れ,寛 解 の深 度 を 高 め る こ とが で き る.こ う して,治 療 を継 続 す る こ とで 体 内 の 白血 病 細 胞 量 は さ らに減 少 し,治 療 を 中 止 して も再 発 し な い レ ベ ル に 至 る と考 え られ て い る (Fig. 1). 小 児 領 域 白血 病 の予 後 改 善 は,新 しい 薬 剤 の登 場 もさ る こ と な が ら,白 血 病 の 多 施 設 共 同治 療 研 究 を通 じた科 学 的 検 証 の 積 み 重 ね に よ る と こ ろ が大 きい.患 者 の予 後 は,診 断 時 の 病 型,白 血 球 数,白 血 病 細 胞 形 質,患 者 の 年 齢 な ど の 初 診 時 の危 険 因子 と相 関 が あ る こ とが 明 らか に さ れ,こ れ に応 じて治 療 強 度 を 変 え た プ ロ トコ ール を 選 ぶ こ とで,患 者 の リス クに応 じた治 療 が可 能 に な っ た. しか し,初 診 時 に決 定 さ れ た プ ロ トコ ー ル は,再 発. 合 併 症 が 出現 しな い限 り内容 が 変 更 され る こ と はな く, 残 存 す る 白血 病 細 胞 が1010個 で あ っ て も106個 で あ って も,は じめ に 決 め られ た 内容 で寛 解 後 治 療 が 続 行 され る.
微 小 残 存 病 変(minimal residual disease, MRD)は,従
来 の検 査 法 で 検 出 で き な い程 度 で 体 内 に存 在 す る白 血 病 を 意 味 す る.こ の ご く微 量 に残 存 す る細 胞 数 を正 確 に モ ニ タ ーで きれ ば,治 療 の テ ー ラー メ ー ド化 が 期 待 で き る. 1980年 代 前 半 ま で,さ ま ざ ま な 方 法 でMRD定 量 が 試 み られ て き た もの の,治 療 に応 用 で き る ほ ど十 分 な 感 度 は得 られ な か った. 1980年 代 後 半 に な り,分 子 生 物 学,免 疫 学 的 手 法 を 用 いて,よ り高 感 度 か つ 特 異 的 な検 出 法 が 編 み 出 さ れ,
Fig. 1 Schematic diagram of numbers of leukemic cells in acute leukemia patients during and after chemotherapy and during development of relapse
Approximately 1012 leukemic cells are present at diagnosis. Two or three log reduction is achieved by induction therapy leaving at least 109 cells residual. The remission which is defined by light-microscopy allows the existence of at least 109 cells. The de-tection limit of morphologic, as well as molecular genetic methods is indicated. Using molecular techniques, residual cells as many as 106 cells can be detected.
急 性 白血 病 にお け るMRD診 断 と そ の 臨床 応 用 73 この 分野 で の急 速 な展 開が み られ,臨 床 応用 が可 能 にな っ て い る. II. MRDの 診 断 法 MRD検 査 を 臨 床 に 役 立 て る に は,以 下 の4つ の ポ イ ン トが重 要 で あ る.ま ず,高 い感度 を もっ こ と(sensitive), 指 標 とす る 白 血 病 マ ー カ ー の 特 異 性 が 高 く(specific), 経 過 中 変 化 しな い こ と(stable),検 出 法 が で き るだ け簡 便 で(simple)で 早 く結 果 を 出 せ る こ と,で あ る.ま た, コ ス トの 抑 制 も求 め られ る.こ の よ うな 条 件 を 満 たす べ く,白 血 病 細 胞 の免 疫 学 的,も し くは分 子 生 物 学 的 な特 徴 を活 か した 方 法 が模 索 され て き た.現 在,実 用 化 さ れ て い る の は,2種 類 以 上 の 分 化 抗 原 を マ ー カ ー と した
multi-color flow cytometry(FCM)や 白 血 病 特 異 的 な
DNA,RNA塩 基 配 列 のpolymerase chain reaction(PCR)
増 幅 で あ る.と くにPCRを 用 い た 白血 病 特 異 的 な 遺 伝 子DNAのin vitro増 幅 はMRD診 断 に飛 躍 的 な進 歩 を も た ら し,104か ら106個 の 正 常 血 液 細 胞 に 混 在 す る1個 の腫 瘍 細 胞 の検 出 が可 能 に な っ た. 1. 表 面 マ ー カ ー を 用 いたMRD診 断 血 球 細 胞 は そ の分 化 成 熟 に伴 い,細 胞 膜,細 胞 質,核 内 に分 化 抗 原 を発 現 させ る.こ れ らの 抗 原 に対 す る モ ノ ク ロ ー ナ ル 抗 体(monoclonalantibody,MAb)を 作 製 し, さ らに 蛍 光 色 素 を結 合 させ る こ とで,そ の 存 在 と量 を 検 出 す る こ とが で き る.白 血 病 細 胞 に特 異 的 な分 化 抗 原 を 用 い るの が 理 想 的 で あ るが,現 在 の と こ ろ,そ の よ うな 抗 原 はな い.し か し,Jannossyら は 白血 病 細 胞 に は2種 類 以 上 の 分 化 抗 原 が 正 常 の血 球 に な い 組 み 合 わ せ で 発 現 して い る こ と を発 見 し,こ れ らを マ ー カ ー とす る方 法 を 編 み 出 し た1).Campanaら は これ を 改 良 してMRDの 診 断 を可 能 に した2). 例 え ば,T細 胞 性 急 性 リ ンパ 性 白血 病(T-ALL)の ほ と
ん ど で,核 内TdT(terminal deoxynucleotidyl transferase)
と 同 時 にCDI,CD3,CD5な ど のT細 胞 マ ー カ ーが 陽 性 に な るが,こ の よ うな 組 み 合 わ せ の 細 胞 は胸 腺 内 を 除 け ば骨 髄,末 梢 血 に は存 在 しな い.こ う い っ た組 み合 わ せ がB細 胞 性ALL(B-ALL)や 急 性 骨 髄 性 白血 病(AML) で報 告 され て い る. 彼 らは さ らに組 み合 わせ る抗 原 の種 類 を増 や す こ とで, よ り多 くの 白血 病 を 対 象 とで き る よ うに し,FCMを 利 用 す る こ と で 大 量 の細 胞 を 短 時 間 で 分 析 し,10"4程 度 の 感 度 を 実 現 した3).で き る だ け少 な い 抗 原 の組 み 合 わ せ で,多 くの 症 例 を対 象 とす る 検 討 が な され て い るが, ■ ら はTablelに 示 す5種 類 の パ ネ ル を 用 い れ ば, precursor B-ALL(precB-ALL)の98%の 症 例 を対 象 とで き,し か も そ れ ぞ れ の 症 例 で2∼3パ タ ー ンの 組 み 合 わ せ を 利 用 で き る と報 告 した4). 2. 分 子 生 物 学 的 診 断 法 白血 病 を は じめ とす る造 血 器 腫 瘍 で は,病 型 特 異 的 な 染 色 体 転 座 や欠 失 が み られ る.こ れ ら染 色 体 異 常 に伴 い 特 定 の 遺 伝 子 が 再 構 成 す る.ま た,染 色 体 異 常 を 伴 わ な い 点 突 然 変 異 や 重 複 な ど の腫 瘍 特 異 的 な遺 伝 子 の 変 異 が 一 定 の 頻 度 で み られ る.こ れ らをPCR法 な ど分 子 生 物 学 的 手 法 で 高 感 度 に検 出 す る こ とが で き る.PCRで は, 指 数 関数 的 にDNAコ ピー 数 が 増 加 しプ ラ トー に達 す る た め,も と も と検 体 内 に存 在 す るDNAコ ピ ー数 を 推 測 す る こ とが 難 しか っ た が,希 釈 法 に よ る半 定 量 やreal time quantitative PcR(RQ-PcR)が 開 発 され,定 量 値 で 表 す のが 一 般 的 に な っ た. 1) 腫 瘍 特 異 的 遺 伝 子 再 構 成 を 利 用 したMRD診 断 染 色 体 転 座 に は,キ メ ラ遺 伝 子 形 成 型 と遺 伝 子 発 現 更 新 型 転 座 型 の2種 類 が あ る.前 者 で は2っ の遺 伝 子 が 転 座 切 断 点 を ま た ぐ形 で 融 合 した キ メ ラ遺 伝 子 か ら転 写 産 物(mRNA)が 形 成 さ れ る の で,こ れ を 逆 転 写 酵 素 で cDNAに 変 換 し,PCR増 幅 す る こ と でMRD診 断 が 可 能 で あ る(Fig.2A). 代 表 的 な も の は,慢 性 骨 髄 性 白血 病(CML)の95% 以 上,成 人ALLの25∼40%,小 児ALLの 約5%に み ら れ る9;22転 座,BCR/A-BL遺 伝 子 再 構 成 で あ る.切 断 点 の9q34に 位 置 す るBcR遺 伝 子 と22q11のABL遺 伝 子 の 内部 の イ ン トロ ンで切 断 が 起 こ り,再 結 合 す る こ と で 生 じ る もの で あ る.BCR遺 伝 子 で はM.BCRと い う5.8 kbの 領 域(CMLと 成 人Ph陽 性ALLの 多 く)か,m.bcr と い う>90kbの 領 域(小 児Ph陽 性ALLの ほ と ん ど) に散 在 し,ABL遺 伝 子 で は約200kbも の 広 い 範 囲 に切 断 点 が 散 ら ば っ て い る こ と か ら,ゲ ノ ムDNAでPCR 増 幅 す る こ と は難 し く,逆 転 写 酵 素(reversetranscriptase, RT)でmRNAをcDNAに 変 換 して 増 幅 を か け るRT-PCR法 が 用 い られ る. 同 様 の手 法 を 用 い る こ と で,20種 に 近 い 病 型 特 異 的 な染 色 体 転 座 に伴 う遺 伝 子 変 異 を増 幅 してMRDの 診 断 が 可 能 に な って い る.代 表 的 な も の は,AML-M2の40 %程 度 に み ら れ る8;21転 座(AMLI-ETO結 合),M3
Table 1 Incidence of aberrant phenotypes in prec B-ALL
A
B
(APL)の ほ ぼ 全 例 に み られ る15;17転 座(PML-RARA 結 合), M4Eoに 特 徴 的 なinv(16)(CBFβ-MYH11結 合), 小 児ALLの5%程 度 に み られ る1;19転 座(E2A-PBX1 結 合),成 人ALLの 約5%を 占 め る4;11転 座(MLL-AF4 結 合)な どで あ る.ま た,光 学 顕 微 鏡 レベ ルで は 同定 さ れ な い1p34の 微 小 な染 色 体 欠 失 を起 こ すTALI遺 伝 子 の欠 失 はT-ALLの20∼30%に み られ,有 用 な マ ー カ ー の1つ で あ る. こ れ ら は,診 断 とMRDの マ ー カ と して も重 要 で,最 近 で はmultiplex PCRで 一 度 に ス ク リー ニ ング で き る よ う に な って い る5). Tab1e2にALL, Table3にAMLの 代 表 的 な 異 常 を ま とめ た. 遺 伝 子 発 現 更 新 型 転 座 で は,キ メ ラmRNAは 形 成 さ れ な い の で ゲ ノ ムDNAが 増 幅 の タ ー ゲ ッ トとな るが, 切 断 点 が 狭 い範 囲 に 集 中 して い るl4;18転 座 のBα1-2と IgH遺 伝 子 の 再 構 成(濾 胞 性 リ ンパ 腫 の 約40∼90%(わ が 国 で は 約50%)で み られ る)を 除 け ば,切 断 点 が 広 範 囲 に散 在 して い る た め,共 通 の プ ライ マ ー を用 い て, 通 常 のPCRで 増 幅 す る こ と は難 しい.数kb以 上 の領 域 を増 幅 す るlong PCRを 利 用 す る こ とで 増 幅 が で き る が, MRD検 出 に必 要 な 感 度 を得 る の は困 難 で あ る. 染 色 体 異 常 が もた らす 遺 伝 子 の変 異 は現 時 点 で も っ と も安 定 した 腫 瘍 マ ー カ ー で あ る.小 児ALLで はBCR/ ABLやTEL/AML1で 定 量 化 も実 用 化 して い る.し か し, Table2に み て と れ る よ う に小 児 のALLで は個 々 の 染 色 体 転 座 の 頻 度 が 低 く,MRD診 断 の適 応 と な る症 例 は 限 られ る.ま た,mRNAは 分 解 さ れ や す く,採 取 後 の 検 体 の 取 り扱 い に は細 心 の注 意 を要 す る.さ らに,細 胞 あ た り の キ メ ラmRNAの コ ピ ー数 が 異 な る可 能 性 が あ り, 定 量 が 不 正 確 に な る こ と も あ る. 小 児 で は成 人 に比 べ 頻 度 が 少 な い が, AMLに み られ る1死73遺 伝 子 のtandem dup1icationもMRD診 断 の マ ー カ ー と な り う る. 2) TCR/Ig遺 伝 子 再 構 成 を 利 用 したMRD診 断 正 常 のB,Tリ ンパ 球 で は抗 体 産 生 と受 容 体 発 現 が み られ る が,こ れ に先 立 ち,免 疫 グ ロ ブ リ ン(Ig)遺 伝 子 とT細 胞 受 容 体(TCR)遺 伝 子 内 のvariable (V), diver-sity(D),joining(J)領 域 の そ れ ぞ れ1つ ず つ が リ コ ン ビナ ー ゼ の作 用 で 切 り 出 さ れ て再 構 成 し,各 領 域 の 間 に は, TdTの 働 きで 数 個 ∼ 十 数 個 程 度 の ラ ンダ ム な塩 基 挿 入 が 起 こる.こ の 部 分 の塩 基 配 列 は 多 様 で,バ ラエ テ ィ に富 ん だ ク ロー ンを 形 成 す る.こ れ に よ り,多 様 な 抗 原 に対 応 可 能 な 抗 体,受 容 体 の遺 伝 子 が 形 成 さ れ る6). リ ンパ 系 腫 瘍 で は,こ れ らの遺 伝 子 再 構 成 が あ る程 度 進 ん だ あ と,造 腫 瘍 的 な遺 伝 子 変 異 を 獲 得,細 胞 が 腫 瘍 化 し,ク ロー ン性 の 自律 増 殖 能 を 獲 得 す る こ とが 多 い. こ れ ら腫 瘍 化 した 細 胞 で は,TCR/Ig遺 伝 子 の 再 構 成 が 凍 結 した形 と な り,す べ て の 細 胞 が 同 じ再 構 成,同 じ塩急 性 白血 病 に お け るMRD診 断 とそ の臨 床 応 用 75 基 配 列 を もつ こ とに な る.こ れ を腫 瘍 細 胞 に特 異 的 な 分 子 生 物 学 的 マ ー カ ー と して 利 用 す る こ とが で き る.こ れ らIg遺 伝 子 やTCR遺 伝 子 の再 構 成 を もつ リンパ 系 腫 瘍 で は,ク ロ ー ン特 異 的 な 塩 基 配 列 をPCR増 幅 しMRD の診 断 が 可 能 で あ る(Fig. 2B). B-ALLで はIgH, TCRδ,γ,β 遺 伝 子 の 再 構 成 は,そ れ ぞ れ95%, 54%, 55%, 33%に み られ る.T-ALLで は これ らの 比 率 は14%, 68%, 91%, 89%で あ る6). 対 象 と す る 白血 病 細 胞 がTCR/Ig遺 伝 子 の ク ロ ー ン性 の再 構 成 を もつ か否 か を 知 る確 実 な方 法 はサ ザ ンプ ロ ッ テ ィ ン グ法 で あ る が,検 査 に 多 量 のDNAを 要 す る こ と か ら,初 診 時DNAを 多 種 類 の 再 構 成 につ い てPCR増 幅 し,ポ リ ア ク リル ア ミ ドゲ ル電 気 泳 動(PAGE)で ク ロ ー ン性 の 有 無 を簡 易 に 判 別 す る方 法 が 一 般 的 で あ る7). (1) TCR δ ・γ鎖 遺 伝 子 の 再 構 成 を 利 用 したMRD診 断 TCRδ 鎖 遺 伝 子 は14番 染 色 体 長 腕(14q11)に 位 置 し, 6個 のV, 3個 のD, 3個 のJ領 域 か らな り,TCRα 鎖 遺 伝 子 のV領 域 群,J領 域 群 に は さ ま れ て 存 在 す る (Fig. 3)6).TCRδ 鎖 遺 伝 子 はT細 胞 の発 生 過 程 にお い て は,γ 鎖 と と も に α鎖 と β鎖 に先 立 ち 遺 伝 子 再 構 成 を起 こ し,γ 鎖-δ 鎖 の ヘ テ ロ ダ イ マ ー がT細 胞 受 容 体 と し て 発 現 す る.成 熟T細 胞 の 大 多 数 のT細 胞 受 容 体 は α 鎖 と β鎖 か らな る ヘ テ ロ ダイ マ ーだ が,リ ンパ 節 や 末 梢 Tリ ンパ 球 の5∼10%に γδ型 のT細 胞 が 存 在 して い る. 正 常T細 胞 に お け る再 構 成 は, DD→DDJ→VDDJの 順 に起 こ り,こ の と きv領 域 と してVδ1, Vδ2, J領 域 と してJδ1が も っ ぱ ら用 い られ る. ALLで はT細 胞 性 だ け で な く, B細 胞 性 で も しば しばTCRδ 鎖 再 構 成 を 認 め るが,そ の パ タ ー ン は病 型 特 異 的 で, T-ALLで は 正 常T細 胞 と 同 様 に完 全 型 のVδ1-D-Jδ1, Vδ2-D-Jδ1タ イ プ の 結 合 が 併 せ て 約50%, nonT-ALLで は不 完 全 型 の Vδ2-Dδ3タ イ プ の 結 合 が 約30%に 認 め ら れ る.こ の よ う に,TCRδ 鎖 遺 伝 子 は 構 成 す るV, D, Jの 各 因 子 の 数 が 少 な い うえ に,再 構 成 のパ タ ー ンは上 に示 した3タ イ プが 圧 倒 的 に 多 い た め,少 な い 種 類 の プ ライ マ ーで 効 率 よ くス ク リー ニ ン グが 行 え る8). TCRγ 鎖 遺 伝 子 は 染 色 体7p14に 位 置 し, 14個 のVγ, 5個 のJγ, 2個 のCγ が160kbの 長 さ に わ た り並 ん で い る こ とが 知 られ る.Vγ は塩 基 配 列 の 類 似 性 か らVγI(Vγ1 ∼Vγ9)とVγII∼VγIII(各1個 のVγ)の4群 に 分 類 さ れ る.こ の 中 で 白血 病 細 胞 の再 構 成 に 用 い られ る の は,
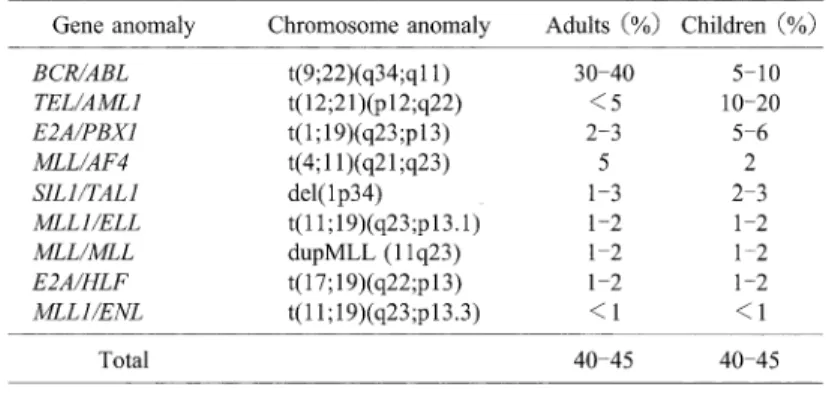
Table 2 Chromosome aberrations as major PCR targets for MRD detection
in ALL
Table 3 Chromosome aberrations as major PCR targets for MRD detection
in AML
ほ と ん ど がVγI群 で あ る9). TCRγ 鎖 遺 伝 子 は,D領 域 を も た な い が,再 構 成 に 際 しV-J結 合 部 にN塩 基 の 挿 入 が あ る な ど,多 様 な 塩 基 配 列 の変 化 を 生 じる の で,こ れ もク ロー ナ ル マ ー カ ー と して 利 用 す る こ と が で き る. (2) IgH遺 伝 子 再 構 成 を利 用 したMRD診 断 IgH遺 伝 子 は14q32に 位 置 し2,500∼3,000kbの 広 範 囲 に ゲ ノ ム上 に 存 在 す る. JH因 子 は6個 だ がVH因 子 は6群123個, DH因 子 は25個 あ り, TCRγ や δ よ り も多 様 性 に 富 む(Fig. 3)6). IgH遺 伝 子 はD-J,v-D-Jの 順 に 再 構 成 す る.塩 基 配 列 の 相 似 し たFR1やFR3の 部 位 に コ ンセ ンサ ス プ ライ マ ー を 設 け,こ れ と6個 のJH 因 子 に ほ ぼ 共 通 な塩 基 配 列 を 利 用 した コ ン セ ンサ ス プ ラ イ マ ー を 利 用 してCDR3領 域 を増 幅 す る10).さ らに塩 基 配 列 を決 定 し,こ れ に 相 当 す る オ リゴ ヌ ク レオ チ ドを 合 成 して増 幅 用 プ ライ マ ー と して用 い る. (3) Igκ鎖 遺 伝 子 再 構i成を 利 用 したMRD診 断 リ ンパ 球 で は, IgH遺 伝 子 再 構 成 の あ と, Igκ→Igλ遺 伝 子 の 順 で 再 構 成 が 進 む. Igκ遺 伝 子 再 構 成 で 生 じた 塩 基 配 列 がnon-senseに な る な ど して 再 構 成 が 失 敗 す る と, Igλの 再 構 成 が 起 こ る.こ の と き, Igκ遺 伝 子 で はVκ 因 子 がCκ の さ らに 下 流 に 位 置 す る κde因 子 と再 構 成 を 起 こす11).こ れ に よ り, Jκ因 子 やCκ 因 子 が 消 失 し,こ れ 以 十 再 構 成 が 起 こ ら な くな る.こ の 再 構 成 も 同 様 に MRD診 断 の マ ー カ ー に で き る11). Szczepanskiら はMRD を 追 跡 す る う え で, Vκ-κde再 構 成 はIg, TCR遺 伝 子 の う ち で も っ と も 安 定 し た マ ー カ ー と 報 告 して い る12). (4) TCRβ 鎖 遺 伝 子 再 構 成 を 利 用 し たMRD診 断 TCRγ,δ, IgH,κ 鎖 遺 伝 子 再 構 成 だ け で 約80∼90% の 症 例 をMRD検 査 の 対 象 に で き る が,さ ら に そ の 比 率 を 高 め る た め,TCRβ 鎖 遺 伝 子 再 構 成 を 用 い る 試 み が な さ れ て い る.TCRβ は27群65個 の 昭,2個 のDβ, 2 群13個 のJβ, 2個 のCβ か ら な り,ほ か の 遺 伝 子 に 比 べ て 構 造 が 複 雑 で あ る.こ の た め,ス ク リ ー ニ ン グ に 多 種 類 のPCR反 応 を 行 う 必 要 が あ り,敬 遠 さ れ て き た. しか し, BFMグ ル ー プ で はmultiplex PCRで こ れ を 簡 素 化 し,MRD診 断 の マ ー カ ー と し て 利 用 し始 め て い る13). TCRβ はT-ALLの90%以 上 で 再 構 成 し て お り 有 用 な マ ー カ ー で あ る が, prec B-ALLで も 約35%で 再 構 成 が み ら れ, MRD検 出 マ ー カ ー と し て 感 度,安 定 性 と も に 他 の 遺 伝 子 と 比 較 して 遜 色 な い. (5) リ ア ル タ イ ムPCRを 用 い たMRD定 量 リ ア ル タ イ ムPCRで は,定 量 性 を も た せ る た め,サ イ ク ル ご と の コ ピ ー 数 の 増 加 を 数 値 化 し て 増 加 曲 線 に 表 し,そ れ を 既 知 の 濃 度 の 反 応 曲 線 と 比 較 す る こ と で,未 知 の 検 体 内 に 存 在 す る 反 応 開 始 前 の コ ピ ー 数 を 割 り 出 す も の で あ る. コ ピ ー 数 の 測 定 は,イ ン カ レ ー シ ョ ン法 と,蛍 光 共 鳴
急 性 白 血 病 に お け るMRD診 断 とそ の 臨 床 応 用 77
A
B
エ ネ ル ギ ー移 動 に よ る発 光 を 利 用 したTaqManプ ロー ブ 法 の い ず れ か に よ る. イ ン カ レ ー シ ョ ン法 は,増 幅 さ れ たDNAの 二 本 鎖 の 間 に エ チ ジ ウ ム プ ロ ミ ドやSYBR GREENIな ど の蛍 光 物 質 を 取 り込 ま せ る方 法 で あ る(Fig.4A)'4).平 易 で 安 価 で あ るが,非 特 異 的 増 幅 が起 こ る と こ の産 物 も光 を 発 す るた め,正 確 な 定 量 が で き な くな る. TaqManプ ロ ー ブ は5'末 端 に レポ ー タ ー蛍 光 色 素,3' 末 端 に ク エ ンチ ャ ー蛍 光 色 素 を もち,PCR増 幅 用 の2 個 の プ ラ イ マ ー の 間 の 領 域 に相 補 的 に結 合 す る よ うデ ザ イ ン さ れ たDNAヌ ク レオ チ ドで あ る.DNApolymerase に よ る伸 長 反 応 が 起 こ る た び に,結 合 して い た プ ロ ー ブ が外 れ 発 光 し,こ の 数 を サ イ クル を 追 っ て カ ウ ン トす る こ とで 増 幅 中 のDNAの コ ピ ー数 を 定 量 す る も の で あ る (Fig.4B)15).特 異 性 が 高 い が,プ ロ ー ブの 合 成 が高 価 な こ と と,3種 類 の ヌ ク レオ チ ドの 設 計 と反 応 条 件 の 設 定 が少 し難 しい. BCR/ABLの よ うに,染 色 体 転 座 に よ り生 じた キ メ ラ mRNAをcDNAに 変 換 後,リ ア ル タ イ ムPCRで 増 幅 す る こ とで,比 較 的 容 易 に正 確 なMRD定 量 が 可 能 で あ る. これ に対 し,IgやTCR遺 伝 子 再 構 成 を マ ー カ ー と し た 場 合,増 幅 す る遺 伝 子 が 多 種 類 でTaqManプ ロ ー ブ も多 数 用 意 しな け れ ば な ら な い こ と,症 例 ご と に増 幅 す るプ ラ イ マ ー が 異 な り,反 応 条 件 の 設 定 に難 渋 す る こ とが 多 か っ た.と く にIgHで は,多 数 のV因 子 が あ る こ と か ら難 度 が 高 か っ た.これ に 対 し,Donovanら はFig.4Bに 示 す よ う にIgH
遺 伝 子 のV因 子3'末 端 近 傍 の 塩 基 配 列 の 似 た 領 域 に consensusなTaqManプ ロ ー ブ を7種 類 デ ザ イ ン し,IgH 遺 伝 子 再 構 成 を もっALLの ほ とん ど で5×10-5の 感 度 で MRD定 量 が 可 能 で あ る と報 告 した16). ま た,■ らはSYBRGREENIを 用 い た イ ン カ レー シ ョ ン法 リア ル タ イ ムPCRでMRDを 定 量 す る 方 法 を 確 立 した17). (6) 再 発 時 の ク ロー ン につ い て TCRδ,γ 鎖 やIgH鎖 遺 伝 子 の 再 構 成 を 利 用 す る方 法 は,ALLの 大 部 分 を対 象 と で き る.し か しな が ら,こ れ らの 遺 伝 子 が,経 過 中,再 び再 構 成 を 起 こ し,初 診 時 に み られ た 再 構 成 が な くな る症 例 が10%以 上 の 頻 度 で み られ る18,19).とくに 観 察 期 間 が 長 く な る と,こ の 頻 度 は高 くな る. ■ ら は,TCR/lgで は 再 発 時 の 再 構 成 の う ち42%が 初 診 時 と全 く同一 で あ っ た が,14%で は オ リ ジナ ル は残 っ て い る も の の新 し い ク ロ ー ン も登 場 し,20%で は初 診 時 の再 構 成 が す べ て が消 失 した と報 告 して い る20). ■ ら は,96例 の 小 児ALLで 初 診 時 と再 発 時
Fig. 4 Real time quantitative PCR
A: Intercalating PCR. DNA-binding dyes such as SYBR Green (circles) are intercalated in
double strand of PCR products along with the DNA polymerization. B: TaqMan PCR.
Quantitative PCR is preformed with appropriate VH consensus primer, patient tumor
spe-cific (ASO) primer, and VH gene family-spespe-cific consensus TaqMan probe. The probes
are labeled at the 5' end with reporter dye (R) and the 3' end with quencher activity (Q).
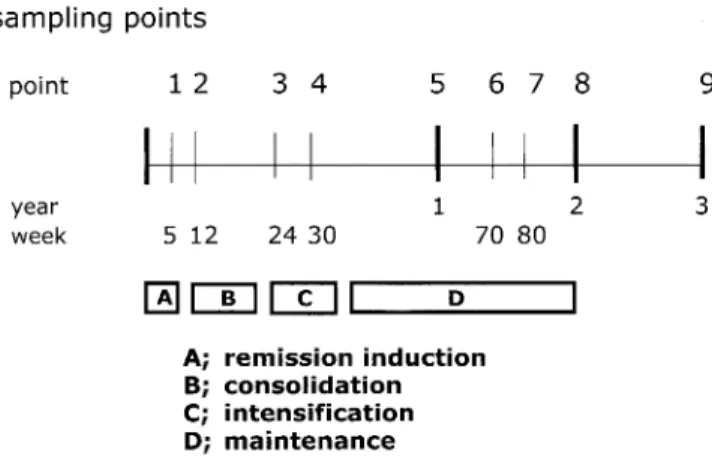
のclonalityを 比 較 し た.両 者 の 一 致 率 は 全 体 で は71% で あ っ た が,遺 伝 子 再 構 成 別 に み る と,Igκ95%,TCRγ 75%,IgH64%,TCRδ63%で あ り,Igκ が も っ と も 安 定 し て い る と 述 べ た12).こ れ に 対 し,Germanoら は,増 幅 さ れ たDNAの 長 さ をGeneScanで 高 精 度 に み る こ と で,初 診 時 と 再 発 時 のclonalityを 比 較 し,こ れ ら の 遺 伝 子 再 構 成 の 間 に 一 致 率 の 差 は な い と 結 論 づ け た21). い ず れ に せ よ,複 数 の マ ー カ ー(例,IgHとTCRδ) を 用 い,場 合 に よ っ て はFCMの デ ー タ と も補 完 さ せ て, MRDの 消 長 を 観 察 す る こ と が 望 ま し い. (7) FCMとRQ-PCRの 比 較 FCMとPCRの ど ち ら も がfalse-negativeな 結 果 を 生 み 出 し う る.FCMで は 表 面 マ ー カ ー の 変 化 が 報 告 さ れ て い る し,TCR/lgで は 再 構 成 の 進 展 に よ る マ ー カ ー の 消 失 が 起 こ る か ら で あ る.FCMは 迅 速 に 結 果 が 得 ら れ, 生 細 胞 を 死 細 胞 と 区 別 し て 判 定 で き る 利 点 を も っ が,感 度 が や や 劣 り,検 査 施 設 が 複 数 に な る と,条 件 設 定 が 難 し い. ■ ら は,同 一 検 体 でTCR/lg遺 伝 子 を 使 っ たRQ-PCRとmulti-colorFCMのMRD検 査 結 果 を 比 較 し た22). MRDが 陽 性 か 陰 性 か の 点 で は 両 者 は72%で 一 致 し た. 不 一 致 の28%の 多 くがFCMの 感 度 不 足 に よ る も の で あ っ た.定 量 値 で は 最 高5倍 も の 開 き が あ り,両 者 が 完 全 に 一 致 す る こ と は な か っ た.Nealeら も 同 様 の 結 果 を 報 告 して い る23). III. MRDと 白 血 病 予 後 の 関 わ り,治 療 へ の 応 用 小 児 を 中 心 に,MRDと 急 性 リ ン パ 性 白 血 病 の 予 後 に 関 して,す で に 多 く の 報 告 が な さ れ て い る.こ こ で は, こ れ ま で に え ら れ て い る知 見 を 整 理 し て み た い. 1. 急 性 リ ン パ 性 白 血 病(A肌) 成 人 のALLで は9;22転 座(BCR/ABL再 構 成)が そ の 30∼40%程 度 と 高 頻 度 で あ る が,小 児 で は5%未 満 で あ り,そ の 他 の 染 色 体 転 座 も 多 種 低 頻 度 で あ る.TCR,Ig 遺 伝 子 再 構 成 に よ るMRD検 査 か,multi.color FCMに よ るMRD検 査 が 主 流 で あ り,治 療 中 の 患 者 のMRDを 経 時 的 に 定 量 した 結 果 が 多 く の 施 設 か ら報 告 さ れ て い る. 1) 未 治 療 の 小 児ALL患 者 の 治 療 初 期 のMRDは 白 血 病 細 胞 の 治 療 反 応 性 を 反 映 し て お り,重 要 な 予 後 因 子 で あ る 1990年 代 に な さ れ たretrospectiveな 検 討 で,MRDが 陰 性 化 す る ま で の 期 間 は 症 例 に よ り大 き な 差 が あ る こ と, 寛 解 導 入 の 強 力 な 治 療 が 終 了 し た 時 点 でMRDが な お 陽 性 で あ る よ う な 症 例 で は,陰 性 で あ っ た 患 者 に 比 較 して そ の 後 再 発 す る 率 が 高 い こ と が 明 ら か に さ れ た22). Briscoら は41例 の 小 児ALLのMRDをretrospetiveに 解 析 し,強 化 療 法 終 了 時 の 残 存 腫 瘍 量 がhigh(≧10-3)の 群 で は 再 発 率 が100%,intermediate(10-3∼2×10-5)で は 40%,low(<10-5)で8%で あ り,MRDと 予 後 に 相 関 が あ る と 報 告 し注 目 を 浴 び た23).ま た ■ ら は 骨 髄 の 腫 瘍 細 胞 比 率 が0.6%以 上 と 未 満 と 長 期 無 病 生 存 率 が 異 な る と 述 べ た24). こ れ ら をlarge scale,prospectiveに 証 明 す べ く,ド イ ツ,オ ラ ン ダ,イ タ リ ア,オ ー ス ト リ ア な ど を 中 心 と し たBFM(Berlin-FrankfUrt-MUnster)グ ル ー プ は,治 療 開 始 後,prospectiveに あ ら か じ め 定 め ら れ た 点(Fig.5) でTCR/lgPCRで 骨 髄MRDを 定 量 し,予 後 と の 関 連 を み た.こ の 結 果,い ず れ の 定 点 に お い て も,MRDと 予 後 が 相 関 す る こ と が 確 認 さ れ た.陰 性 で あ れ ば3年 間 再 発 率 は3∼15%で あ り,陽 性 な ら39∼86%に 跳 ね 上 が っ
急 性 白 血 病 に お け るMRD診 断 と そ の 臨 床 応 用 79 た.と く に 寛 解 導 入 直 後(治 療 開 始5週 目)と 地 固 め 開 始 前(12週 目)の 骨 髄MRDに 注 目 し,両 者 が 陽 性 の 群 をMRDhigh-risk,と も に 陰 性 の 群 をlow-risk,そ の 他 をintermediate-riskと し て,予 後 と の 相 関 を み た.す る とhigh-riskの3年 再 発 率 は75%,intermediate-riskは 23%,low-riskは わ ず か に2%で あ り,各 群 間 に 有 意 の 差 を み た25).ま た,フ ラ ン ス の グ ル ー プ も178例 を 対 象 に, 同 様 の 結 果 を 報 告 し て い る26).St.Judeの ■ ら はmulti.color FCMに よ り158例 を 対 象 と し て,寛 解 導 入 直 後 のMRDと3年 再 発 率 と の 相 関 を 明 ら か に し た27).さ ら に 彼 ら は 対 象 を195例 と 増 や して,寛 解 導 入 直 後 と14週 の 骨 髄MRDを 測 定 し た.そ の 結 果,前 者 で はMRDが10-2以 上,後 者 で10-3以 上 残 存 し て い る 症 例 で は と く に 予 後 が 悪 い こ と が 示 さ れ た28). ら は,さ ら に 早 期,dayl5に お け る 骨 髄MRDを 調 べ た29).5年 生 存 率 は10"2以 上 で65%, 10-2∼10-4で80%,10-4未 満 で100%で,き わ め て 早 期 の MRDが 予 後 と 相 関 す る こ と も 明 ら か に な っ た30).St. Judeの ら は,同 一 プ ロ ト コ ー ル で 治 療 中 の110例 を 対 象 に,multi-colorFCMでdayl9の 骨 髄 MRDを 定 量 し た31).MRDが10'4以 上 の59例 の う ち, 32.2%が 寛 解 導 入 失 敗 も し く は 再 発 し た の に 対 し,10-4 未 満 の51例 で は6%が 導 入 失 敗 も し く は 再 発 し た に す ぎ な か っ た と い う.ま た,寛 解 導 入 治 療 後 のday46の MRDと 比 較 す る と,dayl9陰 性 の ほ う が よ りrelapse-free survivalに 相 関 す る こ と が わ か っ た32). 2)表 面 形 質 の 違 い に よ りMRDの 減 少 速 度 も 異 な る 表 面 形 質 別 と 治 療 反 応 性 を 比 較 す る と,同 一 の 導 入 治 療 を 行 っ た 場 合,治 療 初 期(3カ 月 目 ま で)の 骨 髄 に MRDが 残 存 し続 け る 率 は,T-ALLが28%とprecB-ALL の11%よ り 高 く,治 療 反 応 性 が 悪 い こ と が わ か っ た29). た だ し,5週 目 に 陰 性 化 す る 例 を 比 較 す る と,T-ALLの ほ う がprecB-ALLよ り 予 後 が よ く,MRDの 陰 性 の 意 義 が 大 き い こ と が わ か っ た.Nyvoldら もT-ALLで day29のMRDがprec B-ALLに 比 べ 多 い こ と を 示 し て い る32). 3) 骨 髄,末 梢 血 のMRD定 量 の 意 義 頻 回 の 骨 髄 採 取 は 患 者 に と っ て 苦 痛 で あ る.一 ■ ら は,骨 髄 の 代 わ り に 末 梢 血 を 用 い て もMRDが 予 後 因 子 と な り う る か 検 討 し た.precB-ALLで は 最 大 1,000倍 と 開 き が 大 き く,末 梢 血 を 骨 髄 の 代 わ り に 用 い る こ と は 不 可 能 だ が,T-ALLで は 骨 髄 と 末 梢 血 のMRD に 強 い 相 関 が あ り,末 梢 血 を 用 い たMRD判 定 が 可 能 と 報 告 して い る33). ら も226例 で 末 梢 血 と 骨 髄 のMRDを 定 量 し,T-ALLで は 骨 髄MRD陽 性35例 す べ て で 末 梢 血 も陽 性 で,骨 髄 ・末 梢 血 の デ ー タ の 一 致 率 が 高 く,末 梢 血 でMRDを 追 跡 で き る と し た.一 方,precB-ALL で は 骨 髄MRD陽 性 の104例 の う ち,末 梢 血 も 陽 性 で あ っ た の は わ ず か37例 で あ っ た が,寛 解 導 入 直 後 の 末 梢 血 MRDは 予 後 と の 相 関 が 強 く,こ れ も 有 用 で あ る と 結 論 づ け た34). 4) 既 存 の リ ス ク 因 子 とMRDの 相 関
Children's Oncolog yGroup(COG)で はfbur-color FCM に よ り1,016名 のprecB-ALL MRDを 対 象 にprospective studyを 行 い,MRDと 既 存 の リ ス ク 因 子 と の 相 関 を 検 証 した.寛 解 導 入 直 後(day29)のMRD陽 性 率(≧10-4) は28.6%で,day8でM3marrowで あ っ た も の はM1, M2に 比 べ 陽 性 率 が 高 か っ た.染 色 体 ・遺 伝 子 異 常 と の 相 関 を み る と,治 療 抵 抗 性 と 考 え ら れ るBCR/ABLを も っ も の は,89%でMRD陽 性 で あ る 一 方,予 後 良 好 と さ れ るTEL/AML1で は8.4%と 低 値 で,歴 然 と し た 差 が み ら れ た.し か し 同 様 に,予 後 良 好 と さ れ る4番,10番 染 色 体 の ト リ ソ ミー 症 例 で は 陽 性 率20.3%で あ り,予 後 不 良 と 考 え ら れ て き たE2A/PBXIの13.2%よ り も む し ろ 高 頻 度 で あ り,MRD早 期 陰 性 化 し な い 予 後 良 好 群 も あ る の で は な い か と し て い る35).
Cazzanigaら はBFMグ ル ー プ で のBCR/ABL陽 性ALL に っ い て デ ー タ を 報 告 し た.寛 解 導 入 直 後(day42)で は19/22(86%)がMRD陽 性 で,3ヵ 月 目 で 陰 性 化 す る も の も6/25(24%)に す ぎ ず,と く に 先 行 す る プ レ ドニ ン に 不 応 性 の も の は 全 例,MRDが 陰 性 化 し な か っ た36). 5) 再 発 後 治 療,幹 細 胞 移 植 とMRDの 相 関 再 発 症 例 の 再 寛 解 導 入 治 療 後 のMRDも 検 討 さ れ て い る.Coustan-Smithら は,治 療 中 に 再 発 し た 患 者 に 対 す る 再 寛 解 導 入 直 後 の 骨 髄MRDが10-4以 上 で あ る と,2 年 間 の 再 発 率 が 有 意 に 高 い(70.2±12.3vs.27.9±12.4%) こ と を 示 し た.こ れ は 治 療 終 了 後 の 再 発 で あ っ て も 同 様 (49.1±17.8vs.0%)で あ っ た37).
再 発 例 に 対 し て は,幹 細 胞 移 植(stem cell transplanta-tion,SCT)が 大 き な 選 択 肢 と な る が,治 療 の 成 績 は 移 植 前 のtumor burdenに 大 き く 左 右 さ れ る. Knechtiら は64例 の 小 児ALLでallo BMT実 施 前 (day23)の 骨 髄MRDを 定 量 し,5年 無 イ ベ ン ト生 存 率 (EFS)と の 相 関 を み た と こ ろ,陰 性 例(10 5未 満,33 例)で は73%,105以 上103未 満(11例)で は36%, 10-3以 上(12例)で は0%で あ り,両 者 の 間 に 相 関 を 確 言忍 し た38). Baderら は41例 を 対 象 と し,MRD強 陽 性 群(15例) で78%,軽 度 陽 性 群(l0例)で48%,陰 性 群(17例)
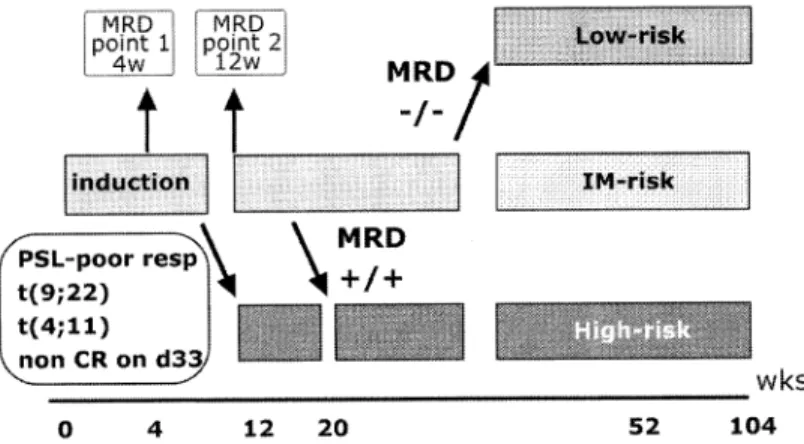
で23%の5年EFSで あ っ た こ とを 報 告 した39). Dutch groupの ら に よ れ ば,MRD陰 性 (<10-4)で のEFSは80%で あ っ た の に対 し,MRD陽 性 (≧10-4)で は33%で あ った40). ま た,Karolinskaの ■ ら も,移 植 前 の 骨 髄MRD が 強 度 陽 性(10-2∼10"3)の 群 で は15例 中8例,軽 度 陽 性(10-4∼10-5)の 群 で は10例 中5例 で 再 発 し た が, MRD陰 性 例 で は5例 中1例 も再 発 し な か っ た と報 告 し た41).■ らはalloSCT後 の骨 髄MRDを 定 期 的 に FCMで 定 量 し,移 植 時 にMRD陽 性 で あ っ た6例 は EFS33.3%と,陰 性18例 の73.5%よ り有意 に予 後 が悪 か っ た.ま た 移 植 後,MRDが 陽 性 化 す る例 は1∼6カ 月 後 に再 発 す る こ と か ら,予 後 不 良 の兆 候 と した42). これ ら の報 告 は い ず れ も,移 植 前 のMRDが 陰 性 な ら ば予 後 良 好,陽 性 な らば 不 良 で あ る こ とを 明 確 に示 して お り,移 植 の 適 応 を 考 え る う え で お お い に参 考 にす べ き で あ ろ う.た だ し,MRD陽 性 で あ って も,T-細 胞 非 除 去 のunrelate ddonorか らの移 植 で 長 期 寛 解 を え て い る報 告 もあ り43),GVL効 果 な ど を 工 夫 し た レ ジメ に よ り改 善 す る余 地 が あ る と考 え た い. 2. 急 性 骨 髄 性 白血 病(AML) AMLで は キ メ ラmRNAをmulti-color FCMとPCR増 幅 に よ るMRD診 断 が 一 般 的 で あ る.し か しな が ら,小 児 で はAMLの 症 例 数 が 少 な く,大 規 模 で 解 析 を 行 っ た 報 告 は少 な い.こ こで は,お も に成 人 で の研 究 に っ いて 触 れ て 参 考 と した い. Multi-color FCMを 用 い て は,■ らが126例 のAMLのMRD解 析 を行 って い る.寛 解 導 入 直 後 の 骨 髄MRDと 予 後 と の 関 連 を み る と,観 察 期 間3年 で の 再 発 率 はMRD10-2以 上 で84%,10-3∼10-2で50%,10b4∼ l0-3で14%,10-4未 満 で0%で あ り,AMLで も小 児ALL 同 様,治 療 早 期 のMRDが 予 後 と相 関 す る こ とが 明 らか に な っ た44).ま た,Kemら も寛 解 導 入 直 後 と地 固 め後 のMRDが 再 発 率 に 相 関 す る と報 告 した45). 遺 伝 子 変 異 別 に み る と,白 血 病 の 病 型 ご とにMRDの 動 態 は 異 な る が,寛 解 導 入 治 療 で2-log以 上 細 胞 減 少 が み られ な けれ ば 長 期 予 後 不 良 で あ る こ とが わ か って い る. こ こ で は,症 例 数 の 多 い15;17転 座 と8;21転 座, inv(16)に つ いて 記 述 した い. AML-M3で は,15;17転 座 で 見 い だ さ れ るPML/RARα 再 構 成(融 合 遺 伝 子mRNA)が,MRDモ ニ タ リ ン グ の よ い 指 標 と な る.APLで は全 ト ラ ン ス型 レチ ノ イ ン酸 (ATRA)併 用 の 化 学 療 法 に よ り短 期 間 に 分 子 生 物 学 的 寛 解 に至 る症 例 が 多 く,治 療 終 了 後 長 期 間寛 解 を 続 け る 症 例 で はMRD陰 性 で あ る こ と も確 認 さ れ て い る.ま た 治 療 早 期 のMRDが 長 期 予 後 に 関 連 す る こ と が 明 ら か に さ れ て い る46).ATRAの 治 療 効 果 も 単 独 で はPCRで MRD陰 性 と な る レ ベ ル ま で 腫 瘍 細 胞 を 駆 逐 で き ず,化 学 療 法 やSCTを 併 用 し な け れ ば な ら な い こ と が こ れ で 裏 付 け ら れ た47). 8;21転 座,inv(16)で は,core-bindingfactor(CBF) 遺 伝 子 が 転 座 に 関 与 し,CBFleukemiaと 呼 ば れ る. t(8;21)(q22;q22)転 座(AML1(CBFα)/ETO)はdenovo AMLの7∼14%を 占 め,AML-M2の40%程 度 に み ら れ る.inv(16)(CBF6/MYH11)はdenovoAMLの3∼10% を 占 め,特 異 的 なAML-M4Eoの 病 型 を 示 す.8;21転 座 とinv(16)で は,そ れ ぞ れAMLl(CBFa)-ETO,CBFβ 一 MYH11融 合 遺 伝 子 の キ メ ラmRNAを タ ー ゲ ッ ト と し た RT-PCR法 がMRD診 断 に 用 い ら れ て い る.こ の2つ の 転 座 を も つAMLは,50%以 上 で 長 期 予 後 が え ら れ る こ と が 知 ら れ て い る.し か し,治 療 が 終 了 し寛 解 を 維 持 し 続 け て い る 患 者 の 多 く で 骨 髄 にMRDが 検 出 さ れ る な ど, MRDの 存 在 と 病 気 の 予 後 と の 関 連 がAPLほ ど 明 確 で な い48,49). IV. 今 後 の 展 望 一MRDに 基 づ く治 療 変 容: 予 後 と 晩 期 副 作 用 の 改 善 を 目 指 し て 強 力 な 治 療 を受 け る患 者 で は,MRDが 引 き 続 き減 少 す るか 再 増 殖 を抑 制 さ れ る た め,再 発 も少 な くな る可 能 性 が あ る.し か しな が ら,す べ て の患 者 に 強 力 な維 持 強 化 療 法 を 行 え ば,入 院 期 間 や 医 療 費 の増 加 を 招 くだ け で な く,抗 癌 剤 の 晩 期 副 作 用,二 次 発 癌 な ど で 患 者 の QOLを 損 な う確 率 が 高 くな る. 現 在,intemationalBFMgroup(1-BFMG)や 日本 の CCLSGで は,治 療 早 期 反 応 性 を 反 映 す るMRD定 量 結 果 に基 づ い て,寛 解 導 入 や地 固 め 療 法 以 後 の治 療 を 強 化 した り,緩 め た りす る治 療 研 究 を多 施 設 で開 始 して い る. 1-BFMGのAIEOP BFM2000プ ロ トコ ール(Fig.6)で は, 寛 解 導 入 療 法 を 一 本 化 し,先 行 投 与 した プ レ ドニ ン に対 す る不 応 例,9;22転 座,4;ll転 座 を もつ 例,day33で 寛 解 導 入 不 能 例 の ほ か,5週 と12週 の 骨 髄MRDが と も に陽 性 例 を 再 発 リス ク の 高 いhigh-risk群 と し,MRDが と も に 陰性 の 症 例 はlow-risk群 と して,治 療 を 弱 め る こ と と した.CCLSGのALL2000MRDプ ロ トコ ー ル(Fig. 7)で は,従 来 の プ ロ トコ ー ル の骨 格 はそ の ま ま に して, 4週,12週 目 のMRDの 結 果 が と も に 陽 性 の 場 合,12 週 目以 降 の リス ク群 を 一 段 あ げ る こ と と した.ま だ,観 察 期 間 が 不 十 分 で あ るが,今 後 これ らの プ ロ トコ ー ル の 予 後 が 注 目 さ れ る.
急 性 白血 病 に お け るMRD診 断 とそ の 臨 床 応 用 81
引
用
文
献
1) Janossy G, Bollum FJ, Bradstock KF, et al: Terminal
transferase-positive human bone marrow cells exhibit the
antigenic phenotype of common acute lymphoblastic
leu-kemia. J Immunol 123: 1525-1529, 1979
2) Campana D, Behm FG: Leukaemia immunophenotyping:
Uses for predicting outcome and assessing treatment
re-sponse, Whittaker JA ed Leukaemia eds Blackwell
Scientific London 1992, 201
3) Campana D: Applications of cytometry to study acute
leukemia: In vitro determination of drug sensitivity and
detection of minimal residual disease. Cytometry 18:
68-74, 1994
4) Lucio P, Gaipa G, van Lochem EG, et al: BIOMED-I
concerted action report: Flow cytometric
immunopheno-typing of precursor B-ALL with standardized
triple-stainings. BIOMED-1 Concerted Action Investigation of
Minimal
Residual
Disease in Acute Leukemia:
International Standardization and Clinical Evaluation.
Leukemia 15: 1185-1192, 2001
5) Elia L, Mancini M, Moleti L, et al: A multiplex reverse
transcriptase-polymerase chain reaction strategy for the
diagnostic molecular screening of chimeric genes: A
clinical evaluation on 170 patients with acute
lympho-blastic leukemia. Haematologica 88: 275-279, 2003
6) van Dongen JJ, Wolvers-Tettero IL: Analysis of
immunoglobulin and T cell receptor genes. Part I: Basic
and technical aspects. Clin Chim Acta 198: 1-91, 1991
7) Langerak AW, Szczepanski T, van der Burg M, et al:
Heteroduplex PCR analysis of rearranged T cell receptor
genes for clonality assessment in suspect T cell
proliferations. Leukemia. 11: 2192-2199, 1997
8) Hansen-Hagge TE, Yokota S, Bartram CR: Detection of
minimal residual disease in acute lymphoblastic
leuke-mia by in vitro amplification of rearranged T-cell
recep-tor delta chain sequences. Blood 74: 1762-1767, 1989
9) d'Auriol L, Macintyre E, Galibert F, et al: In vitro
ampli-fication of T cell gamma gene rearrangements: A new
tool for the assessment of minimal residual disease in
Fig. 6 Therapeutic protocol of BFM and BM sampling points for MRD analysis
acute lymphoblastic leukemias. Leukemia 3: 155-158,
1989
10) Yamada M, Hudson S, Tournay O, et al: Detection of
minimal disease in hematopoietic malignancies of the
B-cell lineage by using third-complementarity-determining
region (CDR-III)-specific probes. Proc Natl Acad Sci
USA 86: 5123-5127, 1989
11) Beishuizen A, de Bruijn MA, Pongers-Willemse M, et
al: Heterogeneity in junctional regions of
immunoglo-bulin kappa deleting element rearrangements in B cell
leukemias: A new molecular target for detection of
mini-mal residual disease. Leukemia 11: 2200-2207 , 1997
12) Szczepanski T, Willemse MJ, Brinkhof B, et al:
Com-parative analysis of Ig and TCR gene rearrangements at
diagnosis and at relapse of childhood precursor-B-ALL
provides improved strategies for selection of stable PCR
targets for monitoring of minimal residual disease. Blood
99: 2315-2323, 2002
13) van der Velden VH, Bruggemann M, Hoogeveen PG , et
al: TCRB gene rearrangements in childhood and adult
precursor-B-ALL: Frequency, applicability as
MRD-PCR target, and stability between diagnosis and relapse.
Leukemia 18: 1971-1980, 2004
14) Higuchi R, Fockler C, Dollinger G, et al: Kinetic PCR
analysis: Real-time monitoring of DNA amplification
re-actions. Biotechnology 11: 1026-1030, 1993.
15) Heid CA, Stevens J, Livak KJ, et al: Real time
quantita-tive PCR. Genome Res 6: 986-994, 1996
16) Donovan JW, Ladetto M, Zou G, et al: Immunoglobulin
heavy-chain consensus probes for real-time PCR
quanti-fication of residual disease in acute lymphoblastic
leuke-mia. Blood 95: 2651-2658, 2000
17) Nakao M, Janssen JW, Flohr T, et al: Rapid and reliable
quantification of minimal residual disease in acute
lymphoblastic leukemia using rearranged
immunoglo-bulin and T-cell receptor loci by LightCycler technology .
Cancer Res 60: 3281-3289, 2000
18) Beishuizen A, Verhoeven MA, van Wering ER, et al:
Analysis of Ig and T-cell receptor genes in 40 childhood
acute lymphoblastic leukemias at diagnosis and
subse-quent relapse: Implications for the detection of minimal
residual disease by polymerase chain reaction analysis.
Blood 83: 2238-2247, 1994
19) Steenbergen EJ, Verhagen OJ, van Leeuwen EF, et al:
Frequent ongoing T-cell receptor rearrangements in
childhood B-precursor acute lymphoblastic leukemia:
Implications for monitoring minimal residual disease.
Blood 86: 692-702, 1995
20) Li A, Zhou J, Zuckerman D, et al: Sequence analysis of
clonal immunoglobulin and T-cell receptor gene
rear-rangements in children with acute lymphoblastic
leuke-mia at diagnosis and at relapse: Implications for
pathogenesis and for the clinical utility of PCR-based
methods of minimal residual disease detection. Blood
102: 4520-4526, 2003
21) Germano G, del Giudice L, Palatron S, et al: Clonality profile in relapsed precursor-B-ALL children by GeneScan and sequencing analyses. Consequences on minimal residual disease monitoring. Leukemia 17: 1573-1582, 2003
22) Cave H, Guidal C, Rohrlich P, et al: Prospective moni-toring and quantitation of residual blasts in childhood acute lymphoblastic leukemia by polymerase chain reac-tion study of delta and gamma T-cell receptor genes. Blood 83: 1892-1902, 1994
23) Brisco MJ, Condon J, Hughes E, et al: Outcome predic-tion in childhood acute lymphoblastic leukaemia by mo-lecular quantification of residual disease at the end of induction. Lancet 343: 196-200, 1994
24) Wasserman R, Galili N, Ito Y, et al: Residual disease at the end of induction therapy as a predictor of relapse dur-ing therapy in childhood B-lineage acute lymphoblastic leukemia. J Clin Oncol 10: 1879-1888, 1992
25) van Dongen JJ, Seriu T, Panzer-Grumayer ER, et al: Prognostic value of minimal residual disease in acute lymphoblastic leukaemia in childhood. Lancet 352: 1731-1738, 1998
26) Cave H, van der Werff ten Bosch J, Suciu S, et al: Clinical significance of minimal residual disease in childhood acute lymphoblastic leukemia. European Organization for Research and Treatment of Cancer •\ Childhood Leukemia Cooperative Group. N Engl J Med 339: 591-598, 1998
27) Coustan-Smith E, Behm FG, Sanchez J, et al: Immunolo-gical detection of minimal residual disease in children with acute lymphoblastic leukaemia. Lancet 351: 550-554, 1998
28) Coustan-Smith E, Sancho J, Hancock ML, et al: Clinical importance of minimal residual disease in childhood acute lymphoblastic leukemia. Blood 96: 2691-2696, 2000
29) Panzer-Grumayer ER, Schneider M, Panzer S, et al: Rapid molecular response during early induction chemo-therapy predicts a good outcome in childhood acute
lymphoblastic leukemia. Blood 95: 790-794, 2000 30) Willemse MJ, Seriu T, Hettinger K, et al: Detection of
minimal residual disease identifies differences in treat-ment response between T-ALL and precursor B-ALL. Blood 99: 4386-4393, 2002
31) Coustan-Smith E, Sancho J, Behm FG, et al: Prognostic importance of measuring early clearance of leukemic cells by flow cytometry in childhood acute lympho-blastic leukemia. Blood 100: 52-58, 2002
32) Nyvold C, Madsen HO, Ryder LP, et al: Nordic Society for Pediatric Hematology and Oncology. Precise quanti-fication of minimal residual disease at day 29 allows identification of children with acute lymphoblastic leuke-mia and an excellent outcome. Blood 99: 1253-1258, 2002
急 性 白血 病 に お け るMRD診 断 とそ の 臨 床 応 用 83