イオン液体の構造と物性相関
山本 博志
*旭硝子(株)中央研究所
(Received January 10,2006 ; Accepted March 14,2006 )
イミダゾリウム、ピリジニウム、テトラアルキルアンモニウムなどのカチオン誘導体と様々 なアニオンとからなるイオン液体の粘度と融点を計算する式を構築した。カチオン分子を特徴 づける説明因子として半経験的分子軌道法の計算結果から得られるダイポールモーメント、軌 道エネルギー、電荷の情報などと分子の表面積、体積、Ovalityを組み合わせ、推算式の係数を 遺伝的アルゴリズムを用いて決定した。融点(Tm)に関しては一部推算値から大きく外れるもの があるが粘度(Vis.)に関してはR2=0.9464と非常に良好に実験値を再現できた。 キーワード: イオン液体 粘度 融点 物性構造相関 * [email protected]
1. 緒言
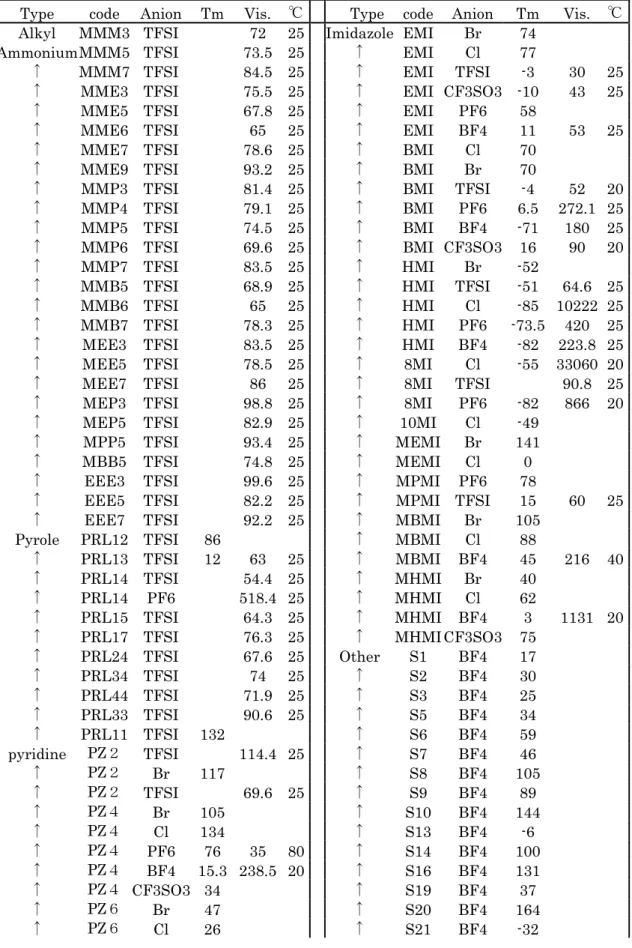
イオン液体と呼ばれる室温で液状の塩が多方面か ら注目されている。これらの塩は,高極性、不揮発 性、難燃性、 耐熱性、 導電性など塩の特徴を有す る液体でありながら融点が低く、室温付近でも液体 で存在する。これらの特徴を生かし電池用電解液、 グリーンケミストリー用反応溶媒、潤滑剤、触媒な どに応用されはじめている。カチオンとしては イ ミダゾリウム、ピリジニウム、テトラアルキルアン モニウム誘導体が一般的だが最近開発された第3 級アミンと酸との中和法を用いる事で様々な構造 のイオン液体を簡便に得る事ができるようになっ てきた。こうしたイオン液体を分子設計しようとし た場合、カチオンの構造、側鎖の長さ、枝分かれ構 造、アニオンの構造など非常に多くの組み合わせが 存在する。しかもこの塩は純度や含水量によって物 性が大きく変化したり、1種のガラスのように過冷 却状態をとったりとカタログや文献値を調べてい ても物性が中々一致しない(Table 1)。 こうしたイオン液体の分子設計に対しては、一般的 には同一化合物群においては、カチオンのアルキル鎖が長くなると粘度は高くなり、カチオン部分の構 造が非対称になれば融点や粘度が低くなる傾向が あることが知られている。
Table 1. Difference of data
また、イミダゾール類のブロモアニオンに限って融 点の相関を行った例[1]やピリジニウム類のブロモ アニオンに限って融点の相関を行った例[2]はある がテトラアルキルアンモニウム塩からイミダゾリ ウム塩まで統一的に粘度や融点を解析した例はな い。今回計算機化学と情報化学の手法を併用し、分 子構造と粘度や融点の構造物性相関式を構築した ので報告する。通常の塩(例えばNaCl)は融点は 801℃と非常に高い。これが室温で液体になるので あるからナトリウムカチオンのように単純な球を 仮定してはこの問題は解けない。
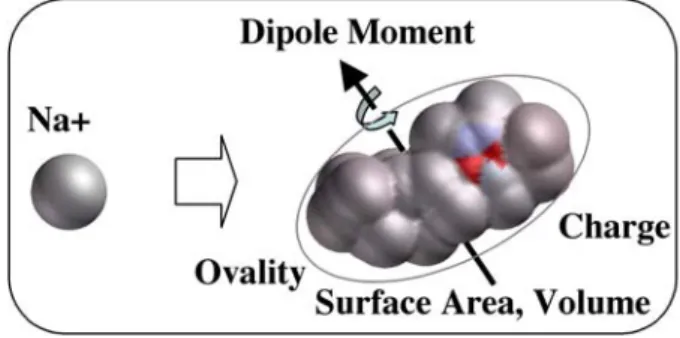
Figure 1. Molecular descriptors
また特定のカチオンに依存しないように、かつ、側 鎖構造を自由に反映できる分子記述子を選択する 必要がある。ここでは分子の大きさを表す分子表面 積や体積、形状を表すOvalityと分子軌道計算の計 算結果を組み合わせて粘度と融点を表す式を検討 した。(図1)
2.データ収集
イオン液体の融点(Tm)、粘度(Vis.)のデータ は『イオン液体』[3]、『イオン性液体の機能創成と 応用』[4]、関東化学カタログ[5]、Aldrichカタログ [6]、日本合成化学カタログ[7]などから収集した。 Table 1 に示したようにデータのばらつきが非常に 大きいが一番信頼性が高いと思われるデータを Table 2にまとめた。3. 計算
3.1. 分子記述子の計算
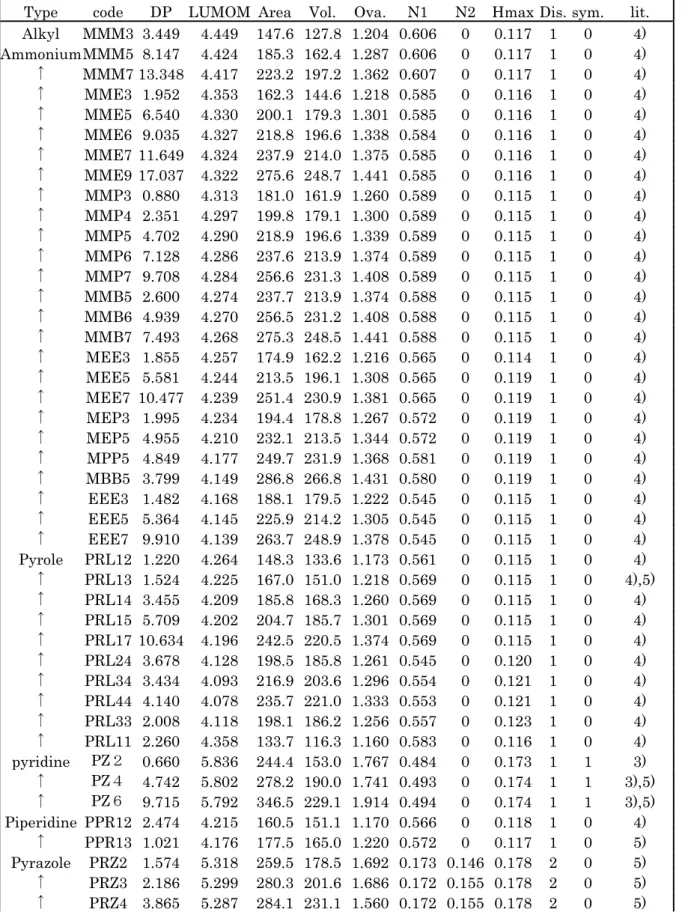
ケンブリッジソフト社製のChemOffice ver. 4.5 for Macに入っているChem3Dを用いて各カチオンを半経 験的分子軌道法(MOPAC97)で計算を行った。計算 のパラメータは、PM3 PRECISE CHARGE=1を指定し た。計算結果から各カチオンのダイポールモーメン ト(DP)、LUMO、窒素上の電荷(窒素を二つ持つも のは大きな電荷をN1)などを取り出した。LUMOの値 はすべての化合物でマイナスであったのでこの値 の符号を逆転したものをLUMOMと表記する。次にケ ンブリッジソフト社製のChemOffice2002に入って いるChem3Dを用い、構造最適化が終了した各カチオ ンの表面積、体積、Ovalityを計算した。 これらの分子記述子をTable 3にまとめた。
3.2. 粘度、融点の非線形推算式の構築
粘度の推算式が Vis.=定数+定数2* Power((A*測定温度[Tref.]+1),B)* Power((C*DP+1),D)* Power((E*LUMOM+1),F)* Power((G*Area+H*Vol.+I*Ova.+1),J)* Power((K*N1+L*N2+1),M)* Power((N*TFSI+O*Br+P*Cl+Q*BF4+R*CF3SO3+1),S) ・・・・式(1) と最も一般的な非線形フィット関数である指数関 数(Power関数)のかけ算で表せると仮定して定数 とA-Sの係数を誤差が一番小さくなるように求めた。 融点の場合は最初の測定温度の項が無く、代わりに 一番プラスに荷電している水素の電荷とその水素 の窒素からの距離、対称性などを入力した。このよ うな非線形な方程式は局所解が多数存在しグロー バルミニマムの解を探索するのは非常に困難であ る。ここでは遺伝的アルゴリズムを用いて未定数を 決定するプログラムを作成し計算を行った。遺伝的 アルゴリズムは個体数2000、世代数300000、エリー ト保存を用い、突然変異確率0.7、交叉確率0.2で探 索を行った。Cation Anion MP ℃ Vis (cP) ℃
PZ4 BF4 15.3 238.5 20 PZ4 BF4 -88 238.5 20 8MI PF6 -82 866 20 8MI PF6 -5 866 20 BMI BF4 -71 118.3 25 BMI BF4 -81 180 25 BMI BF4 -71 100 25
Table 2. Properties of Ionic Liquids
Type code Anion Tm Vis. ℃ Type code Anion Tm Vis. ℃
Alkyl MMM3 TFSI 72 25 Imidazole EMI Br 74
AmmoniumMMM5 TFSI 73.5 25 ↑ EMI Cl 77
↑ MMM7 TFSI 84.5 25 ↑ EMI TFSI -3 30 25
↑ MME3 TFSI 75.5 25 ↑ EMI CF3SO3 -10 43 25
↑ MME5 TFSI 67.8 25 ↑ EMI PF6 58
↑ MME6 TFSI 65 25 ↑ EMI BF4 11 53 25
↑ MME7 TFSI 78.6 25 ↑ BMI Cl 70
↑ MME9 TFSI 93.2 25 ↑ BMI Br 70
↑ MMP3 TFSI 81.4 25 ↑ BMI TFSI -4 52 20
↑ MMP4 TFSI 79.1 25 ↑ BMI PF6 6.5 272.1 25
↑ MMP5 TFSI 74.5 25 ↑ BMI BF4 -71 180 25
↑ MMP6 TFSI 69.6 25 ↑ BMI CF3SO3 16 90 20
↑ MMP7 TFSI 83.5 25 ↑ HMI Br -52
↑ MMB5 TFSI 68.9 25 ↑ HMI TFSI -51 64.6 25
↑ MMB6 TFSI 65 25 ↑ HMI Cl -85 10222 25
↑ MMB7 TFSI 78.3 25 ↑ HMI PF6 -73.5 420 25
↑ MEE3 TFSI 83.5 25 ↑ HMI BF4 -82 223.8 25
↑ MEE5 TFSI 78.5 25 ↑ 8MI Cl -55 33060 20
↑ MEE7 TFSI 86 25 ↑ 8MI TFSI 90.8 25
↑ MEP3 TFSI 98.8 25 ↑ 8MI PF6 -82 866 20
↑ MEP5 TFSI 82.9 25 ↑ 10MI Cl -49
↑ MPP5 TFSI 93.4 25 ↑ MEMI Br 141
↑ MBB5 TFSI 74.8 25 ↑ MEMI Cl 0
↑ EEE3 TFSI 99.6 25 ↑ MPMI PF6 78
↑ EEE5 TFSI 82.2 25 ↑ MPMI TFSI 15 60 25
↑ EEE7 TFSI 92.2 25 ↑ MBMI Br 105
Pyrole PRL12 TFSI 86 ↑ MBMI Cl 88
↑ PRL13 TFSI 12 63 25 ↑ MBMI BF4 45 216 40 ↑ PRL14 TFSI 54.4 25 ↑ MHMI Br 40 ↑ PRL14 PF6 518.4 25 ↑ MHMI Cl 62 ↑ PRL15 TFSI 64.3 25 ↑ MHMI BF4 3 1131 20 ↑ PRL17 TFSI 76.3 25 ↑ MHMICF3SO3 75 ↑ PRL24 TFSI 67.6 25 Other S1 BF4 17 ↑ PRL34 TFSI 74 25 ↑ S2 BF4 30 ↑ PRL44 TFSI 71.9 25 ↑ S3 BF4 25 ↑ PRL33 TFSI 90.6 25 ↑ S5 BF4 34 ↑ PRL11 TFSI 132 ↑ S6 BF4 59 pyridine PZ2 TFSI 114.4 25 ↑ S7 BF4 46 ↑ PZ2 Br 117 ↑ S8 BF4 105 ↑ PZ2 TFSI 69.6 25 ↑ S9 BF4 89 ↑ PZ4 Br 105 ↑ S10 BF4 144 ↑ PZ4 Cl 134 ↑ S13 BF4 -6 ↑ PZ4 PF6 76 35 80 ↑ S14 BF4 100 ↑ PZ4 BF4 15.3 238.5 20 ↑ S16 BF4 131 ↑ PZ4 CF3SO3 34 ↑ S19 BF4 37 ↑ PZ6 Br 47 ↑ S20 BF4 164 ↑ PZ6 Cl 26 ↑ S21 BF4 -32
↑ PZ6 PF6 45 222.2 50 Pyrazole PRZ2 TFSI 22.9 42
↑ PZ6 BF4 -65 552.8 20 ↑ PRZ3 TFSI 18.6 43
piperidine PPR12 TFSI 217 25 ↑ PRZ4 TFSI 55
↑ PPR13 TFSI 12 150 25 R1 N+ R2 Carbon# R3 N+ Carbon# Carbon# PRLXX R1R2R3X N+Carbon# PZX N+ Carbon# Carbon# PPRXX N N+ Carbon# PRZX N N+ R1 R2 R1R2I N N+ R1 R2 R3 R3R1R2I (CF3SO2)2N- TFSI NH+ S1 N+ H CH3 N+ CH3 H S3 N+ H H N H+ N CH3 N+ H S2 N+ H S4 N+H N+H N+H N+H N+H N+H N+ H N N +H N+ H H N+
H
H N N+ H N+ H S5 S6 S7 S8 S9 S10 S12 S13 S14 S16 S17 S18 S19 S20 S21Table 3. Descriptors for Ionic Liquids
Type code DP LUMOM Area Vol. Ova. N1 N2 Hmax Dis. sym. lit. Alkyl MMM3 3.449 4.449 147.6 127.8 1.204 0.606 0 0.117 1 0 4) AmmoniumMMM5 8.147 4.424 185.3 162.4 1.287 0.606 0 0.117 1 0 4) ↑ MMM7 13.348 4.417 223.2 197.2 1.362 0.607 0 0.117 1 0 4) ↑ MME3 1.952 4.353 162.3 144.6 1.218 0.585 0 0.116 1 0 4) ↑ MME5 6.540 4.330 200.1 179.3 1.301 0.585 0 0.116 1 0 4) ↑ MME6 9.035 4.327 218.8 196.6 1.338 0.584 0 0.116 1 0 4) ↑ MME7 11.649 4.324 237.9 214.0 1.375 0.585 0 0.116 1 0 4) ↑ MME9 17.037 4.322 275.6 248.7 1.441 0.585 0 0.116 1 0 4) ↑ MMP3 0.880 4.313 181.0 161.9 1.260 0.589 0 0.115 1 0 4) ↑ MMP4 2.351 4.297 199.8 179.1 1.300 0.589 0 0.115 1 0 4) ↑ MMP5 4.702 4.290 218.9 196.6 1.339 0.589 0 0.115 1 0 4) ↑ MMP6 7.128 4.286 237.6 213.9 1.374 0.589 0 0.115 1 0 4) ↑ MMP7 9.708 4.284 256.6 231.3 1.408 0.589 0 0.115 1 0 4) ↑ MMB5 2.600 4.274 237.7 213.9 1.374 0.588 0 0.115 1 0 4) ↑ MMB6 4.939 4.270 256.5 231.2 1.408 0.588 0 0.115 1 0 4) ↑ MMB7 7.493 4.268 275.3 248.5 1.441 0.588 0 0.115 1 0 4) ↑ MEE3 1.855 4.257 174.9 162.2 1.216 0.565 0 0.114 1 0 4) ↑ MEE5 5.581 4.244 213.5 196.1 1.308 0.565 0 0.119 1 0 4) ↑ MEE7 10.477 4.239 251.4 230.9 1.381 0.565 0 0.119 1 0 4) ↑ MEP3 1.995 4.234 194.4 178.8 1.267 0.572 0 0.119 1 0 4) ↑ MEP5 4.955 4.210 232.1 213.5 1.344 0.572 0 0.119 1 0 4) ↑ MPP5 4.849 4.177 249.7 231.9 1.368 0.581 0 0.119 1 0 4) ↑ MBB5 3.799 4.149 286.8 266.8 1.431 0.580 0 0.119 1 0 4) ↑ EEE3 1.482 4.168 188.1 179.5 1.222 0.545 0 0.115 1 0 4) ↑ EEE5 5.364 4.145 225.9 214.2 1.305 0.545 0 0.115 1 0 4) ↑ EEE7 9.910 4.139 263.7 248.9 1.378 0.545 0 0.115 1 0 4) Pyrole PRL12 1.220 4.264 148.3 133.6 1.173 0.561 0 0.115 1 0 4) ↑ PRL13 1.524 4.225 167.0 151.0 1.218 0.569 0 0.115 1 0 4),5) ↑ PRL14 3.455 4.209 185.8 168.3 1.260 0.569 0 0.115 1 0 4) ↑ PRL15 5.709 4.202 204.7 185.7 1.301 0.569 0 0.115 1 0 4) ↑ PRL17 10.634 4.196 242.5 220.5 1.374 0.569 0 0.115 1 0 4) ↑ PRL24 3.678 4.128 198.5 185.8 1.261 0.545 0 0.120 1 0 4) ↑ PRL34 3.434 4.093 216.9 203.6 1.296 0.554 0 0.121 1 0 4) ↑ PRL44 4.140 4.078 235.7 221.0 1.333 0.553 0 0.121 1 0 4) ↑ PRL33 2.008 4.118 198.1 186.2 1.256 0.557 0 0.123 1 0 4) ↑ PRL11 2.260 4.358 133.7 116.3 1.160 0.583 0 0.116 1 0 4) pyridine PZ2 0.660 5.836 244.4 153.0 1.767 0.484 0 0.173 1 1 3) ↑ PZ4 4.742 5.802 278.2 190.0 1.741 0.493 0 0.174 1 1 3),5) ↑ PZ6 9.715 5.792 346.5 229.1 1.914 0.494 0 0.174 1 1 3),5) Piperidine PPR12 2.474 4.215 160.5 151.1 1.170 0.566 0 0.118 1 0 4) ↑ PPR13 1.021 4.176 177.5 165.0 1.220 0.572 0 0.117 1 0 5) Pyrazole PRZ2 1.574 5.318 259.5 178.5 1.692 0.173 0.146 0.178 2 0 5) ↑ PRZ3 2.186 5.299 280.3 201.6 1.686 0.172 0.155 0.178 2 0 5) ↑ PRZ4 3.865 5.287 284.1 231.1 1.560 0.172 0.155 0.178 2 0 5)
Imidazole EMI 1.757 4.983 217.6 143.7 1.640 0.416 0.394 0.214 1 0 3),5),7) ↑ BMI 5.674 4.932 256.2 180.4 1.659 0.414 0.412 0.214 1 0 3),5),6),7) ↑ HMI 10.144 4.921 294.4 219.8 1.671 0.414 0.412 0.214 1 0 3),5),7) ↑ 8MI 14.952 4.918 310.6 262.0 1.569 0.414 0.413 0.214 1 0 3),5),7) ↑ 10MI 19.997 4.917 357.4 290.0 1.687 0.414 0.412 0.214 1 0 3),5) ↑ MEMI 1.398 4.883 236.4 170.2 1.592 0.400 0.385 0.194 2 0 3) ↑ MPMI 3.130 4.845 238.4 169.4 1.610 0.394 0.393 0.193 2 0 3),6) ↑ MBMI 5.358 4.854 233.5 183.4 1.496 0.400 0.393 0.193 2 0 3),6) ↑ MHMI 10.002 4.846 271.0 221.9 1.529 0.400 0.394 0.193 2 0 3) Other S1 2.275 5.907 138.1 96.7 1.355 0.397 0 0.124 2 0 3) ↑ S2 3.709 5.019 473.7 345.3 1.990 0.804 0 0.160 2 0 3) ↑ S3 3.197 5.094 335.0 223.7 1.880 0.828 0 0.159 2 0 3) ↑ S5 2.861 5.802 246.6 160.5 1.726 0.503 0 0.172 1 0 3) ↑ S6 2.864 5.811 216.6 147.8 1.603 0.539 0 0.175 1 0 3) ↑ S7 3.862 5.797 251.5 151.6 1.829 0.546 0 0.176 1 0 3) ↑ S8 1.290 5.807 249.8 151.1 1.821 0.505 0 0.158 2 1 3) ↑ S9 5.671 4.368 161.3 144.0 1.214 0.651 0 0.125 1 1 3) ↑ S10 9.529 4.489 176.8 162.9 1.226 0.677 0 0.128 1 1 3) ↑ S13 1.940 5.730 183.4 106.3 1.690 0.236 0.172 0.189 1 0 3) ↑ S14 4.290 5.182 268.4 168.0 1.823 0.425 0.394 0.207 1 0 3) ↑ S16 3.700 5.236 297.8 161.5 2.077 0.906 0 0.160 2 0 3) ↑ S19 1.606 5.241 168.5 101.5 1.601 0.461 0.422 0.218 1 0 3) ↑ S20 2.242 4.352 156.1 131.2 1.250 0.610 0 0.117 1 1 3) ↑ S21 2.893 4.527 125.3 94.9 1.245 0.642 0 0.117 1 1 3) code DP LUMOM Area Vol. Ova. N1 N2 Hmax Dis. sym. lit Use for 4MPZ4 3.653 5.668 272.2 212.6 1.580 0.470 0 0.171 1 1 6) Prediction EEP5 4.964 4.11 243.5 232.6 1.332 0.553 0 0.115 1 0 4) ↑ MM56 6.744 4.252 275.0 248.9 1.437 0.592 0 0.119 1 0 4) ↑ MM66 6.941 4.248 293.8 266.2 1.468 0.592 0 0.119 1 0 4) ↑ MBB6 3.314 4.145 306.2 283.9 1.466 0.580 0 0.119 1 0 4) ↑ PPB6 5.161 4.03 316.8 304.0 1.449 0.565 0 0.115 1 0 4) ↑ PP66 6.460 4.019 354.3 338.6 1.508 0.565 0 0.115 1 0 4) DP: Dipole Moment
LUMOM: Reverse sign of LUMO
Area: Connolly Molecular Area (Angstroms Squared) Vol.: Connolly Solvent-Excluded Volume(Angstroms Cubed)
Ova.: Ovality, the ratio of the calculated surface area to the minimum surface area of a molecule which is found by assuming the calculated volume is that of a sphere of radius.
N1,N2: Charge of Nitrogen Atom
Hmax: Charge of Maximum charged Proton
Dis.: Distance from Charged Nitrogen Atom to Maximum charged Proton Sym.: Symmetry on Charged Nitrogen
4. 結果と考察
4.1. イオン液体の粘度
遺伝的アルゴリズムが導きだした粘度式は次の 式であった。 log(Vis.)=1.148+0.0830*power((Tref.* -0.0122+1),0.397)*power((DP*-0.0069+1),0.664)* power((LUMOM*0.1180+1),1.848)*power((Area*-0.1227 +Vol.*0.5272+Ova.*-28.6399 +1), 0.291) *power((N1*1.224+N2*0.0762 +1),1.213) *power((TFSI*-0.066+Br*###+Cl*1.354+PF6* 0.574 +BF4*0.432+CF3SO3*0.146+1),1.575)・・・ 式(2) (Brアニオンを用いた粘度測定系が無かったため Brのパラメータは未決定) 式(2)にデータを入れた相関関係を図2に示す。 1 1.5 2 2.5 3 3.5 4 4.5 5 1 1.5 2 2.5 3 3.5 4 4.5 5Calculated Viscosity by eq. (
2 ) [cP] log(Viscosity) cP MHMI-BF4 PPR12-TFSI PPR13-TFSI R2=0.9464
Figure 2. Calculated vs Literature Viscosity for the set of 62 Ionic Liquids
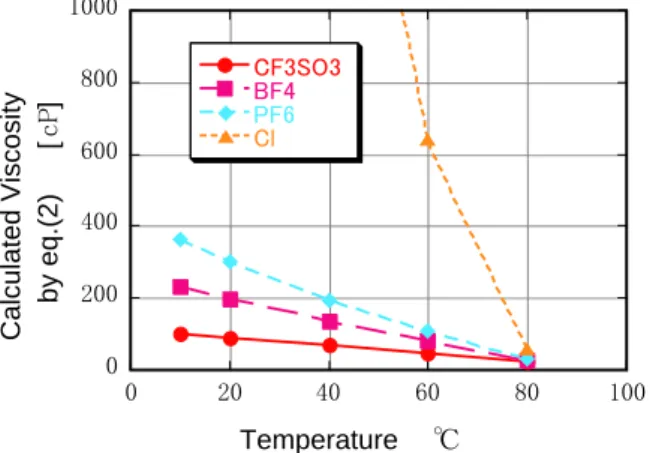
ピペリジン(PPR)類は2点ともに直線から外れ る。MHMI-BF4も直線から外れるが、R2=0.9464と 良好に粘度の実験値を再現できている。このピペリ ジン類がこの推算式から外れる理由としては、この 化合物が舟型、椅子型の配座異性体をとること、窒 素につく置換基の方向がaxialとequatorialがあり、 それらによってダイポールモーメントや分子の表 面積、体積、Ovalityが大きく変化してしまうこと。 さらに舟型を取った場合アニオンとの相互作用が 一種のキレート効果により非常に高まるので異常 値をとると考えられる。 0 200 400 600 800 1000 0 20 40 60 80 100 CF3SO3 BF4 PF6 Cl Calculated Viscosity by eq.(2) [ cP ] Temperature ℃
Figure 3. Temperature Dependency for BMI salts このような粘度式が組み上がると測定温度 (Tref.) を変化させたりアニオンを変えたりしたときの粘 度が自由に計算できる。カチオンとして 1-ブチル-3-メチルイミダゾール(BMI)を使って計算した例を図 3に示す。同じ系での実測値が『イオン液体』[3] p33 にある。20℃以上ではよい一致を示している。低温 での計算値が合わないのは今回作成した粘度式に 20℃未満の粘度の値が一つも入っていないためで ある。 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 10 20 30 40 50 60 70 80 90 Cal cul ated val ue by eq. (3) Temperature ℃
Figure 4. Temperature Effect for the viscosity この時の測定温度(Tref.)の効果は
power((Tref.*-0.0122+1),0.397)・・・式(3) で計算される。(図4)本来は下に凸の曲線になる べきものが上に凸になっている。これは収集した粘
度のデータが20℃のもの7点、40℃、50℃、80℃の ものが各1点、それ以外はすべて25℃のデータであ ったため測定温度の効果を表す式(3)が十分な精度 を持っていないためと考えられる。 粘度が(2)式で表せるとすると Log(Vis.)/(Power((A*Tref. + 1),B)*Power((N* TFSI+O*Br+P*Cl+Q*BF4+R*CF3SO3+1),S)) と粘度を測定温度の効果とアニオンの効果で割っ た値は温度やアニオンによらない正味のカチオン の粘度となる。
Table 4 Net Effect of Cation
Cation Anion Cation Net Ave.
EMI BF4 0.38 EMI CF3SO3 0.45 0.42 EMI TFSI 0.42 BMI BF4 0.73 BMI CF3SO3 0.73 0.72 BMI PF6 0.73 BMI TFSI 0.71 HMI BF4 0.79 HMI Cl 0.86 0.83 HMI PF6 0.83 HMI TFSI 0.85 8MI Cl 0.98 8MI PF6 0.98 1.00 8MI TFSI 1.04 PRL14 PF6 0.89 0.82 PRL14 TFSI 0.76 PZ4 BF4 0.78 PZ4 PF6 0.86 0.85 PZ4 TFSI 0.89 PZ6 BF4 1.01 0.93 PZ6 PF6 0.85 イミダゾール類では良い一致を示すがピロールや ピリジニウム類ではばらつきが大きい。BF4に関し ては平均よりも+にずれる場合と-にずれる場合が ありそのずれ幅が大きい。PF6に関してもBF4ほどで はないが値が大小する。イミダゾール類とPF6の分 子軌道計算[8]によるとイミダゾールのC2位のH原子 とPF6は水素結合することが示されている。この水 素結合のしやすさがカチオンの形やサイズによっ て変わる為このようなばらつきになって現れてい ると考えられる。 アニオンの粘度に対する効果は power((TFSI*-0.066+ Br*###+Cl*1.354+PF6* 0.574 +BF4*0.432+CF3SO3*0.146+1),1.575)・・・ 式(4) で表される。(TFSIからCF3SO3には対応するアニオ ンのところに1が入る。)このアニオンにかかる係 数をアニオンの粘度に対する効果(式4)に対してプ ロットすると図5のようになる。TFSIが一番粘度を 低く、Clが一番粘度を高くする。 0.5 1 1.5 2 2.5 3 3.5 4 20 40 60 80 100 120 140 -0.5 0 0.5 1 1.5
Anion Effect Calculated
by eq. (4)
Anion Volume
Coefficients of Anion in eq. (4)
TFSI CF3SO3
BF4
PF6 Cl
Figure 5. Coefficients of Anion Chem3Dで計算したアニオンの体積を右軸にプロッ トしてある。アニオンが大きくなるにつれ粘度は下 がるがBF4とPF6では逆転している。これはBF4が分 子体積的には小さく粘度を高くするはずであるが がカチオンとの特異的な相互作用で粘度を低くし ている事を示している。 脂肪族アルキルアンモニウム類に限ると炭素鎖 が伸びるといったん粘度が下がりその後は粘度が あがるという興味深い現象が知られている。[4](図 7a)この効果を詳しく検討するためアルキルアンモ ニウム類とピロール類だけを取り出し、アニオンは TFSI、温度は25℃の粘度の計算式を構築した。求 まった粘度式は log(Vis.)=1.322+0.0154* power((DP*63.274+1),-0.08309)* power((LUMOM*-0.217+1),-0.7592 )* power((Area *-0.753+Vol. *0.862+ Ova. * 5.360+1), 0.8185)* power((N1*0.830 +1), -0.3207) ・・・式(5) であった。相関結果を図6に示す。 この時のダイポールモーメントの効果は power((DP*63.274+1),-0.08309) ・・・式(6) で計算される。これを図7bに示す。炭素鎖が長くな るにつれ(ダイポールモーメントが大きくなり)式 (6)の計算値は単調に減少する。基本骨格の種類によ る違いはわずかであることがわかる。 分子の大きさ-形状の効果は
+1), 0.8185) ・・・式(7) で計算される。 これは分子の大きいMEE、PRLで高い値を示し MME、MMPなど小さい分子で小さい値となる。 (図7c) 1.7 1.75 1.8 1.85 1.9 1.95 2 2.05 1.7 1.75 1.8 1.85 1.9 1.95 2 2.05
Calculated Viscosity by eq. (5)
Log(Viscosity) [cP]
Figure 6. Calculated vs Literature Viscosity for the set of 31 Alkyl Ammonium TFSI Salts
50 60 70 80 90 100 2 3 4 5 6 7 8 9 10 MME MMP MMB MEE PRL Exp. Viscosity [cP] Number of Carbon (a) (b) (c) eq. ( 7 ) Calculated Value eq. ( 6 ) Calculated Value 0.55 0.6 0.65 0.7 0.75 2 3 4 5 6 7 8 9 10 6 7 8 9 10 11 2 3 4 5 6 7 8 9 10
Figure 7. Structure vs Viscosity of Alkyl Ammonium TFSI Salt
ダイポールモーメントの効果が主骨格によらずに 単調に減少し、分子の大きさ-形状の効果は傾きはほ ぼ同一だが主骨格が大きい分子ほど大きな値にな る。そこで全体の粘度としては側鎖が伸びるにつれ 最初はダイポールモーメントの粘度低減効果で粘 度が下がるが炭素鎖が増えるに従い分子の大きさ-形状の粘度増大効果で全体としての粘度は増加す る。こうした理由で粘度はいったん下がってその後 あがるという挙動を示す。主骨格が大きなMEE、 PRLでは分子の大きさ-形状の粘度増大効果が大き いので早くダイポールモーメント粘度低減効果に 打ち勝つ。そこで側鎖は炭素鎖4-5で粘度が最小にな る。分子の小さなMEE、MMPでは側鎖の炭素鎖6 で粘度が最小になる。 R2=0.6313
4.2. イオン液体の融点
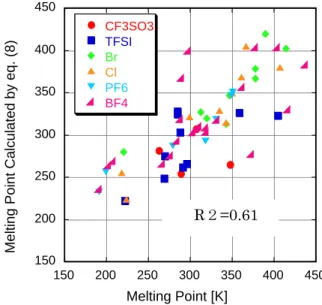
遺伝的アルゴリズムが導きだした融点式は次の 式であった。 Tm=4.967+119.985*power((DP*0.00813 +1), -3.2961)* power((LUMOM*2.827 +1),0.3262)* power((Area * -0.0441+Vol. * 0.0411 + Ova. * 2.856 +1),0.0497)* power((N1*0.406 +N2*0.139 +Hmax *-1.056 +1),1.7334)*power((dis.*-0.185 +1), -0.4598) *power((sym.*0.555 +1),0.2209)* power((TFSI*-0.263 +Br*0.189 +Cl*0.203 +PF6*-0.00309 +BF4*-0.163 +CF3SO3*-0.225 +1),0.4923) ・・・式(8) 150 200 250 300 350 400 450 150 200 250 300 350 400 450 CF3SO3 TFSI Br Cl PF6 BF4Melting Point Calculated by eq. (8)
Melting Point [K]
R2=0.61
Figure 8. Calculated vs Literature Melting Point for the set of 60 Ionic Liquids
相関結果を図8に示す。融点の推算の場合、粘度の推 算値を構築した記述子に加え、Hmax(分子中で一番 プラスに荷電している水素の電荷)、dis.(分子中 で一番プラスの水素が窒素+から何炭素結合分は なれているか)、sym.(窒素+原子を中心とした対称 性があるか)の情報を必要とする。この融点を推算 するのに水素の電荷やその距離などが必要である ということは、アニオンと水素が水素結合し融点を 変化させていることを示しており非常に興味深い。 アニオンが小さい塩素や臭素は比較的式(7)による 計算精度は高い。ずれが大きいのはBF4アニオンの 塩で、特にその中でも中和法で作られた窒素にプロ トンがつくS1, S3, S10, S14 で大きな誤差を持つ。 そこでアニオンをBF4に限りもう一度計算式の作 成を行った。 Tm=-31.963+1.381*power((DP* 7.152 +1 ) ,-0.2027)* power((LUMOM*6.750 +1) ,1.7363)* power((Area*0.333 +Vol.*2.180 +Ova.*4.409 +1),-0.0715)* power((N1*1.723 +N2 *3.779+1), 2.0809)* power((Hmax *-4.444 +1), 0.6463) * power((dis.*-0.260 +1), 0.7180) *power((sym.*0.0730+1),1.2695) ・・・式(9) 相関結果を図9に示す。今度は相関係数R2=0.8370 と非常に良好に実験値を再現できた。 150 200 250 300 350 400 450 150 200 250 300 350 400 450
Melting Point Calculated by eq. (9)
Melting Point [K]
Figure 9. Calculated vs Literature Melting Point for the set of 21 BF4 salts
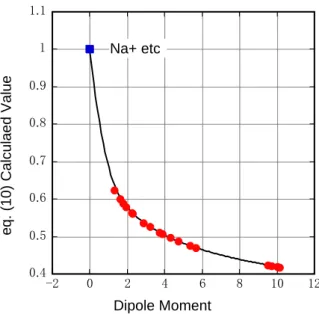
式(8)では収束しないBF4アニオンの塩が式(9)では 収束したことはBF4アニオンとカチオンの相互作用 が他のアニオンとは異なっている事を示している。 ダイポールモーメントの融点に対する影響量は power((DP*7.152+1),-0.2027)・・・式(10) で計算 される。これをプロットすると図10のようになる。 このようにダイポールモーメントが増えるに従い 融点に対する影響は低下することがわかる。逆にダ イポールモーメントが0に近くなる側鎖の長さが 均等なテトラアルキルアンモニウム類やNa+は融 点が高くなる。その効果は融点を倍以上変化させる ことを示しているので電荷の中心を分子の何処に 持ってくるかの分子設計が非常に重要であること がわかる。 0.4 0.5 0.6 0.7 0.8 0.9 1 1.1 -2 0 2 4 6 8 10 12
eq. (10) Calculaed Value
Dipole Moment Na+ etc
R2=0.8370
Figure 10. Effect of Dipole Moment to Melting Point 0.5 0.55 0.6 0.65 0.7 0.75 0.8 150 200 250 300 350 400 450
eq. (11) Calculated Value
Melting point [K]
Figure 11. Effect of Molecular Size and Shape to Melting Point
次に分子の大きさ-形状の効果が融点に及ぼす影 響を考察する。式(9)中の分子の大きさ-形状の融点 に対する影響量は
power((Area*0.333 +Vol.*2.180 +Ova.*4.409 +1), -0.0715) ・・・式(11) で計算される。 これを図示すると図11のようになる。これは粘度の (図7c)場合と大きく異なってカチオンの大きさ-形 状は融点にはほとんど影響を与えないことを示し ている。
4.3. 予測性能
得られた粘度の計算式 (2),(5) を使って計算式の 構築に使わなかった化合物の粘度の予測を行った。Table 4. Prediction of Viscosity
code Anion Vis eq.(2) eq. (5) EEP5 TFSI 90.6 86.4 94.8 MM56 TFSI 65.5 95.9 78.7 MM66 TFSI 66 101.1 82.4 MBB6 TFSI 70.1 106.5 96.2 PPB6 TFSI 93.7 106.1 107.9 PP66 TFSI 110.6 113.4 110.1 4MPZ4 TFSI 72.2 87.5 Table 4 に示す化合物は計算式を構築した化合物群 よりかなり分子のサイズが大きい(外挿データ)カ チオンであるが良好に粘度を予測できている。今回 用いたデータセットでは粘度の推算に分子中で一 番プラスに荷電しているプロトンの情報や対称性 を用いなくても計算式が収束した。今後新たな化合 物(中和法で作られた窒素にプロトンがつくカチオ ンなど)の粘度を推算しようとした場合にはこれら の情報が必要になってくると考えられる。 次に融点の計算式 (8),(9)を使って予測を行った。
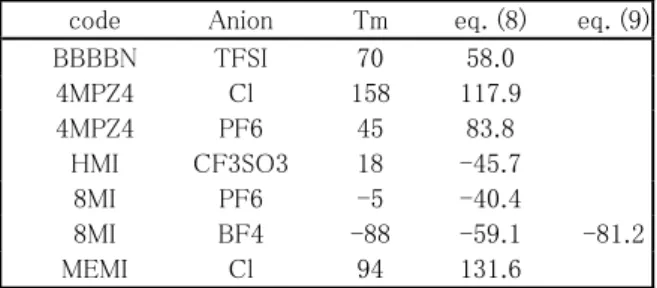
Table 5. Prediction of Melting Point
code Anion Tm eq. (8) eq. (9)
BBBBN TFSI 70 58.0 4MPZ4 Cl 158 117.9 4MPZ4 PF6 45 83.8 HMI CF3SO3 18 -45.7 8MI PF6 -5 -40.4 8MI BF4 -88 -59.1 -81.2 MEMI Cl 94 131.6 HMI-CF3SO3のように50℃以上ずれる系もあるが 融点の実測値のばらつきを考えると良好に融点を 予測できていると言える。
5. まとめ
イオン液体が室温付近で液体でいられるのはカ チオンの電荷の中心が分子の重心からずれること によって発生したダイポールモーメントが主要な 役割をなしていることが明らかとなった。またBF4 アニオンは粘度においても融点においても特異的 なアニオンであることが明らかになった。これは BF4アニオンとカチオンの水素結合の度合いがカチ オンの形状と大きさに依存して急激に変化するた めと考えられる。文献
[1] Alan R. Katritzky et al., J. Chem. Inf. Comput. Sci. 42, 225-231, (2002)
[2] Alan R. Katritzky et al., J. Chem. Inf. Comput. Sci. 42, 71-74, (2002) [3]イオン流体、CMC出版 [4]イオン性液体の機能創成と応用 STN出版 [5]イオン液体 vol.3 vol.4 [6]www.sigma-aldrich.co.jp/aldrich/greenchemist ry/Liquid_Ion/pdf/A-162.pdf [7]www.imidazole.jp/ver_01/catalog/catalog_ion 01.html
[8] Z. Meng et al., J.Mol.Struc., Theochem., 585, 119 (2002)
Structure Properties Relationship of Ionic Liquid
Hiroshi Yamamoto
*Asahi Glass Co. Central Laboratory
The equations for obtaining the viscosity and melting points of ionic liquids were built. These euations could be applied Imidazolium, pyridinium or ammonium cation with some kind of anion. Molecular descriptors for predicting viscosity of these ionic liquids were based on the size and electrostatic properties in the cations. For the melting points, hydrogen bonding force evaluation became important. To determine coefficients in none linear equation, Genetic Algorithm(GA) were adapted. Eight-parameter correlation was obtained for viscosity with R2=0.9464. But melting point correlation was hard to converge especially with BF4 anion salts. So individual equation was built for BF4 anion. Ten-parameter correlation was obtained for melting point with R2=0.837. Experimental melting point itself varied widely, so this squared correlation coefficient is correct enough.
keywords: Ionic Liquid, Viscosity, Melting Point, Structure-properties relationship
この効果を詳しく](https://thumb-ap.123doks.com/thumbv2/123deta/5960664.572529/8.892.82.422.348.859/アニオンプロッアニオン子体積カチオンアルキルアンモニウム.webp)