第 11 回 章 老化 遺伝子
コ ン 遺伝子医療革 を
日紫喜 光良
章 構成
• ン プ progeria
• プ 生化学
• 私 老い
• 動物 老化予防 ン を学ぶ
• 摩耗
• 長 遺伝 ?
章 構成
• 人生 黄金期を奪う 病
• 老化 を落
• サ 後
プ
• チ ン ン プ 症候群 Hutchinson-
Gilford Progeria Syndrome HGPS
– OMIM: 176670
• 新生児期 い 幼年期 好発 全身 老化 異常 進行
早老症疾患
– 早老症 含 疾患 症候群
• ン A LMNA; NCBI Gene ID: 4000 変異
– LMNA lamin A, lamin C をコ
– 片方 染色体 (heterozygous) 点突然変異 (point mutation)
– (de novo) 変異
– 1824C-T
• GGC→GGT
• ン#11, silent gly-to-gly (G608G), プ ン サ を形成
– プ ンA 尾50 酸
• プ ン ば タン 質
ン
Eriksson, M., et al. Recurrent de novo point mutations in lamin A cause Hutchinson-Gilford progeria syndrome. Nature 423: 293-298, 2003.
プ ン
http://www.mls.sci.hiroshima-u.ac.jp/smg/education/splicing.html
ン ン
snRNP RNA タン 質 複合体
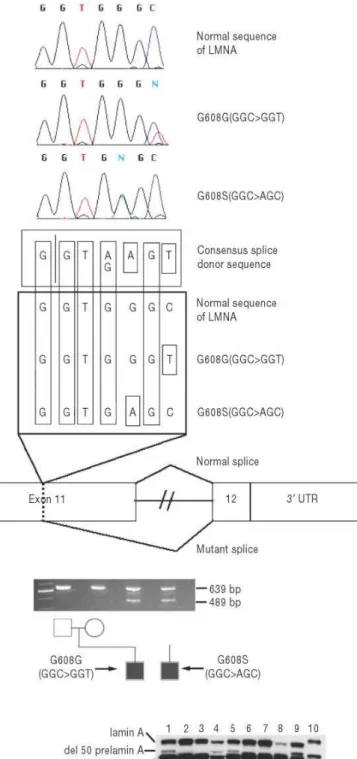
FIGURE 2. Point mutations in exon 11 of LMNA cause HGPS.
a, Sequence traces from a normal control and two HGPS patients. b, Hypothesis for
activation of a cryptic splice donor site in exon 11. c, Demonstration of the abnormal splice product using RT–PCR, showing an abnormal product of 489 bp in the two HGPS probands due to activation of the cryptic splice site. Alternative lanes to the right lack reverse transcriptase. d, Western blot using a monoclonal antibody against lamin A/C. Lanes 1, 5, 8 and 9 are from AG03506, AG03344, AG11498 and AG01972; they all carry G608G(GGC > GGT). Lane 4 is from AG10801, carrying G608S(GGC > AGC); lanes 2 and 3 are from parents of AG03506; lanes 6 and 7 are from father of AG03259 and mother of AG06917, respectively. Lanes 1–5 are from lymphoblastoid cell lines; lanes 6–9 are from fibroblasts. A protein sample from HeLa cells is in lane 10.
LMNA 変異 早老症
Brian A. et al. Werner and Hutchinson–Gilford progeria syndromes: mechanistic basis of human progeroid diseases
Nature Reviews Molecular Cell Biology 8, 394-404 (May 2007)
化
プ ン
ン A/C タン 質 機能
• intermediate filament 中間径線維 / 中間径
ン 一種
– 細胞骨格 構成要素
– チン ン 微小管 中間 太
• ン 機能
– 核膜 内側 あ 核 形 大 を決定
プ 生化学
ン A/C 発現時期
• NCBI UniGene 調
– mRNA 配列 EST 配列
を遺伝子 組織
整理 タベ
• mRNA 一部 多 5'
3' 端 配列を多数
取 タベ
• 組織 程度多
タン 質 作
い 手
新生児期 多 発現
核内 ン A/C 分布
Mislocalization of heterochromatin, centromeres, and telomeres in E145K cells.
Taimen P et al. PNAS 2009;106:20788-20793
©2009 by National Academy of Sciences
別 箇所 変異 プ 患
者 核 形態
制限 延 効果
動物 老化予防 ン を学ぶ
初期 主 論文
Clancy, D. J., et. al. Dietary restriction in long-lived dwarf flies. Science 296, 319 (2002)
Clancy, D. J. et al. Extension of life-span by loss of CHICO, a Drosophila insulin receptor substrate protein. Science 292, 104–106 (2001)
Holzenberger, M. et al. IGF-1 receptor regulates lifespan and resistance to oxidative stress in mice. Nature 421, 182–187 (2003)
Kenyon, C., et al. C. elegans mutant that lives twice as long as wild type. Nature 366, 461–464 (1993)
Tatar, M. et al. A mutant Drosophila insulin receptor homolog that extends life-span and impairs neuroendocrine function. Science 292, 107–110 (2001)
Tu, M. P.et al. The demography of slow aging in male and female Drosophila mutant for the insulin-receptor substrate homologue chico. Aging Cell 1, 75–80 (2002)
ョ ョ
ョ ョ
線虫
ョ ョ
ョ ョ
制限 延
Koubova J, Guarente L. How does calorie restriction work? Genes Dev. 2003 Feb 1;17(3):313-21.
ROS:活性酸素
大 種類考え
酵母 Sir2仮
詳細 明
哺乳類 場合
制限
黒線 抑制 変化
赤線 亢進
1. 適応期 adaptive period
哺乳類 場合
• 定常期 steady state
– ン ン分泌 低
• 細胞 ベ 酸化 抵抗性 増大
– 体温低
– 成長 ン低 GH ン 変化
– 肝臓 IGF-1 分泌低 サ ン
変化
– 変化 臓器 低 亢
進
哺乳類 制限 延
考え い
制限 感染 抵抗性
Kristan DM. Calorie restriction and susceptibility to intact pathogens. Age (Dordr). 2008 Sep;30(2-3):147-56.
サ チュ ン sirtuin 1
• SIRT1 (NCBI Gene ID: 23411)
• ン酵母 yeast Sir1 遺伝子 相同 配列を
• 機能 明 い
– 酵母 ン 脱 チ 化 遺伝子 転写
を抑制 を行う .
サ チュ ン 長 関係 い可能性
• 実験 用い 動物 線虫 ョ ョ
照群 比較 用い 他 変異
混 い 可能性
• サ チュ ン 長 関 を否定
い 実験 頑健性 疑問を投
Burnett C, et al. Absence of effects of Sir2 overexpression on lifespan in C. elegans and Drosophila. Nature. 2011 Sep 21;477(7365):482-5.
摩耗
染色体 端部分を い
い 同 塩基配列 哺乳類
TTAGGG 数百回繰 返
い 細胞分裂 DNA複製
完全 複製
短 い
http://bp.nuap.nagoya-
u.ac.jp/sosui/sumitomo/sitetop4/ newpage3.htm
GGG
いう え 配列を識別
応 RNA 鋳型を使い
を伸ば い 働
生殖細胞や ン細胞 顕著 あ
わ い
遺伝子
• 遺伝因子 いあ ?
– 20~30% 書 70 以 高齢者 い
高
• 関係 あ ン あ
?
– 多 見 い い
長 遺伝 ?
病
• 患者数 米国 450 万人 書
– 日 認知症全体 200~242 万人 2020 年 320 万人 増加
可能性 あ [1]
• 認知症 原因 ひ
– 脳血管性認知症
– 病
• 家族性 病
• 型認知症
– 小体型認知症
• 発症年齢 60 以 多い
– % 書 40 ~ 50 代 発症 早発型
病
• 症状 徐々 進行 認知 害
– →意思疎通 困難 問題行動→運動 害 大脳機能 失
• 脳 病理的所見 老人斑 β - 沈着 神経原線維変化 異常
タ タン 質
人生 黄金期を奪う 病
[1]http://www.mhlw.go.jp/kokoro/speciality/detail_recog.html
病 遺伝
• 早発型 家族 強 関
• 他 95 % 遺伝性 因子 大 い
– 70% を占 いう 書
– APOE 遺伝子 ョン ε4
• 85 病 確率
– コ 30% コ 80% 書
– 一般 10%
• 遺伝以外 因子 頭部外傷 あ
書
書 頁
慢性病 予防 を十分 生 鍵
• 煙を い
• ン 良い食生活
• 低容量 ン 男性 場合
• 日焼 い
• 家族 あ 病気 徴候 気を
老化 を落 ?
書 頁
ン 阻害薬
(FTI)
• 短縮 ン A タン 質 プ ン
化を防
サ 後
通常 老化 プ ン 役割
• 高齢者 細胞内 プ ン 濃度 増
え い
• 希少疾患 プ 研究 一般的 病
気あ い 正常 生物学的プ 解明
可能性を示 一例 いえ
– 異常 老化減少を引 起 希少疾患を研
究 正常 老化プ
ン を理解
書 ~ 頁